局部晚期食管癌患者3DCRT联合雷替曲塞顺铂方案的近期疗效
郭 卿
(江苏省泰州市人民医院肿瘤科,江苏 泰州 225300)
在我国,食管癌是发病率高,且死亡率高的消化道肿瘤,多数患者就诊时已属局部晚期,失去手术机会。因为放疗及化疗方案的选择对局部晚期食管癌患者来说至关重要,所以目前有较多的临床试验和研究均和这个领域有关,但食管癌患者的局部控制率及生存率仍未得到明显的提高,提示目前该领域仍无突破性进展[1]。雷替曲塞属于喹唑啉叶酸盐类似物,胸腺合成酶抑制剂之一。细胞主动摄取雷替曲塞后经过代谢成为聚谷氨酸,可以更明显的抑制胸腺合成酶发挥作用,同时长期储备在肿瘤细胞内抑制细胞合成DNA。因其副反应小,给药方式快,优于传统5-FU,迅速的取代了5-FU[2]。近3年以来,泰州人民医院肿瘤内科采取雷替曲塞顺铂方案联合三维适形放疗(3DCRT)针对局部晚期食管癌患者,临床疗效优于单纯放疗组,同时不良反应较轻。现将结果作如下分析。
1 资料与方法
1.1 一般资料
选取近3年本院收治的局部晚期食管癌患者60人,其中男性30人,女性30人,年龄43~78岁,中位年龄为62岁。60例患者KPS评分均高于60分,预计生存期大于3个月,且无放化疗禁忌症。60例患者按其治疗方式分为雷替曲塞顺铂方案方案化疗联合3DCRT组(联合组)30例及单纯3DCRT组(单放组)30例。
1.2 治疗方法
西门子直线加速器,6MVX线,2.0Gy/天,5次/周,50~60Gy/25~30Fx,3DCRT计划的实施及治疗流程:CT模拟机下体位固定,行胸部CT扫描,传送CT扫描的图像至TPS系统,医师根据辅助检查结果勾画肿瘤靶区,再由物理师设计照射野,通过CT模拟机校位,通过加速器校对照射野后,开始放疗。放射剂量:95%PTV56~60Gy/30次(1.8~2Gy/Fx)。脊髓1%体积的受量<40Gy,心脏受量V40<45%,肺受量V20<25%。使用德国西门子直线加速器6MVX线行3DCRT。治疗时间5~6周左右,从放疗第一天开始雷替曲塞2.25 mg/m2第1天静滴;顺铂30 mg/m2第1~3天静滴,28天为一个周期,至3DCRT结束。
1.3 评价标准
(1)近期疗效评价:按以RECIST1.1疗效评定标准将近期疗效分为:完全缓解(CR)、部分缓解(PR)、稳定(SD)及进展(PD),有效率评价指标为CR+PR。在放化疗结束后1个月评价60例局部晚期不能手术食管癌患者近期疗效。疗效评价按照患者胸部平扫+增强CT和食管钡双重造影或食管碘海醇双重造影为参考指标;
(2)不良反应:按照RTOG(美国肿瘤放射治疗组)急性放射损伤分级标准评价患者不良反应。
1.4 统计学方法
使用SPSS 21.0软件分析,t检验用于均数的比较,x2检验用于两组间率的比较,P<0.05为差异有统计学意义。
2 结 果
2.1 近期疗效
如表1所示,雷替曲塞顺铂方案联合3DCRT组(有效率90%)明显高于3DCRT组(有效率70%)。

表1 联合组和3DCRT组治疗的近期疗效(n,%)
2.2 毒副反应
2组均存在放射性食管炎、放射性肺炎、三系减少和肝功能损害不良反应(P>0.05),但联合组中不良反应,如恶心呕吐、白细胞减少,均明显高于单放组(P<0.05),值得注意的是,这些不良反应中并无III-IV级不良反应,且经对症治疗后可以缓解,并不影响同步放化疗的正常进行。表2显示,联合组中不存在因不能耐受治疗强度而减量甚至停药的患者。
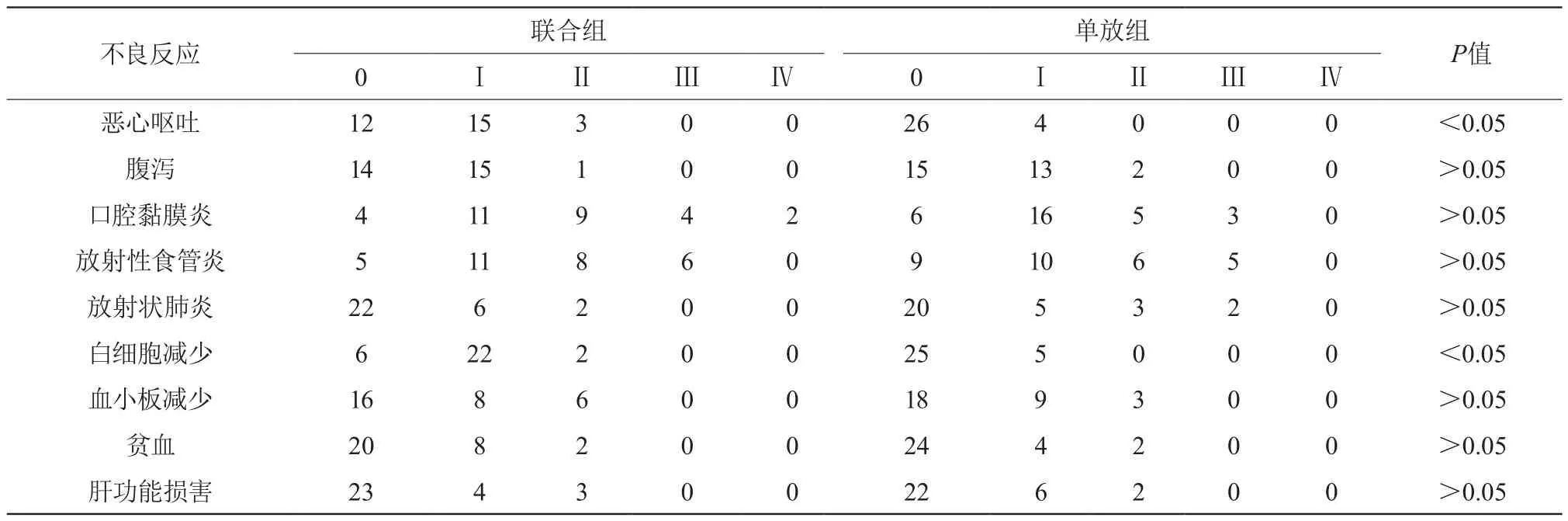
表2 联合组及单纯放疗组治疗的不良反应(n)
3 讨 论
近年来,肿瘤治疗方式越来越倾向于多学科综合治疗模式。但过度的治疗有可能导致生活质量的下降[3]。随着内镜手术越来越多的用于治疗癌前病变及早期食管癌,使食管癌的预后较前有所改善。新辅助化疗或同步放化疗已成为可以手术局部晚期食管癌患者的标准治疗方案。目前针对失去手术机会的局部晚期食管癌患者,放疗和化疗为主要治疗手段。但因常规同步放化疗方案中,5-FU及顺铂同步放疗的毒副反应较大,病人常因不能耐受而中断治疗,影响了食管癌的预后。因此,改进同步放化疗方式可能会提高疗效,改善预后。
对于不能耐受5-FU联合顺铂方案化疗的病人来说,通过提高放疗剂量是否能达到相同治疗疗效也是近年来研究的热点。在一项随机对照试验(INT0123)中,研究者声称提高放疗标准剂量并不能改善局部控制或使生存获益[4,5]。值得注意的是,CROSS(41.4Gy)的放疗剂量低于同步放化疗方案的剂量并获得了好的疗效[6]。因此,我们得出结论,单纯提高放疗技术及放疗剂量,并不能使疗效获得较大收益,而改进同步放化疗方案可能是提高疗效和改善生存的关键所在。
临床工作中,最常使用的氟尿嘧啶类药物主要为5-FU、卡培他滨和替吉奥,但因为此三种药物严重的心脏毒性,使不能耐受的患者只能选择放弃此三种药物,但可以选择雷替曲塞代替。雷替曲塞是胸苷酸合成酶的特异性抑制剂,其安全性已得到临床支持,且关于雷替曲塞的心脏毒性未见报道[7]。
此研究旨在探索雷替曲塞顺铂方案方案化疗联合3DCRT的近期疗效及不良反应。我们发现雷替曲塞顺铂方案化疗联合3DCRT治疗局部晚期食管癌的不良反应同单纯放疗组相比,两组患者腹泻、口腔黏膜炎、放射性食管炎和放射性肺炎无统计学差异,而恶心呕吐及白细胞减少的不良反应,两组间差别有统计学意义,联合组疗效优于单纯3DCRT组。两组患者均耐受并完成治疗,提示雷替曲塞顺铂方案方案化疗联合3DCRT治疗局部晚期食管癌极具潜力。为临床医生选择同步放化疗方案提供了依据和参考。
[1] Hayakawa Y,Sethi N,Sepulveda AR,Bass AJ,Wang TC:Oesophageal adenocarcinoma and gastric cancer:Should we mind the gap? NAT REV CANCER 2016,16:305-318.
[2] Martinez MD,Jafari R,Ignatushchenko M,Seki T,Larsson EA,Dan C,Sreekumar L,Cao Y,Nordlund P:Monitoring drug target engagement in cells and tissues using the cellular thermal shift assay.SCIENCE 2013,341:84-87.
[3] Markar SR,Wiggins T,Ni M,Steyerberg EW,Van Lanschot JJ,Sasako M,Hanna GB:Assessment of the quality of surgery within randomised controlled trials for the treatment of gastro-oesophageal cancer:A systematic review.LANCET ONCOL 2015,16:e23-e31.
[4] Minsky BD,Pajak TF,Ginsberg RJ,Pisansky TM,Martenson J,Komaki R,Okawara G,Rosenthal SA,Kelsen DP:INT 0123 (Radiation Therapy Oncology Group 94-05) phase III trial of combined-modality therapy for esophageal cancer:High-dose versus standard-dose radiation therapy.J CLIN ONCOL 2002,20:1167-1174.
[5] Kachnic LA,Winter K,Wasserman T,Kelsen D,Ginsberg R,Pisansky TM,Martenson J,Komaki R,Okawara G,Rosenthal SA,Willett CG,Minsky BD:Longitudinal Quality-of-Life Analysis of RTOG 94-05 (Int 0123):a Phase III Trial of Definitive Chemoradiotherapy for Esophageal Cancer.Gastrointest Cancer Res 2011,4:45-52.
[6] Shapiro J,van Lanschot J,Hulshof M,van Hagen P,van Berge HM,Wijnhoven B,van Laarhoven H,Nieuwenhuijzen G,Hospers G,Bonenkamp JJ,Cuesta MA,Blaisse R,Busch O,Ten KF,Creemers GM,Punt C,Plukker J,Verheul H,Bilgen E,van Dekken H,van der Sangen M,Rozema T,Biermann K,Beukema JC,Piet A,van Rij CM,Reinders JG,Tilanus HW,Steyerberg EW,van der Gaast A:Neoadjuvant chemoradiotherapy plus surgery versus surgery alone for oesophageal or junctional cancer(CROSS):Long-term results of a randomised controlled trial.LANCET ONCOL 2015,16:1090-1098.
[7] Popov I,Carrato A,Sobrero A,Vincent M,Kerr D,Labianca R,Raffaele BA,El-Serafi M,Bedenne L,Paillot B,Mini E,Sanches E,Welch J,Collette L,Praet M,Wils J:Raltitrexed(Tomudex) versus standard leucovorin-modulated bolus 5- fl uorouracil:Results from the randomised phase III Pan-European Trial in Adjuvant Colon Cancer 01 (PETACC-1).EUR J CANCER 2008,44:2204-2211.

