木薯淀粉接枝共聚物对钢在羟基乙酸溶液中的缓蚀性能
李向红, 邓书端, 李云仙, 刘建祥
(1.西南林业大学 理学院, 云南 昆明 650224; 2.西南林业大学 材料工程学院, 云南 昆明 650224)
木薯淀粉接枝共聚物对钢在羟基乙酸溶液中的缓蚀性能

LI Xianghong
李向红1, 邓书端2, 李云仙1, 刘建祥1
(1.西南林业大学 理学院, 云南 昆明 650224; 2.西南林业大学 材料工程学院, 云南 昆明 650224)
用丙烯酰胺(AA)单体对木薯淀粉(CS)进行接枝共聚化学改性,合成了木薯淀粉接枝共聚物(CSGC),采用失重法和电化学法研究了CSGC对冷轧钢在羟基乙酸溶液中的缓蚀性能。结果表明:CSGC能有效抑制冷轧钢在羟基乙酸中的腐蚀;缓蚀率随CSGC添加量的增大而不断上升,缓蚀率会随着温度的上升和浸泡时间的延长而下降,缓蚀率随着羟基乙酸质量浓度的增加呈先上升后下降的趋势。20 ℃时100 mg/L CSGC在0.3 mol/L羟基乙酸中浸泡24 h缓蚀率(失重法)高达92.1%,浸泡时间延长至72 h缓蚀率可达到89.13%。20~50 ℃时CSGC在0.3 mol/L羟基乙酸中的钢表面吸附符合Langmuir等温式,吸附焓(ΔH⊖)为-23.8 kJ/mol、吸附Gibbs自由能(ΔG⊖)为-28.3~-28.9 kJ/mol、吸附熵(ΔS⊖)为15.4~16.8 J/(mol·K)。羟基乙酸中CSGC在钢表面发生物理吸附/化学吸附的混合吸附,且吸附伴随熵增加的放热过程。在0.3 mol/L羟基乙酸中CSGC为符合“几何覆盖效应”机理的混合抑制型缓蚀剂;由Nyquist图谱显示,钢/羟基乙酸界面上存在H2O、H+、HOCH2COO-和CSGC的吸附/脱附过程,CSGC通过挤走水分子发生吸附。
木薯淀粉;接枝共聚物; 缓蚀剂;钢;羟基乙酸
添加缓蚀剂是防止金属腐蚀的重要手段之一,特别是在酸性介质中的酸洗、酸化、酸浸等化工行业中缓蚀剂得到了广泛应用。随着可持续发展战略和环保意识的增强,缓蚀剂的研究方向主要是研究和开发出价廉、高效的环境友好型缓蚀剂。天然产物作为金属缓蚀剂具有来源广、成本低、直接排放不会污染环境、无毒或低毒等优点,被认为是一种环境友好“绿色”缓蚀剂,其研究颇受国内外关注[1]。近些年来,已有不少关于松香基咪唑啉[2]、木质素磺酸盐[3-4]和竹叶提取物[5]等天然产物缓蚀作用的研究,它们对钢的腐蚀均产生明显的抑制作用,表现出良好的缓蚀性能。我国是农业大国,淀粉资源十分丰富,淀粉主要来源于玉米、大米、麦、木薯和马铃薯等农作物。木薯淀粉与其余淀粉相比最大的优势是木薯为非食用性农作物,故对其充分利用不会存在潜在的“粮食问题”。淀粉是较早被作为金属缓蚀剂应用的天然高分子产物,对钢铁在酸洗以及铝在碱液中都起到很好的缓蚀作用[6]。然而,由于天然淀粉具有腐败、老化、加热糊化后增稠等局限性,其工业应用受到一定限制,故需对淀粉进行改性处理,在各类改性处理方法中,接枝共聚可较大程度克服改性前淀粉的局限性[7]。通过引发剂引发使烯类单体接枝在淀粉半刚性链的骨架上制备的淀粉接枝共聚物是一类新型高分子材料[8]。课题组近期研究报道了木薯淀粉(CS)和丙烯酰胺(AA)接枝共聚所得的木薯淀粉接枝共聚物(CSGC)对冷轧钢在无机酸(1.0 mol/L H2SO4)介质中具有良好的缓蚀性能,最大缓蚀率为93.6%[9]。与HCl、H2SO4和HNO3等无机酸相比,羟基乙酸(HOCH2COOH)作为酸洗剂具有使用安全,分解产物无毒、无刺激气味,可避免二次污染等优点,已逐渐在钢材的酸洗工业中引起关注[10]。在前期研究的基础上,作者通过失重法、动电位极化曲线和电化学阻抗谱(EIS)进一步研究CSGC在有机酸HOCH2COOH溶液中对冷轧钢的缓蚀性能,并探究了CSGC在钢表面的吸附行为和缓蚀机理,为淀粉作为金属缓蚀剂的应用提供基础数据。
1 实 验
1.1 材料和试剂
冷轧钢片(攀枝花钢铁厂)试样的组成为:C 0.07%, Si 0.01%, Mn 0.3%, P 0.022%, S 0.01%,Al 0.030%。市售木薯淀粉(CS);丙烯酰胺(AA)、过硫酸铵、亚硫酸氢钠、羟基乙酸(HOCH2COOH)、无水乙醇和丙酮,均为分析纯。
1.2 木薯淀粉接枝共聚物(CSGC)的制备

称取10 g的CS和量取100 mL蒸馏水,依次加入干燥的250 mL三口烧瓶(分别装上N2管、冷凝管和搅拌装置)中,在80 ℃的恒温水浴中通N2搅拌糊化约30 min,静置冷却至40 ℃时再加入10 g的AA,保持反应温度(40 ℃)搅拌约15 min后加入5 g (NH4)2S2O8,缓慢滴加1.0 mol/L NaHSO3约 10 mL,持续搅拌至反应结束(约4 h);待反应液温度下降至室温(约23 ℃)后,用无水乙醇沉淀、过滤、洗涤,然后将产物置于真空干燥箱中,在50℃下干燥至质量恒定,得到接枝粗产物。以丙酮作为溶剂用索氏提取器对接枝粗产物抽提24 h,以去除粗产物中的均聚物[11],将所得产物于50 ℃再次真空干燥至质量恒定,即可得到精制CSGC。参考文献[11]对CSGC做红外光谱、紫外光谱和拉曼光谱结构表征确定了产物结构,如右图所示。
1.3 缓蚀性能测试
1.3.1 失重法 用500#、 800#和1000#系列耐水砂纸将25.0 mm×20.0 mm×0.6 mm的冷轧钢片试样逐级打磨,丙酮脱脂,用电子天平(±0.1 mg)精确称取初始质量后,用玻璃钩将钢片全部浸泡于250 mL不含(含有)一定质量浓度CSGC的0.3 mol/L羟基乙酸测试液中。恒温24 h后取出钢片,清洗、吹干,再次精确称量钢片腐蚀后的质量。固定CSGC的质量浓度为50和100 mg/L,改变羟基乙酸浓度和腐蚀浸泡时间,重复以上实验,探讨这2个因素对缓蚀率的影响规律。
依据式(1)计算缓蚀率(η):
η=[(W0-W)/W0]×100%
(1)
式中:W0—未添加缓蚀剂时钢片的质量损失,g;W—添加缓蚀剂钢片的质量损失,g。
1.3.2 电化学法 采用三电极体系,在PARSTAT2273电化学工作站(美国普林斯顿公司)上进行电位极化曲线和电化学阻抗谱(EIS)测试。参比电极为套有卢金毛细管的(232型) 饱和KCl甘汞电极(SCE),辅助电极为(213型)铂电极,工作电极为环氧树脂灌封的钢电极,测试软件为PowerSuite。用500#、 800#和1000#耐水砂纸将钢电极的裸露测试面(面积为1.0 cm×1.0 cm)逐级打磨光亮,丙酮脱脂后,浸泡于装有250 mL的0.3 mol/L的羟基乙酸溶液或添加了CSGC的羟基乙酸溶液烧杯中,置于HWS-20型恒温水浴箱中(20±0.1)℃浸泡6 h使开路电位稳定。极化曲线的扫描速率为0.5 mV/s,测试区间为-250~250 mV(相对于开路电位),η可通过式(2)计算:
η=[(icorr(0)-icorr(inh))/icorr(0)]×100%
(2)
式中:icorr(0)—未添加缓蚀剂的腐蚀电流密度,mA/m2;icorr(inh)—添加缓蚀剂的腐蚀电流密度,mA/m2。
EIS的测量频率为0.01~1.0×105Hz,交流激励幅值为10 mV,数据采集点为30个,采用式(3)换算出η:
η=[(Rt(inh)-Rt(0))/Rt(inh)]×100%
(3)
式中:Rt(inh)—添加缓蚀剂时的电荷转移电阻,Ω·cm2;Rt(0)—未添加缓蚀剂时的电荷转移电阻,Ω·cm2。
2 结果与讨论
2.1 CSGC对钢的缓蚀作用
2.1.2 缓蚀剂质量浓度的影响 0.3 mol/L羟基乙酸中20~50 ℃范围内的缓蚀率(η)与CSGC质量浓度(c)的关系曲线见图1。不同温度下,CSGC对冷轧钢的缓蚀率随着缓蚀剂质量浓度的升高而上升,20和30 ℃时,当CSGC质量浓度达到50 mg/L后,继续增加CSGC质量浓度缓蚀率增势趋缓,表明此时缓蚀剂分子在钢表面的吸附趋于饱和。而40和50 ℃时,缓蚀剂质量浓度提升至70 mg/L后,缓蚀剂分子才会在钢表面的吸附趋于饱和。CSGC在20、30、40和50 ℃时的最大缓蚀率分别为92.1%、89.3%、82.6%和77.2%,表明CSGC对冷轧钢在0.3 mol/L羟基乙酸介质中的腐蚀产生了良好的缓蚀作用。此外,随着温度的升高,CSGC对冷轧钢的缓蚀率有所降低,可能是由于高温时分子碰撞频率加快,羟基乙酸对钢表面的腐蚀程度加剧,实验中可观察到钢表面析出H2气泡的速率明显加快,不仅使缓蚀剂CSGC分子很难吸附在钢表面,而且也易使已吸附在钢表面吸附的缓蚀剂分子发生脱附,从而造成缓蚀性能随温度的升高而降低。
为了对比研究淀粉接枝共聚物接枝反应前后的缓蚀性能,相同条件下对比研究了100 mg/L CS、 100 mg/L AA、 100 mg/L CS+100 mg/L AA的缓蚀性能,见图2。从图2可以看出,CS的缓蚀作用不太理想,缓蚀率不超过30%;烯类单体AA具有中等程度的缓蚀作用,最大缓蚀率在50%左右;当CS和AA进行混合使用后,缓蚀率基本和单独使用AA相差不大;接枝共聚产物CSGC的缓蚀率远高于原料CS、AA、CS/AA。以上结果表明:单独使用CS或AA的缓蚀效果均不理想,也不能把CS和AA简单混合使用来提高缓蚀性能,必须对木薯淀粉进行化学改性才能提高其缓蚀性能,且通过接枝共聚后生成的CSGC具有良好的缓蚀作用。
2.1.2 腐蚀浸泡时间的影响 为了进一步考察CSGC的缓蚀性能后效性,用失重法测试了CSGC在不同腐蚀浸泡时间(24~144 h)对冷轧钢的缓蚀性能。图3为20 ℃在0.3 mol/L羟基乙酸溶液中添加50和 100 mg/L CSGC的η与有机酸腐蚀浸泡时间(t)的关系。2个浓度下缓蚀率均随浸泡时间的延长呈下降趋势,72 h时50 mg/L CSGC的缓蚀率达82.84%,100 mg/L时达到89.13%。在浸泡时间超过 72 h 后,缓蚀性能下降更为显著,原因可能是由于随着浸泡时间的延长,羟基乙酸对缓蚀膜层不断浸蚀,造成吸附膜层的缓蚀保护性能下降。当腐蚀浸泡时间到144 h时,50和100 mg/L CSGC的缓蚀率分别下降至70.6%和75.2%。

2.1.3 羟基乙酸浓度的影响 图4为20 ℃腐蚀浸泡时间为24 h,50和100 mg/L CSGC对冷轧钢的η与羟基乙酸浓度(C)的关系曲线图。


图5 钢电极的极化曲线(20 ℃) Fig.5 Polarization curves for steelelectrode (20 ℃)
由图4可见,CSGC的缓蚀率先随酸浓度的增加而增大,到0.3 mol/L时达到极大值,之后继续增加羟基乙酸浓度则缓蚀率下降,在0.5 mol/L羟基乙酸中50和100 mg/L CSGC的η分别下降至71.3%和82.6%。缓蚀率随酸浓度的变化出现极大值的独特变化规律,推测可能是由于钢表面的腐蚀产物参与了缓蚀剂分子在钢表面的吸附所致[12]。
2.2 CSGC缓蚀性能的电化学分析
2.2.1 极化曲线特征 20 ℃钢电极在0.3 mol/L羟基乙酸空白溶液,以及含有不同质量浓度(10、50、100 mg/L)CSGC酸溶液的动电位极化曲线见图5。从图5可以看出,与钢电极在0.3 mol/L 羟基乙酸空白溶液比较,加有缓蚀剂CSGC的阴阳两极极化均显著加大,且向腐蚀电流密度小的方向偏移,故CSGC同时抑制了钢在羟基乙酸中发生腐蚀的阳极氧化和阴极还原反应。表1为通过Tafel拟合得出的极化曲线参数及η结果。表1中数据表明腐蚀电流密度(icorr)在添加CSGC后显著下降,且随着CSGC用量的增加而不断降低,当CSGC质量浓度100 mg/L时η为85.6%,再次印证了CSGC对冷轧钢在羟基乙酸中具有良好的缓蚀性能。腐蚀电位(Ecorr)在添加CSGC前后基本没有变化,说明CSGC对冷轧钢在羟基乙酸介质中为混合抑制型缓蚀剂,并可推断缓蚀剂CSGC的电化学作用机理为“几何覆盖效应”[13]。加入CSGC后阴极Tafel斜率(bc)和阳极Tafel斜率(ba)均发生了变化,这是由于缓蚀剂CSGC吸附覆盖了钢表面的有效反应面积,致使钢/羟基乙酸界面发生改变[13]。
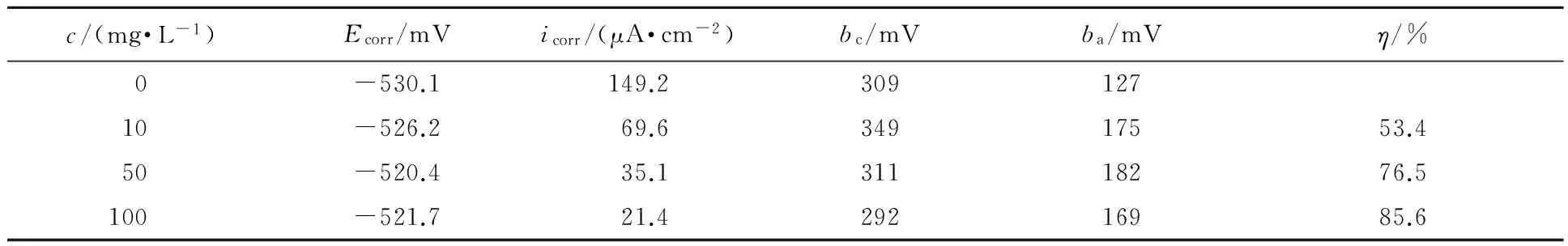
表1 CSGC在羟基乙酸介质中的极化曲线参数(20 ℃)Table 1 Polarization parameters of CSGC in glycolic acid (20 ℃)
2.2.2 电化学阻抗谱(EIS) 20 ℃冷轧钢在含不同质量浓度CSGC的0.3 mol/L羟基乙酸溶液介质中的Nyquist图谱,见图6。由图可知,阻抗谱在高频区呈现大段半圆容抗弧,而在低频区出现一小段感抗弧。容抗弧是压扁的半圆,表明体系中存在溶液离子和分子在电极/羟基乙酸界面上吸附/脱附不均匀引起的频率弥散效应[14]。羟基乙酸中小段感抗弧可能与H+、HOCH2COO-或CSGC在电极表面的吸附所引起的表面状态不稳定有关。在羟基乙酸添加不同质量浓度的缓蚀剂CSGC后,与空白溶液相比,Nyquist图谱的形状保持未变,表明添加缓蚀剂CSGC后未改变冷轧钢在羟基乙酸中腐蚀电化学机理。
容抗弧随缓蚀剂CSGC用量的增大而明显增大,故电极表面的阻抗值增加,表明冷轧钢在羟基乙酸中的腐蚀速率减慢,即缓蚀效果随CSGC用量增加而增大。容抗弧主要对应于电荷转移电阻(Rt)和界面双电层电容(Cdl)所组成的阻容弛豫过程。采用图7中所示的等效电路图拟合容抗弧数据,图中Rs为溶液电阻,Rt为电荷转移电阻,CPE为常相位角元件。EIS拟合参数及η列于表2。


表2 CSGC在羟基乙酸中的电化学阻抗谱参数(20 ℃)Table 2 EIS parameters of CSGC in glycolic acid (20 ℃)
表2中的Rs数据较大,这是由于羟基乙酸为弱电解质,导电能力不如强电解质,溶液中存在欧姆电位降效应。与空白溶液相比,添加CSGC缓蚀剂后Rt明显增大,但Cdl减小,对于缓蚀剂而言,较大的Rt和较小的Cdl往往具有较高的缓蚀率[15]。通过Rt换算出的η随CSGC质量浓度的增加而增大,当质量浓度为100 mg/L,最大η为85.8%,再次表明CSGC缓蚀剂可对冷轧钢在羟基乙酸中的腐蚀产生显著的抑制作用,起到了良好的缓蚀性能。在羟基乙酸中添加CSGC后Cdl减小,这是由于缓蚀剂CSGC吸附到钢表面时挤走了介电常数较大的水分子或使双电层的厚度增大所致[15]。
2.3 CSGC在钢表面的吸附行为分析

图8 Langmuir等温吸附模型模拟Fig.8 Langmuir isotherm adsorption model simulations
2.3.1 吸附等温式 假设0.3 mol/L羟基乙酸中CSGC在钢表面的吸附服从Langmuir吸附等温式[9],则有:
(4)
式中:c—缓蚀剂质量浓度,mg/L;K—吸附平衡常数,L/mg;θ—表面覆盖度(θe/θmax),其数值与η近似相等,%。
图8为20~50 ℃时吸附等温线,其对应的直线参数见表3。表3中的线性相关系数(r)和斜率两者均十分接近1,说明在0.3 mol/L羟基乙酸中CSGC在冷轧钢表面的吸附符合Langmuir吸附等温式。另一参数K随着温度的不断升高而下降,说明高温时CSGC分子在钢表面的平衡吸附量有所下降,这是由于高温时缓蚀体系中的分子碰撞程度加剧,故钢表面受到的腐蚀也显著加快,钢表面吸附的分子离子之间的相互作用力也不断变大,造成CSGC缓蚀剂分子难以在钢表面发生吸附。

表3 CSGC的等温方程参数Table 3 Isotherm equation parameters of CSGC
2.3.2 吸附热力学 钢表面吸附CSGC的热力学参数,标准吸附焓(ΔH⊖)可以根据Van′t Hoff方程求得:
(5)
式中:R—理想气体常数,8.314 J/mol;T—温度,K;I—不定积分常数。
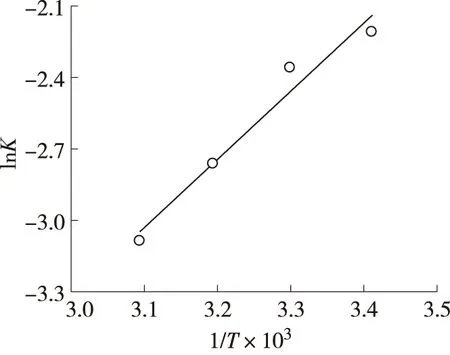
图9 lnK-1/T直线Fig.9 Straight line of lnK-1/T
图9为lnK-1/T直线,r为0.9712,可近似依据其斜率值求得ΔH⊖。标准吸附自由能(ΔG⊖)与K之间存在如下关系式[16]:
(6)
式中:c—水的密度,1 g/L[16]。
可通过如下热力学方程(式(7))求得标准吸附熵(ΔS⊖):
(7)
CSGC在钢表面上的吸附热力学参数的值列于表4。ΔH⊖<0 表明CSGC缓蚀剂分子在钢表面发生吸附是放热过程,即缓蚀剂分子吸附在钢表面后会释放出热量,从而温度升高不利于缓蚀剂分子的吸附,导致缓蚀性能在高温时会有所降低;ΔG⊖<0说明CSGC可自发在钢表面产生吸附,且其值处于-40~-20 kJ/mol之间,故CSGC缓蚀剂分子可以通过物理吸附和化学吸附(混合吸附)两种作用吸附在冷轧钢表面[17]。有机缓蚀剂分子在钢表面的吸附可看作溶液相中的缓蚀剂分子取代了钢表面已吸附的水分子,故ΔS⊖>0表明当一个CSGC分子吸附在钢表面时会挤走多个水分子,导致多个水脱附引起的混乱度增大量远远高于一个CSGC分子吸附在钢表面时的混乱度减小量,从而使吸附体系总的混乱度净增大[17]。

表4 羟基乙酸中CSGC在钢表面的吸附热力学参数Table 4 Adsorption thermodynamic parameters of CSGC on steel surface in glycolic acid
2.4 腐蚀及缓蚀作用机理
依据钢在酸中主要为析氢腐蚀,结合实验中观察到H2气泡从钢表面析出的现象,推测冷轧钢在羟基乙酸溶液中的腐蚀电化学机理。首先羟基乙酸在水溶液中发生部分电离:
HOCH2COOH→HOCH2COO-+H+
(I)
钢在羟基乙酸水溶液中的电化学腐蚀有共轭的阴极和阳极反应构成,H+主要参与阴极反应,而HOCH2COO-则参与了阳极反应。阴极极化曲线(图5)表明阴极析氢反应为活化控制,故可借用钢在无机酸中阴极析氢还原反应的机理[18]:
Fe+H+↔(FeH+)ads
(II)
(FeH+)ads+e↔(FeH)ads
(III)
(FeH)ads+H++e↔Fe+H2
(IV)
根据钢在甲酸(HCOOH)[19]和乙酸(CH3COOH)[20]溶液中阳极溶解机理,可拟定冷轧钢在羟基乙酸中的阳极氧化反应:
Fe+HOCH2COO-→(FeHOCH2COO-)ads
(V)
(FeHOCH2COO-)ads→(FeHOCH2COO)ads+e
(VI)
(FeHOCH2COO)ads→FeHOCH2COO++e
(VII)
FeHOCH2COO+→Fe2++HOCH2COO-
(VIII)
故阳极腐蚀反应最初为HOCH2COO-吸附在冷轧钢表面,进而引发了Fe变为Fe2+。

(IX)
3 结 论
3.1 丙烯酰胺(AA)改性的木薯淀粉(CS)接枝共聚物(CSGC)对冷轧钢在羟基乙酸中的腐蚀产生了良好的缓蚀性能,且其缓蚀率明显高于CS、AA或CS/AA混合物。随CSGC用量的增大,缓蚀率逐步增加,20 ℃时在0.3 mol/L羟基乙酸中加入100 mg/L CSGC 24 h后缓蚀率可高达92.1%,72 h时缓蚀率还可达到89.13%。随温度的升高、浸泡时间的延长,缓蚀性能有所降低。
3.2 CSGC缓蚀性能的电化学分析结果显示:添加CSGC前后腐蚀电位基本没有移动,CSGC可归为通过“几何覆盖效应”同时对阴阳两极产生明显抑制作用的混合抑制型缓蚀剂。钢/HOCH2COOH界面上存在H2O、H+、HOCH2COO-和CSGC的吸附/脱附过程,CSGC通过挤走水分子发生吸附。
3.3 对CSGC在钢表面的吸附行为研究表明:吸附完全服从Langmuir等温方程式,吸附平衡常数随温度的升高而下降。CSGC在钢表面的吸附过程中包含了物理吸附和化学吸附两种主要吸附方式,且吸附过程为伴随总混乱度增加的放热过程。
[1]FAUSTIN M,MACIUK A,SALVIN P,et al.Corrosion inhibition of C38 steel by alkaloids extract ofGeissospermumlaevein 1 M hydrochloric acid:Electrochemical and phytochemical studies[J].Corrosion Science,2015,92:287-300.
[2]王倩,付朝阳.CO2饱和NaCl溶液中松香基咪唑啉季铵盐的缓蚀吸附行为[J].腐蚀科学与防护技术,2012,24 (4):319-322. WANG Q,FU C Y.Corrosion inhibition and adsorption effect of rosinyl imidazolium quaternary ammonium salt on steel in CO2-saturated NaCl solution[J].Corrosion Science and Protection Technology,2012,24 (4):319-322.
[3]易聪华,邱学青,杨东杰,等.改性木质素磺酸盐GCL2-D1的缓蚀机理[J].化工学报,2009,60 (4):959-964. YI C H,QIU X Q,YANG D J,et al.Corrosion inhibition mechanism of modified ligno sulfonate GCL2-D1[J].CIESC Journal,2009,60 (4):959-964.
[4]WANG Y S,ZUO Y,ZHAO X H,et al.The adsorption and inhibition effect of calcium lignosulfonate on Q235 carbon steel in simulated concrete pore solution[J].Applied Surface Science,2016,379:98-110.
[5]邓书端,李向红,付惠.金竹叶提取物的缓蚀性能研究[J].林产化学与工业,2010,30(5):81-86. DENG S D,LI X H,FU H.Study on corrosion inhibition performance ofPhyllostachyssulphurealeaves extract[J].Chemistry and Industry of Forest Products,2010,30(5):81-86.
[6]张天胜,张浩,高红,等.缓蚀剂[M].2版.北京:化学工业出版社,2008:23-25. ZHANG T S,ZHANG H,GAO H,et al.Corrosion Inhibitors[M].2nd ed.Beijing:Chemical Industrial Engineering Press,2008:23-25.
[7]马建中,武文玲,高党鸽.乙烯基类单体接枝共聚改性淀粉的研究进展[J].中国皮革,2012,41 (3):59-62. MA J Z,WU W L,GAO D G.Research progress of grafted copolymer of starch and vinyl monomers[J].China Leather,2012,41 (3):59-62.
[8]GUO Q X,WANG Y Q,FAN Y F,et al.Synthesis and characterization of multi-active site grafting starch copolymer initiated by KMnO4and HIO4/H2SO4systems[J].Carbohydrate Polymers,2015,117 (6):247-254.
[9]LI X H,DENG S D.Cassava starch graft copolymer as an eco-friendly corrosion inhibitor for steel in H2SO4solution[J].The Korean Journal of Chemical Engineering,2015,32 (11):2347-2354.
[10]刘彦锋,马思远,刘世川,等.羟基乙酸酸洗缓蚀剂的性能研究[J].广东化工,2010,112 (8):112-114. LIU Y F,MA Y,LIU S C,et al.Study on performance of the corrosion inhibitor for hydroxyacetic acid[J].Guangdong Chemical Industry,2010,112 (8):112-114.
[11]李向红,付惠,李云仙,等.木薯淀粉改性絮凝剂的光谱研究[J].光谱实验室,2011,28 (1):124-127. LI X H,FU H,Li Y X,et al.The spectrum of the cassava starch flocculent agent[J].Chinese Journal of Spectroscopy Laboratory,2011,28 (1):124-127.
[12]NOOR E A.The inhibition of mild steel corrosion in phosphoric acid solutions by some N-heterocyclic compounds in the salt form[J].Corrosion Science,2005,47 (1):33-35.
[13]曹楚南.腐蚀电化学原理[M].2版.北京:化学工业出版社,2004:235-238. CAO CN.Corrosion Electrochemistry Mechanism[M].2nd ed.Beijing:Chemical Industrial Engineering Press,2004:235-238.
[14]ABD EL-LATEEF H M,ABO-RIYA M A,TANTAWY A H.Empirical and quantum chemical studies on the corrosion inhibition performance of some novel synthesized cationic gemini surfactants on carbon steel pipelines in acid pickling processes[J].Corrosion Science,2016,108:94-100.
[15]POURGHASEMI HANZA A,NADERI R,KOWSARI E,et al.Corrosion behavior of mild steel in H2SO4solution with 1,4-di[1-methylene-3-methyl imidazolium bromide]-benzene as an ionic liquid[J].Corrosion Science,2016,107:96-106.
[16]LI X H,DENG S D,FU H.Inhibition of the corrosion of steel in HCl,H2SO4solutions by bamboo leaf extract[J].Corrosion Science,2012,62:163-175.
[17]ZHENG W,ZHANG S T,LI W P,et al.Investigation of 1-butyl-3-methyl-1H-benzimidazolium iodide as inhibitor for mild steel in sulfuric acid solution[J].Corrosion Science,2014,80:383-392.
[18]ABDEL-GABER A M,KHALIL N,ABOU EL-FETOU A.The dissolution mechanism of steel in inorganic acids[J].Anti-Corrosion Methods and Materials,2003,50 (6):442-447.
[19]SINGH M M,GUPTA A.Corrosion behavior of mild steel in formic acid solutions[J].Materials Chemistry and Physics,1996,46 (1):15-22.
[20]高延敏,王绍明,徐永祥,等.A3钢在乙酸中的腐蚀行为及机理研究[J].腐蚀与防护,2006,27 (1):11-13. GAO Y M,WANG S M,XU Y X,et al.Corrosion behavior and mechanism of A3 steel in acetic acid[J].Corrosion & Protection,2006,27(1):11-13.
Corrosion Inhibition of Steel in Glycolic Acid Solution by Cassava Starch Grafted Copolymer
LI Xianghong1, DENG Shuduan2, LI Yunxian1, LIU Jianxiang1
(1.Faculty of Science,Southwest Forestry University, Kunming 650224, China; 2.Faculty of MaterialsEngineering,Southwest Forestry University, Kunming 650224, China)
Cassava starch grafted copolymer (CSGC) was synthesized via the chemical modification of cassava starch (CS) by grafting the monomer of acryl amide. The inhibition effect of CSGC on the corrosion of cold rolled steel (CRS) in glycolic acid was studied by weight loss method and electrochemical techniques. The results showed that CSGC could effectively retard the corrosion of cold rolled steel in glycolic acid solution. Inhibition efficiency was increased with the rise of dosage of CSGC. Meanwhile, it was decreased with the increasing of temperature and prolonging immersion time. The inhibition concentration, the maxima inhibition efficiency is found at 0.3 mol/L HOCH2COOH. The efficiency rose firstly. The inhibition efficiency was 92.1% as the steel were treated by 100 mg/L CSGC at 20 ℃ in 0.3 mol/L glycolic acid and it could also reach 89.1% even when the immersion time is prolonged to 72 h. The adsorption of CSGC on CRS surface in 0.3 mol/L glycolic acid at 20-50 ℃ obeyed the Langmuir isotherm with the adsorption enthalpy (ΔH⊖) of -23.8 kJ/mol, the adsorption free energy (ΔG⊖) was -28.3 kJ/mol to -28.9 kJ/mol and the adsorption entropy (ΔS⊖) was about 15.4-16.8 J/(mol·K). The adsorption of CSGC on steel surface in glycolic acid was the mixed adsorption of physical and chemical adsorption. Also, it was an exothermic process accompanied with the increase of entropy. CSGC was considered as a mixed-type inhibitor via geometric blocking effect. Nyquist spectra exhibited one large capacitive loop followed by a small inductive loop at low frequencies. The charge transfer resistance significantly increased with the addition of CSGC, while interfacial double layer capacitance decreased.
cassava starch;graft copolymer;inhibitor;steel;glycolic acid
10.3969/j.issn.0253-2417.2017.01.013
2016- 03- 02
国家自然科学基金资助项目(51561027);云南省中青年学术和技术带头人后备人才项目(2015HB049);云南省教育厅科学研究基金重点项目(2013Z080)
李向红(1981— ),男,云南大理人,副教授,博士,主要从事缓蚀剂的研究;E-mail:xianghong-li@163.com。
TQ351
A
0253-2417(2017)01- 0101- 08
李向红,邓书端,李云仙,等.木薯淀粉接枝共聚物对钢在羟基乙酸溶液中的缓蚀性能[J].林产化学与工业,2017,37(1):101-108.

