壳聚糖/纤维素气凝胶球的制备及其甲醛吸附性能
刘志明, 吴 鹏,2
(1.东北林业大学 材料科学与工程学院, 黑龙江 哈尔滨 150040; 2.汉中职业技术学院 药学与医学技术系, 陕西 汉中 723000)
·特邀论文·
壳聚糖/纤维素气凝胶球的制备及其甲醛吸附性能

LIU Zhiming
刘志明1, 吴 鹏1,2
(1.东北林业大学 材料科学与工程学院, 黑龙江 哈尔滨 150040; 2.汉中职业技术学院 药学与医学技术系, 陕西 汉中 723000)
采用液滴悬浮凝胶法分别制备纤维素气凝胶球(CAB)和壳聚糖/纤维素气凝胶球(CCAB),再经酸处理过程分别制得酸处理的CAB(CAB-A)和酸处理的CCAB(CCAB-A),并通过扫描电子显微镜(SEM)、傅里叶变换红外光谱(FT-IR)、X光电子能谱(XPS)和比表面积孔隙测定仪等检测手段对复合气凝胶球的形貌、化学态、表面元素分布以及孔隙结构进行了分析。同时,通过气态甲醛吸附试验对样品的甲醛吸附性能进行测定。结果表明:该法制备的壳聚糖/纤维素复合气凝胶具有均匀的球形形态,CAB、CAB-A、CCAB和CCAB-A的平均粒径分别为(2.67±0.01)、(2.47±0.02)、(2.79±0.05)和(3.34±0.05)mm。壳聚糖引入到纤维素基体中没有发生化学变化,并且通过酸处理使壳聚糖分子在纤维素凝胶网络中进行了重新分布和组装,形成更为密集的气凝胶网状结构,产生了更为丰富的孔隙结构,CCAB-A的比表面积和介孔体积分别为1 350.7 m2/g和4.511 cm3/g。气态甲醛吸附测试结果表明:CCAB-A复合气凝胶球吸附1 h的吸附量高达1.99 mmol/g,远远大于相同用量的椰壳活性炭材料的甲醛吸附量0.39 mmol/g,并且与甲醛分子之间形成了稳定的甲亚胺和席夫碱的化学结合。
纤维素;壳聚糖;气凝胶球;吸附;甲醛
甲醛是一种在室温下无色、具有特殊辛辣和刺激性的气体,也是一种被大家所熟知的室内气体污染物,它主要来自室内家具涂料、地板材料、墙纸以及香烟燃烧所产生的烟雾[1-2]。人们长期处于浓度大于10-7的甲醛环境中会引发一系列室内空气综合症[3],研究表明甲醛对白血病的病发也有着显著的正相关性[4-5]。因此,对于室内甲醛气体的处理关系着人们的健康和生存环境的安全。目前,吸附[6-9]、催化氧化[10-11]以及植物过滤[12]等诸多手段可以用于室内甲醛污染物的处理,从经济学角度考虑,吸附法具有价格低廉和使用便捷等优势,一直是去除甲醛的主要手段,如新装修的房屋内通常会放置多孔活性炭颗粒来吸附甲醛。然而,传统的吸附材料不具备甲醛吸附的特异性,空气内的其它气体小分子也会占据甲醛吸附的活性位点导致吸附去除率较低,而利用多氨基材料与醛类(甲醛或乙醛)分子之间形成甲亚胺和席夫碱的化学结合[13-14],不仅可以使吸附剂对醛类污染物产生特异性吸附,同时也可以在一定程度上保证吸附剂对醛类污染物的吸附稳定性,当甲醛与氨基形成席夫碱,在60 ℃的温度下放置2 h也不会重新释放出甲醛[15]。此外,考虑到人工合成高分子会对环境产生二次污染,因此采用来源丰富、可再生和可生物降解的氨基多糖(壳聚糖)[16]作为甲醛气体吸附的功能组件,应用于甲醛气体的吸附,不仅具备吸附特异性,而且不会产生二次污染,具有广阔的应用前景。本研究以研磨分散的壳聚糖为原料,利用纤维素气凝胶球作为壳聚糖分子的分散附着基体,从而制备出较高氨基吸附表面和孔隙率的壳聚糖/纤维素复合气凝胶球,并对该生物质复合气凝胶材料的结构性能、形成机理及气态甲醛吸附能力进行了分析与表征,旨在开发出一种绿色环保且能高效去除气态甲醛的吸附材料。
1 材料与方法
1.1 材料与仪器
芦苇纸浆(水分4.64%、灰分0.94%、木质素3.81%和硝酸-乙醇纤维素78.65%),工业级,购自黑龙江省牡丹江市恒丰纸业集团有限责任公司;壳聚糖(黏度为55 mPa·s),脱乙酰度大于96%,购自阿拉丁试剂;椰壳活性炭(GAC),购自北京沃特利源环保科技有限公司,比表面积和孔体积分别为590~1 500 m2/g 和0.7~1 cm3/g。甲醛溶液(质量分数10%),分析纯,购自阿拉丁试剂;氢氧化钠、尿素、三氯甲烷、乙酸乙酯、乙酸、叔丁醇、乙醇、浓盐酸(质量分数37%),均为分析纯。
QUANTA 200型扫描电子显微镜(SEM),美国FEI公司;MAGNA-IR 560型傅里叶变换红外光谱仪(FT-IR),美国NICOLET仪器有限公司;THERMO型X光电子能谱(XPS),美国热电有限公司;ASAP 2020型比表面积和孔隙率测定仪,美国MICROMERTICS公司。
1.2 样品制备
1.2.1 纤维素溶液的制备 为降低纸浆原料的聚合度,保证其在碱水体系中完全溶解,参照文献[17]方法制备纤维素溶液。将150 g的芦苇浆加入到4 L的盐酸乙醇溶液(浓HCl和乙醇体积比1 ∶25)中,在70 ℃的条件下不断搅拌反应2 h后过滤洗涤至中性,最后冷冻干燥得到酸解预处理的纤维素纸浆原料。称取10 g预处理的纤维素纸浆原料,加入到一定体积的NaOH/尿素/水(质量比7 ∶12 ∶81)溶液中,在温度-12 ℃下搅拌溶解得到质量浓度为20 g/L的纤维素溶液。
1.2.2 气凝胶样品的制备 参照文献[18],采用液滴悬浮凝胶法将1.2.1节制备的纤维素溶液逐滴加入到由三氯甲烷、乙酸乙酯和乙酸(体积比3 ∶3 ∶1)配制成的酸性再生溶液中,固化5 min后,取出,用蒸馏水置换洗涤2~3次,接着依次用乙醇和叔丁醇溶剂分别置换3次后进行冷冻干燥处理得到球形纤维素气凝胶(CAB)。取200 mL质量浓度20 g/L的纤维素溶液向其中加入4 g壳聚糖,在室温下搅拌混合后倒入JML-50立式胶体磨中研磨10 min,至壳聚糖粒度为2~40 μm,研磨过程中通入-5 ℃的冷却乙醇防止在高温下纤维素凝胶化析出,研磨后得到壳聚糖悬浊液,将该悬浊液真空脱泡10 min后采用制备CAB相似的方法得到壳聚糖/纤维素共混气凝胶球(CCAB)。
考虑到共混的壳聚糖颗粒在强碱性纤维素溶液中不能溶解,不利于壳聚糖分子的分散,因此采用酸处理过程使壳聚糖在纤维素凝胶网络中再次进行溶解-凝胶。取20 g洗涤至中性的壳聚糖/纤维素水凝胶球,置于100 mL质量分数10%的乙酸溶液中浸泡1 h,然后取出放入到无水乙醇中浸泡30 min,最后水洗、溶剂置换和冷冻干燥后得到酸处理的纤维素/壳聚糖气凝胶球(CCAB-A)。纤维素水凝胶也采用该法处理得到酸处理的纤维素气凝胶球作为酸处理过程的对照样品,记为CAB-A。
1.3 结构分析与表征
样品的微观形貌和元素分布,采用SEM和EDX喷金后直接进行观察和测试。样品的化学态采用FT-IR进行测定,扫描范围为650~4000 cm-1。样品的表面元素和价态采用XPS进行分析,其中对C、O和N元素进行高分辨率扫描。样品的孔隙结构采用比表面和孔隙率测定仪进行分析,测定条件为液氮温度(77 K)下N2吸附/脱附,采用Al2O3作为参比物。
1.4 气态甲醛吸附性能分析

图1 甲醛吸附装置图Fig.1 Experimental apparatus for the formaldehyde adsorption test
样品的气态甲醛吸附性能采用如图1所示的自制装置在室温下进行测定,该装置包含一个体积约为5 L的棕色瓶用于装载气态甲醛。在甲醛吸附测试前所有的样品先在温度为100 ℃、真空度为200 Pa的真空烘箱中干燥12 h除去样品中吸附性小分子,然后将10 mg样品用孔径15~20 μm、直径为15 cm的定性滤纸包裹悬挂在棕色瓶的内部。关闭进气阀打开真空泵将气室排空,然后注入8 μL质量分数10%的甲醛溶液使其在低压下气化,并通入氮气调节气室压力等于外界大气压力(即真空表读数为0),样品吸附一定时间后,将4 mL质量浓度为1.5 g/L的2,4-二硝基苯肼(DNPH)乙腈溶液加入到气体采样管中,通入一定体积的氢气将气室内的甲醛气体排入采样管中与DNPH形成DNPH-甲醛加合物,将吸收剂(DNPH乙腈溶液)转移到10 mL容量瓶中用乙腈定容,采用高效液相色谱(HPLC)法对吸收剂中的甲醛加合物浓度进行测量,其中以C18化学键合硅胶为固定相,以乙腈-水(体积比60 ∶40)为流动相,UV检测波长为360 nm,依据测得的加合物与标准甲醛溶液(100 mg/L)-DNPH加合物的HPLC峰面积比求出吸附剂中的甲醛含量[13],从而得出此时气室内的甲醛浓度。根据以上方法分别测出样品在30、60、120、180和300 min下气室内甲醛浓度,并且每个样品测试3次。
2 结果与讨论
2.1 结构分析与表征
2.1.1 宏观形态和微观形貌分析 图2为样品的表观照片,CAB、CCAB及其酸处理样品CAB-A和CCAB-A在水凝胶冷冻干燥过程中的体积收缩较小,因此这些样品都呈现出气凝胶的密度极低的特点,其表观密度分别为0.019 9、0.030 9、0.024 5和0.018 3 g/cm3。同时, 4个样品都具有均匀的球形形态,但是其粒径大小又有较大的差异,CAB、CAB-A、CCAB和CCAB-A的平均粒径分别为(2.67±0.01)、(2.47±0.02)、(2.79±0.05)和(3.34±0.05)mm,可以看出,掺杂壳聚糖的样品其平均粒径大于相应的纤维素气凝胶,即CCAB>CAB,CCAB-A>CAB-A,这是由于纤维素溶液中添加壳聚糖以后单位体积内所包含的固含量增大,在凝胶过程中液滴的收缩阻力也随之增大所致。酸处理对CAB和CCAB样品产生了截然不同的结果,经过酸处理后CAB体积减小而CCAB样品体积变大。样品的微观形貌见图3。

图2 样品的表观图Fig.2 Photographs of samples

图3 样品表面和内部的SEM图Fig.3 SEM images of surface and internal structure
从图3(e)和图3(f)的内部网络结构对比也可以发现,在CAB-A样品的纤维素网络中孔隙较为松散并且出现了片层状聚集。经过酸处理后CAB体积的减小,主要是由于纤维素凝胶在酸性条件下纤维素分子链间的氢键作用增强使纤维素网络紧缩;而经过酸处理后CCAB体积的变大主要是由于CCAB在酸性溶液中浸泡,纤维素网络中包裹的壳聚糖会逐步溶解,但是由于纤维素网络的限制会使壳聚糖分子不能自由运动或者从凝胶中流出,而是在纤维素网络中不断膨胀,从而使CCAB的体积增加。从图3(g)和图3(h)的对比也可以看出酸处理过程对CCAB样品微观结构的影响,CCAB样品的内部网络上出现了较多黏附和包裹的壳聚糖颗粒,而经过酸处理后内部结构中颗粒状的壳聚糖消失,出现了局部较为密集的三维网状,同时在壳聚糖溶解膨胀过程中凝胶表面也出现部分开裂(见图3(c)和图3(d))。从样品的表面形貌图3(a)~图3(d)可以发现,样品表面都存在丰富的可与内部网络相连通的孔洞,这样有利于气体分子的进入和内部网络的吸附。
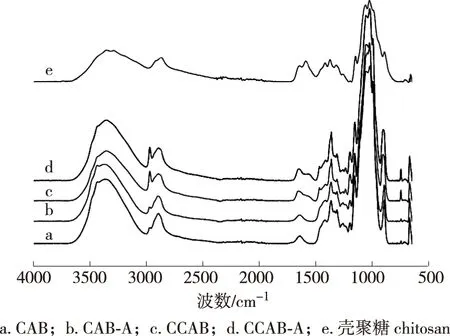
图4 样品的FT-IR谱图Fig.4 FT-IR spectra of the samples

2.1.3 XPS分析 图5为壳聚糖、CCAB和CCAB-A的XPS能谱,同时对酸处理前后纤维素/壳聚糖气凝胶球的表面氮元素含量进行分析,结果见表1。其中Auger是指俄歇效应。

图5 XPS宽带扫描和N1s高分辨能谱Fig.5 XPS spectra and high resolution N 1s spectra of samples


表1 样品的表面元素Table 1 Elemental surface compositions ofsamples %
2.1.4 BET分析 图6(a)和图6(b)分别为样品的N2吸附-脱附等温线和孔径分布图。根据IUPAC的规定[23]这4种气凝胶球的N2吸附-脱附等温线都为Ⅳ型,并且具有H1型滞留环,同时可以发现滞留环形成在较大P/P0的位置,因此可以推测该材料具有丰富的介孔和大孔[24],并且滞留环积分差值的变化与样品的宏观体积变化相似,即CAB>CAB-A、CCAB-A>CCAB。结合表2孔隙结构特征数据进一步说明样品在酸处理前后CAB网络密集化而CCAB网络微细化,因而CAB比表面积从初始的273.7 m2/g降低到238.1 m2/g,CCAB的比表面积从173.0 m2/g提升到1 350.7 m2/g。同时这2个样品在酸处理前后其孔体积也产生相应差异,其中CAB的介孔体积从1.367 cm3/g降低到1.036 cm3/g,而CCAB的介孔体积从0.623 cm3/g增加到4.511 cm3/g。从图6(b)可以发现,CAB的网络收缩过程使部分大孔径转变成较小孔径,而在CCAB内壳聚糖凝胶网络的生成过程中交织形成了许多新的孔,使其孔隙结构更加丰富。因而,从以上孔结构的变化中可以初步说明酸处理有助CCAB网络化,从而更利于壳聚糖分子对气态甲醛分子的捕捉和吸附。

图6 样品的N2吸附-脱附等温线(a)和孔径分布图(b)Fig.6 Nitrogen adsorption-desorption isotherms (a) and pore size distribution (b) of CAB and CCAB

样品samplesBET表面积/(m2·g-1)surfacearea平均孔径/nmaverageporesize微孔体积/(cm3·g-1)microporevolume介孔体积/(cm3·g-1)mesoporevolume总孔体积/(cm3·g-1)porevolumeCAB273.712.640.00581.36749.55CAB-A238.110.490.00561.03640.14CCAB173.013.910.00170.62331.66CCAB-A1350.712.830.04354.51153.90
2.2 形成机理分析


图7 CCAB-A的形成机理Fig.7 Formation mechanism of CCAB-A
2.3 气态甲醛吸附性能分析
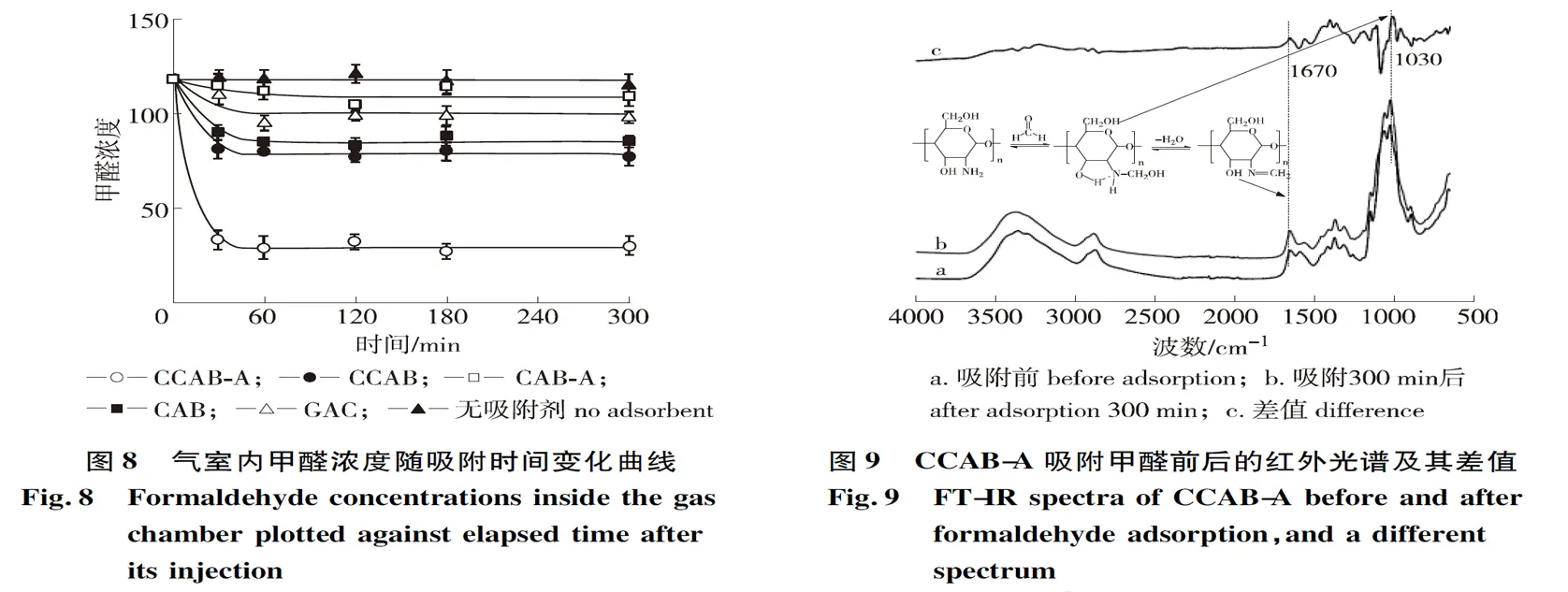
图8为样品的甲醛吸附结果。从图8可以看出,在不放置吸附剂的情况下气室的甲醛浓度为1.18×10-4,并且在吸附测试时间范围内甲醛浓度没有明显变化,表明在吸附测试过程中没有甲醛的泄露和降解。为了表明制备样品对甲醛的吸附能力,采用椰壳活性炭(GAC)作为对比样品,在气室内放入活性炭1 h内,甲醛浓度从1.18×10-4降低到1.00×10-4(为初始值的84.7%),CAB、CAB-A、CCAB和CCAB-A在1 h内使气室内甲醛浓度分别降低到8.5×10-5、1.09×10-4、7.9×10-5和2.9×10-5,依次为初始甲醛浓度的72.0%、92.4%、66.9%和24.6%,根据q=Δc×5/(22.4×m0)可粗略求得甲醛吸附量(q),其中Δc为体系甲醛浓度降低值,m0为吸附剂质量。GAC、CAB、CAB-A、CCAB和CCAB-A的甲醛吸附量分别为0.39、0.74、0.20、0.87和1.99 mmol/g,从甲醛吸附量的变化上也可以看出,CCAB-A有最大的甲醛吸附量为1.99 mmol/g,与活性炭材料相比它是一种高效的气态甲醛吸附材料。通过CCAB-A样品对甲醛吸附前后红外光谱图(见图9)变化,简要分析壳聚糖复合气凝胶对甲醛的化学吸附机理。

3 结 论
3.1 采用液滴悬浮凝胶法和乙酸处理制备壳聚糖/纤维素气凝胶球,并通过SEM、FT-IR、XPS和比表面积孔隙测定等方法对复合气凝胶球的形貌、化学态、表面元素分布以及孔隙结构进行了分析。结果表明:该气凝胶球具有均匀的球形形态,CAB、CAB-A、CCAB和CCAB-A的平均粒径分别为(2.67±0.01)、(2.47±0.02)、(2.79±0.05)和(3.34±0.05)mm。CCAB-A内部纤维素分子和壳聚糖分子通过氢键聚集缠绕在一起,整个过程是物理凝胶过程没有化学交联反应的发生,同时CCAB-A形成了更为密集的气凝胶网状结构,产生了更为丰富的孔隙结构,CCAB-A的比表面积和介孔体积分别为1 350.7 m2/g 和4.511 cm3/g,更有利于对气态甲醛分子的捕捉和吸附。
3.2 气态甲醛吸附测试结果表明:在1.18×10-4的甲醛气氛中,CCAB-A吸附1 h的甲醛吸附量达1.99 mmol/g,去除率为75.4%,远远大于相同用量的椰壳活性炭吸附剂(甲醛吸附量0.39 mmol/g),并且在该壳聚糖气凝胶中甲醛分子与壳聚糖中的伯胺基形成了甲亚胺和席夫碱的化学结合,保证了该吸附作用的稳定性和选择性,因此该材料可以作为一种绿色环保且能高效去除气态甲醛的吸附材料。
[1]AN H B,YU M J,KIM J M,et al.Indoor formaldehyde removal over CMK-3[J].Nanoscale Research Letter,2012,7(1):1-6.
[2]LIANG W J,LI J,LI J X,et al.Formaldehyde removal from gas streams by means of NaNO2dielectric barrier discharge plasma[J]. Journal of Hazardous Materials,2010,175(1/2/3):1090-1095.
[3]CHIN P,YANG L P,OLLIS D F.Formaldehyde removal from air via a rotating adsorbent combined with a photocatalyst reactor:Kinetic modeling[J]. Journal of Catalysis,2006,237(1):29-37.
[4]COGLIANO V J,GROSSE Y,BAAN R A,et al.Meeting report:Summary of IARC monographs on formaldehyde,2-butoxyethanol,and 1-tert-butoxy-2-propanol[J].Environmental Health Perspectives,2005,113(9):1205-1208.
[5]刘世明,刘泽春,郑天可,等.农村室内公共场所甲醛污染及致癌风险评价[J].公共卫生与预防医学,2015,26(1):61-64. LIU S M,LIU Z C,ZHENG T K,et al. Rural indoor formaldehyde pollution in public places and the evaluation on the risk of cancer[J]. Journal of Public Health and Preventive Medicine,2015,26(1):61-64.
[6]LE Y,GUO D P,CHENG B,et al.Bio-template-assisted synthesis of hierarchically hollow SiO2microtubes and their enhanced formaldehyde adsorption performance[J]. Applied Surface Science,2013,274:110-116.
[7]LEE K J,SHIRATORI N,LEE G H,et al.Activated carbon nanofiber produced from electrospun polyacrylonitrile nanofiber as a highly efficient formaldehyde adsorbent[J].Carbon,2010,48(15):4248-4255.
[8]XU Z H,YU J G,LIU G,et al. Microemulsion-assisted synthesis of hierarchical porous Ni(OH)2/SiO2composites toward efficient removal of formaldehyde in air[J]. Dalton Transactions,2013,42(28):10190-10197.
[9]YAMANAKA S,OISO T,KURAHASHI Y,et al.Scalable and template-free production of mesoporous calcium carbonate and its potential to formaldehyde adsorbent[J].Journal of Nanoparticle Research,2014,16(2):1-8.
[10]MA C Y,WANG D H,XUE W J,et al. Investigation of formaldehyde oxidation over Co3O4-CeO2and Au/Co3O4-CeO2catalysts at room temperature:Effective removal and determination of reaction mechanism[J]. Environmental Science and Technology,2011,45(8):3628-3634.
[11]何运兵,纪红兵,王乐夫.室内甲醛催化氧化脱除的研究进展[J].化工进展,2007,26(8):1104-1109. HE Y B,JI H B,WANG L F. Development of the removal of indoor formaldehyde with catalytic oxidation[J]. Chemical Industry Engineering Progress,2007,26(8):1104-1109.
[12]LU N,PEI J J,ZHAO Y X,et al.Performance of a biological degradation method for indoor formaldehyde removal[J].Building and Environment,2012,57:253-258.
[13]EWLAD-AHMED A M,MORRIS M A,PATWARDHAN S V,et al.Removal of formaldehyde from air using functionalized silica supports[J]. Environmental Science and Technology,2012,46(24):13354-13360.
[14]RONG H Q,LIU Z Y,WU Q L,et al.Formaldehyde removal by Rayon-based activated carbon fibers modified byp-aminobenzoic acid[J].Cellulose,2010,17(1):205-214.
[15]PEI J J,ZHANG J S S.On the performance and mechanisms of formaldehyde removal by chemi-sorbents[J]. Chemical Engineering Journal,2011,167(1):59-66.
[16]NGAH W S W,TEONG L C,HANAFIAH M A K M.Adsorption of dyes and heavy metal ions by chitosan composites:A review[J].Carbohydrate polymers,2011,83(4):1446-1456.
[17]TRYGG J,FARDIM P.Enhancement of cellulose dissolution in water-based solvent via ethanol-hydrochloric acid pretreatment[J].Cellulose,2011,18(4):987-994.
[18]刘志明,杨少丽,吴鹏,等.一种球形纤维素气凝胶的制备方法:CN 201310294233.2[P].2014-12-03. LIU Z M,YANG S L,WU P,et al. A kind of preparation method of spherical cellulose aerogel:CN 201310294233.2[P].2014-12-03.
[19]HE G H,WANG Z,ZHENG H,et al.Preparation,characterization and properties of aminoethyl chitin hydrogels[J].Carbohydrate polymers,2012,90(4):1614-1619.
[20]LI M L,XU J,LI R H,et al. Simple preparation of aminothiourea-modified chitosan as corrosion inhibitor and heavy metal ion adsorbent[J]. Journal of Colloid and Interface Science,2014,417:131-136.
[21]LOPEZ-PEREZ P M,MARQUES A P,DA SILVA R M P,et al. Effect of chitosan membrane surface modification via plasma induced polymerization on the adhesion of osteoblast-like cells[J].Journal of Materials Chemistry,2007,17(38):4064-4071.
[22]HSU S H,LIN C H,TSENG C S.Air plasma treated chitosan fibers-stacked scaffolds[J].Biofabrication,2012,4(1):15002-15014.
[23]CHIEN H C,CHENG W Y,WANG Y H,et al.Ultrahigh specific capacitances for supercapacitors achieved by nickel cobaltite/carbon aerogel composites[J].Advanced Functional Materials,2012,22(23):5038-5043.
[24]LI J,LU Y,YANG D J,et al.Lignocellulose aerogel from wood-ionic liquid solution (1-allyl-3-methylimidazolium chloride) under freezing and thawing conditions[J].Biomacromolecules,2011,12(5):1860-1867.
Preparation of Chitosan/Cellulose Aerogel Beads and Its Formaldehyde Gas Adsorption Performance
LIU Zhiming1, WU Peng1,2
(1.Material Science and Engineering College,Northeast Forestry University, Harbin 150040, China; 2.Department of Pharmacy and Medical Technology,Hanzhong Vocational Technical College, Hanzhong 723000, China)
Cellulose aerogel beads(CAB) and chitosan/cellulose aerogel beads(CCAB) were prepared through droplet-suspension gelation processing,and then the acid treated CAB(CAB-A) and acid treated CCAB(CCAB-A) were obtained through acetic acid post-processing from CAB and CCAB. Morphologies,chemical states,element distributions and pore structures of the aerogel beads were characterized and analyzed by SEM,FT-IR,XPS and BET. Meanwhile,formaldehyde adsorption performances of the aerogel beads were measured by gaseous formaldehyde adsorption test. The results showed that the prepared aerogels had uniform spherical shape,and the average particle sizes of CAB, CAB-A,CCAB and CCAB-A were (2.67±0.01), (2.47±0.02), (2.79±0.05) and (3.34±0.05) mm, respectively. Chitosan molecules were introduced into the cellulose matrix and no significant chemical changes occurred during the preparation. In addition,chitosan molecules by acid treatment were renewably distributed and self-assembled in the network of cellulose gel, formed more intensive aerogel network structure,and provided abundant pore structure with the specific surface area and mesoporous volume of CCAB-A of 1 350.7 m2/g and 4.511 cm3/g,respectively. Thus the adsorbing capacity of the composite aerogel beads reached up to 1.99 mmol/g after adsorption for 1 h which was far greater than that by coconut shell activated carbon material with same dosage (0.39 mmol/g). The chemical combination of azomethine and schiff base was formed between primary amine and formaldehyde molecule in the aerogel beads.
cellulose;chitosan;aerogel beads;adsorption;formaldehyde
10.3969/j.issn.0253-2417.2017.01.004
2016- 05-26
林业公益性行业科研专项(201504602-5);黑龙江省自然科学基金项目(C2015055);浙江省林业工程重中之重一级学科开放基金重点项目(2014lygcz002)
刘志明(1971— ),男,黑龙江明水人,教授,博士,博士生导师,主要从事生物质材料化学、纤维素气凝胶和纳米纤维素、木质素及其复合功能材料的研究;E-mail:zhimingliuwhy@126.com。
TQ35
A
0253-2417(2017)01- 0027- 09
刘志明,吴鹏.壳聚糖/纤维素气凝胶球的制备及其甲醛吸附性能[J].林产化学与工业,2017,37(1):27-35.

