Pd/Al2O3-Novozyme 435动态动力学拆分1,1,1-三氟异丙胺
蒋成君,徐国明,袁慎峰
Pd/Al2O3-Novozyme 435动态动力学拆分1,1,1-三氟异丙胺
蒋成君1,2,徐国明3,袁慎峰1
(1浙江大学化学工程与生物工程学院,浙江杭州 310027;2浙江科技学院生物与化学工程学院,浙江杭州 310023;3捷马化工股份有限公司,浙江龙游 324400)
应用响应面优化的方法研究Pd/Al2O3和 Novozyme 435动态动力学拆分1,1,1-三氟异丙胺(TFPA)的协同作用。根据Box-Behnken实验设计原理,对实验进行设计与分析,以转化率和ee值为响应量建立回归模型,分析各因素的显著性与交互作用。结果表明:反应条件对值的影响较小,以转化率为响应量时,Pd/Al2O3和Novozyme 435交互作用显著,两种催化剂有相互抑制作用。最佳工艺条件为:Pd/Al2O3催化剂用量5g/L、反应温度50℃、Novozyme 435的用量10g/L、TFPA的浓度0.5mol/L,预测转化率可以达到98.56%,与实验相符。产物-[(1)-2,2,2-三氟-1-甲基乙基]-乙酰胺的值可达到96.69%。
酶;催化;化学反应;选择性
金属催化剂和酶催化剂在很长时间被认为是两个不同的领域,有机化学家难以发现有效的酶催化剂,生物化学家难以了解金属催化体系。动态动力学拆分反应(DKR)是金属-酶协同的催化反应的一个重要应用[1-3]。光学纯的胺,是一类重要的医药、农药中间体,可以通过DKR获得[4-7]。1996年,REETZ等[8]首次报道了胺的DKR,CALB酶催化拆分与Pd/C催化消旋化协同完成1-苯乙胺的DKR。DKR反应在三乙胺存在下进行,温度50~55℃,使用乙酸乙酯作为酰基供体,发现过程缓慢,8天只得到了60%的转化率。反应效率低的原因是消旋催化剂和拆分催化剂之间缺乏良好的协同[9]。JACOBS等[10-11]研究了作为载体的碱性氧化物如何影响固定化钯粒子的外消旋化活动,研究表明Al2O3作为载体时具有很高的活性和选择性。DKR在70℃和0.01MPa氢气压力下进行,反应可以用乙酸乙酯或者乙酸异丙酯作为酰基供体。ANDRADE 等[12]证实了这些催化剂对含硒的苄基伯胺DKR也适用。催化动力学拆分的酶通常为脂肪酶,Novozyme 435是一种常用的脂肪酶,用于动力学拆分[13]。本文将在此基础上,采用响应面的方法研究Pd/Al2O3与Novozyme435动态动力学拆分1,1,1-三氟异丙胺(TFPA),探讨反应温度、底物浓度、催化剂之间的交互作用。
1 实验部分
1.1 仪器与试剂
1,1,1-三氟异丙胺,分析纯,阿拉丁试剂(上海)有限公司;5% Pd/Al2O3,Evonik Specialty Chemicals(Shanghai)Co.,Ltd,批号PMPC156029;乙酸异丙酯,分析纯,国药集团化学试剂有限公司;环己烷,分析纯,国药集团化学试剂有限公司;Novozyme 435,诺维信(中国)生物技术有限公司;岛津GC2014气相色谱仪,日本岛津公司。
1.2 动态动力学拆分三氟异丙胺
动力学拆分反应在10mL的反应瓶中进行。典型的反应条件为:5mL环己烷,0.5mmol TFPA(0.1mol/L),2mmol乙酸异丙酯(0.4mol/L),30mg Novozyme 435(6g/L),15mg Pd/Al2O3催化剂(3g/L),40℃,200r/min,反应24h。反应式见式(1)。
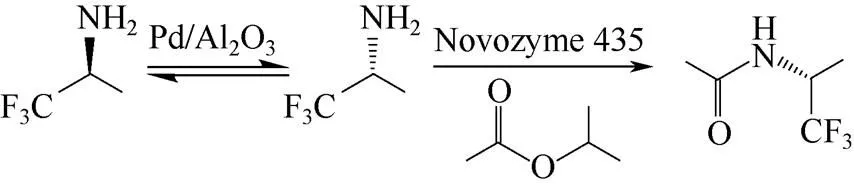
1.3 分析条件
岛津GC2014气相色谱,气相色谱条件:Astec® CHIRALDEX® B-DM 手性柱(30m×0.25mm×0.12μm),进样口温度250℃,检测器温度260℃,柱温50~120℃(5min),5℃/min,载气为氮气。
1.4 实验设计
使用Design-Expert(V8.0.6.1)软件对实验进行研究,根据Box-Behnken原理对实验进行设计与分析。选取Pd/Al2O3催化剂用量、反应温度、Novozyme 435的用量,TFPA的浓度4 个因素,TFPA的转化率和-(2,2,2-三氟-1-甲基乙基)乙酰胺的ee值为响应量进行设计。Box-Behnken因素及实验编码见表1。
2 结果与讨论
2.1 实验设计与结果
根据表1使用Design-Expert软件对实验进行Box-Benhnken响应面设计,在设计条件下进行实验,得到各条件下得底物转化率和产物值见表2。
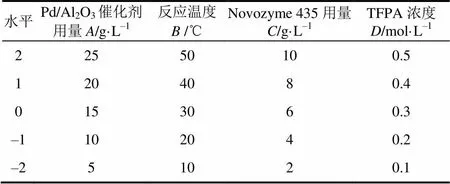
表1 响应面设计因素编码
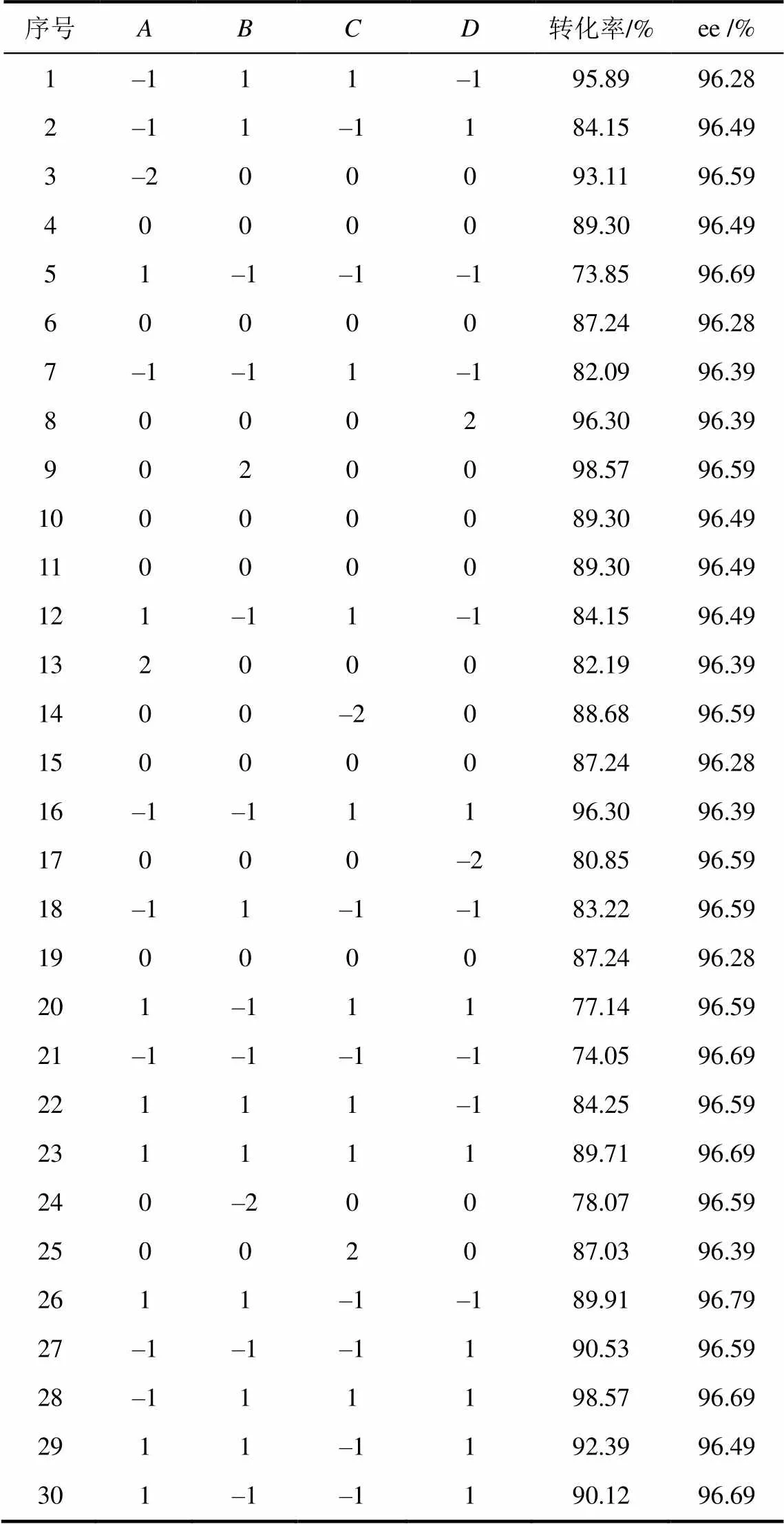
表2 实验的响应面设计与结果
2.2 回归分析
使用Analysis 选项对实验结果进行分析,分别以TFPA的转化率和-(2,2,2-三氟-1-甲基乙基)乙酰胺的值为响应量。从表2数据可以看出,不同的条件对产物的值影响很小,均能大于96%。但对转化率影响较大,重点对转化率进行研究。回归模型用检验判定变量对响应量的影响是否显著,且越小,相应变量对响应量的影响越显著。方差分析见表3所示。如表3所示,根据转化率建立的回归模型为极显著(<0.0001),当“Prob>”值小于0.05时,表示该指标显著,表明回归方程描述各因子与响应值之间的关系时,因变量与所有自变量之间的线性关系显著,即这种实验方案是可靠 的[14];失拟相不显著(>0.5),表明回归模型正确。、、对转化率有显著的影响(<0.05),因素之间存在显著交互作用(<0.05)。
通过计算得到转化率响应值的回归方程(代码方程)如下:
转化率=87.36–1.88+3.79+1.11+3.43+0.76–3.24–1.07+0.48–1.77–1.30
2=0.95说明该模型可靠性较好。
2.3 响应面分析
4种影响因素通过相应面分析共产生6种交互项。图1(a)~(f)分别描述了反应温度与Pd/Al2O3催化剂用量,Novozyme 435的用量与Pd/Al2O3催化剂用量,TFPA的浓度与Pd/Al2O3催化剂用量,Novozyme 435的用量与反应温度,TFPA的浓度与反应温度,TFPA的浓度与Novozyme 435的用量对转化率的交互影响。
从图1(a)可以看出在Pd/Al2O3催化剂用量一定的情况下,温度越高转化率越高,Pd/Al2O3催化剂用量增加转化率反而略有下降,这说明消旋催化剂的增加,不一定加快反应速度,消旋必须与拆分协同作用。图1(b)描述了Novozyme 435的用量与Pd/Al2O3催化剂用量对转化率的交互影响,其交互影响显著。从图1(b)看出,在Pd/Al2O3催化剂用量较低时,增加Novozyme 435的用量,转化率提高,在Novozyme 435的用量较低时,增加Pd/Al2O3催化剂用量,转化率也提高,但是在两者用量都较高时,转化率反而下降,这说明这两种催化剂具有相互的抑制作用。从图1(c)可以看出,Pd/Al2O3催化剂用量一定的情况下,浓度高转化率高。从图1(d)中可以看出,酶的用量一定的情况下,温度高,转化率高。图1(e)表示高温和高浓度都有利于转化率的提高。图1(f)表示Novozyme 435用量一定的情况下,浓度高转化率高。从响应面的分析可以看出,Novozyme 435的用量与Pd/Al2O3催化剂用量之间的交互作用最为显著,在固定一种催化剂的条件下,增加另一个催化剂有助于转化率的提高,同时增加两种催化剂,反而有抑制作用。

表3 转化率的方差分析
2.4 最优反应条件下的DKR
按照Desin-expert软件优化得到的最优条件为Pd/Al2O3催化剂用量5g/L、反应温度50℃、Novozyme435的用量10g/L,TFPA的浓度0.5mol/L,转化率可以达到98.56%。在最优条件下重复3次实验,转化率分别为98.56%、98.55%、98.57%,与软件计算得到的模型计算理论值相符。因此,采用响应面法得到的条件参数较为可靠,具有使用价值。
3 结论
对不同条件下的转化率和值数据进行了Design-Expert软件优化、分析,结果表明反应条件对值的影响较小,均能大于96%。对于底物的转化率,Pd/Al2O3和Novozyme435交互作用显著,两种催化剂有相互抑制作用。最佳工艺条件为:Pd/Al2O3催化剂用量5g/L、反应温度50℃、Novozyme 435的用量10g/L,TFPA的浓度0.5mol/L,响应量预测转化率值为98.56%,与实验相符。最优条件下,产物-[(1R)-2,2,2-三氟-1-甲基乙基]-乙酰胺的ee值可达到96.69%。
[1] wallace s,balskus e p. Opportunities for merging chemical and biological synthesis[J]. Current Opinion in Biotechnology,2014,30:1–8.
[2] Verho O,Bäckvall J E. Chemoenzymatic dynamic kinetic resolution:a powerful tool for the preparation of enantiomerically pure alcohols and amines[J]. Journal of The American Chemical Society,2015,137(12):3996-4009.
[3] Gustafson K P J,Lihammar R,Verho O. Chemoenzymatic dynamic kinetic resolution of primary amines using a recyclable palladium nanoparticle catalyst together with lipases[J].Journal of Organic Chemistry,2014,79(9):3747-3751.
[4] 郭跃平,应向贤,赵冉冉,等.酶法制备手性芳香胺化合物的研究进展[J]. 化工进展,2010,29(4):728-732.
GUO Y P,YING X X,ZHAO R R,et al. Progress in enzymatic production of chiral arylamines[J]. Chemical Industry and Engineering Progress,2010,29 (4):728-732.
[5] Kamal A,Azhar M A,Krishnaji T,et al. Approaches based on enzyme mediated kinetic to dynamic kinetic resolutions:a versatile route for chiral intermediates[J]. Coordination Chemistry Reviews,2008,252:569-592.
[6] Ghanem A,Aboul-Enein H Y. Lipase-mediated chiral resolution of racemates in organic solvents[J]. Tetrahedron Asymmetry,2004,15:3331-3351.
[7] Breuer M,Ditrich K,Habicher T,et al. Industrial methods for the production of optically active intermediates[J]. Angewandte Chemie International Edition,2004,43:788-824.
[8] Reetz M T,Schimossek K. Lipase-catalyzed dynamic kinetic resolution of chiral amines:use of palladium as the racemization catalyst[J]. Chimia,1996,50:668-669.
[9] 蒋成君,吕力琼,黄俊. 金属-酶协同催化动态动力学拆分反应研究进展[J]. 化工进展,2016,35(3):807-814.
JIANG C J,LÜ L Q,H J. Recent progress in dynamic kinetic resolution by metal catalysis cooperate with enzymes[J]. Chemical Industry and Engineering Progress,2016,35(3):807-814.
[10] Parvulescu A,De Vos D,Jacobs P. Efficient dynamic kinetic resolution of secondary amines with Pd on alkaline earth salts and a lipase[J]. Chemical Communications,2005,42:5307-5309.
[11] Parvulescu A N,Jacobs P A,De Vos D E. Palladium catalysts on alkaline earth supports for racemization and dynamic kinetic resolution of benzylic amines [J]. Chemistry:A European Journal,2007,13:2034-2043.
[12] Andrade L H,Silva A V,Pedrozo E C. First dynamic kinetic resolution of selenium-containing chiral amines catalyzed by palladium(Pd/BaSO4)and Candida antartica lipase (CAL-B)[J]. Tetrahedron Letters,2009,50:4331-4334.
[13] 王亮,徐刚,杨立荣. 动力学拆分制备(R)-3,5-双三氟甲基苯乙醇[J]. 化工进展,2013,32(11):2691-2694.
WANG L,XU G,YANG L R. Preparation of (R)-3,5-bis(trifuoromethyl)phenyl ethanol by kinetic resolution[J]. Chemical Industry and Engineering progress,2013,32(11):2691-2694.
[14] 陈玉,徐颖,冯岳阳. 利用响应面法优化皂角苷浸提飞灰中重金属的处理条件[J]. 化工学报,2014,65(2):701-710.
CHEN Y,XU Y,FENG Y Y. Optimizing extraction process of heavy metals in fly ash using saponins by response surface methodology[J]. CIESC Journal,2014,65(2):701-710.
Research on the dynamic kinetic resolution of 1,1,1-trifluoroisopropylamine by Pd/Al2O3and Novozyme 435
JIANG Chengjun1,2,XU Guoming3,YUAN Shenfeng1
(1College of Chemical and Biological Engineering,Zhejiang University,Hangzhou 310027,Zhejiang,China;2School of Biological and Chemical Engineering,Zhejiang University of Science & Technology,Hangzhou 310023,Zhejiang,China;3JingMa Chemicals Co.,Ltd.,Longyou 324400,Zhejiang,China)
Response Surface Methodology (RSM) was successfully applied to study the synergistic effect of Pd/Al2O3and Novozyme 435 on the dynamic kinetic resolution of 1,1,1-trifluoroisopropylamine(TFPA). The variables taken into consideration were reaction temperature,substrate concentration,the Pd/Al2O3amount,and the Novozyme 435 amount. Experiments were designed and analyzed based on Box-Behnken principle. A statistical model was used to evaluate the influence of the variables on the conversion and enantiomeric excess(). It was found that the interaction between the Novozyme 435 and Pd/Al2O3was a significant parameter that affected TFPA conversion. The optimum conditions for RSM were:reaction temperature of 50℃,TFPA concentration of 0.5mol/L,10g/L of Novozyme 435,and 5g/L of Pd/Al2O3. The actual experimental conversion rate under optimum conditions was similarly as the maximum predicted value of 98.56%.The product-[(1)-2,2,2- trifluoro-1- methylethyl]- acetamidewas obtained with enantiomeric excesses of 96.69%.
enzyme;catalysis;chemical reaction;selectivity
TQ463
A
1000–6613(2017)01–0324–05
10.16085/j.issn.1000-6613.2017.01.041
2016-05-20;修改稿日期:2016-09-08。
中国博士后科学基金(2014M551745)及浙江省自然科学基金(LY15B060008)项目。
蒋成君(1981—),男,博士,高级工程师。E-mail:jcj312@163.com。

