“整体分析法”在化学解题中的应用
◇ 江苏 张 梅
“整体分析法”在化学解题中的应用
◇ 江苏 张 梅
整体分析法避开问题局部细节或单个因素的影响,站在整体的高度综合分析问题,使学生纵览全局,能透过“树木”看见“森林”,直接而快速地解决问题.本文对“整体分析法”进行讨论,以期能够帮助学生剥开解题的迷雾,实现思维能力的突破.
1 氧化还原问题中的整体分析
在氧化还原的试题中,常常会涉及一些连续、循环的氧化还原反应,例如A和B反应生成C和D,C和E反应生成B和F.逐一地看,2个反应都有B的参与,其实B发生了先被氧化(还原)又被还原(氧化)的过程,通过B的介入,电子完成了一次循环.那么,在解题过程中,可以将电子的转移当成一个整体进行分析,利用其中的“守恒”来解决问题.
例1将一铜块放入硝酸溶液中,铜块全部溶解后,将收集到NO和NO2混合气体的试管倒扣于水槽中,试管中的液面上升,再通过标准状况下0.84LO2之后,试管中充满了水.试计算,铜块的质量为____g.
分析题中给的数据太少,需要的数据又太多,难免让学生觉得烦琐复杂.但如果将其中的电子转移看作一个整体,则这2个过程中的电子转化如图1所示,不难看出,Ⅰ、Ⅱ中转移的电子数相同,整个过程相当于铜将电子转移给了氧气,即铜失去电子的总数等于氧气得到电子的总数,求得铜的质量为4.8g.
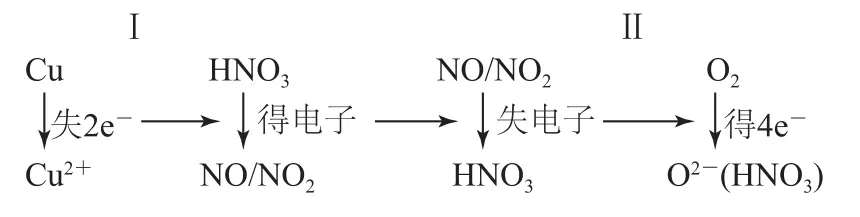
图1
2 元素化合物问题中的整体分析
有关元素化合物反应的问题,一般要根据方程式来确定已知量与未知量之间的关系,有些元素化合物之间要进行一系列的反应,复杂的过程无疑增添了学生的思考负担,整体分析法可以将整个过程当成一个整体,避开过程中的烦琐,快速解决问题.
例2在100mL一定物质的量浓度的盐酸溶液中,投入一定质量的镁、铝合金,合金全部溶解,向所得溶液中逐滴滴入5mol·L-1的NaOH溶液至过量,则加入NaOH溶液的体积与生成沉淀质量之间的关系如图2所示,盐酸溶液的物质的量浓度为多少?
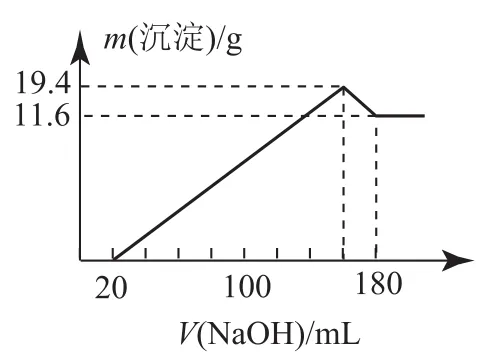
图2
分析按照题中思路,需要将所有的方程式书写出来,找出相互之间的关系,利用二元一次方程组进行求解,这样需要学生对整个实验反应、细节有全面的了解,无疑增加了学生的思考负担.然而进行整体分析,就可以得到Mg(OH)2和Al(OH)3的质量,再根据元素守恒进行求解,方便快捷.根据关系式可求出合金中镁的质量为4.8g,铝的质量为2.7g.再根据题意,加入盐酸后无固体剩余,则当加入180mLNaOH溶液时,根据相互之间的比例关系,可得出盐酸溶液中HCl物质的量为0.8mol,故c(HCl)=8mol·L-1.
3 电化学问题中的整体分析
电化学问题需要从电解的实质、电极反应和电极产物等方面对电解的过程进行分析,需要学生对阴阳极材料、电解质溶液及放电顺序熟练掌握,才能实现对问题的解决.
例3利用惰性电极分别电解下列溶液一段时间,若要使电解后的溶液能够恢复与原溶液相同,则下列选项中,加入一定量的另一物质(方括号中)可以达到此目的是( ).
ACuCl2[CuCl2];BNaOH[NaOH];
CNaCl[HCl];DCuSO4[Cu(OH)2]
分析从整体上看,溶液能恢复到与原来完全相同,不仅要求溶液中溶质的种类相同,还要求浓度也必须与原溶液一致.结合电解原理,电解CuCl2溶液时,实质上电解的是溶质CuCl2,故加入适量的CuCl2就可以使溶液复原;电解NaOH溶液时,实质上电解的是水,故加入适量的水就可以使溶液复原;电解NaCl溶液时,析出的是H2和Cl2,相当于HCl脱离溶液体系,故应通入适量的HCl气体;电解CuSO4溶液,析出的是Cu和O2,相当于CuO脱离溶液体系,故可以加入一定量的CuO.
整体分析法解决问题,优化了解题过程,通过已知量和未知量之间的某种关系直取捷径,不仅极大地提高了解题效率,而且有助于培养学生思维的广阔性、高度性和整体性,形成把握全局的能力.
(作者单位:苏州大学材料化学部,江苏省东台市第一中学)

