富硒酵母中硒赋态的研究
朱 慧, 邵 雷, 陈代杰, 谭 俊
中国医药工业研究总院 上海医药工业研究院 创新药物与制药工艺国家重点实验室,上海 201203
富硒酵母中硒赋态的研究
朱 慧, 邵 雷, 陈代杰, 谭 俊*
中国医药工业研究总院 上海医药工业研究院 创新药物与制药工艺国家重点实验室,上海 201203
硒是人体必需的一种微量元素,参与合成硒代半胱氨酸、硒代甲硫氨酸以及多种硒代蛋白(酶),具有抗肿瘤、抗氧化、增强人体免疫等多种生物学活性,与人体的健康有着密切关系。硒以不同的形式存在于自然界中,大致可分为无机硒和有机硒两种,其生物活性与毒性也各有不同。富硒酵母作为补充硒元素的主要形式之一,具有生物利用度高、食用安全、毒性低等优点。研究富硒酵母中的硒的赋态,对合理摄取硒元素,促进人体健康具有重要意义,因此成为近年来研究的热点。
硒; 富硒酵母; 形态分析; 硒蛋白
1817年,瑞典科学家Berzelius发现了硒。1957年,Schwarz和Foltz发现硒参与了酵母中“因子3”的合成,而其对小鼠肝脏的坏死具有保护作用,并指明“因子3”是一种有机物,而不是硒化合物。由此,在学术界开展了大量有关硒与人体疾病的研究[1]。 1973 年, 世界卫生组织确认, 硒是人类生命和健康不可缺少的一种元素, 合理地摄取硒元素, 可有效预防多种疾病的发生[2]。
在自然界中,硒可以分为无机硒和有机硒两种,并主要以Se(-Ⅱ)、Se(0)、Se(+Ⅳ)和Se(+Ⅵ)四种价态存在,其生物活性与毒性各有不同。研究表明,有机硒的生物活性明显优于无机硒,而毒性则大大低于无机硒。因此有机硒是人体补充硒元素的较好来源。富硒酵母是目前研究、应用最为广泛的一类富硒益生菌,具有无机硒含量低,有机硒含量高的特点。随着分析技术方法的发展与完善,针对富硒酵母中硒的赋态研究更加深入,对我们有效利用硒元素,促进人体健康具有重要的指导意义。
1 硒与富硒酵母

随着生命科学的发展,硒与疾病的关系不断地被揭示,人们发现,硒之所以具有这些广泛的生物学活性,很大程度上是因为硒参与了与人体重要生命活动相关的蛋白(酶)的合成,从而影响了人体的多个主要代谢途径,如甲状腺激素代谢、抗氧化防御系统和免疫功能等。与此同时,科学家还进行了卓有成效的基础研究。特别是到了上世纪的七十至八十年代,硒蛋白不断地被发现,其结构和功能也不断被解析。值得一提的是发现了硒代半胱氨酸(SeCys),即所谓的“第21种标准氨基酸”,特异性掺入蛋白合成的机理——通过特殊的终止密码子(UGA)、tRNASec合成酶,以及一段位于mRNA终止子附近的插入顺序(SECIS)的参与,实现了SeCys的特异性掺入,由此改写了只有20种标准氨基酸才能通过密码子途径进行蛋白合成的“法典”[4]。至九十年代,应用基因工程技术,已经能够在体外对硒蛋白进行改造。经过漫长的、艰难的、长达200年的历程,最终形成了比较完整和系统的硒生物学研究分支[5]。
但硒在体内的安全阈值较窄,过高的硒摄入会导致产生一系列的毒性反应。有研究表明每天的补硒剂量超过400 μg/d~700 μg/d就会对人体产生毒性,超过推荐剂量会产生遗传毒性。但是,对于病人而言:连续12个月每天服用1 600 μg/d的硒也没有发生不良反应;其毒性剂量高达3 200 μg/d。
作为补硒产品,目前应用最为广泛的是在美国1974年上市的富硒酵母。针对动物体内硒的缺乏,美国FDA还批准了亚硒酸盐和硒酸盐作为动物饲料添加剂。目前,尽管补硒产品琳琅满目,但最为流行的还是富硒酵母。这是因为其制造成本低、历史悠久、研究深入,且其中的硒代甲硫氨酸(SeMet)含量较高,是硒蛋白合成的前体。尽管从理论上来计算(所有甲硫氨酸中的S都被Se取代),富硒酵母中的最大硒含量可以达到6 000 mg/kg,但实际上无法实现。目前,在富硒酵母的培养过程中,最高硒含量可以达到3 000 mg/kg,一般为500 mg/kg~2 000 mg/kg。通常,市售富硒酵母中的SeMet含量大于60%,亚硒酸盐和硒酸盐的含量不超过2%,比较好的硒酵母中的无机硒含量不超过1%[6]。
富硒酵母作为最佳的补硒产品,在世界范围内已经应用了40多年。但是,还是有不少学者对其质量和安全性提出了质疑:存在于酵母中的硒代化合物不恒定,以及很多硒代化合物没有得到鉴定,没有达到质量可控的要求。最终导致欧洲议会和欧洲联盟理事会(European Parliament and Council of the European Union)将富硒酵母从食品补充剂指导(directive 2002/46/EC)中剔除[7]。但是,也有不少学者认为,这些问题并非硒酵母本身的问题,而是需要开发更为先进的分析方法,以能够真正回答市售富硒酵母中硒物质是否恒定,以及富硒酵母中究竟有多少硒赋态的形式(不同的含硒物质)。这种定量的“指纹图谱”,不仅能够作为衡量稳定生产和产品质量的“唯一”标准,也可以用来甄别市场上良莠不齐的产品,特别是鉴别那些用硒代甲硒氨酸与常规酵母混合的“冒牌产品”[8]。当然,有关富硒酵母中的哪种“生物标志物”与实际反映出的“效果与安全性”具有直接的关系,以及受体生物体(这里的生物体指的是服用了富硒酵母的生物体)中的哪种“生物标志物”与实际反映出的“效果与安全性”具有直接的关系,这些问题都远没有得到解答。这也可能是这类产品还没有能够作为药物应用于临床的重要原因。
2 富硒酵母中的硒赋态
Se位于元素周期表的VIA,与S相同,都属于氧属元素。Se与S具有很多相似性:相近的电荷性和原子大小,以及具有相同的氧化态。因此,许多硫化物都有其硒类似物,如二硒化物、硒酸盐、亚硒酸盐、甲基硒化物,以及亚硒酸等。Se与S也能够容易地进行相互间的反应,形成Se-S键。但是,在两种元素之间,以及其不同的取代物之间的化学性质区别甚大,如H2Se的pKa为3.73,而 H2S的pKa为6.96;SeCys的pKa为5.2,而Cys的pKa为8.3。在生理pH条件下,SeCys上的Se主要是以阴离子形态存在,而Cys上的S主要主要是被质子化的,因此,SeCys比Cys具有更强的反应性[9]。

2.1 富硒酵母中的代谢产物
在培养基中添加的无机硒(硒酸盐或亚硒酸盐),被酵母利用转化后,可以得到一系列的小分子硒化合物:第一类是硒醇(R1-CH2-Se-H),SeCys就是其中的一种。与硫醇不同的是,它的化学性质更加活泼,会进一步形成Se-Se、S-Se、S-Se-S、或Se-S-Se桥。此外由于SeCys具有α-氨基,可以与其他氨基酸缩合形成肽键,从而产生了多种形式的硒肽,如硒谷胱甘肽就是其中具有代表性的一个。第二类是硒醚(R-Se-R’),它们可以被进一步氧化为硒氧化物(R-Se(O)-R’),如硒代砜(R-Se(O2)-R’),或者可以通过Se与C原子间形成双键(R-C=Se-R’)。这些小分子硒化合物的活泼基团,如氨基和羧基,不仅可与其他的氨基,如甘氨酸和谷氨酸形成寡聚物,还可以进行N-乙酰化或2,3-二羟基丙酰化反应。
针对硒的形态分析,各种分析技术的联用是最主要的分析手段。其中以高效液相串联电感耦合等离子体质谱(HPLC-ICP-MS)以及高效液相偶联二级串联质谱(HPLC-MS-MS)应用较为广泛。其共同点是以高效液相色谱作为分离工具,以高灵敏度的质谱作为检测器,从而实现了对各种不同硒赋态物质的定性与定量检测。特别是ICP-MS,作为近年来发展迅速的痕量元素分析方法,以其灵敏度高(检测限可达到ng/L以下级别),重复性好,分析过程简便快捷等特点,越来越多地应用于元素分析及其形态分析等领域。此外,根据分析对象的不同,所使用的分离色谱条件也各不相同。如分析极性相对较强的硒代谢产物,一般使用离子交换色谱(Ion exchange chromatography)或离子对色谱(Ion pair chromatography),而分析极性较弱的硒蛋白时,一般选择常规的反向色谱(Reversephase Chromatograph)来作为分离手段。
蒲云霞等[13]采用反相离子对色谱和电感耦合等离子质谱联用的方法对富硒酵母中的水溶性的小分子硒化物进行了分析,共检测到Se (IV)、Se (VI)、SeCys、SeMet等七种小分子硒化物。Szpunar等[14],首次采用尺寸排阻阳离子交换液相色谱法测定质谱和电喷雾离子阱检测法(size-exclusion—cation-exchange HPLC with the parallel ICP-MS and electrospray orbital ion trap detection),对来自美国肯塔基、中国、巴西、加拿大,以及法国的富硒酵母的水溶性浸提部分进行研究,结果鉴定了21种硒代谢产物。Lobinski等[15],利用互补反相/亲水离子相互作用(HILIC)液相色谱和喷雾混合四极阱/Orbitrap质量光谱法,测定了经超声粉碎和水浸提的富硒酵母中的硒代谢产物。结果发现:水浸提部分的硒含量占总硒的14.7%;鉴定了64个硒代谢产物(有43个为新鉴定的),其中硒醚类化合物14个、含有SeCys的二肽和三肽化合物28个、偶尔也发现有硒醇和硒氧化物。
2.2 富硒酵母中的含硒蛋白
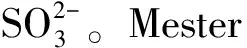
随着蛋白组学技术的发展,研究在富硒环境下生物体内形成的含硒蛋白具有重要的意义:可以作为制定富硒产品质量标准的“指纹图谱”,以此来确认产品制备过程的稳定性,以及甄别市场上的“假冒伪劣”产品;二是可以为深入研究富硒产品的活性物质(生物标志物)打下基础,寻找出真正发挥生理活性的物质。
Szpunar等[18],首次利用MALDI TOF-MS和ESI-MS/MS技术,从富硒酵母的水溶性蛋白中发现了两个富硒蛋白——SIP18 和 HSP12。随后,他们又发现了YMZ 7含硒蛋白。但是,在Mester等[19]对富硒酵母的蛋白组学研究时发现:在其鉴定的14个含硒蛋白中,却没有发现SIP18 和 HSP12蛋白。说明不同的富硒酵母其蛋白组特性是不尽相同的。Lobinski等[20]利用ICP-MS 技术,在富硒酵母中鉴定了17个含硒蛋白,其中12个含硒蛋白是新发现的。Lobinski等[21]对商品名为Sel-Plex®的富硒酵母进行了蛋白组学的研究,尽管在酵母的基因组中缺少用于SeCys掺入到蛋白中去的密码子UGA,但结果发现有大量的硒蛋白合成。进一步用胰蛋白酶处理19种含硒的蛋白,分别测定其中SeMet/Met和SeCys/Cys的比例。结果发现:平均各含硒蛋白中甲硫氨酸的S被Se取代的比例为42.9±35.0%,Cys的S被Se取代的比例为14.1±4.8%。经过物料平衡计算:在整个所研究的酵母蛋白中,Cys/Met的平均比例为2∶1,SeCys占总硒的10%~15%。
Somiari等[22],从另外一个角度研究了富硒酿酒酵母的蛋白组,旨在揭示富硒环境下培养的酵母蛋白的变化情况。他们利用二维凝胶电泳(DIGE)串联质谱(MS/MS)的方法,对美国FDA批准上市的、商品名SelenoExcell®的酿酒酵母进行了研究。该酵母中的总硒含量为1 200 μg/g,所有的含硒物质都为有机硒,其中SeMet的含量为70%。经研究鉴定了在二维电泳上展现的96个蛋白中的37个蛋白,这些蛋白的功能涉及到代谢过程、糖酵解、ATP、金属、核苷和核苷酸结合、蛋白的折叠/松弛,以及压力和信号传导等。有趣的是,其中的11个蛋白与前列腺,乳腺癌、结肠癌、肺癌等许多的癌变有关。进一步分析其中的5个蛋白,发现丙酮酸激酶、热休克蛋白70(HSP70)、延长因子2的表达显著地提高,而真核生物转译因子5A-2和磷酸丙糖异构酶的表达显著的降低。这一研究提示,富硒酵母能够抗癌的原因可能与这些蛋白有关。
2.3 其他富硒益生菌中的硒的赋态研究
作为益生菌,乳杆菌和双歧杆菌不仅被广泛地用为常规的食品和保健(功能)食品,且被作为治疗药物用于临床。如嗜酸乳杆菌是应用历史悠久的一种益生菌,在欧美国家非常常见,它具有抗肿瘤、抗衰老、增强免疫力、降低胆固醇等功能[23]。但这样的富硒益生菌还鲜有报道。
Pessione等[24]对罗伊氏乳杆菌(Lactobacillusreuteri)的蛋白组学进行研究,鉴定了25种含硒蛋白,可以分为5个功能类别:Se代谢、能量代谢、压力/粘附、细胞形状和运输,以及其他功能。Amoresano等[25]的研究发现,在富硒培养基上生长的罗伊氏乳杆菌,有一半的含硒蛋白存在于水提取物中,且与富硒酵母不同,这些含硒蛋白中富含的是SeCys而不是SeMet。

3 展望
目前,绝大多数有关富硒酵母中的硒赋态研究,都集中在上述的小分子有机硒代谢产物以及含硒蛋白(酶)上。只有少量的文献报道了在其他生物中存在的一些大分子硒化合物,如含硒多糖、含硒磷脂和含硒核酸等。这是因为,一方面这些大分子硒化合物在酵母中的含量甚低,另一方面,这些大分子物质是否具有生物活性尚未可知。
富硒酵母作为人体的补硒剂已经被广泛应用。尽管大量的研究表明其对人体的多种疾病具有显著的治疗作用,但还没有成为治疗药物用于临床。其主要的原因可能是以下这几个问题还未得到解答:一是富硒酵母的疗效是如何发挥的?也即富硒酵母中的哪些“生物标志物”,是直接引起产生治疗作用的;二是富硒酵母是如何引起机体产生毒性的?也即引起机体产生各种毒性的“生物标志物”是什么?三是作为药物,如何进行ADME(吸收、分布、代谢、排泄)的研究?另外,根据已有的文献报道,硒的治疗剂量与毒性剂量差异较小(治疗窗窄),这可能也是一个重要的因素。
作为补硒产品,富硒酵母的应用已有40多年的历史,各种富硒产品相继被开发,并得到广泛的认可。作为补硒产品,各个国家都有严格的规定,而在这样的规定剂量下不太可能产生显著的、对某一疾病的治疗作用。因此,想要把富硒酵母,或其他富硒产品,包括富硒益生菌开发成为用于治疗某一疾病的临床药物,必须对上述提出的三个科学问题予以解答。这样的产品,与现在的“复方中药”产品有许多相似之处,但要其成为药物,可能更具有挑战性。
[1] Birringer M, Pilawab S, Flohé L. Trends in selenium biochemistry.Nat Prod Rep, 2002,19(6):693-718.
[2] 贾洪锋, 贺稚非, 刘丽娜. 富硒酵母的研究进展. 四川食品与发酵, 2005,41(3):8-12.
[3] Ge K, Xue A, Bai J, Wang S. Keshan disease-an endemic cardiomyopathy in China. Virchows Archiv, 1983,401(1):1-15.
[4] Allmang C, Krol A. Selenoprotein synthesis: UGA does not end the story. Biochimie, 2006,88(11):1561-1571.
[5] Flohe L. The labour pains of biochemical selenology: the history of selenoprotein biosynthesis. Biochimica et Biophysica Acta-General Subjects, 2009,1790(11):1389-1403.
[6] Schrauzer GN. Selenium yeast: Composition, quality, analysis, and safety. Pure and Applied Chemistry, 2006,78(1):105-109.
[7] European Parliament and Council of the European Union. DIRECTIVE 2002/46/EC, 2002.
[8] Bierla K, Szpunar J, Yiannikouris A,etal. Comprehensive speciation of selenium in selenium-rich yeast. TrAC Trends in Analytical Chemistry, 2012,41:122-132.
[9] Johansson L, Gafvelin G, Arner ESJ. Selenocysteine in proteins-properties and biotechnological use. Biochimica et Biophysica Acta-General Subjects, 2005,1726(1):1-13.
[10] Kieliszek M, Blazejak S, Placzek M. Spectrophotometric evaluation of selenium binding bySaccharomycescerevisiaeATCC MYA-2200 andCandidautilisATCC 9950 yeast. Journal of Trace Elements in Medicine and Biology, 2016, 35:90-96.
[11] Tarze A, Dauplais M, Grigoras I,etal. Extracellular production of hydrogen selenide accounts for thiol-assisted toxicity of selenite againstSaccharomycescerevisiae. The Journal of Biological Chemistry, 2007,282(12):8759-8767.
[12] Debieux CM, Dridge EJ,Mueller CM,etal. A bacterial process for selenium nanosphere assembly. PNAS, 2011,108(33):13480-13485.
[13] 蒲云霞. 富硒酵母中硒的种态分析.硕士学位论文.内蒙古科技大学包头医学院,2008.
[14] Casal SG, Far J,Bierla K,etal. Study of the Se-containing metabolomes in Se-rich yeast by size-exclusion-cation-exchange HPLC with the parallel ICP MS and electrospray orbital ion trap detection. Metallomics, 2010,2(8):535-548.
[15] Arnaudguilhem C, Bierla K, Ouerdane L,etal. Selenium metabolomics in yeast using complementary reversed-phase/hydrophilic ion interaction (HILIC) liquid chromatography-electrospray hybrid quadrupole trap/Orbitrap mass spectrometry. Analytica Chimica Acta, 2012,757:26-38.
[16] Díaz Huerta V, Hinojosa Reyes L, Marchant-Gayon JM,etal. Total determination and quantitative speciation analysis of selenium in yeast and wheat flour by isotope dilution analysis ICP-MS. J Anal At Spectrom, 2003,18(10):1243-1247.
[17] Dumont E, De Cremer K, Van Hulle M,etal. Identification of the major selenium compound, Se-Methionine, in three yeast (Saccharomycescerevisiae) dietary supplements by on-line narrowbore liquid chromatography-electrospray tandem mass spectrometry. Journal of Chromatography A, 2005,1071(1-2):191-196.
[18] Giusti P, Schaumlöffel D, Preud’homme H,etal. Selenopeptide mapping in a selenium-yeast protein digest by parallel nanoHPLC-ICP-MS and nanoHPLC-electrospray-MS/MS after on-line preconcentration. J Anal At Spectrom, 2006,21(1):26-32.
[19] McSheehy S, Kelly J,Tessier L,etal. Identification of selenomethionine in selenized yeast using two-dimensional liquid chromatography-mass spectrometry based proteomic analysis. The Analyst, 2005,130(1):35-37.
[20] Tastet L, Schaumlöffel D, Lobinski R. ICP-MS-assisted proteomics approach to the identification of selenium-containing proteins in selenium-rich yeast. J Anal At Spectrom, 2008,23(3):309-317.
[21] Bierla K, Bianga J, Ouerdane L,etal. A comparative study of the Se/S substitution in methionine and cysteine in Se-enriched yeast using an inductively coupled plasma mass spectrometry (ICP MS)-assisted proteomics approach. Journal of Proteomics, 2013,87:26-39.
[22] El-Bayoumy K, Das A, Russell S,etal. The effect of selenium enrichment on baker's yeast proteome. Journal of Proteomics, 2012,75(3):1018-1030.
[23] 胡学智. 国外微生态制剂的研究与市场概况.工业微生物, 2002,32(3):56-61.
[24] Lamberti C, Mangiapane E, Pessione A,etal. Proteomic characterization of a selenium-metabolizing probioticLactobacillusreuteriLb2 BM for nutraceutical applications. Proteomics, 2011,11(11):2212-2221.
[25] Galano E, Mangiapane E, Bianga J,etal. Privileged Incorporation of Selenium as Selenocysteine inLactobacillusreuteriProteins Demonstrated by Selenium-specific Imaging and Proteomics. Molecular & Cellular Proteomics, 2013,12(8):2196-2204.
[26] 靳志强. 富硒双歧杆菌中硒的赋存形态及分布. 食品与发酵工业, 2010,36(1):25-28.
[27] 梁佳, 李玉锋,赵金璇等. 富硒双歧杆菌中硒的含量与形态研究.食品科学, 2010,31(5):121-124.
Speciation study of selenium in selenium-enriched yeast
ZHU Hui, SHAO Lei, CHEN Dai-jie, TAN Jun
State Key Laboratory of New Drug and Pharmaceutical Process, Shanghai Institute of Pharmaceutical Industry, China State Institute of Pharmaceutical Industry, Shanghai 201203, China
Selenium is an essential trace element in human body, which participates in the synthesis of selenomethionine, selenocysteine and a variety of selenoprotein (enzyme). Selenium has many biological activities, such as anti-cancer, antioxidant and enhancing the immunity of human body. Selenium exists in different forms, which can be roughly characterized as inorganic selenium and organic selenium. The toxicity and activity of these two forms of selenium are very different. Selenium-enriched yeast is one of the major form of selenium supplement, which has high bioavailability, edible safety and low toxicity. The speciation study of selenium in selenium-enriched yeast will lead to a more reasonable use of selenium and therefore has become a research hotspot in recent years.
selenium; selenium-enriched yeast; speciation analysis; selenium-containing proteins
10.3969/j.issn.1001-6678.2016.06.010
国家“重大新药创制”科技重大专项(No:2013ZX09301302,No.2014ZX09507009-025)国家自然科学基金(No.81573329)国家青年科学基金(No.81603004)。
朱 慧(1993~),女,在读硕士研究生。电话:021-20572000-2049,E-mail:jolie_zh@163.com。
*通信作者:谭 俊,女,助理研究员。E-mail:baiyuge1113@163.com。

