不同剂量的右美托咪定术前经鼻雾化给药对小儿喉罩置入时七氟醚EC50的影响
徐 瑾,邓晓明,魏灵欣,杨 冬,刘具会,郅 娟,李亚男
中国医学科学院 北京协和医学院 整形外科医院麻醉科,北京 100144
·论 著·
不同剂量的右美托咪定术前经鼻雾化给药对小儿喉罩置入时七氟醚EC50的影响
徐 瑾,邓晓明,魏灵欣,杨 冬,刘具会,郅 娟,李亚男
中国医学科学院 北京协和医学院 整形外科医院麻醉科,北京 100144
目的 观察术前经鼻雾化给予不同剂量的右美托咪定对小儿喉罩置入时七氟醚EC50的影响。方法 将41例年龄3~6岁,美国麻醉医师协会Ⅰ级,择期全麻下行整形手术的患儿按照随机数字表法随机分为2组:右美托咪定1 μg/kg组(D1组,n=21)、右美托咪定2 μg/kg组(D2组,n=20)。进入手术室前30 min所有患儿经鼻雾化喷入观察药物。进入手术室后所有患儿经面罩行七氟醚吸入诱导,七氟醚浓度为8%,氧气流量为6 L/min。患儿瞳孔固定中位后七氟醚浓度降为5%,氧气流量为3 L/min。静脉置管成功后根据Dixon’s 序贯法调整患儿喉罩置入时呼气末七氟醚浓度,维持10 min后置入喉罩,序贯法实施的初始浓度为2%,相邻浓度比值为1∶1.2,根据上一例患儿喉罩置入的情况调整下一例患儿呼气末七氟醚浓度。观察患儿入室时的脑电双频指数、对吸入诱导时面罩的接受程度、置入喉罩时的反应情况,记录喉罩置入时呼气末七氟醚气体浓度。结果 患儿入手术室时的脑电双频指数值D2组为77.4±3.6,显著低于D1组的87.4±1.9(P<0.05);患儿对面罩的接受程度D1组为76.2%,D2组为90.0%,两组差异无统计学意义;喉罩置入时七氟醚EC50D1组为1.59% (95%CI=1.41%~1.78%),D2组为1.09%(95%CI=0.89%~1.28%),D2组显著低于D1组(P<0.05)。结论 较右美托咪定1 μg/kg相比,麻醉前30 min经鼻雾化喷入右美托咪定2 μg/kg,可显著降低喉罩置入时七氟醚的EC50。
右美托咪定;经鼻雾化给药;小儿;七氟醚EC50
ActaAcadMedSin,2016,38(6):627-631
七氟醚气味芳香,血/气分配系数低,临床应用起效迅速、恢复快、刺激性小,是目前小儿麻醉诱导和麻醉维持的最常用吸入麻醉药,也是小儿喉罩置入的主要麻醉方式[1]。由于小儿七氟醚吸入麻醉诱导时,常发生躲闪拒绝面罩,有时还出现呛咳、咬管、喉痉挛等各种呼吸道并发症,增加了小儿吸入诱导的难度和风险[2- 3]。而术前使用一定剂量的镇静镇痛药物,可以减少小儿的紧张和焦虑,使吸入诱导更加平稳顺畅,并降低喉罩置入的麻醉深度[4]。右美托咪定(dexmedetomidine,DEX)是一种高选择性α2-肾上腺素能受体激动剂,具有镇静、抗焦虑、抗交感、减弱应激和镇痛等多重作用,术前使用可增强麻醉药作用,使吸入诱导更平稳[5]。与肌肉注射和口服用药相比,经鼻给药操作简单方便、无创伤、无刺激,是小儿术前用药的理想方式[6]。本研究观察不同剂量DEX术前经鼻雾化给药对七氟醚吸入诱导及小儿喉罩置入时七氟醚EC50的影响。
对象和方法
对象及分组 选取2015年11月至2016年4月在整形外科医院择期全麻下行整形外科手术的患儿41例,其中男29例、女12例,年龄3~6岁,体重10~30 kg,均为美国麻醉医师协会分级Ⅰ级,手术时间1~2 h。所有患儿按照随机数字表法随机分为两组:D1组(n=21):右美托咪定(批号:H20090248,江苏恒瑞药业股份有限公司)1 μg/kg,D2组(n=20):右美托咪定2 μg/kg。排除标准:患儿体重超重、气道异常、上呼吸道感染、支气管哮喘、对右美托咪定过敏或高反应、心律失常、先天性心脏病、精神异常、自闭症或其他心理发育障碍病史。本研究经本院医学伦理委员会批准,所有患儿的监护人均签署知情同意书。
麻醉前准备 与家长签署知情同意书,所有患儿均禁食8 h,禁饮4 h,取斜卧位,由家属陪同。按照双盲法,在患者术前接诊室由1名医生用经鼻雾化给药装置(LMA MAD Nasal,美国)予患儿喷入观察药物。根据患儿体重及分组计算所需药物浓度,并采用生理盐水稀释右美托咪定原液。采用1 ml注射器抽取稀释后的药液,总量为0.6 ml,连接经鼻雾化给药装置,双侧鼻孔等量喷入全部观察药物。另1名医生监测患儿血氧饱和度(oxygen saturation,SpO2)及心率(heart rate,HR),给药30 min后患儿转入手术室。入室后常规监测血压、HR、SpO2(型号:S/5 AM,GE Healthcare Finland Oy,芬兰)及脑电双频指数(bispectral index,BIS) (VISTA,美国),吸入诱导采用同型号麻醉机(型号:Primus IE,Draeger Medical GMbH,德国)。回路气体提前由8%七氟醚(挥发罐)及氧气排空,新鲜气体流量为6 L/min。
麻醉诱导 用面罩紧扣于患儿口鼻进行“肺活量法”麻醉诱导,记录患儿对面罩的接受程度,按4分法分级[7](1分:抵抗、哭闹;2分:对面罩有些害怕,不容易平静;3分:安慰后予以配合;4分:平静、配合)。评分为1分或2分表示患儿对面罩诱导不接受,评分为3分或4分表示患儿接受面罩诱导。于面罩处采集七氟醚呼出气体浓度(endtidal sevoflurane, ETsevo)及呼气末CO2浓度。患儿瞳孔固定于中位后新鲜气体流量降至3 L/min,挥发罐七氟醚浓度降至5%。保持患儿自主呼吸至足背静脉穿刺置管(24GA 0.75IN,BD Insyte,美国)完成,必要时行辅助通气维持呼气末CO2于35~45 mmHg(1 mmHg=0.133 kPa)。静脉置管成功后根据Dixon’s 序贯法调整ETsevo,维持10 min后置入一次性单管喉罩(Ambu AuraOnce,美国),序贯法实施的初始浓度为2%,相邻浓度间隔比值为1.2,下一例患儿ETsevo的设定根据上一例患儿喉罩置入的情况进行调整,如患儿喉罩置入顺利且1 min内无体动、咳嗽、窒息、吞咽、喉痉挛等情况,视为喉罩置入成功,下一例患儿ETsevo下降一个浓度梯度;如患者难以置入喉罩或喉罩置入1 min内有体动、咳嗽、窒息、吞咽、喉痉挛等情况,视为喉罩置入失败,下一例患儿ETsevo将升高一个浓度梯度。如患儿喉罩置入失败,加深七氟醚吸入浓度并静脉给予丙泊酚2 mg/kg。喉罩置入成功并通气正常后常规固定喉罩,根据BIS调整吸入麻醉深度,复合60% N2O,维持呼气末二氧化碳分压在35~45 mmHg,必要时行辅助通气。手术开始前给予芬太尼2 μg/kg,手术结束停止吸入麻醉。观察期间,患儿发生心动过缓(HR<60 次/min)时,采用阿托品矫正,发生低氧血症(SpO2<90 次/min)时采用面罩吸氧矫正。
观察指标 观察患儿入手术室时的HR、SpO2、BIS值及对面罩的接受程度,记录喉罩置入时HR、平均动脉压、BIS、呼气末七氟醚气体浓度及患儿的体动反应。
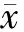
结 果
一般资料 共72例患儿排除31例,其中13例为唇腭裂患儿、8例上呼吸道感染、5例拒绝经鼻给药、5例超重,其余41例完成实验观察。两组患儿的一般资料差异无统计学意义(P>0.05)(表1)。
循环监测及BIS值 两组患儿经鼻给药至麻醉诱导均未发生需治疗的心动过缓及呼吸抑制。两组患儿入手术室时的HR、SpO2差异均无统计学意义,但D2组患儿入手术室时的BIS值为77.4±3.6,显著低于D1组的87.4±1.9(P<0.05);喉罩置入时的HR、平均动脉压及BIS值,两组差异无统计学意义(表2)。
面罩接受程度 患儿对面罩的接受程度D1组为76.2%,D2组为90.0%,两组差异无统计学意义(表3)。

表 1 两组患儿一般资料
D1组:右美托咪定1 μg/kg组;D2组:右美托咪定2 μg/kg组
Group D1: dexmedetomidine 1 μg/kg; Group D2: dexmedetomidine 2 μg/kg

表 2 两组患儿入室时HR、SpO2、BIS及喉罩置入时HR、MAP、BIS的比较 (x-±SD)
1 mmHg=0.133 kPa;HR:心率;SpO2:血氧饱和度;BIS:脑电双频指数;MAP:平均动脉压;与D1组比较,aP<0.05
HR:heart rate;SpO2:oxygen saturation;BIS:bispectral index;MAP:mean arterial pressure;aP<0.05 compared with group D1
喉罩置入结果 Dixon’s序贯法采集的各组患儿喉罩置入时ETsevo,D1组21例患儿,七氟醚诱导成功完成小儿喉罩置入11例、失败10例;D2组20例患儿,七氟醚诱导成功完成小儿喉罩置入11例、失败9例(图1)。D1组七氟醚完成小儿喉罩置入的EC50为1.59% (95%CI=1.41%~1.78%),EC95为2.02% (95%CI=1.82%~2.56%),D2组七氟醚成功完成小儿喉罩置入的EC50为1.09%(95%CI=0.89%~1.28%),EC95为1.52%(95%CI=1.32%~2.04%),D2组显著低于D1组(P<0.05)(图2)。
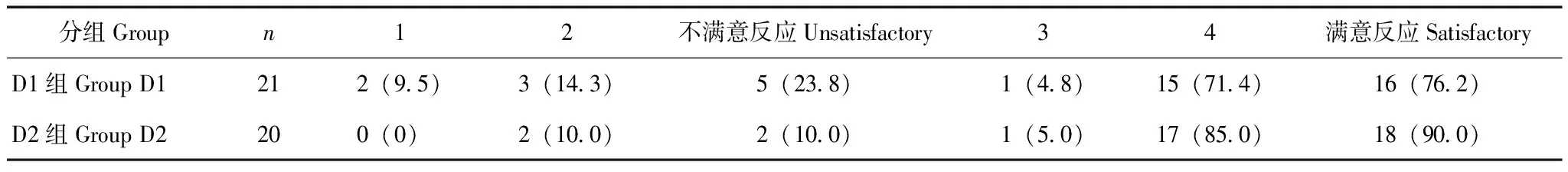
表 3 两组患儿面罩诱导质量[n(%)]
患儿对面罩的接受程度采用4分法:1=抵抗、哭闹;2=对面罩有些害怕,不容易平静;3=安慰后予以配合;4=平静、配合
The child’s compliance with the mask was evaluated using a different 4-point scale: 1=combative and angry; 2=fear of the mask and not easily calmed; 3=fear of the mask but easily calmed; 4=calm and cooperative
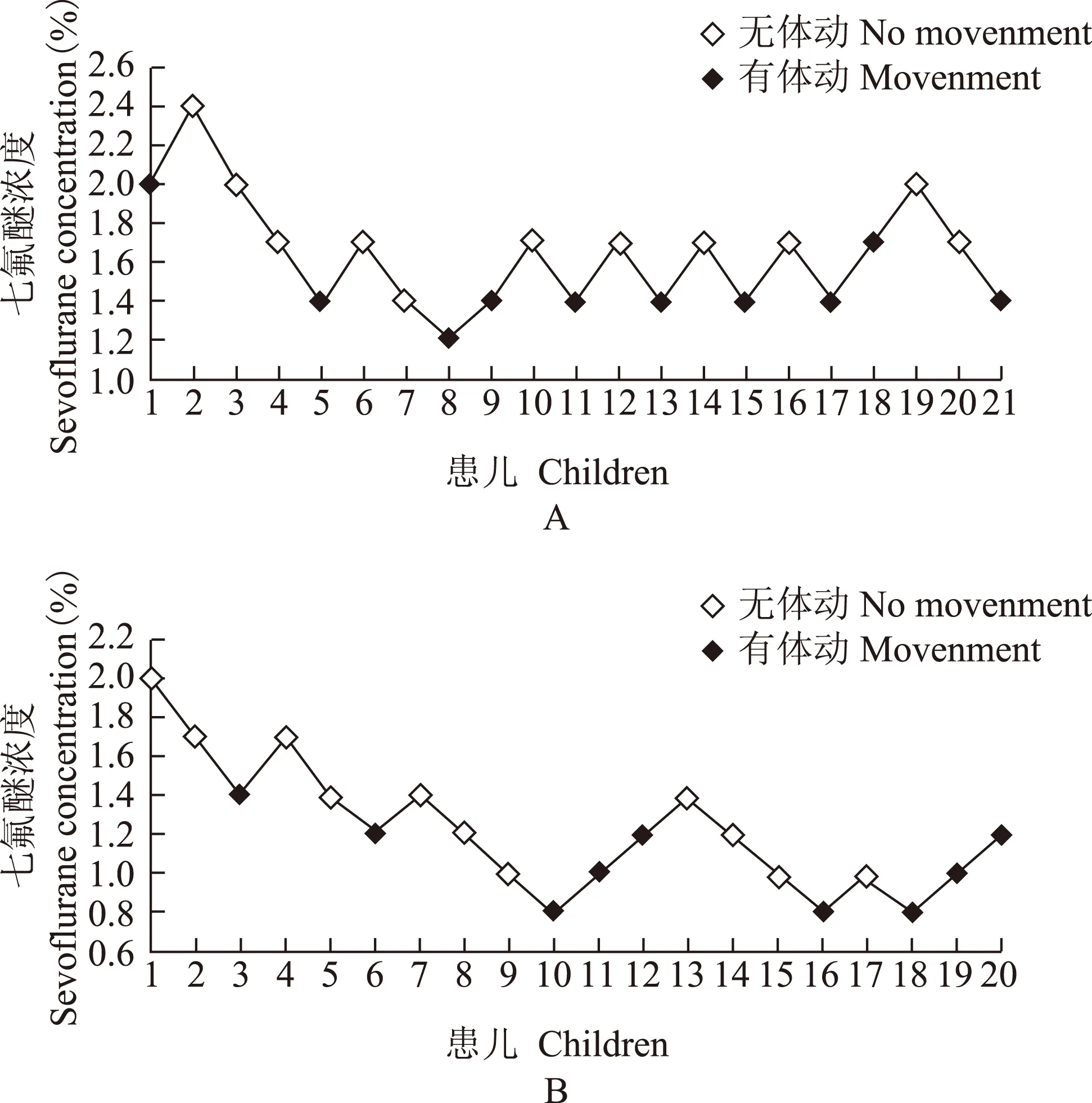
A.D1组;B.D2组
A. group D1;B. group D2
图 1 两组患儿喉罩置入时呼气末七氟醚气体浓度
Fig 1 End-tidal sevoflurane concentrations at laryngeal mask airway insertion
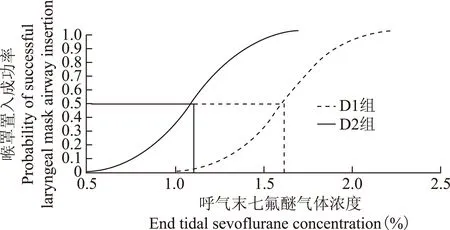
图 2 两组患儿喉罩置入时七氟醚浓度反应曲线
Fig 2 Concentration-response curves of sevoflurane of laryngeal mask airway insertion
讨 论
经鼻给药是一种有效且无创的用药方式。呼吸区鼻黏膜下有丰富的毛细血管,可将药物迅速经鼻黏膜转运至血液循环;嗅觉区分布有嗅神经,药物可经此途径进入脑脊液,进而直接作用于中枢神经系统[8]。DEX作为高选择性α2-肾上腺素能受体激动剂,可经鼻黏膜快速吸收,这种给药方式生物利用度高,能避免口服给药时肝脏的首关消除作用,达到静脉给药的治疗阈值[9- 10],可用于小儿术前,缓解患儿焦虑、恐惧心理。
Yuen等[11]对1~12岁的100例患儿滴鼻给予DEX 1 μg/kg,发现DEX镇静的起始时间为25 min,持续时间为85 min。而Yuen等[12]的另一项研究证实,小儿经鼻给予DEX 1 μg/kg及DEX 2 μg/kg,镇静作用分别在30 min和25 min后出现。因此,本研究选择在患儿入室前30 min经鼻雾化给药。研究显示,术前经鼻雾化使用右美托咪定1 μg/kg及2 μg/kg,患儿入室时的BIS值D2组显著低于D1组,表明DEX 2 μg/kg术前经鼻雾化使用能够为患儿入室及面罩诱导提供较好的镇静深度,同时并不降低心率且无呼吸抑制的情况发生。虽然两组患儿对面罩的接受程度差异无统计学意义,但D2组患儿的面罩诱导满意率可达90.0%,高于D1组的76.2%,表明术前经鼻雾化使用DEX 2 μg/kg较DEX 1 μg/kg相比用药安全,可在一定程度上减少患儿对面罩吸入诱导的抵抗,使整个吸入诱导过程更加平稳、顺畅。
既往研究证实,小儿喉罩置入时七氟醚EC50为1.57%~2.01%,术前适量使用镇静镇痛药物可增加麻醉深度,降低吸入麻醉药浓度[13- 15]。Nishina等[16]研究表明,术前口服可乐定4 μg/kg喉罩置入时七氟醚EC50能降低38%。Savla等[4]的研究也提示,术前口服咪达唑仑0.5 mg/kg和经鼻给予DEX 2 μg/kg可使喉罩置入时七氟醚的EC50分别下降17%和21%。本研究也证实,患儿入室前经鼻雾化喷入右美托咪定1 μg/kg和2 μg/kg,喉罩置入的七氟醚EC50为1.59%(95%CI=1.41%~1.78%)和1.09%(95%CI=0.89%~1.28%),而EC95为2.02%(1.82%~2.56%)和1.52%(1.32%~2.04%),D2组较D1组减少了31.4%,与Yao等[17]报道基本一致。但本研究DEX 2 μg/kg组的七氟醚EC50和EC95值明显低于Savla等[4]的研究结果,可能与Savla等[4]采用滴鼻给药方式,部分药物流入口腔,而本研究采用鼻腔内雾化给药的方式,药液与鼻腔黏膜接触更充分、吸收更好有关[18]。
本研究仅观察3~6岁患儿DEX经鼻雾化给药复合七氟醚抑制喉罩置入反应的量效关系,对于其他年龄患儿上述药物对喉罩置入反应抑制的量效关系尚需进一步研究观察。
综上,麻醉前30 min予患儿经鼻雾化喷入DEX 1 μg/kg 和2 μg/kg均可获得良好的镇静镇痛效果,能增加患儿吸入诱导时对面罩的顺应性,其中DEX 2 μg/kg 组的镇静效果更好。D2组喉罩置入时七氟醚的EC50为1.09%,低于D1组的1.59%,因此,较DEX 1 μg/kg相比,麻醉前30 min经鼻雾化喷入DEX 2 μg/kg可显著降低小儿喉罩置入时七氟醚EC50。
[1]Goa KL, Noble S, Spencer CM. Sevoflurane in paediatric anaesthesia: a review[J]. Paediatr Drugs, 1999,1(2):127- 153.
[2]Asai T, Morris S. The laryngeal mask airway: its features, effects and role[J]. Can J Anaesth, 1994, 41(10):930- 960.
[3]Nishina K, Mikawa K, Uesugi T, et al. Oral clonidine premedication reduces minimum alveolar concentration of sevoflurane for laryngeal mask airway insertion in children[J]. Paediatr Anaesth, 2006,16(8):834- 839.
[4]Savla JR, Ghai B, Bansal D, et al. Effect of intranasal dexmedetomidine or oral midazolam premedication on sevoflurane EC50 for successful laryngeal mask airway placement in children: a randomized, double-blind, placebo-controlled trial [J]. Paediatr Anaesth, 2014,24(4):433- 439.
[5]Rosenbaum A, Kain ZN, Larsson P, et al. The place of premedication in pediatric practice[J]. Paediatr Anaesth, 2009,19(9):817- 828.
[6]Wolfe TR, Braude DA. Intranasal medication delivery for children: a brief review and update [J]. Pediatrics, 2010,126(3):532- 537.
[7]Messeri A, Caprilli S, Busoni P. Anaesthesia induction in children: a psychological evaluation of the efficiency of parents’ presence[J]. Paediatr Anaesth, 2004,14(7):551- 556.
[8]Graff CL, Pollack GM. Nasal drug administration: potential for targeted central nervous system delivery[J]. J Pharm Sci, 2005,94(6):1187- 1195.
[9]Wolfe TR, Braude DA. Intranasal medication delivery for children: a brief review and update[J]. Pediatrics, 2010, 126(3):532- 537.
[10]Roback MG, Carlson DW, Babl FE, et al. Update on pharmacological management of procedural sedation for children[J]. Curr Opin Anaesthesiol, 2016, 29(Suppl 1):S21-S35.
[11]Yuen VM, Hui TW, Irwin MG, et al. Optimal timing for the administration of intranasal dexmedetomidine for premedication in children[J]. Anaesthesia, 2010,65(9):922- 929.
[12]Yuen VM, Hui TW, Irwin MG, et al. A randomised comparison of two intranasal dexmedetomidine doses for premedication in children[J]. Anaesthesia, 2012, 67(11):1210- 1216.
[13]Kihara S, Yaguchi Y, Inomata S, et al. Influence of nitrous oxide on minimum alveolar concentration of sevoflurane for laryngeal mask insertion in children[J]. Anesthesiology, 2003, 99(5):1055- 1058.
[14]Aantaa R, Takala R, Muittari P. Sevoflurane EC50 and EC95 values for laryngeal mask insertion and tracheal intubation in children[J]. Br J Anaesth, 2001,86(2):213- 216.
[15]贺琳,张学锋.小儿喉罩通气道置入时呼气末七氟烷的最低肺泡有效浓度[J].中华医学杂志,2009, 89(15):1021- 1023.
[16]Nishina K, Mikawa K, Uesugi T, et al. Oral clonidine premedication reduces minimum alveolar concentration of sevoflurane for laryngeal mask airway insertion in children[J]. Paediatr Anaesth, 2006, 16(8):834- 839.
[17]Yao Y, Qian B, Lin Y, et al. Intranasal dexmedetomidine premedication reduces minimum alveolar concentration of sevoflurane for laryngeal mask airway insertion and emergence delirium in children: a prospective, randomized, double-blind, placebo-controlled trial[J]. Paediatr Anaesth, 2015,25(5):492- 498.
[18]Sheta SA, Al-Sarheed MA, Abdelhalim AA. Intranasal dexmedetomidine vs midazolam for premedication in children undergoing complete dental rehabilitation: a double-blinded randomized controlled trial[J]. Paediatr Anaesth, 2014,24(2):181- 189.
Effects of Two Intranasal Dexmedetomidine Doses as Premedication on Sevoflurane EC50for Successful Laryngeal Mask Airway Placement in Children
XU Jin, DENG Xiao-ming, WEI Ling-xin, YANG Dong, LIU Ju-hui, ZHI Juan, LI Ya-nan
Department of Anesthesiology, Plastic Surgery Hospital, CAMS and PUMC, Beijing 100144,China
DENG Xiao-ming Tel:010- 88772082,E-mail:dengxiaoming2003@sina.com
Objective To observe the effects of two different intranasal dexmedetomidine doses as premedication on the EC50of sevoflurane for successful laryngeal mask airway placement in children. Methods Children aged 3- 6 years, of American Society of Anesthesiologists physical status Ⅰ, and scheduled for plastic surgery were enrolled in this study. Children were assigned to receive either spray administration of intranasal dexmedetomidine 1 μg/kg (group D1,n=21) or 2 μg/kg (group D2,n=20) approximately 30 minutes before anesthesia. Anesthesia was induced with sevoflurane up to 8% in 100% O2, with fresh gas flow set to 6 L/min. After the pupil fixed to the middle position, sevoflurane dial setting was reduced to 5% and fresh gas flow reduced to 3 L/min. The endtidal sevofluran (ETsevo) concentration for laryngeal mask airway insertion sustained for 10 minutes after vein intubation, which was determined according to the Dixon’s up and down method. The initial endtidal sevoflurane concentration in each group was set at 2%. ETsevowas increased/decreased (1∶1.2) in the next patient according to the response to laryngeal mask airway insertion. Bispectral index, mask acceptance, all response to laryngeal mask airway insertion, and ETsevoof laryngeal mask airway insertion of children were recorded. Results The bispectral index value was 77.4±3.6 in group D2, which was significantly lower than that (87.4±1.9) in group D1 when children entered operation room (P<0.05). Mask acceptance was 76.2% in group D1 and 90.0% in group D2. The EC50of sevoflurane for laryngeal mask airway insertion was 1.09% (95%CI=0.89%-1.28%) in group D2, which was lower than 1.59% (95%CI=1.41%-1.78%) in group D1 (P<0.05). Conclusion Compared with the dose of 1 μg/kg, spray administration of intranasal dexmedetomidine 2 μg/kg as premedication can reduce the sevoflurane EC50for successful laryngeal mask airway placement in children.
dexmedetomidine; spray administration of intranasal; child; EC50of sevoflurane
邓晓明 电话:010- 88772082,电子邮件:dengxiaoming2003@sina.com
R614
A
1000- 503X(2016)06- 0627- 05
10.3881/j.issn.1000- 503X.2016.06.001
2016- 07- 27)

