羧甲基壳聚糖/海藻酸钠包埋柠檬醛精油微球制备工艺优化及其性能分析
刘 欢 夏光辉 何文兵 张 雯 王冰玉
羧甲基壳聚糖/海藻酸钠包埋柠檬醛精油微球制备工艺优化及其性能分析
刘 欢 夏光辉 何文兵 张 雯 王冰玉
(通化师范学院长白山食品工程研究中心;通化师范学院制药与食品科学学院,通化 134000)
以羧甲基壳聚糖和海藻酸钠为壁材制备柠檬醛微球,考察了羧甲基壳聚糖、氯化钙和海藻酸钠浓度对柠檬醛微球包埋率的影响。采用响应面法优化柠檬醛微球包埋工艺,并进一步对其性能进行分析。研究结果表明,适量的羧甲基壳聚糖、氯化钙和海藻酸钠能较好形成柠檬醛微球;微球的优化工艺参数分别为羧甲基壳聚糖质量浓度3.5 g/L、氯化钙质量浓度4.5 g/L和海藻酸钠质量浓度8.5 g/L,此时包埋率值为81.79%。柠檬醛微球性能研究表明,其具有控释和抗油脂氧化性能;外观呈圆型,乳白色半透明状,表面平滑有光泽;红外光谱证实柠檬醛精油被完好包裹在微球内部。由此可见,微球化有效提高柠檬醛精油的稳定性和利用率。
羧甲基壳聚糖 海藻酸钠 柠檬醛精油 微球 性能
柠檬醛精油是一种具有强烈柠檬香气和风味的天然香料物质,被广泛用于食品添加剂、保鲜剂、饮料和化妆品中[1,2]。但柠檬醛精油化学性质极其不稳定,容易挥发和被氧化,导致失去其原有的功能活性[3]。目前,研究人员利用微胶囊化技术,使封装在天然材料中柠檬醛精油具有较好的缓释性和稳定性,从而扩大柠檬醛的应用范围[4]。
复凝聚法是制备微囊或微球的常用方法,一般使用海藻酸钠、壳聚糖等天然高分子材料作为壁材,它们通过静电作用形成复杂空间网状结构,将生物活性物质封装在其内部[5]。海藻酸钠是天然的阴离子多糖化合物,与多价阳离子(如Ca2+)交联形成网络结构,产生具有良好相容性和电离子敏感性的水凝胶微球[6]。但海藻酸盐微球凝胶强度低,尺寸和结构稳定性较差,严重影响了对活性物质的缓释效果。目前,利用海藻酸盐与壳聚糖及其衍生物正、负电荷吸引形成聚电解质膜,可以改善海藻酸盐微球的结构,提高其对活性物质的控释作用和稳定性[7]。
羧甲基壳聚糖是含有丰富羧基和氨基的一类壳聚糖衍生物,比壳聚糖具有更好的生物相溶性,与Ca2+也能交联形成水凝胶微球,对活性物质具有很好的吸附性和控释作用[8]。韩晓娜等[9]制备不同取代度的O-羧甲基壳聚糖,与海藻酸钠混合后滴入CaCl2溶液中制备微球,与海藻酸钠微球相比,羧甲基壳聚糖/海藻酸钠微球的强度和稳定性有所增加,pH值敏感性有所加强。闻燕等[10]以CaCl2为交联剂制备了一系列羧甲基壳聚糖/海藻酸钠水凝胶,红外光谱研究发现羧甲基壳聚糖/海藻酸钠中氨基和羧基基团结构受pH值变化所影响。因此,在海藻酸盐中加入羧甲基壳聚糖,即有效加强海藻酸盐水凝胶微球的机械强度,又可提高其稳定性和控释性,在活性物质的微胶囊化上具有良好的发展前景[11]。本试验以羧甲基壳聚糖和海藻酸钠为壁材、CaCl2为交联剂,采用复凝聚法制备柠檬醛水凝胶微球(以下简称柠檬醛微球),进一步对柠檬醛微球性能进行初探,为柠檬醛微球的研制提供参考。
1 材料与方法
1.1 材料与试剂
柠檬醛精油(纯度≥95%):国药集团化学试剂有限公司;羧甲基壳聚糖(羧化度≥80.0%):浙江澳兴生物科技有限公司;海藻酸钠:北京康普汇维科技有限公司;氯化钙:天津市科欧化学试剂有限公司;无水乙醇:天津市致远化学试剂有限公司。
1.2 仪器与设备
UV-2600型紫外可见分光光度计:日本岛津公司;SPX-250型恒温恒湿培养箱常州诺基仪器有限公司;SMZ1500(CCD)型体视显微镜:日本尼康仪器有限公司;Nicolet iS50(Smart iTR diamond ATR)型傅里叶红外光谱仪:美国赛默飞世尔科技公司。
1.3 方法
1.3.1 微球制备方法
称取一定质量的羧甲基壳聚糖和一定质量的氯化钙,将羧甲基壳聚糖溶解于20 mL 60℃蒸馏水中,使其完全溶解,溶解后的状态为透明液体,然后加入氯化钙于溶液中,均质5 min,形成壁材溶液。
称取一定质量的海藻酸钠充分溶解于20 mL蒸馏水中,将0.6 mL的柠檬醛加入到海藻酸钠溶液中(现用现配),均质10 min,形成柠檬醛和海藻酸钠混合溶液。
用注射器将混合溶液以每秒钟1滴的速率滴入到壁材溶液中,半封闭静置12 h。用95%乙醇溶液清洗已固化后的柠檬醛微球,去除杂质。放入干燥器中,干燥至微球表面没有残余的溶液为止,得到柠檬醛水凝胶微球成品,置于称量瓶中保藏。
1.3.2 柠檬醛含量测定
1.3.2.1 最大吸吸光谱
取0.5 mL的柠檬醛精油溶于5 mL 95%乙醇溶液中,充分混合均匀,再移入25 mL容量瓶中,用95%乙醇溶液定容。利用紫外-可见光进行光谱扫描,确定柠檬醛乙醇溶液的最大吸收光谱值。当柠檬醛乙醇溶液的最大吸光度值为0.116时,柠檬醛乙醇溶液吸收光谱λ值为242 nm。
1.3.2.2 标准曲线测定
分别取不同体积的柠檬醛精油溶于5 mL 95%乙醇溶液中,充分混合均匀,再移入25 mL容量瓶中,用95%乙醇溶液定容,形成0、4、8、12、16,20、24、28、32μL/mL柠檬醛乙醇溶液,用95%乙醇溶液为空白,测定吸光度值(A),绘制出柠檬醛乙醇溶液的标准曲线。用吸光度值(y)对柠檬醛乙醇溶液浓度(x,μL/mL)进行线性回归分析,得回归方程y=0.003x-0.001,R2=0.999。
1.3.3 微球包埋率测定
称取0.1 g柠檬醛微球于研钵中,加入10 mL 95%乙醇溶液,研磨至柠檬醛微球全部破碎,将混合液全部放入离心机中,2 000 r/min离心10 min,取上清液倒入25 mL容量瓶,定容至25 mL,以乙醇溶液为空白,测定吸光度的值,根据回归方程计算柠檬醛浓度。计算柠檬醛的包埋率见公式。
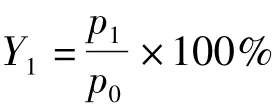
式中:Y1为包埋率/%;p0为加入柠檬醛体积浓度/μL/mL;p1为微球内部的柠檬醛体积浓度/μL/mL。
1.3.4 试验设计
1.3.4.1 单因素试验设计
分别以不同的羧甲基壳聚糖质量浓度(2.0、2.5、3.0、3.5、4.0、4.5 g/L)、氯化钙质量浓度(2.5、3.0、3.5、4.0、4.5、5.0 g/L)、海藻酸钠质量浓度(3.75、5.00、6.25、7.50、8.75、10.00 g/L)为单因素进行试验,考察一种单因素对微球包埋率影响时,其他各因素分别为羧甲基壳聚糖质量浓度3.0 g/L、氯化钙质量浓度3.0 g/L、海藻酸钠质量浓度7.5 g/L。
1.3.4.2 优化工艺设计
以单因素试验为基础,采用Design-Expert 8.0.6软件数据分析,建立Box-Betoken数学模型,试验因素为羧甲基壳聚糖质量浓度(X1)、氯化钙质量浓度(X2)和海藻酸钠质量浓度(X3),微球包埋率(Y)作为指标进行分析,试验因素水平、变化值及编码见表1。
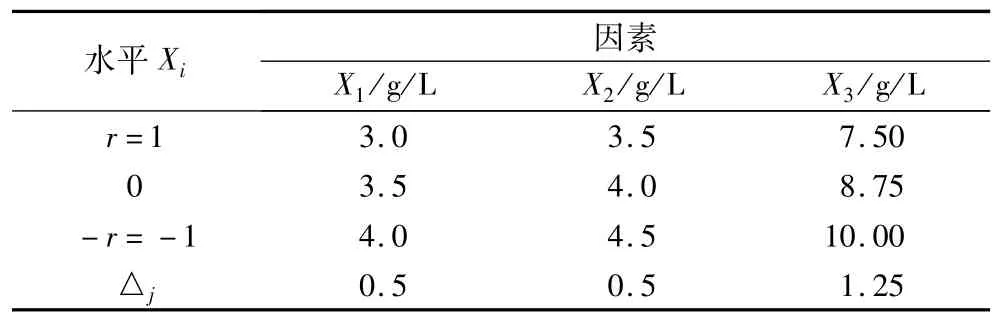
表1 试验因素水平编码表
1.3.5 微球缓释性能的测定
1.3.5.1 微球保留率的测定
准确称取1 g柠檬醛精油和柠檬醛含量相同的微球放于称量瓶中,贮存在相对湿度为90%和温度为20℃恒温恒湿箱中,每隔15 d称量样品质量。计算柠檬醛微球和柠檬醛保留率见公式。
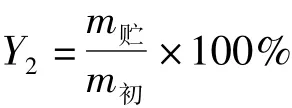
式中:Y2为柠檬醛保留率/%;m贮为贮存一定时间样品质量/g;m初为贮存前样品质量/g。
1.3.5.2 柠檬醛微球释放的分析方法
利用Avrami′s方程对柠檬醛微球释放过程进行分析[12],计算见公式。
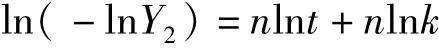
1.3.6 微球抗油脂氧化性能的测定
准确称取1 g柠檬醛精油和柠檬醛含量相同的微球放入1 kg大豆油中,充分搅拌均匀,贮存在相对湿度为90%和温度为60℃恒温恒湿箱中,每隔1 d取样,大豆油为空白对照。根据GB/T 5538—2005《动植物油脂过氧化值测定》测定大豆油的过氧化值(POV)。
1.3.7 微球结构的测定
采用带Smart iTR diamond ATR附件的傅里叶红外光谱仪对柠檬醛精油、羧甲基壳聚糖、海藻酸钠、羧甲基壳聚糖/海藻酸钠微球、羧甲基壳聚糖/海藻酸钠柠檬醛微球的结构进行表征。取少量的以上样品于金刚石ATR模块表面上,保证样品完全覆盖光路表面,在600~4 000 cm-1扫描。红外光谱图使用OMNIC9和OMNIC Specta进行分析。
1.3.8 数据统计
每组试验重复3次,其结果表示为平均值±标准偏差,采用SPSS19.0软件进行试验数据分析(ANOVA),用Duncan′s新复极差法进行显著性分析,检验其差异显著性;工艺优化采用响应面法,用Design-Expert 8.0.6 软件数据分析;采用Origin 8.0 作图。
2 结果与讨论
2.1 单因素试验
2.1.1 羧甲基壳聚糖浓度对柠檬醛微球包埋率的影响
试验结果如图1所示。从图1可知,羧甲基壳聚糖浓度对包埋率的影响存在显著性差异(P<0.05)。随着羧甲基壳聚糖浓度的增加,包埋率先增加后减小;当羧甲基壳聚糖质量浓度为4.0 g/L时,包埋率最大值为66.69%;随后包埋率缓慢变小。因为在静电作用下,羧基与钙离子配位形成微球框架,氨基再与海藻酸钠形成聚电解质膜,羧甲基壳聚糖浓度越高,形成微球框架越结实,壁膜结构越致密,芯材被包裹也越严实,但当羧基过多时,游离的阴离子破坏原有致密结构,芯材从内部扩散出来[13]。
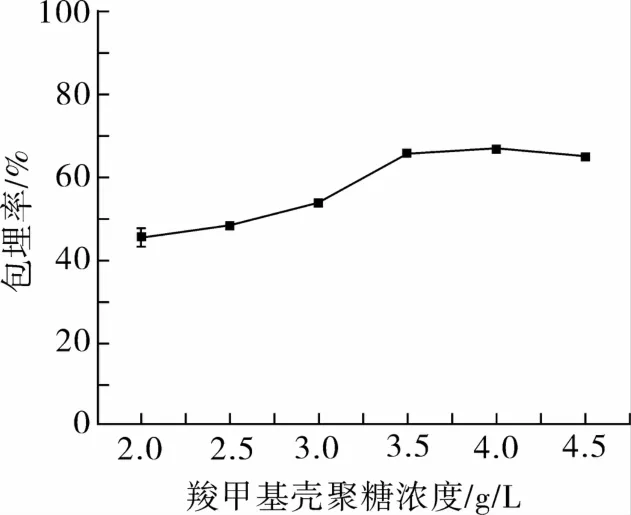
图1 不同羧甲基壳聚糖浓度对柠檬醛包埋率的影响
2.1.2 氯化钙浓度对柠檬醛微球包埋率的影响
试验结果如图2所示。从图2可知,氯化钙浓度对包埋率的影响存在显著性差异(P<0.05)。随着氯化钙的增加,包埋率先增加后减小;当氯化钙质量浓度为4.5 g/L时,包埋率达到最大为64.20%;随后包埋率变小。因为钙离子浓度越高提供阳离子越多,微球离子间交联越密集,但钙离子过多破坏了微球框架结构,形成非球型,也影响羧甲基壳聚糖和海藻酸钠聚电解质膜的形成速度,芯材透过微球扩散出来[14]。
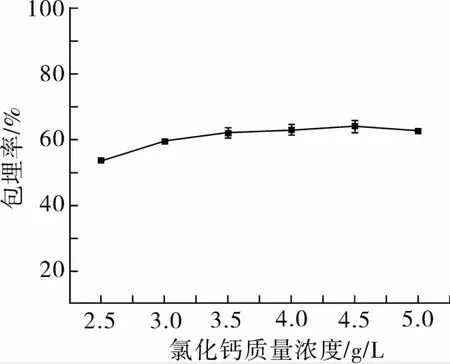
图2 不同氯化钙浓度对柠檬醛包埋率的影响
2.1.3 海藻酸钠浓度对柠檬醛微球包埋率的影响
试验结果如图3所示。从图3可知,海藻酸钠浓度对包埋率的影响存在显著性差异(P<0.05)。随着海藻酸钠的增加,包埋率增加;当海藻酸钠质量浓度为10 g/L时,包埋率达到最大为83.61%。因为当海藻酸钠浓度低时,羧甲基壳聚糖与海藻酸钠形成的聚电解质膜过薄,机械强度较低,对芯材阻止能力较差[15]。
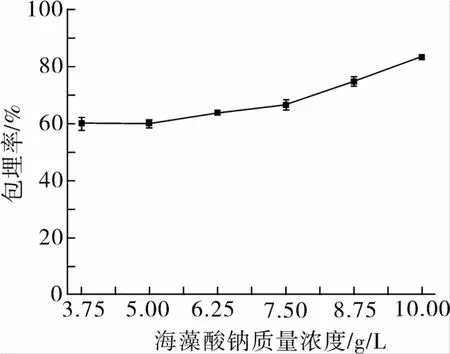
图3 不同海藻酸钠浓度对柠檬醛包埋率的影响
2.2 包埋工艺优化
2.2.1 试验设计和试验结果
试验以柠檬醛微球包埋率(Y,%)作为指标,以羧甲基壳聚糖质量浓度(X1,g/L)、氯化钙质量浓度(X2,g/L)和海藻酸钠质量浓度(X3,g/L)为试验因素,建立柠檬醛微球包埋工艺的Box-Behnken数学模型,试验设计及试验结果见表2。
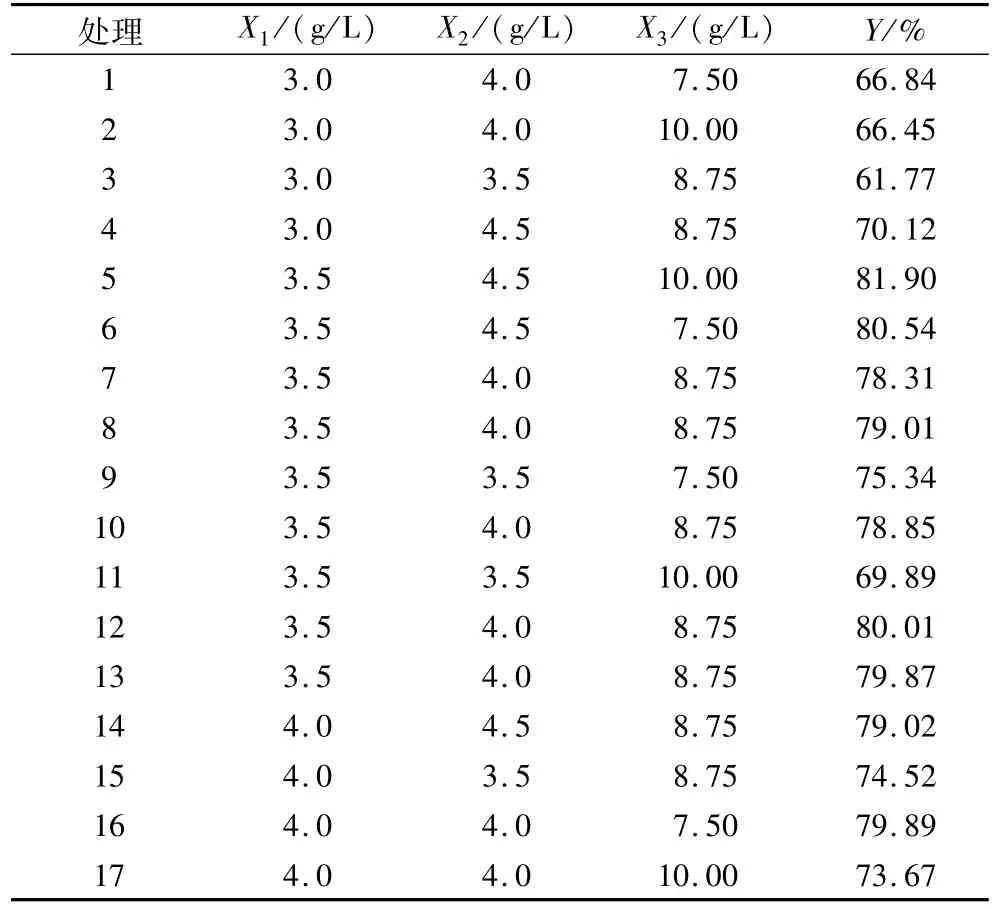
表2 工艺优化试验设计及试验结果
2.2.2 方差分析及回归方程的建立
柠檬醛微球包埋率的二次回归模型方差分析结果见表3。由表3可知,回归模型,P=0.000 1<0.01,说明二次回归模型极显著;F失=2.21,P =0.229 3>0.05,失拟项不显著;模型的相关系数R2为0.990 5,预测值与实测值之间具有高度的相关性。由此可知,二次回归模型在显著水平时不失拟,回归模型与实际情况拟合性好,可以用此模型来分析和预测柠檬醛微球包埋率试验中。
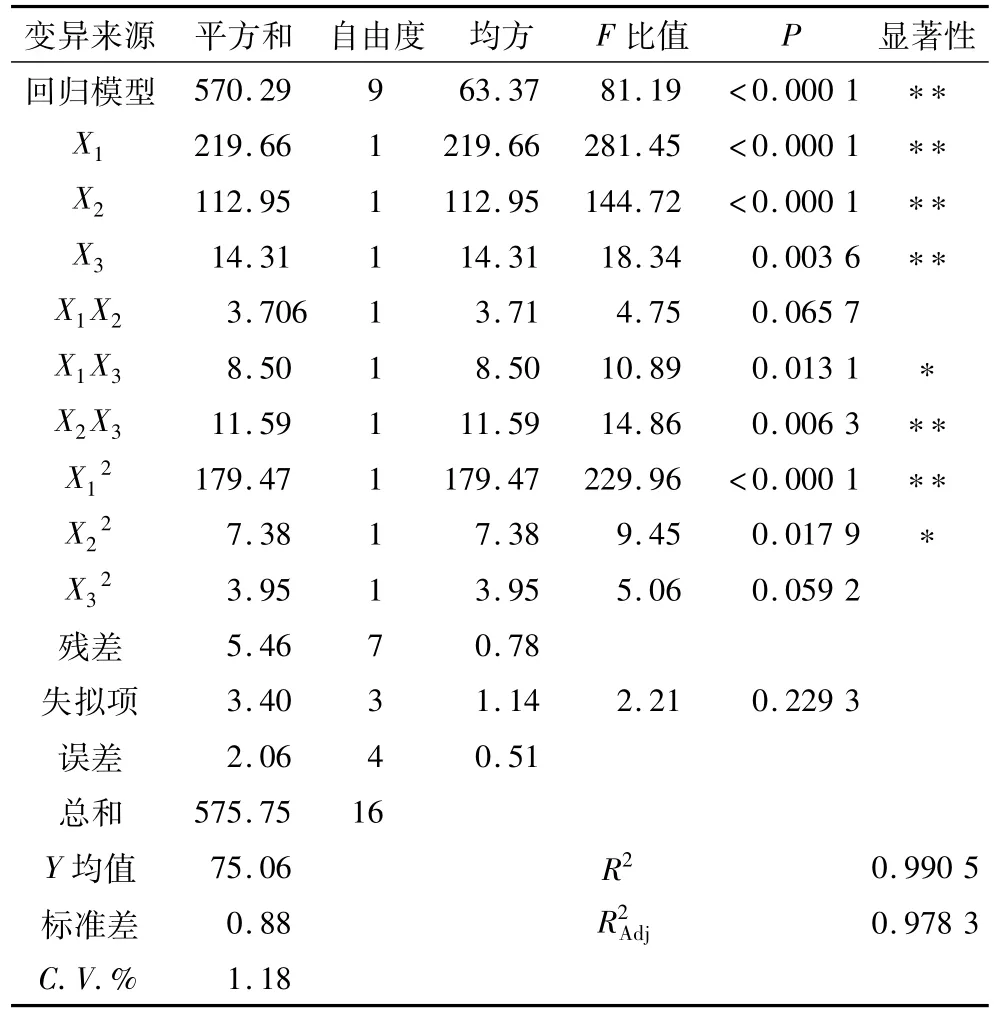
表3 二次回归模型方差分析
以柠檬醛微球包埋率为(Y)值,以羧甲基壳聚糖质量浓度(X1,g/L)、氯化钙质量浓度(X2,g/L)和海藻酸钠质量浓度(X3,g/L)为试验因素,通过二次回归分析对试验数据进行回归拟合,确立柠檬醛包埋率的最优拟合二次多项式方程:Y=-460.243+229.09X1+39.515X2+7.046X3-26.115X12-3.85X1X2-2.332X1X3-5.295X22+2.724X2X3-0.62X23
2.2.3 工艺优化及验证
对二次回归模型方程进行优化验证,柠檬醛微球包埋率的优化实验验证结果:柠檬醛微球包埋率(Y)的最大预测值为82.26%,此时3个因素水平分别为羧甲基壳聚糖质量浓度(X1)3.67 g/L、氯化钙质量浓度(X2)4.44 g/L 和海藻酸钠质量浓度(X3)8.57 g/L。将优化试验验证结果修正为羧甲基壳聚糖质量浓度(X1)3.5 g/L、氯化钙质量浓度(X2)4.5 g/L 和海藻酸钠质量浓度(X3)8.5 g/L。在此条件下进行验证试验,柠檬醛微球包埋率(Y)值为81.79% 。
2.3 柠檬醛微球性能
2.3.1 缓释性能
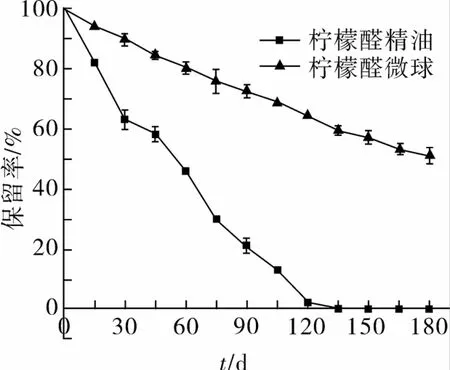
图4 微球化对柠檬醛精油保留率的影响
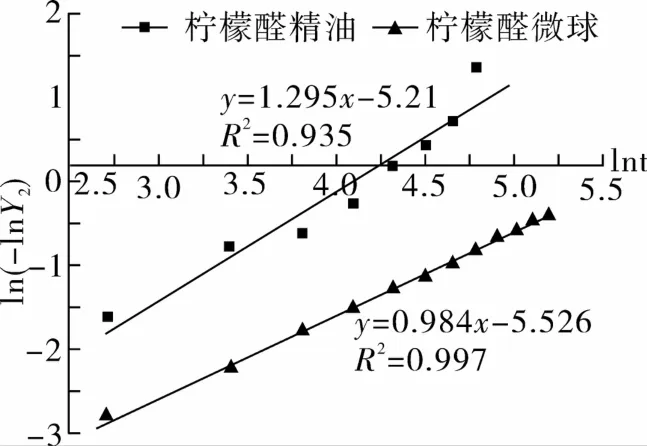
图5 柠檬醛微球的Avrami′s回归分析
柠檬醛微球缓释性能试验结果见图4和图5。由图4可知,随着贮藏时间延长,柠檬醛精油和柠檬醛微胶囊的保留率逐渐减小,柠檬醛精油挥发速率显著大于柠檬醛微球(P<0.05)。当贮藏到60 d时,柠檬醛精油保留率为46%,柠檬醛微球保留率为80.3%,是柠檬醛精油保留率的1.74倍;当贮藏到135 d时,柠檬醛精油保留率为0,说明柠檬醛精油已经全部挥发,而柠檬醛微球保留率为59.5%。说明微球化明显降低柠檬醛的挥发速率,有效保持柠檬醛精油的稳定性[16]。
采用控制释放公式Avrami′s进行分析,当n=0.54时代表的是扩散限制动力学反应,当n=1代表是一级动力学反应。由图5所示以及柠檬醛和柠檬醛微球的Avrami′s回归分析可知,柠檬醛精油的释放机理参数(n)为1.295,拟合方程的R2为0.935,释放速率常数(k)为0.04;柠檬醛微球的释放机理参数(n)为0.984,拟合方程的R2为0.998,释放速率常数(k)为0.014。由此可知,柠檬醛精油的n远远大于1,柠檬醛微球的n介于0.54与1之间,柠檬醛精油释放速率远远高于柠檬醛微球,柠檬醛微球释放反应介于扩散限制动力学和一级反应动力学之间,微球化对柠檬醛挥发有明显限制作用。
2.3.2 抗油脂氧化性能
过氧化值(POV)评价油脂过氧化程度的一项重要指标,其值越小,油脂发生过氧化的程度越弱,油脂的稳定性越高。试验结果如图6所示。由图6可知,随着贮藏时间延长,大豆油的POV逐渐增加;对照大豆油的POV极显著高于柠檬醛精油和柠檬醛微球(P<0.01);从贮藏时间8 d以后,柠檬醛精油与柠檬醛微球之间的大豆油POV差异显著(P<0.05)。说明柠檬醛精油具有较好的抗氧化活性,但其自身性能极其不稳定,所以在贮藏后期POV值迅速增加;而柠檬醛微球化后,缓释效应发挥作用,柠檬醛能持续抵抗油脂氧化,稳定性和利用率得到了提高。由此可见,天然活性成分经微胶囊化后,具有较强的抗油脂氧化的能力[17]。
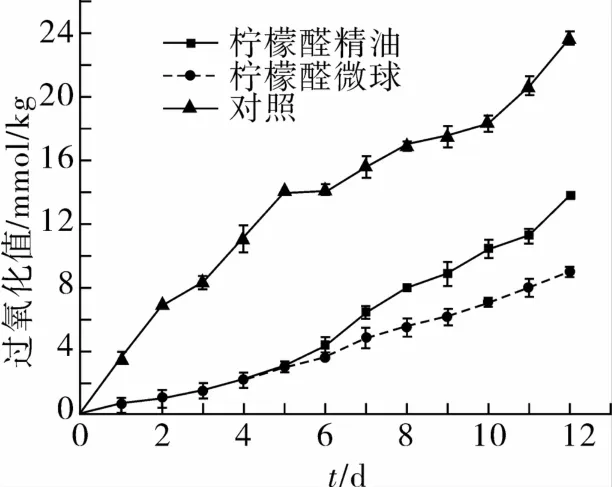
图6 柠檬醛精油和柠檬醛微球对抗油脂氧化的影响
2.4 柠檬醛微球外观
在贮藏过程中柠檬醛微球外观变化见图7。从图7a可以看出,在贮藏前,柠檬醛微球呈圆型,颜色为乳白色半透明状,表面平滑有光泽,微球平均粒径在0.7~1.0 mm。随着贮藏时间的延长,柠檬醛微球发生了缓慢的变化,从图7b可以看出,在贮藏第180天时,柠檬醛微球一部分仍呈圆型,但体积减小,另一部分发生了变形,颜色变为线黄色,透明度降低,表面有油性物质析出,微球平均粒径在0.3~0.6 mm。说明在长期贮藏过程中柠檬醛发生缓慢释放,从微球内向外扩散,再由微球表面挥发到环境中,使微球外观发生变化。

图7 柠檬醛微球外观(×75倍)
2.5 柠檬醛微球结构的测定
红外光谱图见图8。从海藻酸钠的谱图分析可知,1 579.88 cm-1和1 021.51 cm-1附近特征吸峰分别是海藻酸钠COOH和OH的伸缩振动峰;从羧甲基壳聚糖的谱图分析可知,在1 588.82 cm-1附近特征吸峰和1 047.20~989.70 cm-1分别是羧甲基壳聚糖NH2和OH的伸缩振动峰;从羧甲基壳聚糖/海藻酸钠微球的谱图分析可知,海藻酸钠COOH和羧甲基壳聚糖NH2特征峰消失,海藻酸钠和羧甲基壳聚糖OH特征峰的峰强度大幅度减小;从柠檬醛的谱图分析可知,1 672.28 cm-1附近特征吸峰和2 849.65~2 971.85 cm-1分别是柠檬醛=O和CH3的伸缩振动峰。从柠檬醛微球的谱图分析可知,海藻酸钠COOH和羧甲基壳聚糖NH2特征峰消失,海藻酸钠和羧甲基壳聚糖OH特征峰消失,柠檬醛特征峰消失。由此可知,羧甲基壳聚糖NH3+和海藻酸钠COO-之间、Ca2+与O-、COO-之间发生了静电作用形成微球,使NH2、COOH基团特征峰消失、OH基团特征峰减弱;同时,柠檬醛提供阳离子基团与O-之间也发生静电作用,使OH基团特征峰完全消失。静电作用力形成的微球完好将柠檬醛精油封装在内部,使柠檬醛=O和CH3基团特征峰消失。
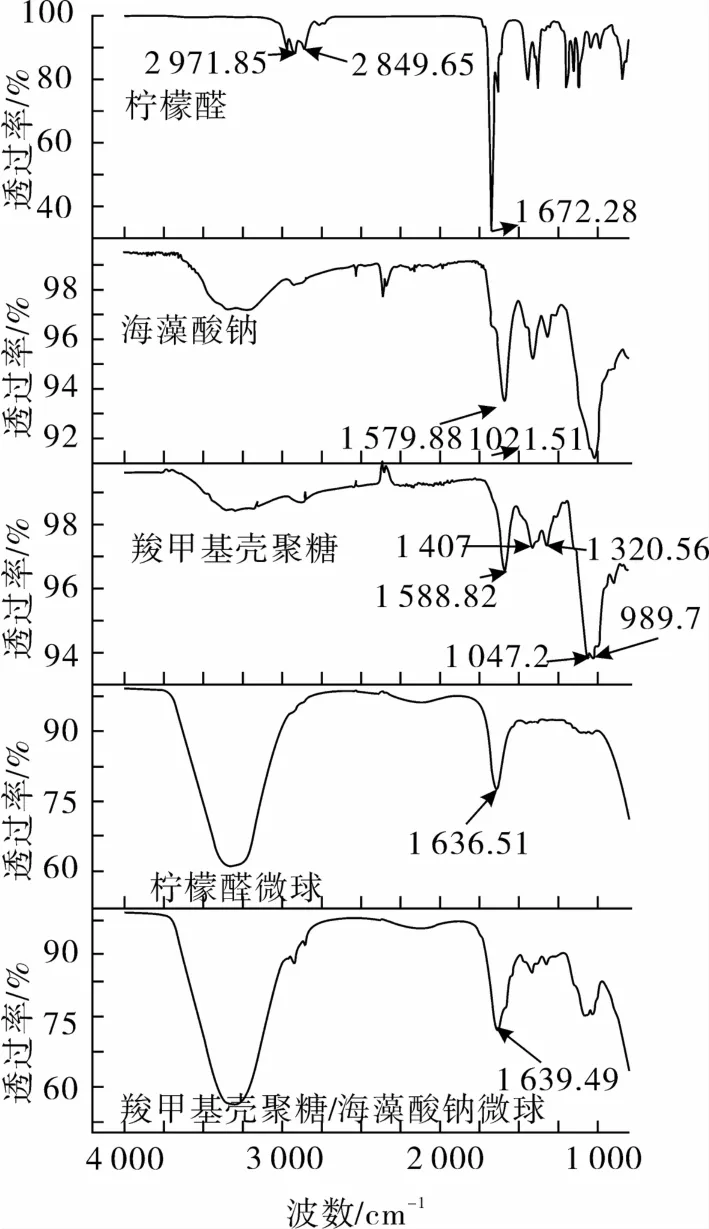
图8 傅里叶红外光谱图
3 结论
3.1 羧甲基壳聚糖、氯化钙和海藻酸钠浓度对柠檬醛微球包埋率影响显著;随着羧甲基壳聚糖和氯化钙浓度增加,包埋率先增加后减小;随着海藻酸钠浓度增加,包埋率逐渐增加。表明了在静电作用下,当羧基与钙离子等量匹配时,形成结实的微球框架,而海藻酸钠与羧甲基壳聚糖再形成致密的聚电解质膜,使微球很好包裹住柠檬醛精油,有效阻止柠檬醛从内部向外扩散。
3.2 柠檬醛微球包埋率的优化试验验证结果:柠檬醛微球包埋率的最大预测值为82.26%,此时3个因素水平分别为羧甲基壳聚糖质量浓度3.67 g/L、氯化钙质量浓度4.44 g/L和海藻酸钠质量浓度8.57 g/L。将优化试验验证结果修正为羧甲基壳聚糖质量浓度3.5 g/L、氯化钙质量浓度4.5 g/L 和海藻酸钠质量浓度8.5 g/L。在此条件下进行验证试验,柠檬醛微球包埋率值为81.79%。
3.3 稳定性测定结果表明,在贮藏到135 d时,柠檬醛精油保留率为0,柠檬醛微球保留率为59.5%,说明羧甲基壳聚糖/海藻酸钠包埋作用明显降低柠檬醛的挥发速率;对柠檬醛微球控释作用分析发出,柠檬醛微球释放机理参数(n)为0.984,释放反应介于扩散限制动力学和一级反应动力学之间,说明柠檬醛微球具有缓释作用;对照大豆油的POV极显著高于柠檬醛微球,说明柠檬醛能持续抵抗油脂氧化。由此可见,柠檬醛微球化有效保持柠檬醛精油的稳定性和利用率。外观性能观测表明,柠檬醛微球呈圆型,颜色为乳白色半透明状,表面平滑有光泽;在长期贮藏过程中,柠檬醛发生缓慢释放,经过一段时间后,柠檬醛微球外观才发生明显改变。红外光谱分析结果证实,柠檬醛微球形成过程以及柠檬醛精油完全被封装在微球内部。羧甲基壳聚糖和海藻酸钠能很好形成水凝胶微球,并能将柠檬醛精油完好包裹,确保了柠檬醛的缓释性和稳定性,提高了柠檬醛的利用率。
[1]Choi SJ,Decker E A,Henson L,et al.Inhibition of citral degradation in model beverage emulsions using micelles and reverse micelles [J].Food Chemistry,2010,122(1):111-116
[2]Muriel-galet V,Cerisuelo J P,López-Carballoa G,et al.Evaluation of EVOH-coated PP films with oregano essential oil and citral to improve the shelf-life of packaged salad[J].Food Cotrol,2013,30(1):137-143
[3]Djordievic D,Cercaci L,Alamed J.Chemical and physical stability of citral and limonene in sodium dodecyl sulfate-chitosan and gum arabic-stabilized oil-in-water emulsions[J].Journal of Agricultural and Food Chemistry,2007,55(9):3585-3591
[4]Maswal M,Dar A A.Formulation challenges in encapsulation and delivery of citral for improved food quality[J].Food Hydrocolloids,2014,37(6):182-195
[5]Lucinda-Silva R M,Salgado H R N,Evangelista R C.Alginate-chitosan systems:in vitro controlled release of triamcinolone and in vivo gastrointestinal transit[J].Carbohydrate Polymers,2010,81(2):260-268
[6]Mession J L,Blanchard C,Mint-dah F V,et al.The effects of sodium alginate and calcium levels on pea proteins cold-set gelation [J].Food Hydrocolloids,2013,31(2):446-457
[7]Ceki c′N D,Mili c′J R,Savi c′S D,et al.Influence of the preparation procedure and chitosan type on physicochemical properties and release behavior of alginate-chitosan microparticles [J].Drug Development and Industrial Pharmacy,2009,35(9):1092-102
[8]Teng Z,Luo Y C,Wang Q.Carboxymethyl chitosan-soy protein complex nanoparticles for the encapsulation and controlled release of vitamin D3[J].Food Chemistry,2013,141(1):524-532
[9]韩晓娜,黄国清,肖军霞.O-羧甲基壳聚糖/海藻酸钠微球的制备及取代度对微球溶胀性的影响[J].中国食品学报,2014,14(10):67-74
Han Xiaona,Huang Guoqing,Xiao Junxia.Preparation of o-carboxymethyl chitosan/sodium alginate hydrogel beads and the effect of degree of substitution of o-carboxymethyl on the swelling properties of the beads[J].Journal of Chinese Institute of Food Science and Technology,2014,14(10):67-74
[10]闻燕,杨志会.羧甲基壳聚糖/海藻酸钠水凝胶pH值对溶胀行为的影响[J].天津商学院学报,2007,27(6):12-16
Wen Yan,Yang Zhihui.Effect of pH value on swelling behavior of carboxymethyl chitosan and sodium alginate hydrogels[J].Journal of Tianjin University of Commerce,2007,27(6):12-16
[11]Li X Y,Chen X G,Sun Z W,et al.Preparation of alginate/chitosan/carboxymethyl chitosan complex microcapsules and application in Lactobacillus casei ATCC 393 [J].Carbohydrate Polymers,2011,83(4):1479-1485
[12]Ho B T,Joyce D C,Bhandari B R,et al.Release kinetics of ethylene gas from ethylene-cyclodextrin inclusion complexes[J].Food Chemistry,2011,129 (2):259-266
[13]Zhu A M,Chen J H,Liu Q L,et al.Controlled release of berberine hydrochloride from alginate microspheres embedded within carboxymethyl chitosan hydrogels [J].Journal of Applied Polymer Science,2011,120(4):2374-2380
[14]赵武奇,殷涌光,梁歧,等.壳聚糖/海藻酸钠微球对红景天苷控制释放的研究[J].吉林农业大学学报,2006,28(6):687-693
Zhao Wuqi,Yin Yongguang,Liang Qi,et al.Controlled release of salidroside from chitosan/alginate microsphere[J].Journal of Jilin Agricultural University,2006,28(6):687-693
[15]李强,吴彩娥.壳聚糖/海藻酸钠制备八角茴香油微胶囊的研究[J].农业机械学报,2007,38(1):96-99
Li Qiang,Wu Caie.Study on the productive technology of star aniseed oil microcapsulation with chitosan and alginate[J].Transactions of the Chinese Society for Agricultural Machinery,2007,38(1):96-99
[16]徐晶,刘欢,夏光辉,等.β-环糊精包埋柠檬醛微胶囊工艺优化及其缓释性能[J].食品科学,2014,35(14):82-86
Xu Jing,Liu Huan,Xia Guanghui,et al.Process Optimization of Microencapsulation and Controlled-Release Properties on the Citra Oil by β -cyclodextrin [J].Food Science,2014,35(14):82-86
[17]高丽,傅虹飞,崔芳,等.β-谷甾醇微胶囊工艺优化及抗油脂氧化研究[J].食品科学,2010,31(12):28-32
Gao Li,Fu Hongfei,Cui Fang,et al.Production optimization ofβ-sitosterol microcapsules and their protective effect against lipid oxidation [J].Food Science,2010,31(12):28-32
[18]Ribeiro A J,Silva C,Ferreira D,et al.Chitosan-reinforced alginate microspheres obtained through the emulsification/internal gelation technique[J].European Journal of Pharmaceutical Sciences,2005,25 (1):31-40.
Process Optimization of Preparation and Properties Analysis of Citral Oil Microsphere Embedded by
Carboxymethyl Chitosan/Sodium Alginate
Liu Huan Xia Guanghui He Wenbing Zhang Wen Wang Bingyu
(Research Center of Changbai Mountain Food Engineering,Department of Pharmaceutics and Food Science,Tonghua Normal University,Tonghua 134002)
In this paper the microspheres of citral oil were prepared of the carboxymethyl chitosan and sodium
alginate as wall materials was studied.The effects of the carboxymethyl chitosan,calcium chloride and sodium alginate on the embedding rate of citral oil were investigated.Quadratic rotary combinational design was applied to optimize the embedding process on the microspheres of citral oil.Their properties were analyzed.The results showed that,moderate carboxymethyl chitosan,calcium chloride and sodium alginate could form the microspheres of citral oil.The optimized conditions were the carboxymethyl chitosan concentration of 3.5 g/L,the calcium chloride concentration of 4.5 g/L,the sodium alginate concentration of 8.5 g/L and the encapsulation yield was81.79%.Meanwhile,the microspheres of citral oil had the properties of controlled release and anti-lipid oxidation.They were around,milky white and translucent.Their appearance was smooth and gloss.It was confirmed that citral oil was well embedded in the microsphere by FTIR.Thus the microsphere method was effective to improve the stability and utilization of citral oil.
carboxymethyl chitosan,sodium alginate,citral oil,microsphere,property
TS221
A
1003-0174(2016)11-0055-08
吉林省科技发展计划(20130522093JH)
2015-03-27
刘欢,女,1981年出生,副教授,食品贮藏与加工

