高效液相色谱法监测癫痫患儿血清中左乙拉西坦的血药浓度
李 容,王 刚,吕凤俊
(1.重庆市涪陵中心医院,重庆 408000; 2.重庆医科大学附属儿童医院,重庆 400014)
高效液相色谱法监测癫痫患儿血清中左乙拉西坦的血药浓度
李 容1,王 刚2,吕凤俊2
(1.重庆市涪陵中心医院,重庆 408000; 2.重庆医科大学附属儿童医院,重庆 400014)
目的 建立测定抗癫痫药左乙拉西坦血药浓度的高效液相色谱(HPLC)法。方法 根据液-液萃取法,利用乙酸乙酯从血清中提取出左乙拉西坦,于40℃恒温水浴中经氮气恒流吹干富集浓缩,再用甲醇复溶后进样25 μL;流动相为磷酸盐缓冲液(pH=4.0)-乙腈(93∶7,V/V),流速1.0 mL/min,柱温为40℃,色谱柱采用岛津RP-C18柱(150 mm×3.9 mm,5 μm),检测波长为210 nm。结果 左乙拉西坦线性回归方程为 Y=46 853 X+23 250,r=0.999 8(n=5),质量浓度在5.120~51.20 μg/mL范围内与峰面积线性关系良好。结论 该方法验证符合血清样品的测定要求,可用于临床血药浓度测定及药代动力学研究。
高效液相色谱法;左乙拉西坦;血药浓度;血清
左乙拉西坦(levetiracetam,LEV)是第2代乙酰胆碱激动剂,是吡咯烷酮衍生物,化学结构不同于传统的抗癫痫药物,结构和作用机制也与其他抗癫痫药物不同,主要是选择性地抑制癫痫样突发放电的超同步性和癫痫发作的传播而发挥作用,经口服吸收迅速,体内少部分通过水解酶的乙酰化代谢转化失活,大多以原形药经肾脏排出体外;其具有选择性预防局限性和原发全身性癫痫的独特药理作用,耐受性良好,药物相互作用低,是一种新型广谱抗癫痫药物,具有广阔临床应用前景。LEV已于2000年4月获得美国食品药物管理局(FDA)批准上市,于2007年引入国内,用于癫痫部分性发作和全身性发作。LEV治疗癫痫,具有显著的临床效果与临床应用价值[1]。参考LEV体内药物浓度监测相关的文献[2-4],结合本实验室条件,建立LEV的血清药物浓度测定的高效液相色谱方法,现报道如下。
1 材料与方法
1.1 仪器
高效液相色谱仪:日本岛津 Shimadzu系列产品(LC-10AT,SPD-10A,SCL-10A,CTP-10AS);Shimadzu AUW120型电子天平(日本岛津公司);PHS-3C型精密PH计(上海雷磁仪器厂);高速离心机(ABBOTT Made in Germany CAT);YKH-I型涡旋混合器(江西医疗器械厂)。
1.2 试药
左乙拉西坦对照品(纯度≥99.9%,CAT.NO1359404 USP TOCKVILLE,批号为FOH295);乙腈、甲醇为色谱醇,乙酸乙酯(分析纯,成都市科龙化工试剂厂,批号为2015111801);磷酸(分析纯,重庆川东化工<集团>有限公司,批号为20150801);磷酸二氢钠(二水,分析纯,成都化学试剂厂,批号为861128),磷酸氢二钠(分析纯,重庆川东化工<集团>有限公司,批号为20101101)。
2 方法与结果
2.1 色谱条件
色谱柱:岛津RP-C18柱(150 mm×3.9 mm,5 μm);柱温:40℃ ;流动相:磷酸盐缓冲液(pH=4.0)-乙腈(93∶7,V/V);流速:1.0 mL/min;检测波长:210 nm;进样量:25 μL。
2.2 溶液配制
对照品贮备液:称取LEV 512.0 mg,精密称定,用甲醇溶解定容至100 mL容量瓶中,得512.0 μg/mL的LEV溶液,作为对照品贮备液。
对照品溶液:精密量取贮备液适量,分别用甲醇稀释使成 51.20,102.40,204.80,409.60,512.0 μg/mL的系列对照品溶液。
2.3 模拟生物样品处理
分别精密移取上述系列质量浓度对照品溶液20.0 μL,精密加入空白血清180.0 μL,置10 mL尖底刻度玻璃具塞离心管中,混匀,精密加入乙酸乙酯3.00 mL,涡旋振荡1 min,2 000 r/min离心10 min,精密移取上清液2.50 mL于5 mL尖底刻度玻璃具塞离心管中,于40℃恒温水浴中氮气恒流吹干,加入甲醇100.0 μL复溶,摇匀,取上清液25 μL进样。取200.0 μL空白血清,同法处理,进样作空白对照。
2.4 方法学考察
专属性试验:按拟订色谱条件进样测试。结果LEV的保留时间为7.787 min(n=5),且血清中内源性物质对其无干扰,见图1。
干扰试验:根据癫痫患儿临床可能联合用药的情况,制备含卡马西平、氯硝西泮、拉莫三嗪、奥卡西平、硝西泮、苯巴比妥对照品的血清临床模拟样本,按2.3项下方法进行模拟血清样本处理。干扰试验结果见图2。可见,与LEV可能联用药物CBZ,CNP,LTG,OXC,NP,PB对LEV的测定基本无影响。
标准曲线制备:取出-20℃冷冻空白血清,常温融化,精密移取180.0 μL于10 mL尖底刻度玻璃具塞离心管中,加入系列质量浓度的LEV溶液20.0 μL,配成血清中LEV质量浓度依次为5.120,10.240,20.480,40.960,51.20 μg/mL的对照品溶液,依次加入提取液乙酸乙酯3.00 mL,涡旋振荡1 min,2 000 r/min离心10 min,取上清液 2.50 mL,于 5 mL尖底刻度玻璃具塞离心管中,40℃水浴下,氮气恒流吹干,精密移取100.0 μL甲醇复溶,进样。以LEV的峰面积对相应的质量浓度进行线性回归,得线性回归方程 Y=46 853 X+23 250,r=0.999 8(n=5)。结果表明,LEV质量浓度线性范围5.120~51.20 μg/mL。
回收试验:配制LEV血清质量浓度分别为10.240,20.480,40.960 μg/mL的模拟血清生物样品,并按2.3项下方法处理,进样,测定药物峰面积,根据标准曲线计算得浓度,并计算方法回收率。结果见表1。

图1 专属性试验高效液相色谱图
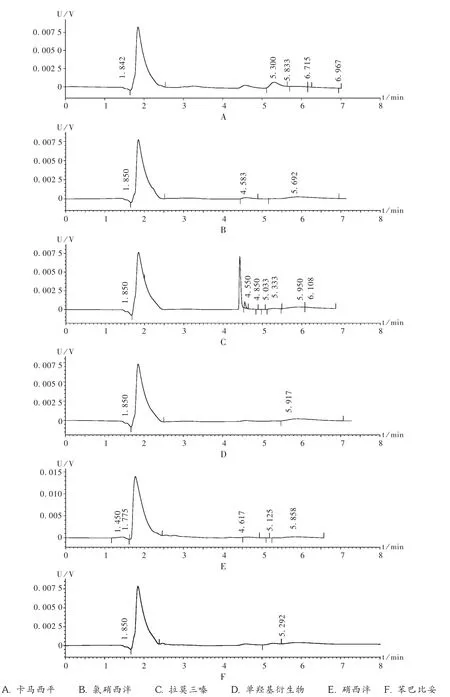
图2 干扰试验高效液相色谱图
精密度试验:配制高、中、低质量浓度分别为51.20,30.720,5.120 μg/mL的模拟血清样品,均按2.3项下方法处理,日内连续测定高、中、低质量浓度各2组的峰面积,得到峰面积,根据标准曲线计算日内精密度;日间连续测定5 d高、中、低质量浓度的模拟生物样品,根据标准曲线计算日内、日间精密度。结果见表2。
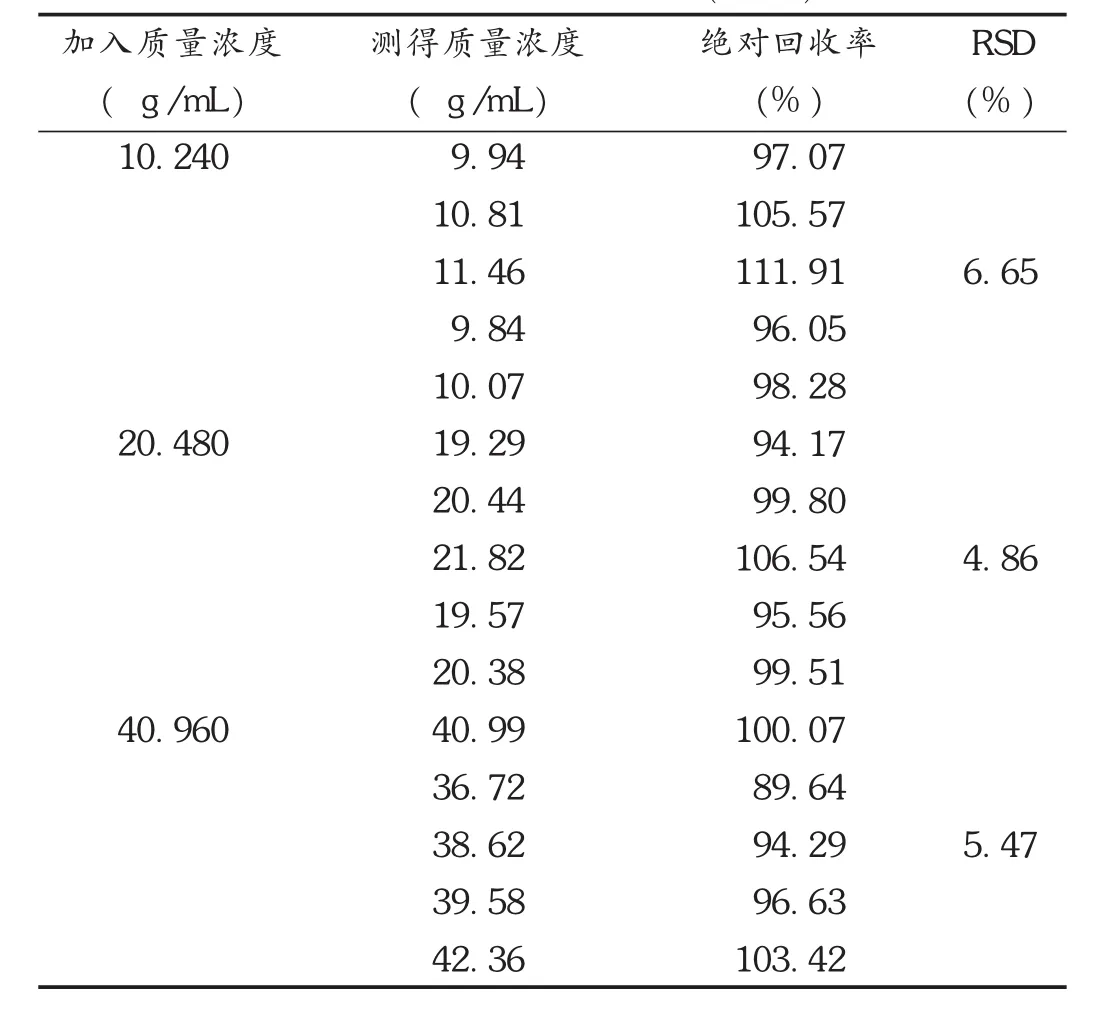
表1 LEV回收试验结果(n=5)
稳定性考察:分别精密移取系列质量浓度为128.0,128.0,256.0,256.0,512.0,512.0 μg/mL的20.0 μL LEV,各精密加入180.0 μL空白血清,置10 mL玻璃刻度具塞离心管中,按2.2项下处理方法进行处理,考察于-20℃低温保存4 d、反复冻融3次的稳定性,见表3。
2.5 临床标本测定
取临床血标本,2 000 r/min离心15 min,取上清液200.0 μL,置 10 mL刻度玻璃具塞离心管中,在氮气挥干装置下加入3.00 mL乙酸乙酯,涡旋振荡1 min,2 000 r/min离心 10 min,再在氮气挥干装置下取2.50 mL,置5 mL刻度玻璃具塞离心管中,把离心管放入40℃水浴锅中,小心用恒流氮气挥干,再加入100.0 μL甲醇复溶,进样20.0 μL。
本次试验临床标本来源:来自于测定奥卡西平(OXC)、硝西泮(NP)、氯硝西泮(CNP)、丙戊酸(VPA)、妥泰血药浓度的临床患儿,通过询问患儿家属服药情况,得知患儿同时服用LEV,于是收集临床标本,共计11例,收集好标本保存于-20℃的冰箱中。取出冷冻标本,按上述方法处理测定,测定结果见表4。
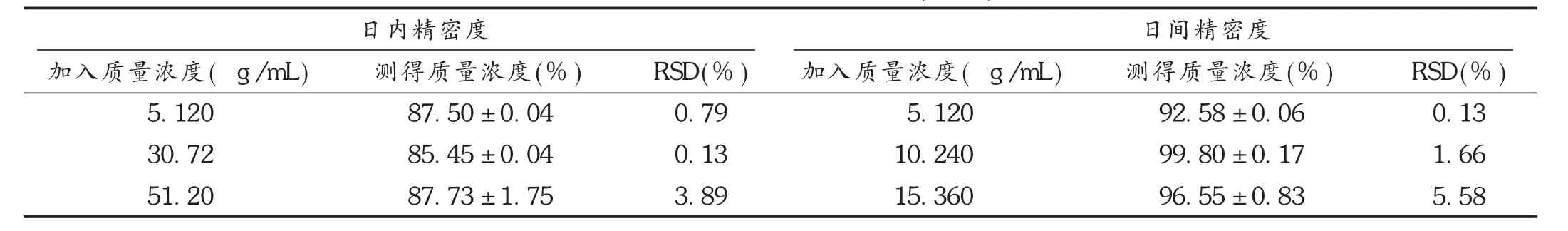
表2 LEV的精密度试验结果(n=5)
3 讨论
3.1 LEV药物监测(TDM)
LEV作为新药在中国上市,在儿科治疗中沿用中国成人参数是不科学的,需要建立儿童群体药代动力学模型指导儿童用药。国际TDM抗癫痫药物治疗指南认为,在特殊人群(如儿童、老年人和孕妇)服用癫痫药物时有必要对所用药物进行TDM;抗癫痫药物的剂量或剂型改变、联合用药需要做TDM;服用抗癫痫药物的患者有肝肾疾病或胃肠道疾病时也需要做TDM。
LEV抗癫痫常用于儿童,常与其他抗癫痫药物联用。本试验中收集的11例癫痫病患儿均为联合用药。根据癫痫患儿临床可能联合用药的情况,制备含 CBZ,CNP,LTG,NP,MHD,PB对照品的临床血清模拟样本,进行干扰试验,结果表明,CBZ,CNP,LTG,NP,MHD,PB几乎无色谱吸收,故联合用药对LEV测定几乎无干扰。本研究中临床标本分两次测定,第1次测定前6例,测定结果在5.38~12.57 μg/mL;第2次测定后5例,结果在5.28~7.95 μg/mL,有1例未测出,可能是患儿家属描述错误。本研究中收集的11例患儿都是联合用药,无单独用LEV治疗患儿,对LEV剂量与血药浓度相关分析,由表4可知,联合用药时LEV用药剂量与血药浓度间相关性不大。
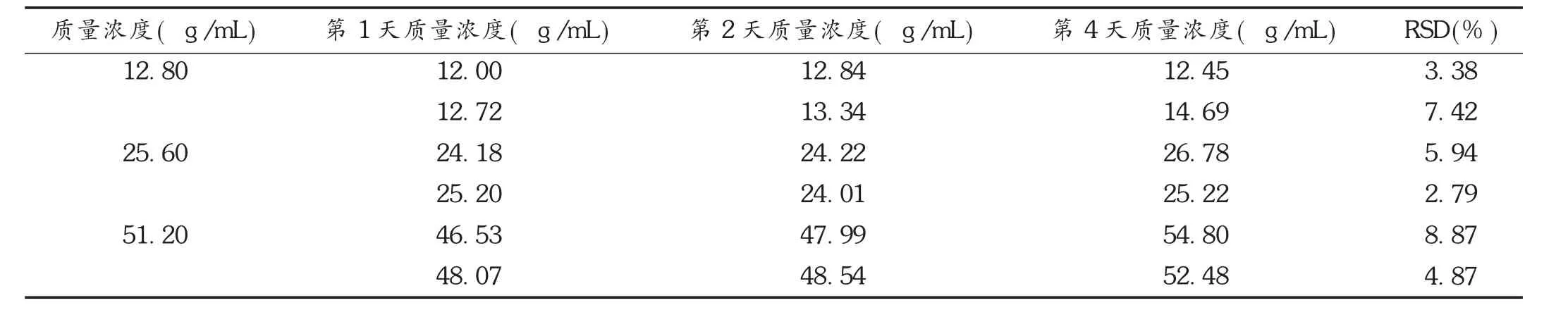
表3 LEV 反复冻融测定结果
3.2 萃取液选择
LEV易溶于水、乙醇、三氯甲烷等,乙腈中溶解,微溶于乙酸乙酯(在一定条件下,100 g乙酸乙酯溶解0.01~0.1 g LEV),以溶解度为0.01 g计算,3 mL乙酸乙酯能溶解LEV约为300 μg。本试验中的测定限性范围远小于300 μg,且乙酸乙酯对大多数药物的溶解性较好,易挥发,毒性小,液-液萃取较完全。采用乙酸乙酯,有利于LEV从血样中充分提取,而且乙酸乙酯位于萃取层的最上层,有利于吸取分层液的最上部,避免引入过多的内源性物质干扰测定[5]。

表4 11例服用LEV患儿服药情况及测定结果
3.3 流动相选择
流动相为甲醇-水(体积比20∶80)[4],进样20 μL,得到的峰形较宽,出峰时间约为3.3 min,出峰太早,临床标本中内源性物质干扰大。调整流动相比例为甲醇-水(15∶85),进样20 μL,出峰时间约为5 min,得到的峰形仍较宽,仍可考虑临床标本内源性物质会干扰。再调整进样量为 10 μL,流动相比例为甲醇 -水(15∶85),此时峰形稍好,出峰时间约为5 min,继续考虑临床标本内源性物质干扰大。流动相为磷酸盐缓冲液[磷酸氢二钠7.0 g,磷酸二氢钠(二水)[2]2.0 g,用温水溶解,加水至2 000 mL,用磷酸调节pH至4.0)-乙腈(90∶10),进样25 μL,出峰时间约为5.6 min,峰形较好,但目标峰前有一小峰分离不好,于是把流动相磷酸盐缓冲液与乙腈比例调整为93∶7,其他条件不变,得到的峰较对称,峰形较好,出峰时间约为7.8 min,临床标本内源性物质干扰几乎没有。
3.4 干扰试验、质控试验
采用只服用丙戊酸(VPA)的患儿血清配制模拟标本,由丙戊酸的化学结构可知,其无紫外吸收特征,并且每次都做空白对照,故排除了内源性物质的干扰。
LEV是一种新型抗癫痫药物,可使难治性偏头痛患者头痛发一频率下降50%以上[6]。LEV联合氟桂利嗪预防顽固性偏头痛能更好地改善颅脑血流动力学,增强临床疗效,虽有啬不良反应的趋势,但ADR可控[7]。
本试验中监测11例LEV患儿的血药浓度,其血药浓度范围为5.28~12.57 μg/mL,与Lancelin等[8]报道LEV有效血药浓度范围为12~46 μg/mL[3]有较大的差异,是否为联合用药等原因所致还有待进一步深入研究。
[1]金 超.LEV治疗小儿癫痫80例及智力分析[J].中国药业,2015,24(9):14-16.
[2]王 刚,张君梅,易晓燕,等.高效液相色谱法测定癫痫患儿血清中左乙拉西坦的浓度[J].中国新药与临床杂志,2011,30(6):476-480.
[3]周春华,张志清,何文娟,等.高效液相色谱法测定左乙拉西坦血药浓度[J].河北医科大学学报,2014,35(2):170-172.
[4]王慧颖,魏敏吉,王云秀,等.高效液相色谱法测定左乙拉西坦血药浓度[J].儿科药学杂志,2010,16(4):34-36.
[5]肖拥军,罗湘冀 .高效液相色谱法测定左乙拉西坦片的含量[J].广东药学院学报,2005,21(6):687-688.
[6]Krusz JC.Levetiracetam sa prophylaxis for resistant headaches[J].Cephalalgia,2001,21(4):2-12.
[7]李运良.左乙拉西坦联合氟桂利嗪预防顽固性偏头痛47例[J].中国药业,2015,24(1):80-81.
[8]Lancelin F,Franchon E,Kraoui L,et al.Therapeutic drug monitoring of levetiracetam by high-performance liquid chromatography with photodiode array ultraviolet detection:preliminary ovservations on correlation between plasma concentration and clinical response in patients with refractory epilepsy[J].Ther Drug Monit,2007,29(5):576-783.
Determination of Levetiracetam in Serum of Children with Epilepsy by HPLC
Li Rong1,Wang Gang2,Lü Fengjun2
(1.Chongqing Fuling Central Hospital,Chongqing,China 408000;
2.Children′s Hospital Affiliated to Chongqing Medical University,Chongqing,China 400014)
Objective To establish an HPLC method for the serum concentration of antiepileptic drug levetiracetam.M ethods Levirairacetam was extracted from serum by ethyl acetate using liquid-liquid extraction method,and was concentrated in a constant temperature water bath at 40℃ by constant nitrogen drying.After reconstituted with methanol,25 μL was injected.The RP-C18column(Shimadzu 150 mm×3.9 mm,5 μm)was used;the mobile phase was phosphate buffer(pH=4.0)-acetonitrile(93∶7,V/V),the detection wavelength was set at 210 nm,at a flow rate of 1.0 mL/min and the column temperature was 40℃.The chromatographic peak of levetiracetam was recorded,and the linear regression equation was made according to the peak area and fitted concentration.Results The linear regression equation was Y=46 853 X+23 250(r=0.999 8).The linear range was 5.120-51.20 μg/mL.Conclusion The method is proved to be suitable for the determination of serum samples,which can be used for the serum concentration in the clinic and in the pharmacokinetics study.
HPLC;levetiracetam;serum concentration;serum
R969.1;R971+.6
A
1006-4931(2016)23-0028-05
2016-08-11;
2016-09-20)

