枸橼酸坦度螺酮治疗抗抑郁药所致性功能障碍的疗效和安全性研究
顾成宇 邢葆平 张滢 任志斌
枸橼酸坦度螺酮治疗抗抑郁药所致性功能障碍的疗效和安全性研究
顾成宇 邢葆平 张滢 任志斌
目的 探讨枸橼酸坦度螺酮在新型抗抑郁药所致性功能障碍中的治疗作用。方法 选取82例符合DSM-IV-TR药物所致性功能障碍诊断标准的患者,按照随机数字表法1:1随机分为枸橼酸坦度螺酮研究组(研究组)41例和安慰剂对照组(对照组)41例,分别予枸橼酸坦度螺酮40mg/d和安慰剂治疗6周,在基线和治疗第2、4、6周进行临床评估,采用亚利桑那性体验量表(ASEX)和不良反应量表(TESS)评定疗效和不良反应。结果 研究组在第4、6周ASEX总分均低于对照组(P<0.05或0.01);研究组在治疗第2、4、6周ASEX总分低于基线(P<0.01)。对照组在第2、4、6周ASEX总分低于基线(P<0.01)。对照组ASEX总分第4周与第2周相比、第6周与第4周相比差异均无统计学意义(均P>0.05)。研究组TESS总分在第2周高于对照组(P<0.01)。两组TESS总分在基线、第4、6周差异无统计学意义。结论 枸橼酸坦度螺酮治疗抗抑郁药所致性功能障碍可能有较好的疗效,且不良反应少,存在一定的临床应用价值。
枸橼酸坦度螺酮 抗抑郁药 抗焦虑药 性功能障碍
新型抗抑郁药如选择性5羟色胺再摄取抑制剂(SSRIs)、5羟色胺和去甲肾上腺素再摄取抑制剂(SNRIs)在临床上使用越来越多,已经成为主要的抗焦虑、抗抑郁药物。但是新型抗抑郁药所致性功能障碍的发生率高达50%以上[1-2],其对患者生活质量影响和服药依从性的影响更不容小觑。事实上,性功能障碍在抑郁症症状尚未控制时,患者也许能够接受,但随着抑郁症状的改善,由于药物引起的性功能障碍严重地妨碍了患者的生活方式,影响家庭和谐,成为停药的主要原因[3-5]。有研究认为,抗抑郁药所致的性功能障碍与5-羟色胺1A(5-HT1A)受体阻断作用有关,且5-HT1A受体激动剂(如丁螺环酮)可以有效治疗抗抑郁药所致的性功能障碍[6-8]。枸橼酸坦度螺酮作为新型的5-HT1A受体激动剂,从精神药理学理论上说应该可以有效治疗抗抑郁药所致的性功能障碍,但目前尚未发现相应的临床研究。笔者对枸橼酸坦度螺酮治疗抗抑郁药物所致的性功能障碍进行临床对照研究,探讨其疗效及安全性,以便能更好地解决患者的实际问题。
1 对象和方法
1.1 对象 收集2013年1月至2015年6月我院精神科门诊患者82例,按随机数字表法分为研究组和对照组,各41例。研究组服用帕罗西汀12例,氟西汀5例,草酸艾司西酞普兰7例,文拉法辛缓释片8例,西酞普兰3例,舍曲林5例,度洛西汀1例;对照组服用帕罗西汀9例,氟西汀7例,草酸艾司西酞普兰11例,文拉法辛缓释片7例,西酞普兰5例,舍曲林2例,度洛西汀0例。两组患者年龄、性别、受教育程度(小学为1、初中为2、高中为3、大学为4、研究生及以上为5)、病程、复发次数、宗教信仰、药物种类、药物剂量以及基线HAMD-17和HAMA-14评分比较差异均无统计学意义(均P>0.05),详见表1。本研究获我院伦理委员会批准,所有患者签署知情同意书。

表1 两组患者一般资料的比较
1.2 纳入与排除标准 纳入标准:(1)符合美国精神疾病诊断与统计手册第4版修订版(DSM-IV-TR)药物所致性功能障碍的诊断标准,由2位主治及以上精神科医师独立诊断;(2)符合抑郁症缓解期的标准;(3)入组前汉密尔顿抑郁量表(HAMD)17项总评分≤10分(不是≤7分,因为抗抑郁药所致功能障碍可能会使该量表在抑郁症缓解时评分增高);入组前汉密尔顿焦虑量表(HAMA)14项总评分≤10分(不是≤7分,因为抑郁药所致性功能障碍可能会使该量表在焦虑症缓解时评分增高);(4)性别不限,已婚,年龄男性22~55岁,女性20~50岁且未绝经或月经规律紊乱;(5)服用新型抗抑郁药(SSRIs或SNRIs)中的某一种至少8周且剂量稳定至少4周;(6)经历持续性性功能障碍至少4周;(7)本人能签署知情同意书。排除标准:(1)任何使用枸橼酸坦度螺酮禁忌证;(2)除抗抑郁药外,服用能够导致性功能障碍的其他药物,如降压药、消化系统药、激素、抗肿瘤药、心血管药、前列腺癌的药物等;(3)有酒精、精神活性物质滥用史;(4)妊娠期、哺乳期妇女或者预期要在实验过程中怀孕的患者;(5)诊断为性功能障碍,但不是由抗抑郁药或者抑郁症引起者;(6)生殖器畸形;(7)伴或不伴卵巢切除的子宫切除术;(8)没有控制的其他精神疾病;(9)罹患有糖尿病、心脏疾病、脑卒中、心律失常;(10)性伴侣正在或者即将因为性功能障碍接受治疗者;(11)使用多种抗抑郁药或者在研究过程中可能改变抗抑郁药种类或者改变剂量者;(12)使用激素治疗的患者;(13)各种原因导致的无月经1年以上者;(14)性功能障碍与环境因素以及夫妻关系因素有关;(15)女性近3个月出现月经规律紊乱。
1.3 方法 研究组:继续服用原来治疗有效的抗抑郁药,同时加用枸橼酸坦度螺酮(大日本住友制药株式会社茨木工厂,每粒10mg),剂量为固定剂量40mg/d,平均分2次服用。对照组:继续服用原来治疗有效的抗抑郁药同时加用与枸橼酸坦度螺酮外形一样的安慰剂治疗,服药方法与干预组一致。医生对患者采用盲法评估,最后一例患者最后一次评分完成后进行揭盲。
1.4 疗效评价 在入组时(基线)和治疗第2、4、6周末进行患者自评亚利桑那性体验量表(ASEX)。ASEX分为男性用和女性用量表,共5个条目,均为6级评分(1~6分),分值越高,表明症状明显。由经过培训的精神科医师在基线和治疗第2、4、6周末评定不良反应量表(TESS)。HAMD-17项和HAMA-14项由经过培训的2位精神科医师仅在入组和6周末时评定。
1.5 统计学处理 应用SPSS 18.0统计软件,符合正态分布的计量资料采用表示,两组间比较采用t检验,组内不同时点资料比较采用重复测量方差分析(双侧)。计数资料组间比较采用χ2检验或Fisher确切概率法。
2 结果
2.1 两组患者ASEX量表的比较 两组患者基线ASEX总分差异无统计学意义;对照组在治疗第4、6周末评分大于研究组(均P<0.05)。研究组治疗6周后,ASEX分值明显下降,治疗第2、4、6周与基线相比均降低(均P<0.01),且第4周与第2周、第6周与第4周相比评分均有降低(均P<0.01);对照组第2、4、6周与基线比较均有降低(均P<0.01),但是对照组第4周与第2周、第6周与第4周相比差异均无统计学意义(均P>0.05),详见表2。

表2 两组患者ASEX量表的比较(分)
2.2 两组患者HAMD-17和HAMA-14评分的比较 治疗6周后,研究组HAMD-17和HAMA-14评分明显下降,与基线比较差异均有统计学意义(均P<0.01),而对照组分值评分基线后无明显下降;治疗第6周末,研究组比对照组分值评分明显下降(均P<0.01),详见表3。
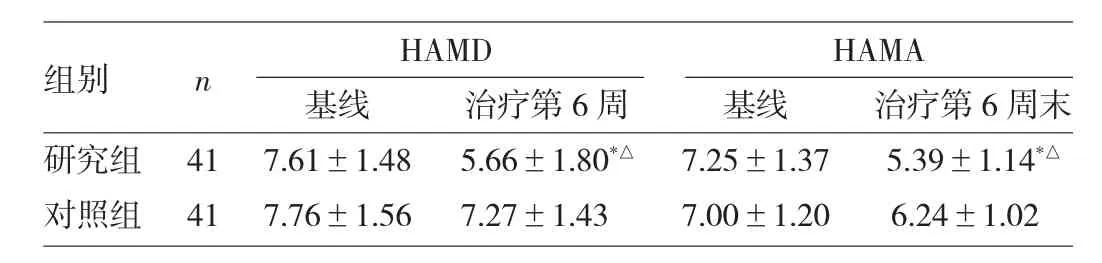
表3 两组患者HAMD-17和HAMA-14评分的比较(分)
2.3 两组患者不良反应的比较 两组患者TESS量表总分基线差异无统计学意义;治疗第2周末TESS总分研究组评分高于对照组(P<0.01),治疗第4、6周两组比较差异无统计学意义。研究组主要的不良反应为嗜睡、恶心、食欲下降等,但均比较轻微,无需特殊处理,且随着治疗的进展逐渐消退。研究组有1例在研究过程中出现AST轻度增高,给与护肝治疗后好转,详见表4。

表4 两组6周末TESS量表的比较
3 讨论
抗抑郁药的长期维持治疗已经成为世界各国抑郁症治疗指南的统一认识,如果一种药物,因为性功能障碍而被迫替换的话,可能面临诸多困难。首先,选择面窄,对抑郁症患者性功能影响较小的药物极为少见,换药有时难以做到;其次,其他药可能有其他不良反应;再者,也是更为重要的因素是,换药可能存在疗效欠佳而致病情复发的风险。而抗抑郁剂可能通过以下5种机制引起性功能障碍:(1)非特异性中枢神经作用,例如:镇静,影响性兴趣和性功能;(2)对中枢神经递质的特异性作用,例如引起多巴胺(DA)降低或5-HT增加;(3)通过神经递质对靶器官的外周作用,例如抗胆碱能药物通过影响外周肾上腺素/胆碱能平衡或α1肾上腺素能拮抗剂而导致阴茎异常勃起;(4)通过激素起作用,例如由于5-HT升高导致催乳素增加,从而引起性欲下降;(5)通过酶起作用,例如抑制硝酸氧化合成酶,该酶能催化阴茎和阴蒂内硝酸氧化物的生成[9]。根据以上作用机制,临床中常采用增加抗胆碱能药物、增加DA能药物、中枢兴奋剂,拮抗中枢5-HT能药物等治疗,但由于这些药物本身的不良反应,而未得到广泛使用。既往有用丁螺环酮治疗抗抑郁治疗所致性功能障碍的研究[10],且已经写入2010年的APA的抑郁症治疗指南中[11-12]。对丁螺环酮治疗SSRIs所致性功能障碍的机制尚存争议,一种推测是与其所具有的5-HT1A受体激动作用有关,另一种推测则认为疗效来源于丁螺环酮代谢后的产物具有α1肾上腺素能拮抗作用[13]。枸橼酸坦度螺酮作为新型的5-HT1A受体激动剂药物,从精神药理学理论上推测,对治疗抗抑郁药所致性功能障碍可能有效,虽然目前尚未发现相关临床研究文献。
本研究通过随机、双盲、安慰剂对照设计,探索枸橼酸坦度螺酮治疗新型抗抑郁药所致性功能障碍的疗效和安全性。本研究结果显示,枸橼酸坦度螺酮相比较安慰剂,能有效改善抗抑郁药所致性功能障碍。起效时间较快,第2周和基线相比ASEX总评分就有降低,这与之前的丁螺环酮研究结果较接近[8]。但是这种起效快的阳性治疗效应可能是安慰剂效应,因为安慰剂对照组在第2周与基线相比,ASEX总评分也有降低,且第2周两组之间比较ASEX总评分差异无统计学意义;但是安慰剂组在第4、6周与第2周相比,ASEX总评分差异无统计学意义;且与安慰剂组相比较,在第4、6周ASEX总评分差异有统计学意义。既往研究也表明,治疗抗抑郁药所致性功能障碍的药物可能存在安慰剂效应[10],但也有研究不支持该结论[14-15]。枸橼酸坦度螺酮组的不良反应与安慰剂比较在第2周增加,但均较轻,且很快消失,呈一过性的特征。
综上所述,枸橼酸坦度螺酮能有效治疗新型抗抑郁药所致性功能障碍,且不良反应少、程度轻且呈一过性,安全性高,耐受性好,可以作为治疗新型抗抑郁药所致性功能障碍的有效选择。由于本研究样本量较小,未作进一步的亚组分析,前者也是本研究局限所在。未来可以考虑进一步扩大样本量和进行多中心协作,进一步验证枸橼酸坦度螺酮在治疗新型抗抑郁药所致性功能障碍患者中的疗效和安全性。
[1] Kyoung-Uk Lee,Young Min Lee,Ji-Min Nam,et al.Antidepressant-Induced Sexual Dysfunction among Newer Antidepressants in a Naturalistic Setting[J].Psychiatry Investig,2010,7(1): 55-59.
[2] Montejo A L,Llorca G,Izquierdo J A,et al.Incidence of sexual dysfunction associated with antidepressant agents:a prospective multicenter study of1022 outpatients[J].J Clin Psychiatry,2001,62 (Suppl3):10-21.
[3] Alireza Zahiroddin,Farhad Faridhosseini,Azar Zamani,et al. Comparing the Efficacy of Bupropion and Amantadine on Sexual Dysfunction Induced by a Selective Serotonin Reuptake Inhibitor [J].Iran Red Crescent Med J,2015,17(12):e24998.
[4] Taylor MJ,Rudkin L,Bullemor-Day P,et al.Strategies for managing sexual dysfunction caused by antidepressants.Cochrane Summaries[J].Cochrane Database Syst Rev,2013,5:CD003382.
[5] BullS A,Hunkeler E M,Lee J Y.Discontinuing or switching Selective serotonin reuptake inhibitors[J].Ann pharmacother,2002,36 (4):578-584.
[6] Hu XH,BullS A,Hunkeler E M.Incidence and duration of side effects and those rated as bothersome with selective serotonin reuptake inhibitor treatment for depression:patient report versus physician estimate[J].J Clin Psychiatry,2004,65(7):959-965.
[7] Van RooijK,Poels S,Worst P,et al.Efficacy of testosterone combined with a PDE5 inhibitor and testosterone combined with a serotonin(1A)receptor agonist in women with SSRI-induced sexual dysfunction.A preliminary study[J].Eur J Pharmacol,2015, 753:246-251.
[8] 李一云,屠监源.丁螺环酮在42例抗抑郁药所致性功能障碍患者中的运用[J].中国新药与临床杂志,2004,23(11):813-815.
[9] 汤宜朗,蔡焯基.新型抗抑郁剂与性功能障碍[J].中华精神科杂志, 2000,33(1):58-60.
[10] David Michelson,John Bancroft,Steven Targum,et al.Female Sexualdysfunction Associated With Antidepressant Administration:A Randomized,Placebo-Controlled Study of Pharmacologic Intervention[J].Am J Psychiatry,2000,157:239-241.
[11] Alan J Gelenberg,Marlene P Freeman,John C Markowitz,et al. Practice Guideline for the Treatment of Patients With Major Depressive Disorder[J].Third Edition,2010,10.
[12] 赵靖平.2010版美国抑郁症治疗指南要点介绍[J].中华精神科杂志, 2012,45(3):177-180.
[13] Landen Mikael,Eriksson Elias,Agren Hans,et al.Effect of Buspirone on SexualDysfunction in Depressed Patients Treated With Selective Serotonin Reuptake Inhibitors[J].Journal of Clinical Psychopharmacology,1999,19(3):268-271.
[14] H.George Nurnberg,Paula L.Hensley,Alan J.Gelenberg,et al. Treatment of Antidepressant-Associated Sexual Dysfunction With Sildenafil:A Randomized Controlled Trial[J].JAMA,2003,289 (1):56-64.
[15] H.George Nurnberg,Paula L.Hensley,Julia R.Heiman,et al.SildenafilTreatment ofWomen With antidepressant-Associated Sexual Dysfunction A Randomized Controlled Trial[J].JAMA,2008, 300(4):395-404.
(本文由浙江省医学会精神病学分会推荐)
Efficacy and safety of tandospirone in treatment of sexual dysfunction associated with antidepressant administration
GU Chengyu, XING Baoping,ZHANG Ying,et al.Department of Psychiatry,Tongde Hospital of Zhejiang Province,Hangzhou 310012,China
【 Abstract】 Objective To evaluate the efficacy and safety of tandospirone in treatment of sexual dysfunction associated with antidepressant administration. Methods Eighty two depressive patients receiving antidepressant treatment for at least 8 wk in Tongde Hospital between January 2013 and June 2015,who met the criteria of DSM-IV-TR for sexual dysfunction associated with antidepressant were enrolled in the study.Patients were randomly assigned to receive a 6-week treatment with tandospirone (n=41,study group)or 6-wk treatment with placebo(n=41,control group).Outcomes were assessed by using Arizona Sex Experience Scale(ASEX)for efficacy and toxic exposure surveillance system(TESS)for side effects before treatment and at the end of 2nd,4th and 6th week after treatment. Results The ASEX scores at the end of 2nd,4th and 6th week were significantly lower than baseline scores in study group(P<0.01).The ASEXscores of study group were significantly lower than those of control group at the end of 4th and 6th week after treatment(P<0.05 or 0.01).The TEES scores of study group was higher than that of control group at the end of 2nd week(P<0.01),however,there were no significant differences at the end of 4th and 6th week between two groups. Conclusion Tandospirone is effective in ameliorating antidepressant-associated sexual dysfunction with mild and transitory adverse effects
Tandospirone Anti-depressive agents Anti-anxiety agents Sexualdysfunction
2015-11-24)
(本文编辑:严玮雯)
310012 杭州,浙江省立同德医院精神卫生科
邢葆平,E-mail:freewills@126.com

