160例消化性溃疡出血的病因及临床特点分析
张兴光 陈金梅 王佐妤 谢立群
·临床报告·
160例消化性溃疡出血的病因及临床特点分析
张兴光 陈金梅 王佐妤 谢立群
目前,消化性溃疡出血的发病机制已不再局限于幽门螺杆菌(Hp)感染,随着老龄化社会的进展,老年患者伴随基础性疾病增加,非类固醇类抗炎药物(NSAID)的应用越来越广泛,尤其抗血小板药物(阿司匹林)因在心脑血管疾病一级和二级预防中使患者受益而被广泛应用。然而,NSAID相关的胃肠道不良反应限制了其应用,比如可导致消化道出血、穿孔等,全世界每年NSAID相关胃溃疡及十二指肠球部溃疡的发生率在9%~22%,严重的出血或穿孔发生率<1%[1]。Hp、NSAID包括小剂量阿司匹林(50~150 mg/24 h,LDA)已成为消化性溃疡发病机制的独立危险因素。根除Hp能够治疗消化性溃疡,并能够预防溃疡复发已成为共识。然而NSAID相关的消化性溃疡常因症状不典型而易被忽视,认识其临床特点,早期及时预防治疗能够减少出血、穿孔的发生率,使患者受益。本研究通过分析160例消化性溃疡出血的临床资料,探讨其病因及临床特点,为提高临床诊治提供依据。
1 对象与方法
1.1 对象
纳入2014年1月至12月在武警后勤学院附属医院消化内科住院的消化性溃疡出血患者160例,其中男104例,女56例,年龄为14~82岁,平均(54.62±17.07)岁。其中22例NSAID相关性消化性溃疡出血患者伴随的基础疾病有冠心病或冠脉支架术后、房颤、高血压病、脑梗塞或脑支架术后、类风湿性关节炎、颈椎病、慢性头痛、颈胸腰椎间盘突出等。应用的药物包括阿司匹林肠溶片、美洛昔康片、氨基比林(去痛片)、双氯芬酸钠缓释片以及其他止痛药。
纳入标准:呕血、黑粪,呕吐物或隐血试验呈强阳性,24 h内完成胃镜检查明确消化性溃疡伴出血,既往无溃疡病史,住院期间完成肠镜检查且结直肠未见异常者。排除标准:呼吸道、口、鼻、咽部出血者,不除外小肠病变者,不同意行胃镜检查、资料不完整或未签署知情同意书者。
1.2 研究方法
1.2.1 资料收集 记录患者年龄,性别,入院时症状(包括腹痛、腹胀、嗳气、反酸、烧心、呕血、黑粪、有无休克),血红蛋白,尿素氮,血小板,凝血酶原时间,胃镜、肠镜结果,13C尿素呼气试验或血清Hp抗体,心脑血管疾病及用药情况(名称、剂量、服药时长),饮酒及吸烟情况。
1.2.2 分组 根据导致消化性溃疡的不同病因,分为Hp组、NSAID组、Hp+NSAID组及非Hp+NSAID组(包括饮食、心理因素、环境因素、遗传因素及不明原因)4组,分析并比较不同病因临床特点之间的差异。
1.3 统计学分析
采用SPSS13.0统计软件,数值变量以(均数±标准差)表示,计数资料样本率的比较采用χ2检验,计量资料采用两独立样本t检验。P<0.05表示差异有统计学意义。
2 结果
2.1 病因组成
在160例患者中,Hp组88例占55%,NSAID组22例占14%,Hp+NSAID组20例占12.5%,非Hp+NSAID组30例占18.7%,可知Hp组患者多于其他各组,且差异具有统计学意义(P<0.05)。
2.2 NSAID组与不同病因组临床特点的比较
研究显示,NSAID组平均年龄均高于Hp组及非Hp+NSAID组,差异具有统计学意义(P<0.05);NSAID组腹痛发生率低于Hp组及非Hp+NSAID组,差异具有统计学意义(P<0.05);NSAID组嗳气发生率均低于Hp组及Hp+NSAID组,差异有统计学意义(P<0.05);NSAID组黑粪及休克发生率、血红蛋白下降水平及尿素氮升高水平均高于Hp组,差异有统计学意义(P<0.05);NSAID组呕血发生率、尿素氮升高水平均高于非Hp+NSAID组,差异有统计学意义(P<0.05);NSAID组腹胀、反酸及烧心的发生率低于其余3组,但差异无统计学意义(P>0.05)。见表1。
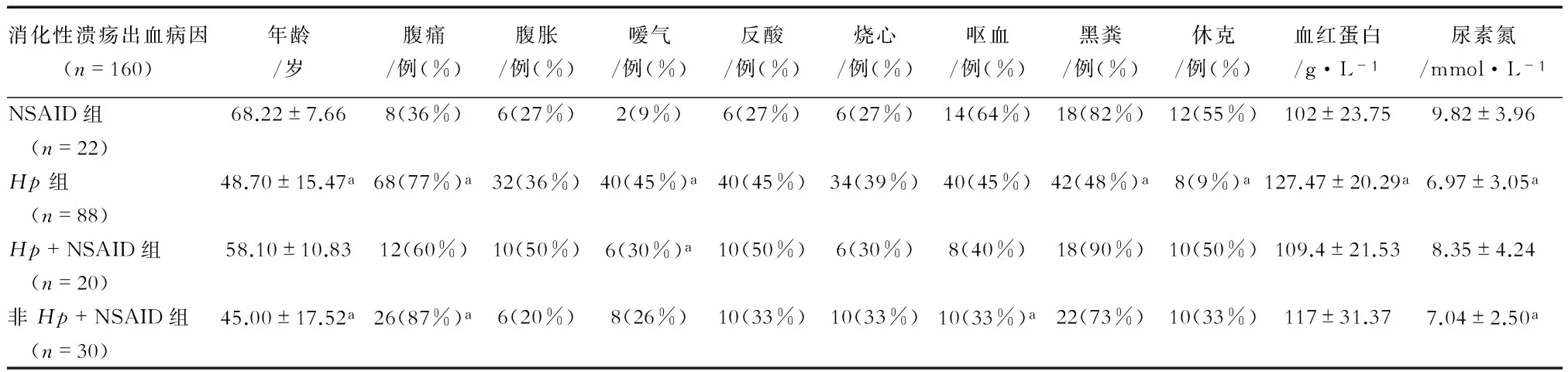
表1 消化性溃疡出血不同病因临床特点的比较
3 讨论
上消化道出血是指屈氏韧带以上的消化道出血,常表现为呕血、黑粪等,并伴有血容量减少引起的急性周围循环障碍,是临床常见急症,严重者可危及生命。多数研究认为,上消化道出血以消化性溃疡出血为主,占22%~67%,十二指肠球部溃疡比胃溃疡更常见。进入21世纪以来,随着内镜诊治水平的提高、Hp的根除以及抑酸药物的广泛应用,使消化性溃疡的发生率有所下降。芬兰一项回顾性研究收集了2000年至2008年共8 146例消化性溃疡住院患者的资料,发现消化性溃疡平均年发生率从2000年至2002年的121/10万下降至2006年至2008年的79/10万[2]。然而也有研究显示,消化性溃疡出血30 d的病死率仍然较高,并认为消化性溃疡的病因不再局限于Hp感染,NSAID已成为消化性溃疡出血的主要原因,且多发于老年患者[3]。有研究表明,患者的死亡原因很少直接为溃疡出血,而与并发症的加重导致心肺疾病的恶化相关[4]。Hp感染、NSAID是消化性溃疡发病机制的独立和重要的危险因素,并占据消化性溃疡病因的90%[5]。本研究对消化性溃疡出血的病因进行分析,发现Hp组患者明显多于其他各组,与文献报道基本相符[5]。
NSAID导致消化性溃疡分为直接及间接作用。大多数NSAID为弱有机酸,能够产生细胞毒作用,直接损伤胃肠黏膜细胞。间接作用指抑制环氧合酶(COX)发挥作用,包括COX-1和COX-2两种异构体,前者可促进前列腺素的合成而参与生理功能的调节,后者在病理条件下由炎性因子刺激诱导产生,可促使炎性前列腺素的合成。传统的NSAID(如LDA)特异性较差,同时抑制COX-1和COX-2,导致在黏膜防御和修复功能中起重要作用的前列腺素E合成不足,另一方面COX是花生四烯酸合成前列腺素的关键限速酶,NSAID 抑制COX可导致大量自由基的产生,共同作用下可导致消化性溃疡的发生[6]。LDA在NSAID中较为常用,与中国人口老龄化趋势明显,心脑血管疾病发生率上升有关,其可通过抑制血小板活化和血栓形成达到预防和治疗心脑血管疾病目的。已有大量临床研究证实,LDA治疗能够使血栓栓塞性疾病一级和二级预防的患者受益,包括心肌梗死、缺血性脑血管病、心绞痛、外周血管疾病及心房纤颤[7]。在本研究中,LDA主要应用于冠心病或冠脉支架术后、房颤、高血压病、脑梗塞或脑支架术后患者,而美洛昔康片、氨基比林(去痛片)、双氯芬酸钠缓释片等主要应用于类风湿性关节炎、颈椎病、慢性头痛、颈胸腰椎间盘突出的患者。一项包括9个随机对照试验共有100 076例一级预防心血管疾病的荟萃分析显示,LDA可使胃肠道出血的概率增至1.37倍[8]。在2000年至2007年间,英国初级保健卫生网络数据库观察了年龄在50~80岁、共38 077例服用LDA二级预防心脑血管患者,发现上消化道出血的年发生率在1.1‰[9]。另一项病例对照研究显示,接受LDA的患者与定期接受其他NSAID的患者其上消化道出血的发生率相似[10]。
本研究中NSAID相关性消化性溃疡出血具有以下临床特点:(1)NSAID组以老年患者居多,平均年龄较Hp组、非Hp+NSAID组明显增高,老年患者常常伴随心脑血管疾病、颈胸腰椎间盘突出等慢性疾病,需要抗凝、止痛或抗炎等药物治疗。另一方面老年患者前列腺素合成减少,更易出现NSAID相关消化道黏膜损伤。(2)NSAID组的临床特点不典型,腹痛症状发生率均低于其他组,一方面老年患者胃肠道黏膜对疼痛的敏感性下降,另一方面常合并脑梗塞、脑萎缩等基础疾病,不能够准确描述症状。相关文献报道也认为消化性溃疡出血患者的年龄越大,早期症状越不典型,预后越差[11-12]。一项前瞻性、开放式研究,评估了应用LDA超过3个月且无症状患者的胃肠黏膜的损伤程度,发现对于无症状患者,胃镜下消化性溃疡或糜烂性病变占47.83%[13]。也有研究认为,LDA相关消化性溃疡无症状患者占1/3[14]。(3)NSAID诱发消化性溃疡出血的程度严重,本研究中表现为NSAID组休克发生率、血红蛋白下降水平及尿素氮升高水平均高于Hp组,这与老年患者以巨大溃疡、不规则溃疡及多发溃疡多见,诊治不及时,黏膜愈合率下降,血管弹性差,凝血功能下降等有关。(4)NSAID相关消化性溃疡出血患者常以黑粪为首要表现,本研究中NSAID组黑粪发生率高于Hp组。对于服用NSAID的患者,尤其是年龄较大者,消化性溃疡的腹痛、反酸、烧心等症状常不典型,应进行知识教育及宣传普及,关注大便颜色,早发现早治疗。
Hp感染作为消化道出血的独立危险因素,对于长期服用NSAID的患者,根除Hp可降低溃疡和出血的复发概率。在本研究中,Hp+NSAID组发生率占12.5%,腹痛症状、出血程度与NSAID组比较差异无统计学意义。国内外指南推荐,在接受NSAID治疗前或正在接受NSAID治疗的患者应检测和治疗Hp。但近期有文献报道认为,Hp与NSAID作为消化性溃疡的出血危险因素,两者之间没有相互作用,根除Hp并不能降低NSAID相关消化性溃疡出血的发生率[15]。
目前研究认为,对于正在接受NSAID治疗的患者,同时使用抑酸药物可以有效降低上消化道出血的发生风险。如对于LDA使用患者,使用PPI不仅可以降低上消化道出血的发生率,而且在上消化道出血稳定后可以有效预防再出血,应用H2受体拮抗剂(H2RA)会有黏膜侵蚀的风险,但不会发展成溃疡。瑞典有研究报道,接受LDA治疗的患者其胃肠道溃疡的发生风险取决于是否坚持服用PPI[16]。在发生胃肠道出血后,许多患者停止LDA治疗,这会增加缺血性事件发生的风险,因此内科医生应鼓励这些患者继续口服LDA,同时预防性应用PPI。国内指南认为,不同PPI与氯吡格雷的相互作用存在差异,在抗血小板药物治疗的同时如需联合PPI治疗,应尽量避免使用奥美拉唑或埃索美拉唑[17]。朱国琴等[18]认为,前列腺素类药物、硫糖铝、表皮生长因子、替普瑞酮等胃黏膜保护剂的应用对于消化性溃疡的治疗及降低其复发率同样重要,可能与NSAID导致消化性溃疡的发病机制以及削弱胃黏膜的防御机制密切相关。
总之,Hp感染、NSAID可作为消化性溃疡发病机制的独立和重要的危险因素。对于NSAID治疗患者,消化性溃疡的腹痛症状不明显,常以呕血、黑粪等消化性溃疡出血入院,这类患者普遍年龄较大、基础疾病较多、出血程度严重,所以病死率较高。建议应严格掌握NSAID应用的适应证,同时预防性应用PPI治疗。
1 Shim KN, Song EM, Jeen YT, et al. Long-term outcomes of NSAID-induced small intestinal injury assessed by capsule endoscopy in Korea: a nationwide multicenter retrospective study[J]. Gut Liver, 2015, 9: 727-733.
2 Malmi H, Kautiainen H, Virta LJ, et al. Incidence and complications of peptic ulcer disease requiring hospitalisation have markedly decreased in Finland[J]. Aliment Pharmacol Ther, 2014, 39: 496-506.
3 Rosenstock SJ, Møller MH, Larsson H, et al. Improving quality of care in peptic ulcer bleeding: nationwide cohort study of 13,498 consecutive patients in the Danish Clinical Register of Emergency Surgery[J]. Am J Gastroenterol, 2013, 108: 1449-1457.
4 Quan S, Frolkis A, Milne K, et al. Upper-gastrointestinal bleeding secondary to peptic ulcer disease: incidence and outcomes[J]. World J Gastroenterol, 2014, 20: 17568-17577.
5 Hunt RH, Bazzoli F. Review article: should NSAID/low-dose aspirin takers be tested routinely for H. pylori infection and treated if positive Implications for primary risk of ulcer and ulcer relapse after initial healing[J]. Aliment Pharmacol Ther, 2004, 19: 9-16.
6 张文燕, 袁耀宗. 非甾体抗炎药的胃肠损害及其预防[J]. 药物不良反应杂志, 2008, 10: 190-194.
7 Antithrombotic Trialists′ Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients[J]. BMJ, 2002, 324: 71-86.
8 Raju N, Sobieraj-Teague M, Hirsh J, et al. Effect of aspirin on mortality in the primary prevention of cardiovascular disease[J]. Am J Med, 2011, 124: 621-629.
9 Cea Soriano L, Rodríguez LA. Risk of upper gastrointestinal bleeding in a cohort of new users of low-dose LDA for secondary prevention of cardiovascular outcomes[J]. Front Pharmacol, 2010, 1: 126.
10 Sakamoto C, Sugano K, Ota S, et al. Case-control study on the association of upper gastrointestinal bleeding and nonsteroidal anti-inflammatory drugs in Japan[J]. Eur J ClinPharmacol, 2006, 62: 765-772.
11 朱锦青. 不同年龄段上消化道出血患者临床特点及治疗措施探讨[J]. 白求恩医学杂志, 2015, 13: 80-81.
12 王薇, 付肖岩. 急性非静脉曲张性上消化道出血老年患者的临床特点分析[J]. 国际消化病杂志, 2014, 34: 358-360.
13 Niv Y, Battler A, Abuksis G, et al. Endoscopy in asymptomatic minidose aspirin consumers[J]. Dig Dis Sci, 2005, 50: 78-80.
14 Cryer B, Mahaffey KW. Gastrointestinal ulcers, role of aspirin, and clinical outcomes: pathobiology, diagnosis, and treatment[J]. J Multidiscip Healthc, 2014, 7: 137-146.
15 Sostres C, Carrera-Lasfuentes P, Benito R, et al. Peptic ulcer bleeding risk. The role of helicobacter pylori infection in NSAID/low-dose aspirin users[J]. Am J Gastroenterol, 2015, 110: 684-689.
16 Hedberg J, Sundström J, Thuresson M, et al. Low-dose acetylsalicylic acid and gastrointestinal ulcers or bleeding--a cohort study of the effects of proton pump inhibitor use patterns[J]. J Intern Med, 2013, 274: 371-380.
17 抗血小板药物消化道损伤的预防和治疗中国专家共识组. 抗血小板药物消化道损伤的预防和治疗中国专家共识(2012更新版)[J]. 中华内科杂志, 2013, 52: 264-270.
18 朱国琴, 施瑞华. 胃粘膜保护剂的研究进展[J]. 国际消化病杂志, 2006, 26: 311-313.
(本文编辑:周骏)
300162 天津,武警后勤学院附属医院消化内科
10.3969/j.issn.1673-534X.2016.05.017
2016-05-12)

