COPD急性加重合并活动性肺结核患者的危险因素及临床特征分析
谢一潋 褚金国 钱国清 李国祥
COPD急性加重合并活动性肺结核患者的危险因素及临床特征分析
谢一潋 褚金国 钱国清 李国祥
目的 分析慢性阻塞性肺疾病(COPD)急性加重合并活动性肺结核患者的危险因素及临床特征,以指导临床治疗。方法 选取COPD急性发作合并活动性肺结核患者42例(合并组)及同期单纯COPD急性发作的患者72例(对照组),比较两组患者的临床特征,并采用单因素分析及logistic回归分析其危险因素。 结果 两组患者的部分临床特征有统计学差异(均P<0.05)。单因素分析表明,吸烟史、营养不良、长期吸入糖皮质激素史及既往有肺结核史是COPD急性发作合并活动性肺结核的主要危险因素(均P<0.05)。多因素分析发现,营养不良(OR=4.100,95%CI∶1.471~11.431)、长期吸入糖皮质激素史(OR=2.695,95%CI∶1.078~6.739)及既往肺结核史(OR=11.102,95%CI∶3.076~40.065)为独立危险因素(均P<0.05)。结论 根据危险因素早期识别合并活动性肺结核的高危COPD患者,可尽早明确诊断,给予积极治疗。
慢性阻塞性肺疾病 肺结核 危险因素
慢性阻塞性肺疾病(COPD)是老年人常见的呼吸系统疾病,近来发现COPD急性加重的患者合并有肺结核的情况越来越多,发病率呈上升趋势,两种疾病互相影响并互相促进,严重威胁患者的生命。由于COPD与肺结核的临床表现相似,常造成误诊,给治疗带来困难。笔者对本院收治的COPD急性发作合并活动性肺结核患者的临床特征作一分析,并探讨两病并发的危险因素,以期指导临床治疗,现报道如下。
1 对象和方法
1.1 对象 本院2010年8月至2015年8月收治的COPD急性发作合并活动性肺结核患者42例(合并组),其中男37例,女5例,年龄56~94(73.67±8.14)岁;同期单纯COPD急性发作患者72例(对照组),其中男58例,女14例,年龄57~88(72.74±7.63)岁。两组患者性别、年龄比较均无统计学差异(均P>0.05)。
1.2 方法 回顾并比较两组患者的临床资料,包括性别、年龄、个人史、临床表现、辅助检查等情况。临床表现包括有无发热(体温>37.3℃)、咳嗽、咳痰、盗汗、消瘦、咯血等。辅助检查包括有无血白细胞升高(>9.5× 109/L)、贫血(Hb女<11.5g/dl,男<13g/dl)、ESR升高(男≤60岁:≥21mm/h,>60岁:≥43mm/h;女≤50岁:≥26mm/h,>50岁:≥38mm/h)、C反应蛋白(CRP)升高(>8mg/L)、Hb降低(<30g/L)、肺部多发病灶(影像学检查示多发病灶)等。本研究COPD急性发作的诊断标准:COPD患者在稳定状态下出现持续的状态恶化,超出平时的正常变异,并需要调整原来的治疗方案[1]。COPD急性发作合并活动性肺结核的诊断标准:COPD急性加重的患者由痰涂片找到抗酸杆菌,影像学检查提示肺部有可疑浸润性病灶,常规抗感染治疗效果不佳。
1.3 统计学处理 应用SPSS 21.0统计软件;计量资料以表示,两组间比较采用t检验;计数资料以构成比表示,两组间比较采用χ2检验;多因素分析采用logistic回归分析。
2 结果
2.1 两组患者临床特征的比较 见表1。
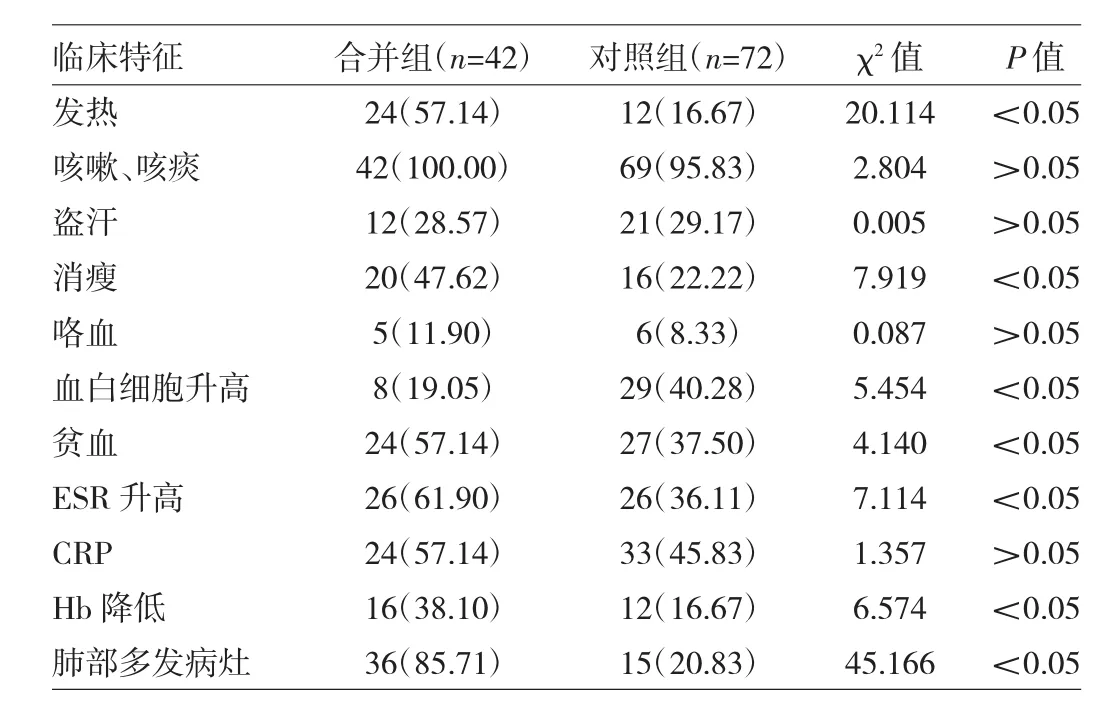
表1 两组患者临床特征的比较[例(%)]
由表1可见,合并组患者发热、消瘦、血白细胞升高、贫血、ESR升高、Hb降低及肺部多发病灶的比例较对照组升高,差异均有统计学意义(均P<0.05);两组患者咳嗽、咳痰、盗汗、咯血及CRP升高的比例比较均无统计学差异(均P>0.05)。
2.2 COPD急性发作合并活动性肺结核危险因素的单因素分析 见表2。

表2 COPD急性发作合并活动性肺结核危险因素的单因素分析[例(%)]
由表2可见,吸烟史、营养不良、长期吸入糖皮质激素史及既往有肺结核史是COPD急性发作合并活动性肺结核疾病发生的主要危险因素(均P<0.05)。
2.3 COPD急性加重合并活动性肺结核危险因素的多因素分析 根据单因素分析结果进行多因素分析,见表3。

表3 COPD急性加重合并活动性肺结核危险因素的多因素分析
由表3可见,营养不良、长期吸入糖皮质激素史及既往肺结核史为COPD急性加重合并活动性肺结核的独立危险因素。
3 讨论
COPD是一种具有气流受限特征的疾病,气流受限不完全可逆,呈进行性发展,与肺部对有害气体或有害颗粒的异常炎症反应有关[1]。患有COPD的患者免疫功能低下,更容易感染肺结核[2-3],因此COPD合并肺结核的患者日益增多。其在临床症状上常表现为咳嗽、咳痰、气促等不典型症状,与单纯COPD患者的临床症状有较多相似之处,易漏诊和误诊,延误患者的治疗,甚至威胁到患者的生命。本研究旨在通过分析COPD急性加重合并活动性肺结核患者的临床特征和危险因素来指导临床治疗。
从临床特征来看,COPD急性加重合并肺结核的患者更易有发热、消瘦的临床症状,实验室检查易出现贫血、低蛋白血症及高血沉的表现,而血白细胞一般不高,这些相较单纯COPD急性加重的患者,均有统计学差异;而咳嗽、咳痰、盗汗、CRP的鉴别诊断意义不大(无统计学差异);从影像学表现来看,合并组中有85.71%的患者表现为多发病灶混合存在,具有较高的鉴别诊断意义。
从危险因素来看,本研究的单因素分析表明,吸烟史、营养不良、长期吸入糖皮质激素史及既往有肺结核史是COPD急性加重合并活动性肺结核发生的主要危险因素。而多因素分析发现,营养不良、长期吸入糖皮质激素及既往肺结核史为独立危险因素。
吸烟是引起COPD最常见的致病因素,Caballero等[4]的研究发现,COPD病史与肺结核的发生有一定的相关性,而吸烟史会进一步增加这一相关性。Cao等[5]的研究也显示,吸烟对个体的肺功能、免疫功能和结核病的预后均有负面作用,通过病例对照研究发现主动吸烟是活动性肺结核发生的独立危险因素,吸烟强度与COPD、结核患病呈一致性,因此吸烟者更容易患COPD及肺结核,为COPD合并肺结核发病的危险因素。
本研究结果显示,营养不良是COPD急性加重合并活动性肺结核发生的独立危险因素。COPD患者多为老年患者,基础免疫力差,加上长期反复的咳嗽、咳痰、气促及肺部感染,容易导致营养不良及低蛋白血症,使免疫功能进一步下降,成为肺结核的易感人群。有研究显示,肺结核合并COPD患者的细胞免疫和体液免疫功能均受到较大的损害,受损程度较单纯肺结核患者更为严重[6]。
吸入性糖皮质激素为另一独立危险因素。在COPD长期的治疗过程中,随着气道气流受限加剧,需要通过糖皮质激素来控制和缓解病情,但糖皮质激素的使用,会影响COPD患者的免疫力,使感染肺结核的风险增加。Ernst等[7]研究发现,即使以前从未接受过全身激素治疗,长期吸入糖皮质激素的患者比普通人群更容易发生活动性肺结核(概率约是4倍);同时他们还发现,对于之前1年停用全身性糖皮质激素治疗的患者,吸入高剂量糖皮质激素也是活动性肺结核病发生的危险因素。另有研究也显示,长期吸入糖皮质激素会增加COPD患者合并结核病的风险,吸入糖皮质激素是胸部X线片尚正常的患者发生肺结核的独立危险因素[8]。
既往肺结核史也是COPD合并活动性肺结核发生的独立危险因素之一。很多COPD老年患者在年轻时曾感染过结核菌,结核菌素以稳定状态停止发展,潜伏在不同脏器。结核分枝杆菌会破坏肺的正常结构,造成呼吸道的不可逆损伤,使该部分患者比普通人群更易患COPD,且对于已经患有COPD的患者而言,肺结核所致的一些肺部损伤可进一步降低其原有的通气功能[9]。当患者年龄逐渐增大,肺功能进一步下降,COPD会反复发作,导致免疫功能受到抑制,使患者体内潜伏的结核病灶重新活动,造成结核发病。已有研究发现,COPD合并陈旧性肺结核的患者感染肺结核的风险要比单纯COPD患者感染的风险更大[10]。
因此在临床工作中,对于COPD急性加重的患者,特别是有吸烟史、营养不良、长期吸入糖皮质激素史及既往有肺结核史的患者,需高度警惕合并活动性肺结核的可能性,在治疗的同时要积极行痰涂片找抗酸杆菌检查,并行肺部CT检查,必要时支气管镜行肺泡灌洗或组织活检明确病理,以尽早明确诊断,给予积极治疗。
[1] 陈灏珠,林果为.实用内科学[M].北京:人民卫生出版社,2009:1743-1752.
[2] Chakrabarti B,Calverley P,Davies P D.Tuberculosis and its incidence,special nature,and relationship with chronic obstructive pulmonary disease[J].Inter COPD,2007,2(3):263-721.
[3] Ghimire H,LiJ.Role ofLatent Tuberculosis Infection in the Pathogenesis and Severity of COPD[J].Chest,2011,140(4 Meeting Abstracts):564A.
[4] Caballero A,Torres-Duque C A,Jaramillo C,et al.Prevalence of COPD in five Colombian cities situated at low,medium,and high altitude(PREPOCOLstudy)[J].Chest,2008,133(2):343-349.
[5] Cao J,Zhang L,LiD,et al.IL-27 is elevated in patients with C0PD and patients with pulmonary TB and induces human bronchial epithelialcells to produce CXCI10[J].Chest,2012,141(1):121-130.
[6] 沈芸,唐神结,孙华,等.肺结核合并慢性阻塞性肺疾病患者免疫功能的变化及意义[J].同济大学学报,2012,33(1):53.
[7] Ernst P,Suissa S.Systemic effects of inhaled corticosteroids[J]. Curr Opin Pulm Med,2012,18(1):85-89.
[8] Salvi S S,Barnes P J.Chronic obstructive pulmonary disease in non-smokers[J].Lancet,2009,374(9691):733.
[9] 吴俐健,邹博,吴立华,等.老年慢性阻塞性肺病合并肺结核临床分析[J].中国老年学杂志,2011,31(8):1308-1310.
[10] Kim J H,Park J S,Kim K H,et al.Inhaled corticosteroid is associated with an increased risk of tuberculosis in patients with chronic obstructive pulmonary disease[J].Chest,2013,143(4): 1018.
Risk factors of acute exacerbation of chronic obstructive pulmonary disease in patients with active pulmonary tuberculosis
XIE Yilian, CHU Jinguo,QIAN Guoqing,et al.Department of Infectious Disease,Ningbo First Municipal Hospital,Ningbo 315000,China
Objective To analysis the risk factors ofacute exacerbation ofchronic obstructive pulmonary disease(COPD)in patients with active pulmonary tuberculosis(sputum positive). Methods The clinical data of 42 active pulmonary tuberculosis patients with acute exacerbation COPD(case group)and 72 patients with acute exacerbation COPD(controlgroup)admitted in the same period were analyzed.Univariate analysis and multivariate logistic regression were used for statistical analysis. Results Univariate analysis revealed that smoking history,malnutrition,history oflong-term intake ofinhaled cortieosteroids(ICS),history of tuberculosis were associated with exacerbation of COPD combined with pulmonary tuberculosis(all P<0.05).Multivariate logistic regression analysis identified malnutrition(OR=4.100,95%CI:1.471~11.431),history of long-term ICS intake(OR=2.695,95%CI: 1.078~6.739)and history of tuberculosis(OR=11.102,95%CI:3.076~40.065)were independent risk factors for exacerbation of COPD combined with pulmonary tuberculosis. Conclusion The high-risk acute exacerbation COPD patients with tuberculosis infection should be identified according to risk factors and the appropriate management should be given to improve therapeutic efficacy.
Chronic obstructive pulmonary disease Pulmonary tuberculosis Risk factor
2015-10-19)
(本文编辑:李媚)
宁波市科技计划项目(2013A610233)
315000 宁波市第一医院感染科
谢一潋,E-mail:suger842003@163.com

