3-(2-噻吩)丙烯酸的合成工艺研究
董乙文,严 丽,王晓丽,褚朝森*,
(1. 江苏联合职业技术学院 连云港中医药分院,江苏 连云港 222007; 2. 连云港市药物研发共性技术中心,江苏 连云港 222007)
3-(2-噻吩)丙烯酸的合成工艺研究
董乙文1,严 丽2,王晓丽1,褚朝森*1,2
(1. 江苏联合职业技术学院 连云港中医药分院,江苏 连云港 222007; 2. 连云港市药物研发共性技术中心,江苏 连云港 222007)
以噻吩-2-甲醛为原料,与磷酰基乙酸三乙酯在氢化钠存在下反应制备 3-(2-噻吩)丙烯酸乙酯,后通过水解制备3-(2-噻吩)丙烯酸,总收率78.5%,纯度98.6%,可制备121 g每批。考察了原料滴加速度、物料摩尔比、溶剂用量、柱层析硅胶用量对化合物2合成的影响,确定了最佳条件为:滴加速度8 mL/min、噻吩-2-甲醛与膦酰基乙酸三乙酯摩尔比为1:1.2,溶剂1.6 L,柱层析用硅胶与粗产物重量比为1:15,该步反应收率92.3%,水解后产物经重结晶获得纯品,收率85%。产物结构通过质谱、核磁鉴定正确。
3-(2-噻吩)丙烯酸; 磷酰基乙酸三乙酯; 水解
α,β-不饱和羧酸是有机酸家族的典型代表,可用于合成多种医药中间体和抗菌药物[1,2],同时,它们也是多种天然产物的结构组成部分[3]。由于应用广泛,其合成备受学者关注。3-(2-噻吩)丙烯酸是最简单的杂环α,β-不饱和羧酸之一,具有不饱和羧酸的典型特征,可用于合成多种具有应用价值的化合物[4-6]。
3-(2-噻吩)丙烯酸的合成已有报道。Taduri, Ashok Kumar等[7]以噻吩-2-甲醛为原料,通过Knoevenagel反应与丙二酸作用制备目标化合物,该方法技术成熟,原料便宜易得,但反应过程需要高温甚至微波反应,操作不便;Tang, Yi-Qiang[8]等以2-溴噻吩为原料,与丙烯酸作用制备目标化合物,该反应体系需要金属钯催化剂的参与,且反应过程需要惰性气体保护,成本高且操作不易;Schweizer, Stephane等[9]以 2-碘噻吩为原料,与丙烯酸甲酯作用制备目标化合物,反应体系需要金属钯催化剂的参与,并且以致癌物乙腈为溶剂,成本高,毒性大;Lawrence Camillo Creemer 等[10]通过噻吩-2烯腈的水解制备目标化合物,方法简单易操作,但原料不易购买,市场不可得。总体看来,3-(2-噻吩)丙烯酸的合成存在着成本高、毒性大、操作困难的缺点,寻找一种低成本、易操作的合成方法具有现实意义。本研究以此为切入点,用噻吩-2-甲醛为原料,依据Horner-Wadsworth-Emmons反应原理,设计合成了目标产物,在小试的基础上进行了放大实验,成功制备了百克级产品,为其工业化提供参考。
1 实验部分
1.1 材料与仪器
反应用原料噻吩-2-甲醛为分析纯,购自国药集团化学试剂有限公司;磷酰基乙酸三乙酯、氢化钠均为化学纯,购自南京鳄鱼试剂公司;柱层析用硅胶200~300目(青岛海洋化工厂)。
1HNMR在德国Bruker公司AM500MHz共振仪上测定;质谱(MS)在德国SPECTRO(ICP-MS)仪器上测定;熔点在上海申光 WRS-2型熔点仪上测定;纯度在日本岛津高效液相色谱仪(LC-2010型)上测定。
1.2 方法
3-(2-噻吩)丙烯酸的合成路线见图1。

图1 3-(2-噻吩)丙烯酸的合成路线Fig.1 The synthetic route of 3-(2-thienyl)acrylic Acid
1.2.1 化合物2的制备
在5 L的圆底烧瓶中,加入称量好的膦酰基乙酸三乙酯1.2 mol(269 g)和1.6 L二氯甲烷,开启电动搅拌,冰水浴下,缓慢加入氢化钠1.2 mol(29 g),自然升温至室温,用恒压滴液漏斗加入噻吩-2-甲醛1 mol(112 g)的250 mL二氯甲烷溶液,TLC监测反应,当反应结束后加入事先配制好的饱和氯化铵溶液1.6 L,搅拌使其分层,有机相用饱和碳酸氢钠溶液和饱和氯化钠溶液洗涤,浓缩除去溶剂,柱层析纯化得淡黄色油状产物 2,该步反应收率92.3%。
1.2.2 化合物3的制备
取上步反应产物0.92 mol,于10 L四口玻璃反应瓶中加入二氯甲烷7.2 L,甲醇800 mL,开启电动搅拌,加入2 mol/L氢氧化钠的甲醇溶液800 mL,保持室温,TLC监测反应,当反应结束后,浓缩除去溶剂,加入4 L水溶解,异丙醚2 L萃取除去未水解的酯,水相用1mol/L的盐酸水溶液调节pH至2~3,用乙酸乙酯1 L萃取3次,合并乙酸乙酯相,加入无水硫酸钠干燥,浓缩(-0.09 MPa)除去溶剂得白色固体产物,甲醇重结晶得纯品121 g,该步反应收率85%。
两步反应总收率 78.5%;熔点 145~147 ℃;MS:154.1(M+);1HNMR(CDCl3):δ=6.24(d,1H,CH=);7.07(m,1H,CH=);7.30(t,1H,CH=);7.42(d,1H,CH=);7.89(d,1H,CH=)。1.3 高效液相色谱(HPLC)检测产物纯度
色谱柱:岛津Shim-pack VP-ODS型色谱柱(150 mm × 4.6mm,5μ m)
流动相:乙腈:水=75:25
检测波长:254 nm;柱温:35 ℃;进样量:10μ L;流速:1.0 mL/min。
2 结果与讨论
文献[11]对该反应小试实验条件的优化已做了详细说明,在此不再赘述,在进行放大实验的过程中发现,依照文献条件进行比例放大遇到了困难,通过尝试,发现噻吩-2-甲醛的加入方式和速度、物料摩尔比、溶剂用量、柱层析硅胶用量等因素对反应的影响较大,实验对以上因素进行了考查,并对水解放大反应进行了解析。
2.1 噻吩-2-甲醛的加入方式和速度对反应影响
依据文献方法进行放大实验,原料噻吩-2-甲醛增加至1 mol(112 g),发现向反应体系中加入原料时容易产生大量气泡,需要将其稀释后添加,经过尝试,将原料配制成250 mL的二氯甲烷溶液采用恒压滴液漏斗加入比较合适,然而滴加速度不同导致反应液的颜色产生明显变化,实验考查了不同滴加速度下反应液呈现的状态,结果见表1。
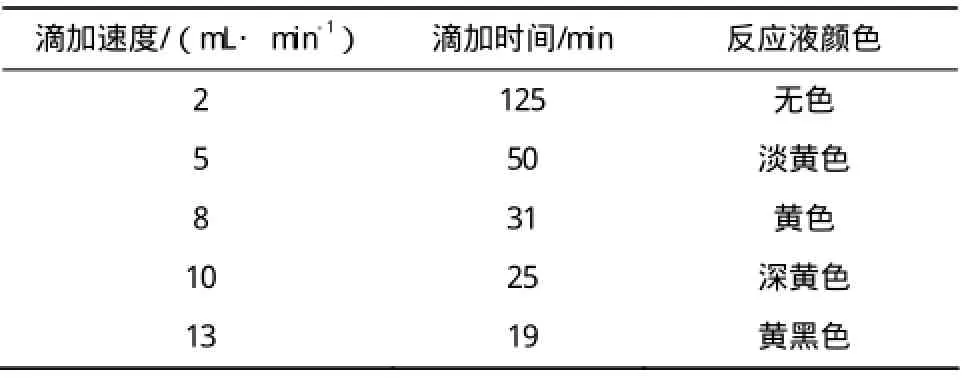
表1 滴加速度对反应的影响Table 1 The influence of dropping speed on the reaction
实验结果表明,滴加速度越快反应液颜色越深,滴加速度为2 mL/min时,需要滴加125 min,时间最长;当滴加速度为13 mL/min时,滴加需要的时间最短,仅19 min,然而反应液的颜色呈现黄黑色,后处理需要采用活性炭脱色,增加了工作量,不利于工业化;综合考虑,滴加速度为8 mL/min时,半小时内可以滴加完,需时较短,反应液颜色为黄色,对后续反应影响不大,无需脱色处理,故最佳滴加速度为8 mL/min。
2.2 物料摩尔比对反应的影响
文献中确定的最佳物料摩尔比为噻吩-2-甲醛、磷酰基乙酸三乙酯摩尔比为1:1.5,由于磷酰基乙酸三乙酯过量,放大反应后是纯化所要去除的主要杂质,实验以化合物2的收率为考查指标,用噻吩-2-甲醛1 mol(112 g),研究了不同情况下对反应的影响,结果见表2。
研究结果表明,膦酰基乙酸三乙酯的用量减少直接导致反应时间延长,当比例大于1:1.2时收率在90%以上,降至1:1.1以下,需要的反应时间大幅度提升,收率显著下降。这是由于膦酰基乙酸三乙酯用量的减少导致反应不完全,原料噻吩-2-甲醛和产物2的极性非常接近,柱层析纯化不彻底导致产物部分浪费。综合考虑,1:1.2的比例反应时间适中,产物有较高的收率(92%),为最佳反应比例。
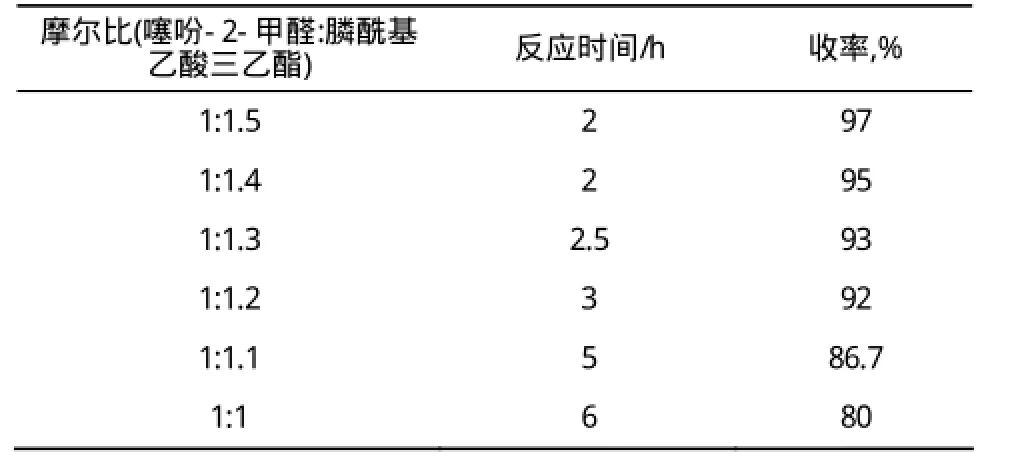
表2 物料摩尔比对收率的影响Table 2 The influence of mole ratio on the yield
2.3 反应溶剂用量对收率的影响
依据小试实验所用溶剂量进行比例放大,会导致反应处理量太大,适当缩小溶剂用量是工业化过程中需要解决的关键问题。实验用噻吩-2-甲醛1 mol,磷酰基乙酸三乙酯1.2 mol,室温下,考查二氯甲烷不同用量对反应收率的影响,结果见表3。

表3 溶剂用量对收率的影响Table 3 The influence of solvent dosage on the yield
实验结果表明,溶剂用量减少,反应时间逐渐缩短,这是由于反应液浓度增大,分子接触的概率增大,反应加快。收率随着溶剂量的减少出现了不同的变化趋势,在溶剂量为1.8 L时收率最高,达到93.5%,随后出现了下降的趋势。当溶剂量减少到一定程度时(小于1.4 L),反应液浓度过大,在加入氢化钠时,大量气泡产生,且产生的热量不易散去,使得反应液发黑,影响了反应的进行,导致收率明显下降。对比溶剂用量1.6 L和1.8 L时的收率,比较接近,而1.6 L的溶剂量时的反应时间有着明显的优势,从工业化的角度出发,优选 1.6 L为最佳溶剂用量。
2.4 硅胶用量对纯化过程的影响
化合物2为液体,无法用重结晶的方法纯化,反应中多余的磷酰基乙酸三乙酯如果不去除,在下一步水解反应中会以黄色粘稠状固体的形式出现,不利于终产物的纯化,且水解消耗大量的氢氧化钠,不经济,故选择柱层析纯化将其去除。实验考查了粗产物2和硅胶的不同重量比情况下,柱层析溶剂(乙酸乙酯与石油醚体积比为1:20的混合溶剂)的用量及对收率的影响,结果见表4。
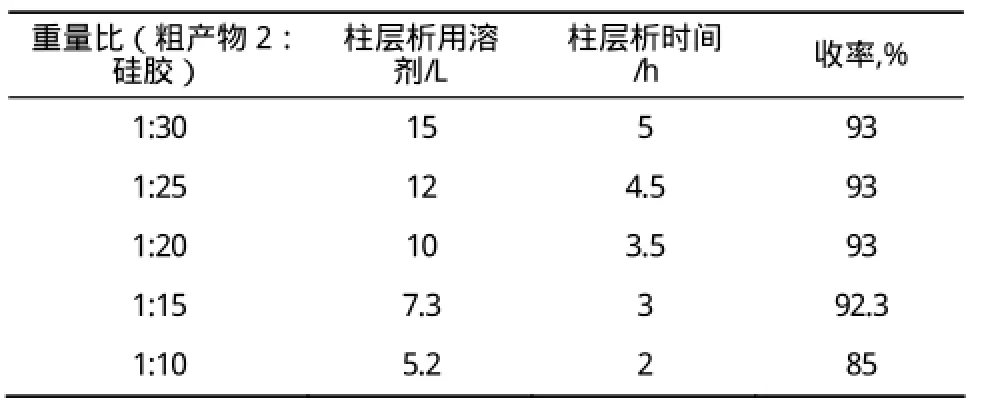
表4 硅胶用量对收率的影响Table 4 The influence of silica gel dosage on the yield
实验结果表明,硅胶用量越大,需要的层析溶剂越多,消耗的层析时间越长。当硅胶用量大于1:20时,分离效果相同,收率最高,均为93%。当硅胶用量为1:15时,需要的溶剂量较少,需要时间适中(3 h),收率较高,为92.3%。当硅胶用量低至1:10时,溶剂用量最少,耗时最短,但分离效果最差,损失较大,收率仅为85%。综合考虑,1:15的比例最佳。
综上所述,原料噻吩-2-甲醛用量为1 mol(112 g)的前提下,化合物2的制备最佳条件为:噻吩-2-甲醛与膦酰基乙酸三乙酯摩尔比为1:1.2,溶剂用量为1.6 L,柱层析用硅胶与粗产物重量比为1:15,该步收率为92.3%,可制得化合2产品168 g。
2.5 水解反应
方法,用二氯甲烷与甲醇体积比为9:1的混合溶剂进行水解,3-(2-噻吩)丙烯酸乙酯与氢氧化钠摩尔比为 1:1.6,氢氧化钠最终浓度为 0.18 mol/L,室温下搅拌反应,约45 min时产生白色沉淀3-(2-噻吩)丙烯酸钠盐,该盐不溶于甲醇和二氯甲烷。随着时间的推移,沉淀物不断蓄积,约4小时,TLC监测水解基本完全。调节pH至2~3后,用乙酸乙酯萃取3-(2-噻吩)丙烯酸的效果明显优于二氯甲烷,可制得 136 g 3-(2-噻吩)丙烯酸,纯度为96.7%,为进一步提高纯度,采用经甲醇重结晶后得121 g纯品,收率85%,液相色谱检测产物纯度98.6%,符合外商采购要求。
3 结 论
以磷酰基乙酸三乙酯和噻吩-2-甲醛为原料,反应制得3-(2-噻吩)丙烯酸乙酯,经水解得到3-(2-噻吩)丙烯酸。通过研究确定了最佳反应条件为:原料滴加速度8 mL/min、噻吩-2-甲醛与膦酰基乙酸三乙酯摩尔比为1:1.2,溶剂用量为1.6 L,柱层析用硅胶与粗产物重量比为1:15,两步反应总收率为78.5%,可制备121 g每批。
该方法反应条件温和,操作简便,成本低,为3-(2-噻吩)丙烯酸的进一步工业提供了参考。
[1] Marquardt U,Schmid D, Jung G. Racemic Synthesis of the New Antibiotic Tetramic Acid Reutericyclin [J]. Synlett , 2000(8):1131-1132.
[2] Jiangao Song,Manfred Hesse. Synthesis of (±) tetrahydromyricoidine [J]. Tetrahedron,1993,49(31):6797-6804.
[3] Bellassoued M,Gaudemar M. Stereoselective synthesis of (E)- α, β -unsaturated acids from C,O,O-tri (trimethylsilyl) ketene acetal and aldehydes[J]. Tetrahedron Lett.,1988,29(36):4551-4554
[4] Otake, Kazuya,Azukizawa, Satoru,Fukui, Masaki,et al. Novel (S)-1,2,3,4-tetrahydroisoquinoline-3-carboxylic acids: Peroxisome proliferator-activated receptor γ selective agonists with protein-tyrosine phosphatase 1B inhibition[J]. Bioorganic and Medicinal Chemistry,2012,20(2):1060-1075
[5] Zhang, Lijing,Li,Yan,Wang,Ke,et al. Synthesis and anti-proliferative activity evaluation of sorafenib derivatives with a 3-arylacryloyl hydrazide unit[J]. Medicinal Chemistry Research,2015,24(4):1733 -174.
[6] Zhang Hong-Jia,Zhu Di-Di,Li Zi-Lin,et al. Synthesis, molecular modeling and biological evaluation of β-ketoacyl-acyl carrier protein synthase III (FabH) as novel antibacterial agents [J]. Bioorganic and Medicinal Chemistry,2011,19(15):4513-4519.
[7] Taduri, Ashok Kumar,Devi, B. Rama. Alum-Cs2CO3as a New Recyclable Solid Base Catalyst for the Efficient Syntheses of Arylidenemalononitriles, Esters and Arylcinnamic Acids in Water[J]. Asian Journal of Chemistry,2014,26(7):1938-1942.
[8] Yi-Qiang Tang, Chun-Yan Chu, Lei Zhu,et al. N-Heterocyclic carbene–Pd(II) complex derived from proline for the MizorokiHeck reaction in water [J]. Tetrahedron,2011,67(49): 9479-9483
[9] Schweizer, Stephane, Becht, Jean-Michel, Le Drian, Claude. Development of Efficient and Reusable Diarylphosphinopolystyrene-Supported Palladium Catalysts for C-C Bond Forming Cross-Coupling Reactions[J]. Advanced Synthesis and Catalysis,2007,349(7):1150-1158.
[10] Lawrence Camillo Creemer, Janice Rhea Herring, Edward Deorsey McGruder. Immunopotentiator agents: US, 6664271[P].2003-12-6
[11] 褚朝森,王晓丽,胡玉涛,等. 一种肉桂酸及其衍生物合成新方法研究[J]. 应用化工,2015,44(3):442-44.
Research on synthesis of 3-(2-Thienyl)acrylic Acid
DONG Yi-wen1,YAN Li1,WANG Xiao-li1,CHU Chao-sen1,2
(1. Lianyungang TCM Branch of Jiangsu Union Technical Institute,Jiangsu Lianyungang 222007,China;2. Lianyungang Common Technological Center for Drug Research and Development,Jiangsu Lianyungang 222007,China)
Using 2-thenaldehyde as starting material, ethyl 3-(2-thienyl)acrylate was synthesized with triethyl phosphonoacetate in the presence of sodium hydride. 3-(2-thienyl)acrylic acid was prepared through hydrolysis of the ester in 78.5% total yield. 121 g per batch can be synthesized with 98.6% purity. The reaction conditions such as dropping speed, reactant ratio, solvent dosage, silica gel dosage were studied. The best reaction conditions were determined as follows:the dropping speed 8 mL/min, 2-thenaldehyde and triethyl phosphonoacetate mole ratio 1:1.5, solvent 1.6 L, silica gel and crude product weight ratio 1:15.The yield of ethyl 3-(2-thienyl)acrylate reached 92.3%. The pure product with 85% yield was prepared via hydrolysis and recrystallization. Its structure was characterized by mass spectrometry and nuclear magnetic.
3-(2-thienyl)acrylic acid; triethyl phosphonoacetate; hydrolysis
TQ 201
A
1671-0460(2016)11-2517-04
江苏省青蓝工程培养基金(2014)。
2016-10-12
董乙文(1963-),男,江苏省连云港市人,中级实验师,毕业于北京中医药大学中药专业,研究方向:从事药学服务与开发研究。E-m ail:498997974@qq.com。
褚朝森(1982-),男,副教授,硕士,研究方向:生物有机合成。E-m ail:chuchaosen@126.com。

