经冠状窦心室起搏与传统右室起搏超声特征比较
马雪娟,赵玲,王钰,郭涛,李琳,孙旭杜,闫世然
· 论著 ·
经冠状窦心室起搏与传统右室起搏超声特征比较
马雪娟1,赵玲1,王钰1,郭涛1,李琳1,孙旭杜1,闫世然1
目的 比较经冠状窦(CS)心室起搏与传统右室起搏患者超声心动图指标变化特征。方法 选取2012年12月~2014年5月于昆明医科大学第一附属医院符合常规心脏起博治疗适应证患者50例,随机分为传统右室起搏和经CS心室起搏,最终32例患者行传统右室起搏,18例经CS心室起搏。所有患者分别于术前、术后3月、6月、1年行超声心动图检查,收集指标包括心脏左、右房室内径、左室射血分数(LVEF)、左室短轴缩短率(LVFS),反映左室内收缩同步性指标左室12节段收缩达峰时间标准差(TS-12-SD)、三尖瓣反流面积(TRA)。结果 32例患者行右室起搏,其中男性16例,平均(64.47±11.40)岁,18例患者行CS心室起搏,其中男性11例,平均(62.22±12.95)岁,两组患者术前所有基线指标包括人口学特征、疾病构成及伴随疾病、起搏器植入类型及用药比较差异无统计学意义(P>0.05);术前两组所有超声指标差异无统计学意义(P>0.05);两组患者术前TS-12-SD均高于正常值;术后3月、6月及1年随访CS心室起搏组LVEF及LVFS高于右室起搏组,差异有统计学意义(P<0.05);术后1年CS心室起搏组TS-12-SD恢复正常,与术前比较差异有统计学意义(P<0.05)。结论与右室起搏相比,经CS起搏可提高左室收缩功能,改善左室内同步性。
心脏起搏;冠状静脉窦;心室起搏;超声心动图
传统右室起搏因操作简便、固定容易、脱位率低、起搏可靠被广泛应用于临床,但其影响左室电机械活动、损伤心室收缩同步性、减低射血分数、增加三尖瓣反流等诸多弊端近年被研究和证实[1-3]。国外陆续相关报道[4,5]及本课题组前期研究[6]证实经冠状窦(CS)心室起搏为三尖瓣人工瓣膜置换术患者提供有效、安全、可行的起搏方式。但因经CS起搏在常规心脏起搏中缺乏大样本、多中心研究证实其可行性、安全性及有效性,故未被广泛应用于临床。在本课题组前期研究证实[7]经CS心室起搏安全可行的基础上,拟通过超声心动图对经CS心室起搏与传统右室心内膜起搏患者随访观察,收集血流动力学相关超声指标,比较二者对于心脏结构和功能、左室收缩同步性、三尖瓣反流等影响,为经CS心室起搏可行性及优势等提供科学依据。
1 资料与方法
1.1 研究对象及分组 选取2012年12月~2014年5月于昆明医科大学第一附属医院心内科住院符合2008年ACC/AHA/HRS心律失常器械治疗指南普通心脏起搏Ⅰ类适应证患者并植入普通起搏器,包括双腔起搏器(DDD)或心室按需型起搏器(VVI)患者共50例,其中男性27例,女性23例,年龄35~83岁;合并冠心病9例,高血压15例,糖尿病12例,入选患者在手术前后规律服用药物。本研究通过伦理委员会批准,所有患者均签署知情同意书。纳入标准:符合2008年ACC/AHA/HRS心律失常器械治疗指南普通心脏起搏Ⅰ类适应证患者;年龄18~85周岁;同意入组、能配合随访者。排除标准:严重心力衰竭心功能Ⅳ级(NYHA分级)者;肥厚型梗阻性心肌病患者;伴有心房颤动;合并原发性肝、肾器质性病变、严重感染性疾病、精神疾病及恶性肿瘤患者,预期寿命不超过1年者;不愿配合随访者。50例入选对象均完成术后一年随访。50例患者随机分为右室起搏组及经CS心室起搏组,经CS心室起搏电极植入失败者改为右室起搏。32例患者施行右室起搏,其中男性16例,女性16例,年龄35~83岁,平均(64.47±11.40)岁;18例患者行经CS心室起搏,其中男性11例,女性7例,年龄35~78岁,平均(62.22±12.95)岁。
1.2 手术方法 右室起搏组采用右室心尖部翼状被动电极或间隔下部螺旋主动电极跨过三尖瓣口植入右心室流出道或心尖部;经CS心室起搏组采用普通翼状心室电极(图1)或用经CS专用左室电极(图2)通过CS口植入进入分支静脉固定电极。若心室电极起搏参数不满意,尝试调整电极深度或进入其他分支,若反复尝试后仍无法获得满意参数,改行传统右室起搏。
1.3 随访情况及评价指标收集 分别于术前、术后3月、6月、1年对所有研究对象进行超声心动图检查。每次超声检查均由研究者本人进行操作,使用设备为德国Siemens Acuson Sequoia 512超声诊断仪,配有“syngo”速度向量成像技术脱机分析工作站,4V1C探头,频率2.0~4.0 MHz。本研究选用速度向量成像技术是基于二维斑点追踪原理上的一种分析方法,其能准确追踪组织内超声斑点,判断斑点相互位置时间,在心肌长轴、短轴和圆周方向上量化任意点结构力学参数。选用的分析左室同步性指标为左室12节段达峰时间标准差(TS-12-SD),参考YU等[8,9]在多项研究中应用速度向量成像技术测量左室不同区域峰值速度和达峰时间,将二尖瓣水平及二尖瓣乳头肌水平两个短轴平面的前间隔、前壁、前侧壁、下侧壁、下壁及后间隔一共12个节段室壁收缩达峰时间标准差定义为左室同步指数,当TS-12-SD>34 ms时,提示左室内收缩不同步。
患者取左侧卧位,平静呼吸,连接体表心电图,二维超声测量左、右房室内径,M型超声测量左室收缩功能,TRACE勾勒法描记TR面积。启动速度向量成像模式,选取清晰心尖四腔心、两腔心、三腔心切面及胸骨旁二尖瓣水平、乳头肌水平短轴切面,连续采集三个心动周期二维动态灰阶图像储存后以待脱机分析。随后进入速度向量成像脱机分析工作站,将图像定帧在收缩期,手工逐点描记心内膜边界,选取两个左室短轴切面的前间隔、前壁、前侧壁、下侧壁、下壁及后间隔6个点自动跟踪分析得出上述一共12个节段室壁各节段100%收缩达峰时间及达峰时间标准差。所有指标均测量3次,取平均值记录。
1.4 统计学分析 采用SPSS 20.0统计软件包进行分析。计数资料以例数(百分比)表示,组间比较采用χ2检验,计量资料以均数±标准差(±s)表示,先经过正态性和方差齐性检验,符合正态分布组间比较采用独立样本t检验,重复测量设计计量资料采用重复测量方差分析,以P<0.05,为差异具有统计学意义。
2 结果
2.1 研究对象基线资料 共50例患者入选,32例行右室起搏,其中男性16例,女性16例,年龄35~83岁,平均(64.47±11.40)岁,其中病态窦房结综合征(SSS)18例,三度房室传导阻滞(三度AVB)7例,二度房室传导阻滞(二度AVB)7例,其中合并冠心病6例,高血压8例,糖尿病7例,服用β受体阻滞剂12例,血管紧张素转换酶抑制剂/血管紧张素受体拮抗剂(AECI/ ARB)7例,钙通道阻滞剂6例,他汀类药物6例;18例患者行经CS心室起搏,其中男性11例,女性7例,年龄35~78岁,平均(62.22±12.95)岁,其中SSS 9例,三度AVB7例,二度AVB2例,其中合并冠心病3例,高血压7例,糖尿病5例,服用β受体阻滞剂4例,AECI/ARB4例,钙离子拮抗剂4例,他汀类药物3例。右室起搏组共植入DDD起搏器28例,VVI起搏器4例,CS组植入DDD起搏器16例,VVI起搏器2例。两组患者入选年龄、性别、病因构成、伴随疾病、口服药物治疗情况及起搏器植入类型比较差异无统计学意义(P>0.05)(表1)。
2.2 两组患者术前超声指标比较 术前两组左右房室内径、室壁运动幅度、心脏收缩功能、左室收缩同步性及TRA等超声指标比较,差异无统计学意义(P>0.05);术前两组TS-12-SD均高于正常值(>34 ms)(表2)。
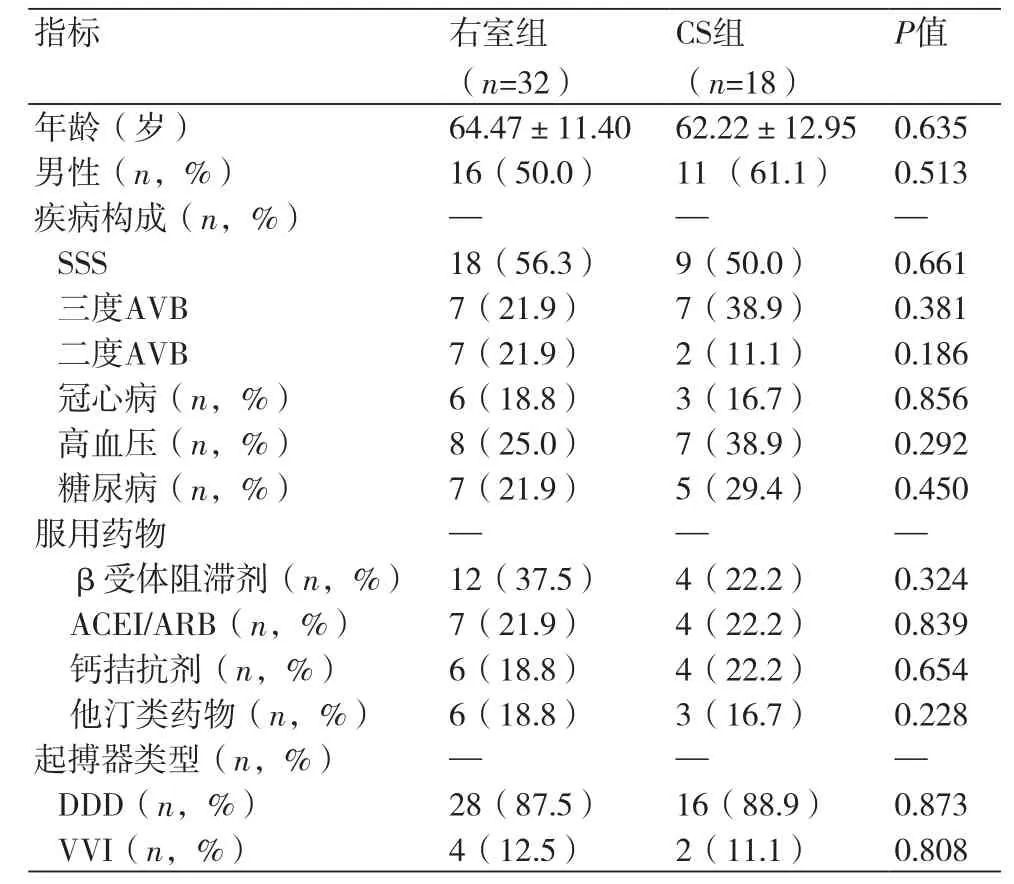
表1 研究对象基线资料比较
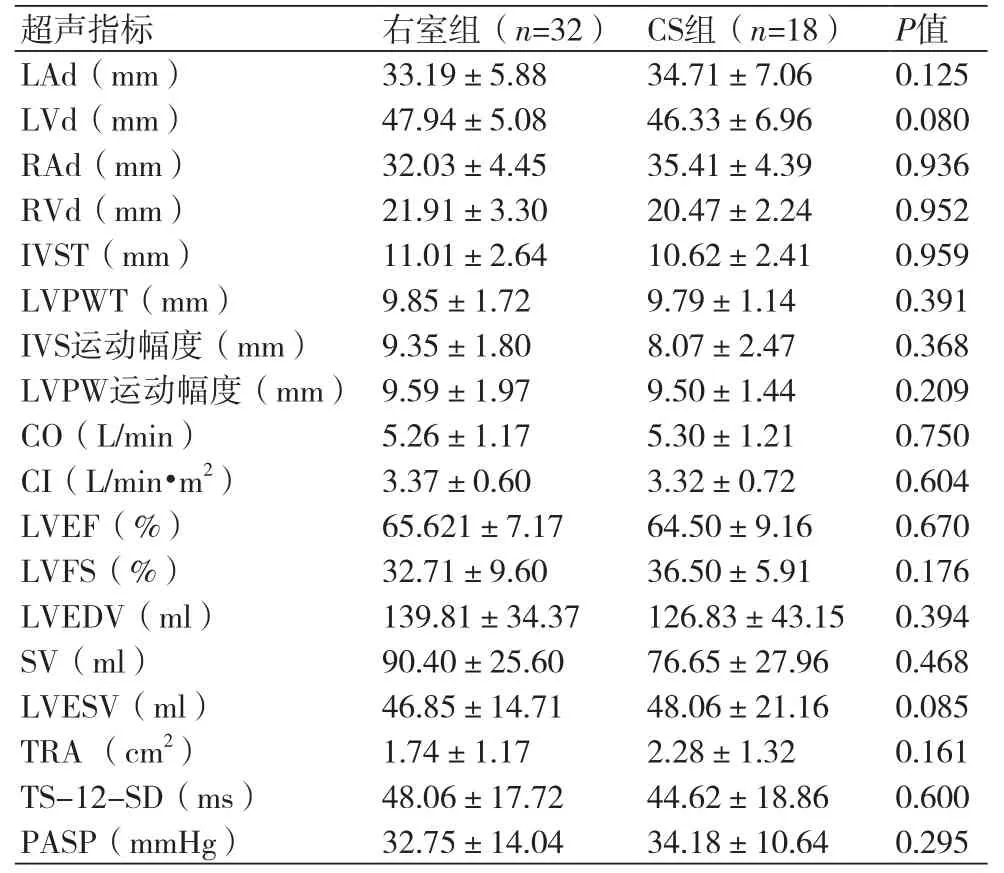
表2 两组术前各超声指标比较
2.3 两组患者术后超声指标比较 与术前相比右室起搏组术后所有超声指标均未出现显著变化(P>0.05)。与术前相比经CS起搏组术后TS-12-SD逐渐下降并恢复于正常范围内,差异有统计学意义(P<0.05)。术后两组间比较,经CS起搏组LVEF、LVFS值均高于右室起搏组,差异有统计学意义(P<0.05)。右室起搏组术后TRA虽呈逐渐增加趋势,差异无统计学意义(P>0.05),经CS起搏组则TR面积变化不明显(表3)。
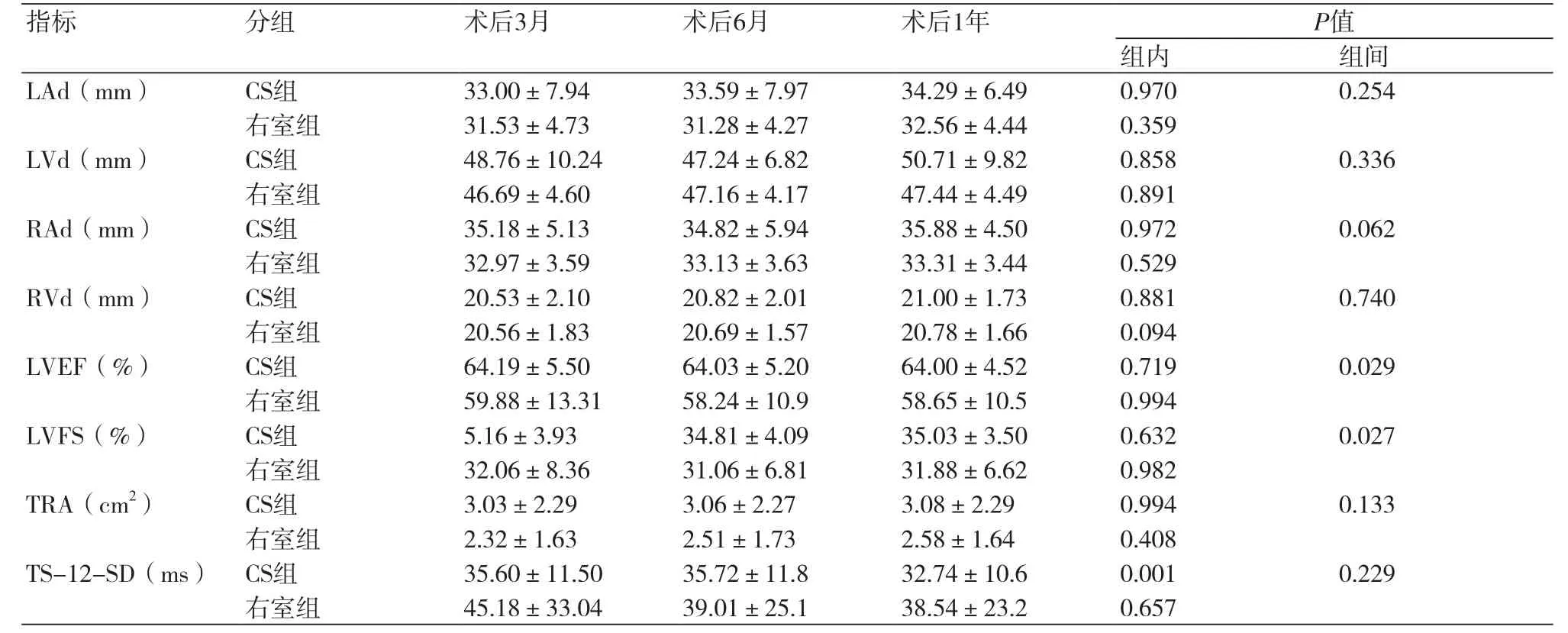
表3 术后组内及组间超声指标变化比较
3 讨论
长期右室起搏使电激动沿希浦系逆向、缓慢传导,不同于心肌正常激动传导,引起医源性左束支传导阻滞,导致心功能恶化及心室重构,增加患者心衰住院率,且引起右室内膜局部病理变化,如心肌细胞结构破坏、营养不良性钙化等,导致心室丧失运动协调性及心肌结构受损[10,11]。2012年Henry Dreger等[12]研究发现右室起搏超过15年即会出现心脏扩大,心脏功能减低,诱发“起搏器诱导心肌病”。本研究随访一年,传统右室起搏术后与术前相比,心脏结构及收缩功能等超声指标未发生明显变化,分析可能与样本量小,随访时间短相关,需要大样本、长期随访发现右室起博与心脏结构出现变化的时间节点。
右心室植入电极引起异常TR最重要原因是电极导线对三尖瓣直接产生机械性影响,包括瓣叶穿孔、导线缠绕三尖瓣环、导线撞击瓣叶及导线黏附于瓣叶等;其次是右室心尖部起搏造成房室舒缩顺序发生变化,引起右室机械不同步,导致TR出现或增多[13-15]。但是目前右室电极导线介导TR缺乏相关前瞻性、流行病学、诊断及治疗资料,尚无专家共识表明在右室电极植入后多久会出现TR。在电极植入后数周内或几个月内电极导线引起TR出现并不多见,Webster等[16]报告平均年龄16岁的123例儿科起搏器亚组随访资料,在右室起搏电极植入术前与术后1年和2年做了超声心动图对比研究,发现术后1年内起搏器随访未发现TR恶化,而2年后TR增加(P<0.02)。经CS起搏可彻底避免起搏电极对三尖瓣产生撞击、撕裂、粘连、缠绕等机械性损伤,彻底规避电极导线介导TR风险。该优势也为本课题研究目的之一,在32例的传统右室起搏组中,电极导线对TR的影响并表现出差异性变化,仍需要对纳入研究对象进行长期随访。
此外,经CS心室起搏为三尖瓣置换术后患者提供心室起搏的替代路径。心室电极通过三尖瓣机械瓣膜实施右室起搏时,随着心脏周期瓣膜不断开放和关闭对电极形成持续剪切力,可引起机械瓣卡瓣及右室电极断裂;即使是三尖瓣生物瓣,电极会损伤瓣膜,使瓣膜使用寿命缩短,因此为三尖瓣置换术后的患者施行传统右室起搏存在绝对风险。并且与二次开胸手术将电极缝在心外膜,或通过穿刺房间隔途径将电极植入左室心内膜等方法相比,经CS心室起搏有创伤小、风险小、安全、简便优势。加之右室腔残留废弃电极或右室电极导线反复脱位的患者CS起搏成为替代路径。
本研究发现,在起搏器植入术后,经CS起搏组LVEF、LVFS值均高于右室起搏组,并且经CS电极植入后TS-12-SD明显降低,并恢复于正常范围内,表明经CS植入心室电极可使心脏收缩功能提高、左室收缩同步性更好。在解剖上CS参与后间隔的构成,其属支心大静脉走行于左侧房室沟内,心中静脉走行于后室间沟;希氏束沿室间隔膜部左侧下行,右心室流出道后间隔下部、三尖瓣环1~2点、二尖瓣环10~11点位置均属于希氏束区域,冠状静脉窦系统与希氏束系统二者在解剖位置上存在交叉,尝试将起搏电极置于CS属支静脉内,起搏激动可进一步靠近希氏束,模拟希氏束起搏。当电极植入分布于左室侧壁的CS分支静脉如心大静脉、侧后静脉时,则实现左室心外膜起搏;当起搏电极植入心中静脉时,则起搏点在后室间隔处,使电激动传导更趋向中心性。
经CS起搏心室模式模仿了右房左室起搏的心脏再同步化治疗(CRT)起搏模式。本研究团队曾对心力衰竭患者施行右房左室起搏做过许多探索[17-19],如配合设置频率适应性房室间期(AVd)实现单左室起搏,发现优化药物治疗基础上右房左室起搏模式效果不劣于标准双心室起搏。普通起搏器植入适应症的患者多合并有高血压、冠心病、糖尿病等原发疾病,心功能受到不同程度的影响,且随着疾病的发展心脏会逐渐扩大,出现心功能不全等症状。可将经CS心室起搏的获益应用于存在心衰风险的常规起搏上,则可能收获延缓心脏器质性病变进程、降低心衰发生率风险、相比CRT手术降低操作复杂程度、降低医疗费用等益处。综上所述,从超声心动图指标变化上来说,经CS心室起搏相对于传统右室起搏有保持心脏收缩功能、提高心脏收缩同步性、不增加TR等优势。样本量少,随访时间短是本研究的局限性,需进一步扩大样本量继续随访研究。
[1] Dreger H,Maethner K,Bondke H,et al. Pacing-induced cardiomyopathy in patients with right ventricular stimulation for >15 years[J]. Europace,2012,14(2):238-42.
[2] Ahmed FZ,Khattar RS,Zaidi AM,et al. Pacing-induced cardiomyopathy: pathophysiological insights through matrix metalloproteinases.[J]. Heart Fail Rev, 2014, 19(5):669-80.
[3] 王秋林,周鹏,蔡国才,等. 长期右心室尖起搏致起搏诱导性心肌病临床分析[J]. 实用医学杂志,2013,29(1):64-6.
[4] Iskandar SB,Ann Jackson S,FahrigS,et al. Tricuspid Valve Malfunction and Ventricular Pacemaker Lead: Case Report and Review of the Literature[J]. Echocardiogr,2006, 23(8):692-7.
[5] Grimard C,ClémentyN,FauchierL,et al. Ventricular Pacing Through Coronary Sinus in Patients With Tricuspid Prosthesis[J]. Ann Thorac Surg,2010,89(6):51-2.
[6] 郭涛,华宝桐,赵玲,等. 三尖瓣置换术后完全性房室传导阻滞经冠状静脉窦实现DDD起搏一例13年随访[J]. 中国心脏起搏与心电生理杂志,2013,(5):460-1.
[7] 孙旭杜,李淑敏,赵玲,等. 经冠状窦植入永久心室电极实现心室起搏方法学初探[J]. 临床内科杂志,2014,31(4):279-80.
[8] Yu CM,Fung WH,Lin H,et al. Predictors of left ventricular reverse remodeling after cardiac resynchronization therapy for heart failure secondary to idiopathic dilated or ischemic cardiomyopathy[J]. Am J Cardiol,2003,91(6):684-8.
[9] Yu CM,Lin H,Fung WH,et al. Comparison of acute changes in left ventricular volume, systolic and diastolic functions, and intraventricular synchronicity after biventricular and right ventricular pacing for heart failure[J]. Am Heart J, 2003,145(5):846.
[10] Manolis AS. The Deleterious Consequences of Right Ventricular Apical Pacing: Time to Seek Alternate Site Pacing[J]. Pacing Clin Electrophysiol,2006,29(3):298-315.
[11] Thambo JB,Bordachar P,Garrigue S,et al. Detrimental Ventricular Remodeling in Patients With Congenital Complete Heart Block and Chronic Right Ventricular Apical Pacing[J]. Circulation,2004,110 (25):3766-72.
[12] Dreger H,Maethner K,Bondke H,et al. Pacing-induced cardiomyopathy in patients with right ventricular stimulation for >15 years[J]. Europace, 2012,12(3):311-21.
[13] Lin G,Nishimura RA,Connolly HM,et al. Severe Symptomatic Tricuspid Valve Regurgitation Due to Permanent Pacemaker or Implantable Cardioverter-Defibrillator Leads[J]. J Am Coll Cardiol, 2005,45(10):1672-5.
[14] Vaturi M,Kusniec J,Shapira Y,et al. Right ventricular pacing increases tricuspid regurgitation grade regardless of the mechanical interference to the valve by the electrode[J]. Euro J Echocardiogr, 2010,11(6):550-3.
[15] Pfannmueller B,Hirnle G,Seeburger J,et al. Tricuspid valve repair in the presence of a permanent ventricular pacemaker lead[J]. Euro J cardiothorac surg,2011,39(5):657-61.
[16] Webster G,MargossianR,Alexander ME,et al. Impact of transvenous ventricular pacing leads on tricuspid regurgitation in pediatric and congenital heart disease patients[J]. J Interv Card Electrophysiol, 2008,21(1):65-8.
[17] 蒲里津,刘可,骆志玲,等. 右室感知触发左室起搏心脏再同步化治疗慢性充血性心力衰竭[J]. 中国心脏起搏与心电生理杂志,2011,25(6):488-92.
[18] Pu LJ,Wang Y,Zhao L,et al. Cardiac resynchronization therapy (CRT) with right ventricular sense triggered left ventricular pacing benefits for the hemodynamics compared with standard CRT for chronic congestive heart failure: A cross-over study[J]. Cardiol J,2014,22(1):80-6.
[19] 蒲里津,王钰,郭涛,等. 双腔起搏器频率适应性AV单左室起搏实现心脏再同步化治疗超应答一例[J]. 中国心脏起搏与心电生理杂志,2015,(1):85-6.
本文编辑:阮燕萍
A comparative study on ultrasound characteristics between coronary sinus ventricular pacing and traditional right ventricular pacing
MA Xue-juan*, ZHAO Ling, WANG Yu, GUO Tao, LI Lin, SUN Xu-du, YAN Shi-ran.*Department of Cardiology, First Affiliated Hospital of Kunming Medical University, Kunming 650032, China.
Objective To compare the change characteristics of echocardiogram indexes between coronary sinus (CS) ventricular pacing and traditional right ventricular pacing. Methods The patients with indications accorded with conventional cardiac pacing (n=50) were chosen from the First Affiliated Hospital of Kunming Medical University from Dec. 2012 to May 2014, and randomly divided into traditional pacing group (n=32) and CS pacing group (n=18). All patients were given echocardiogram examinations before and 3 m, 6 m and 1 y after the procedure for collecting the indexes of left atrial diameter (LAD), right atrial diameter (RAD), left ventricular ejection fraction (LVEF), left ventricular fraction shortening (LVFS), TS-12-SD (reflecting left ventricular systolic synchrony) and tricuspid regurgitation in area (TRA). Results Among 32 cases in traditional pacing group, there were 16 were male and average age=(64.47±11.40), and among 18 cases in CS pacing group, there were 11 were male and average age=(62.22±12.95). The difference in all baseline indexes, including demographic characteristics, disease constitution and concomitance diseases, types pacemaker implantations and medications had no statistical significance between 2 groups (P>0.05) before the procedure. The difference in all ultrasound indexes had no statistical significance between 2 groups (P>0.05) before the procedure, and TS-12-SD was higher than normal value in 2 groups before the procedure. LVEF and LVFS were higher in CS pacing group than those in traditional pacing group 3 m, 6 m and 1 y after the procedure (P<0.05). TS-12-SD was recovered to normal in CS pacing group 1 y after the procedure (P<0.05). Conclusion CS pacing can improve left ventricular systolic function and synchrony compared with traditional right ventricular pacing.
Cardiac pacing; Coronary sinus; Ventricular pacing; Echocardiogram
R318.11
A
1674-4055(2016)11-1319-04
云南教育厅科学研究基金资助(2013C236)
1650032 昆明,昆明医科大学第一附属医院心内科
赵玲,E-mail:zhaoling580@126.com
10.3969/j.issn.1674-4055.2016.11.10

