血细胞分析系统自动审核规则建立与确认
王剑飚 上海瑞金医院检验科 (上海 200000)
血细胞分析系统自动审核规则建立与确认
王剑飚 上海瑞金医院检验科 (上海 200000)
目的:建立一套血细胞分析系统的自动审核规则,并对该套规则进行有效性验证。方法:参照国际血液学组织提出的“41条复检规则”及Mindray BC-6800全自动血细胞分析仪的技术水平,建立初步的样本审核规则并录入Mindray labXpert样本审核系统;选取上海瑞金医院约1000例临床样本对规则的假阳性、假阴性及自动审核通过率等指标进行验证;根据验证结果对规则进行调整及确认,规则确认后选取不少于1万例样本进行自动审核验证,测试自动审核通过率,人工审核所占比例及镜检审核所占比例。结果:对初步的审核规则验证结果表明,假阴性率小于2%,假阴性的样本主要为中晚幼粒细胞低值(幼稚比例在3%以内)红细胞形态异常及血小板形态异常等情况,假阴性样本中不存原始细胞增多及幼稚比例3%以上的样本,临床风险较小;假阳性率较高,接近18%,从而也影响了自动审核通过率。根据假阳性分析结果对规则进行了调整,规则调整后,假阴性率与调整前基本一致,但假阳性率有明显降低,且自动审核通过率有较大的提升;采用确定的规则运行了1万多例样本,自动审核通过率为76.4%。而导致自动审核不通过的主要因素为IMG%增高、未成熟细胞报警及WBC超出设定的范围等因素;采用该套系统后,平均TAT(turnaround time)缩短了4.1分钟。结论:采用Mindray CAL 8000血细胞分析系统及配套的LabXpert样本审核软件对样本进行分析及自动审核,制定严谨的自动审核规则,可以保证较低假阴性前提下,实现大部分样本自动审核(75%以上),提高检验科的工作效率。同时医生可以将更多的时间与精力用于异常样本复检上,使血常规报告的质量大大提高。
血细胞分析 自动审核 规则
随着临床实验室样本量的增加,实验室人员面临巨大挑战,目前大型医院均有全自动化的检验设备,检验工作效率相比过去已经有了很大的提高,如果需要进一步节省人力成本,缩短TAT,同时保证报告质量,分析后结果处理方法尤为重要。另外,实验室人员素质要求也越来越高,目前实验室人员素质参差不齐的现象也会影响报告质量。因此,建立实验室的样本自动审核系统为解决上述问题提供了一种有效的途径。目前检验科生化、免疫及凝血系统采用自动审核的较为多见。另外也有文献介绍了如何制定与确认生化分析仪自动审核系统,但血细胞分析系统采用自动审核发报告较少,可能与血细胞分析结果特殊性有较大关系。要得出一个高质量的血细胞分析结果,需要同时考虑以下因素:样本性状(考虑样本有无凝血、溶血等因素)、仪器状态(如结果有无堵孔、通道有无异常等)、参数及报警情况、与该病人的历史结果进行对比(Delta Check)等其他各方面的因素。labXpert为深圳迈瑞公司开发的连接血常规检测仪器与实验室信息管理系统(LIS)中间软件。我们可以在该系统上设置自动审核规则,该软件的自动审核路径依照CLSI Auto 10-A进行设计,将规则录入该系统后,所有样本的结果根据该套规则进行判断,实现样本的自动审核,也可以在该套系统上对异常样本进行人工审核及镜检审核,提高样本审核效率。自动审核能够大大提高检验科室的工作效率,但是我们同时也要考虑样本审核的临床风险,因此,制定科学的审核规则尤为重要。为了制定一套合理有效的规则,我院对审核规则进行充分的验证,且根据验证结果对规则进行了适当的调整,使规则更加合理。根据确定的规则再进行大量样本的验证。
1.材料与方法
1.1 样本选择
规则确定样本选择:选取门诊及住院的EDTA-K2抗凝的样本约1000例,其中初诊的病人约占80%,复诊的病人约20%。
自动审核通过率验证样本选择:选取不少于10000例EDTA-K2抗凝的样本。
上述所有的样本均在采集后4小时内在Mindray CAL 8000上进行分析。
1.2 仪器与试剂
CAL 8000血液细胞分析流水线(两台BC-6800+一台SC-120推片染色机)、配套试剂、全血质控物及校准物,由深圳迈瑞生物医疗电子股份有限公司生产。
1.3 自动审核系统
labXpert系统是由深圳迈瑞公司开发的血液细胞分析专家系统软件。软件的样本审核模块是该系统最核心的模块之一,该模块主要包括,自动审核、人工审核及镜检审核三个部分。样本审核路径参照CLSI Auto 10-A设定,建立了严格的审核逻辑关系,该逻辑关系也符合人工审核样本的思路,具体审核路径见图1,且所有的规则设置在图1中完成。
1.4 方法
所有标本严格按照CAL 8000使用说明书的要求对血常规进行检测。所有用于自动审核规则评估的样本,经血液分析仪检测后均用SC-120自动进行推片染色,每个样本制作3张血涂片。参照CLSI H20-A2的镜检方法,由两名有经验的中级以上技术职称的技术人员对所有样本进行镜检。规则确定后,再选取不少于1万例样本进行分析。
1.5 初步规则的制定
参照国际血液学复检专家组提出的“41条复检规则”及BC-6800血细胞分析仪的技术水平,制定出了CAL 8000血细胞分析工作站自动审核初步规则及镜检条件初步规则,具体规则见表1及表2。
1.6 阳性标准的制定
参照国际血液学复检专家组制定的阳性标准作为本次评估的镜检阳性标准:红细胞(RBC)形态有中度或更大改变;血片中发现有疟原虫;血小板(PLT)形态有中度或更大改变;血小板聚集比较多见;杜勒氏小体、毒性改变、空泡的粒细胞有中度或更大改变;原始细胞≥1个;早/中幼阶段细胞≥1个;晚幼阶段细胞>2个;异型淋巴细胞≥5个;有核红细胞(NRBC)≥1个,浆细胞≥1个。
仪器阳性标准:样本结果没有通过自动审核的均为阳性。
1.7 自动审核规则的评估
以镜检结果作为金标准,对初步自动审核规则进行评估。参照CLSI H20-A2的镜检方法,每个标本由两位主管技师进行镜检,每个主管技师分类计数200个白细胞(WBC)。当两位技师镜检结果偏差超过允许范围时,再由第三位技师镜检复核,最后取两位相近结果的均值做为最终的镜检结果。根据镜检结果及labXpert自动审核结果,计算自动审核假阳性率、假阴性率及自动审核通过率等指标,并对假阳性及假阴性样本构成进行分析,根据分析结果对审核规则进行调整。
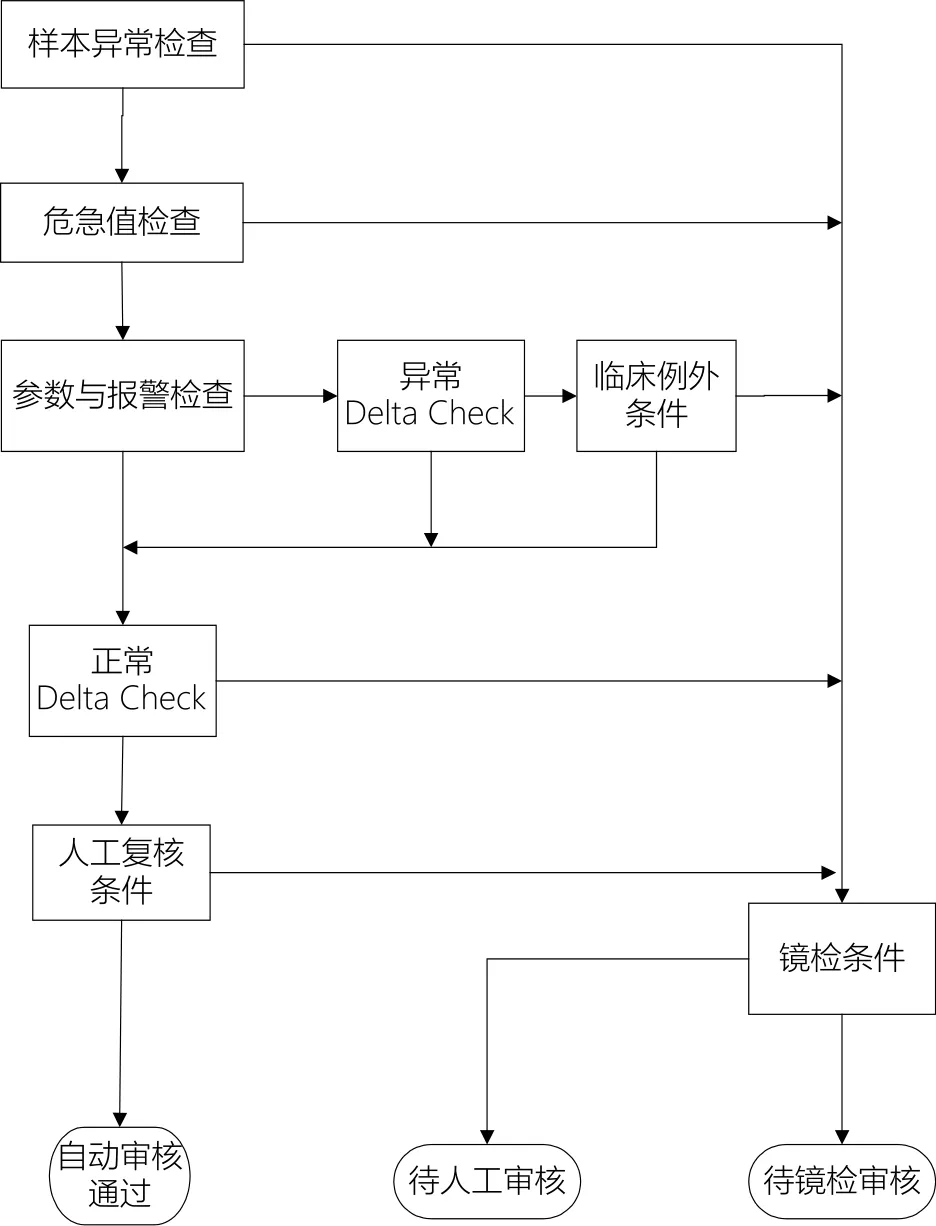
图1. labXpert软件样本审核路径图
1.8 统计学分析
实验数据用Microsoft Excel 2007及labXpert内部统计功能进行统计学处理,统计自动审核规则评估的约1000例样本的假阴性率,假阳性率及通过率,并对假阴性及假阳性情况进行分析;规则调整后重新统计上述样本假阴性率,假阳性率及通过率。统计批量样本的自动审核通过率及需人工审核及镜检审核的比例。
假阳性:仪器提示人工审核或镜检审核,但是镜检为阴性的样本。
假阴性:仪器提示自动审核,但是镜检为阳性的样本。
真阳性:仪器提示需人工审核或镜检审核,且镜检为阳性的样本。
真阴性:仪器提示自动审核,且镜检为阴性的样本。
一致性:真阳性的样本和真阴性样本数之和。
自动审核通过率:自动审核通过的样本数/所有分析的样本数×100%。

表1. 自动审核规则初稿
单条规则触发率:反应该条规则被运行且被触发的情况,指所有的样本结果使用规则树运行时,该规则被运行且被触发的次数/该规则总的运行的次数。

表2. 镜检条件初稿
1.9 质量控制
用配套的校准物将BC-6800血液细胞分析仪进行校准且校准验证通过。每天实验前,均先测试全血质控物,质控在控。
2.结果
2.1 初步自动审核规则验证
通过检测1024份标本对自动审核规则有效性进行评估,统计自动审核规则的假阳性率、假阴性率、一致性及自动审核通过率,并且对假阴性样本及假阳性的构成进行分析,自动审核规则验证统计具体结果见下表3,假阴性样本分布见下表4,假阳性样本分布见下表5。
2.2 自动审核规则调整及确认
根据上述规则验证结果对自动审核规则进行调整:对假阴性样本进行分析,假阴性率小于2%,假阴性的样本主要为中晚幼粒细胞低值(幼稚比例在3%以内)、红细胞形态异常及血小板形态异常等情况,假阴性样本中不存原始细胞增多及幼稚比例3%以上的样本,临床风险较小;对假阳性样本进行分析,由于镜检阳性标准中主要为形态异常指标,没有把计数参数增高、减低作为阳性标准,因此,假阳性的样本中计数参数的异常占了较高的比例。结合临床风险及BC-6800的技术水平考虑,我们对参数范围中WBC、PLT及MCV的要求进行调整。为了进一步降低临床风险,我们决定在参数范围检查中增加IMG%≤0.8的要求,目的为在保证报告的质量的同时提高自动审核通过率,同时镜检条件也做了适当的调整,调整方案见表6及表7。

表3. 初步自动审核规则验证统计

表4. 假阴性样本分布表
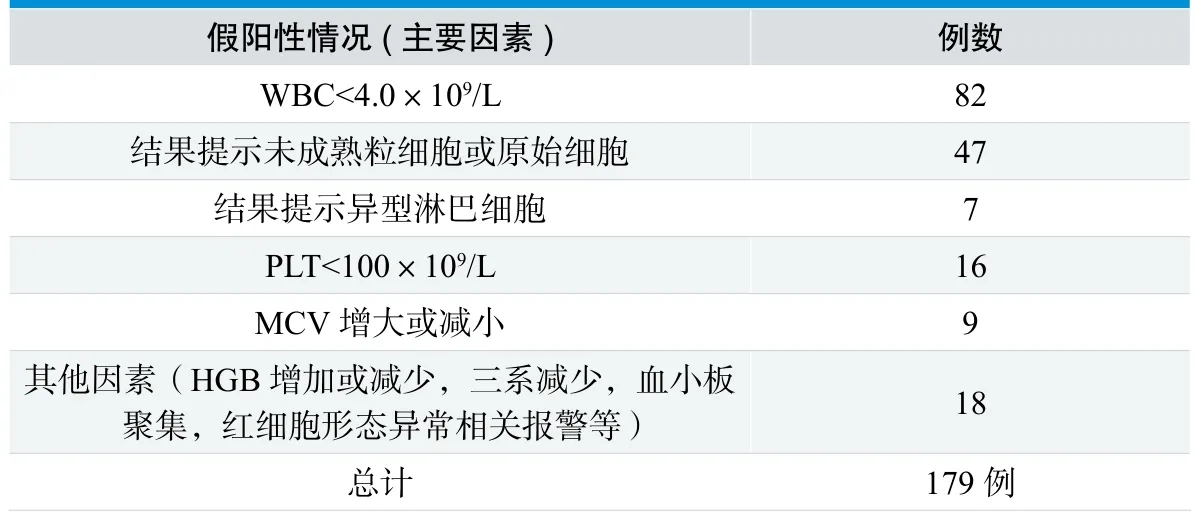
表5. 假阳性样本分析
规则调整后,再将1024例样本重新运行新规则,根据运行结果重新统计假阳性率、假阴性率、一致性及自动审核通过率等结果,结果见表8。数据分析发现,假阴性率与规则调整前变化不明显,且均在2%以内,临床风险较小,但假阳性 率降低明显,同时自动审核通过率也有明显提高。

表6. 参数规则调整方案

表 7 镜检条件调整方案

表8. 自动审核规则调整后数据统计

表9. 主要规则触发率分析
2.3 规则调整后大量样本验证
自动审核规则确认后,将规则录入labXpert系统,选择大量样本对自动审核系统进行验证。共收集住院及门诊的样本总计11790例,将所有样本结果通信到labXpert系统中,统计样本危急值样本比例、自动审核通过率、待人工审核比例及待镜检审核比例,其结果为样本危急值样本比例6.4%、自动审核通过率76.4%、待人工审核比例3.3%及待镜检审核比例20.3%。同时分析影响自动审核不通过的主要因素。统计数据表明,导致自动审核不通过的主要节点为参数与报警检查节点,我们分析了该节点主要导致自动审核不通过的因素,具体分析结果见表9。
2.4 采用自动审核系统后发报告时间差异对比
TAT有不同的定义,因为不同的职位的人员关注的时间有差异,对于检验者来说主要关注的是从样本在检验科签收到报告发出的时间,而对于临床医生则关注的是从申请单开出到获取到报告的时间。我们本次临床试验主要统计的是检验科签收到报告发出的时间,选取了1000例样本。传统审核方式平均TAT耗时26.4分钟,labXpert软件审核平均TAT耗时22.3分钟,缩短了4.1分钟。
3.讨论
labXpert为血液细胞分析仪配套使用的样本审核系统,该系统完全按照人工审核样本的思路设计,审核过程结合了样本状态检查、危急值检查、参数结果及报警提示检查、Delta Check及镜检确认。同时医院可以根据自身病源特征及技术水平设定临床例外条件及人工复核条件,从而提高自动审核效率及报告质量。医院采用该系统后,符合设定规则的报告将自动审核,因此自动审核规则尤为重要,自动审核规则设置是否合理,直接决定了最后发报告的质量及自动审核通过率。我们根据国际血液学复检专家组制定的“41条复检规则”及BC-6800血细胞分析仪的实际技术指标,制定了初版的自动审核规则及镜检规则,并对规则做了科学、细致的评估。评估结果为假阴性均小于2.0%,假阳性约为18%。我们对假阴性及假阳性做了详细的分析,根据分析结果对该套规则进行调整,增加IMG%做为审核条件,降低幼稚粒细胞的假阴性率。同时对WBC、MCV及PLT范围进行了适当的调整,调整后假阴性率仍可以保证在2%以内,且假阳性率得到了明显的降低而自动审核通过率有明显的提高,在保证报告质量的同时,提高了自动审核通过率,最终得出了一套较为理想的自动审核规则。
根据确定的规则,我们选择了大量的样本(超过10000例)对规则进行验证,验证结果显示,自动审核通过率为76.4%。自动审核通过率较低的原因是血液科是瑞金医院的优势科室,异常样本较多,因此自动审核通过率较低,同时危急值样本比例较高。所以,考虑到瑞金医院的实际特点,我们后续还需要对规则进一步优化,比如将血液科做为人工审核的条件,危急值分科室进行设定等均可以考虑。自动审核的实现节省了大量审核正常样本的时间。同时CAL 8000(Mindray 血细胞分析流水线)可以将剩下的约20%~30%的异常样本进行自动重测、推片染色或者仅需人工审核确认。镜检审核的样本可以直接用labXpert上的镜检计数器进行细胞计数,计数完后直接将各分类结果转化成百分比进行发报告。
同时,我们也发现采用自动审核系统后的另一个较大的优势是可以使不同的检验医生审核报告统一化,所有的医生均采用同一套规则审核报告,避免了不同医生经验和掌握知识的差异而导致报告质量的差异,也避免了同一个医生在不同场景,不同工作状态下发报告的差异。
总之,采用自动审核系统对血常规报告进行审核,在保证报告质量的前提下可以提高效率,但是各实验室由于病源差异,自动审核率有一定的差异,建议各医院要结合所在医院病人特点及所用仪器的技术水平制定一套符合实验室自身特点的自动审核规则,且在使用过程中,不断根据使用效果对规则进行优化,最终形成一套合理、可靠的规则。
Establishment and Validation of Automatic Verification Procedures for Blood Cell Analysis System
WANG Jian-biao Department of laboratory, Shanghai Ruijin Hospital (Shanghai 200000)
Objective: To establish a series of automatic verification procedures for blood cell analysis system, and verify the validity of these procedures. Methods: The initial verification procedures were established and input into Mindray labXpert sample verification system by reference to “41 review rules” settled by the international hematological organization and the technical level of Mindray BC-6800 automatic blood cell analyzer. About 1000 blood samples were collected from Shanghai Ruijin Hospital and detected by Mindray BC-6800 to achieve false positive rate, false negative rate and the pass rate of automatic verification of such initial procedures. After analyzed the obtained data, the verification procedures were adjusted and confirmed. Subsequently more than 10000 blood samples were collected to test the pass rate of automatic verification, the proportion of human review and the proportion of microscopic examination. Results: The results of initial automatic verification procedures examination showed that false negative rate was lower than 2% and false positive rate was relatively high that is almost 18%.And the false negative samples were the samples with low level of myelocyte and metamyelocyte (naive ratio is less than 3%), abnormal morphologicalerythrocyte, abnormal morphological platelet and so on. And what is most important that there was no false negative sample with increased archaeocyte or more than 3% naive ratio, leaving small clinical risk. Relatively high false positive rate also infiuenced the pass rate of automatic verification. Verification procedures were adjusted by reference to false positive results, and after adjustment, false negative rate had a great consistency with before and false positive rate had a significant reduction along with the rising of pass rate of automatic verification. More than 10000 blood samples were detected under the confirmed automatic verification procedures, and the pass rate of automatic verification was 76.4%. The major factors influence the pass rate of automatic verification were that increasing IMG%, warning of immature blood cells, WBC counting beyond setting and so on. Moreover, average turnaround time was shortened 4.1 minutes after such procedures were employed. Conclusion: Mindray CAL 8000 blood cell analysis system and suitable LabXpert sample verification software were employed and simultaneously precise automatic verification procedures were settled. After that more than 75% blood samples could be automatic verified with assured lower false negative rate, leaving higher work efficiency in department of laboratory. At the same time, doctors could spend more time and energy on the review of abnormal samples, to improve the quality of blood routine report greatly.
blood cells analysis, automatic verification, rules
1006-6586(2016)07-0005-07
R446.1
A
2016-04-26

