U PLC同时测定脑安颗粒中6种人参皂苷类成分的含量
胡紫艳 孙夏荣 史达 朱颖 蒋健
(南京市食品药品监督检验院,江苏 南京210000)
U PLC同时测定脑安颗粒中6种人参皂苷类成分的含量
胡紫艳孙夏荣史达朱颖蒋健
(南京市食品药品监督检验院,江苏 南京210000)
目的:采用超高效液相色谱法(UPLC)分离测定脑安颗粒中 6种人参皂苷的含量。方法:采用ACQUITY BEH C18(2.1 mm×100 mm,1.7 μm)色谱柱,流动相乙腈(A)-水(B),梯度洗脱,流速0.45 mL/min,检测波长203 nm,柱温35℃。结果:6种人参皂苷Rg1、Re、Rb1、Rb2、Rb3和Rd分别在8.096~ 202.4,20.008~500.2,16.112~ 402.8,8.24~ 206,16.048~ 401.2和16.048~ 401.2 μg/mL与相应峰面积呈良好线性关系,平均加样回收率(n=6)分别为:98.92%,98.78%,97.91%,98.00%,98.13%,98.10%,RSD分别为 0.46%,0.43%,0.26%,0.70%,0.62%,0.76%。结论:UPLC分离效果及重复性好,且快速简便,可作为脑安颗粒的质量控制方法。
超高效液相色谱;脑安颗粒;人参皂苷;含量测定
脑安颗粒由川芎、当归、红花、人参与冰片5味药组成。有活血化瘀、益气通络的功效,用于治疗脑血栓形成急性期、恢复期气虚血瘀[1]。临床应用证实脑安颗粒对血管性头痛的治疗效果较好,且不良反应少[2];对老年神经衰弱也具有显著疗效[3-4]。目前标准采用的是薄层色谱法测定人参皂苷Re[1],操作复杂且准确度不高,而对其他人参皂苷类成分没有规定。目前也尚未见同时测定脑安颗粒中人参皂苷Rg1、Re、Rb1、Rb2、Rb3、Rd这6种成分含量的报道。由于脑安颗粒成分复杂,若采用普通液相色谱法测定6种人参皂苷耗时较长,效率低下。超高效液相色谱(UPLC)技术的发展,为复杂体系中药的分离分析提供了良好的平台[5]。为提高脑安颗粒质量控制标准,进一步保证药物疗效,本研究采用UPLC技术,建立了同时测定脑安颗粒中人参皂苷 Rg1、Re、Rb1、Rb2、Rb3、Rd 6种成分的分离分析方法,此方法快捷、准确,重复性好,为脑安颗粒质量标准提供依据。
1 仪器、试剂与试药
1.1仪器
超高效液相色谱系统(ACQUITY UPLC,美国Waters公司);天平XS 205(METTLER TOLEDO);色谱柱:ACQUITY BEH C18(2.1 mm×100 mm,1.7 μm)。
1.2试剂与试药
乙腈为色谱纯,水为超纯水;人参皂苷Rg1对照品(批号:110703-201530,含量91.7%)、人参皂苷Re对照品(批号:110754-201525,含量92.3%)、人参皂苷Rb1对照品(批号:110704-201424,含量93.7%)、人参皂苷Rb2对照品(批号:110715-200802,含量94.8%)、人参皂苷Rb3对照品(批号:111686 -201002,含量 92.7%)、人参皂苷 Rd对照品(批号:111818-201001,含量94.4%),对照品均来源于中国食品药品检定研究院。脑安颗粒 (批号:20140610),河南省百泉制药有限公司生产。
2 方法与结果
2.1色谱条件
色谱柱为 Waters Acquity UPLC HSS T3 C18(100 mm × 2.1 mm,1.8 μm);柱温 35℃;样品温度10℃;进样体积1 μL;流速0.45 mL/min;检测波长 203 nm;流动相 A为乙腈,流动相B为水,梯度洗脱程序见表1。在此条件下,6种人参皂苷分离度均大于1.5,对照品与样品UPLC色谱图见图1。

表1 脑安颗粒中6种皂苷类成分测定的梯度洗脱程序

图1 UPLC图
2.2溶液的制备
2.2.1对照品溶液的制备取人参皂苷 Rg1、Re、Rb1、Rb2、Rb3、Rd对照品适量,精密称定,分别置于100 mL量瓶中,加乙醇溶解并稀释至刻度,摇匀,使其浓度分别为1.012,2.501,2.014,1.030,2.006,2.058 mg/mL,作为对照品储备液 1~ 6。精密量取上述6个对照品溶液各1 mL,置于25 mL量瓶中,用甲醇稀释至刻度,摇匀,配成含人参皂苷 Rg1(40.48 μg/mL)、Re(100.04 μg/mL)、Rb1(80.56 μg/mL)、Rb2(41.20 μg/mL)、Rb3(80.24 μg/mL)、Rd(82.32 μg/mL)的对照品溶液。
2.2.2供试品溶液的制备取约4 g,精密称定,加入甲醇 50 mL,超声提取 40 min,放冷,滤过,滤液蒸干,加水20 mL使溶解,用二氯甲烷洗涤2次,每次20 mL,弃去二氯甲烷液,水液用水饱和正丁醇提取2次,每次30 mL,合并正丁醇液,用1%氢氧化钠溶液洗涤二次,每次 20 mL,弃去碱液层,用正丁醇饱和的水洗涤 2次,每次20 mL,再将正丁醇液蒸干,残渣加甲醇使溶解,并转移至10 mL量瓶中,用甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
2.3方法学考察
2.3.1线性关系考察精密量取对照品溶液0.20,0.30,0.50,1.00,2.00,3.00,5.00 μL,分别进样,测定峰面积。分别以各色谱峰面积(Y)对其浓度(X)进行线性回归,得回归方程,结果见表 2。
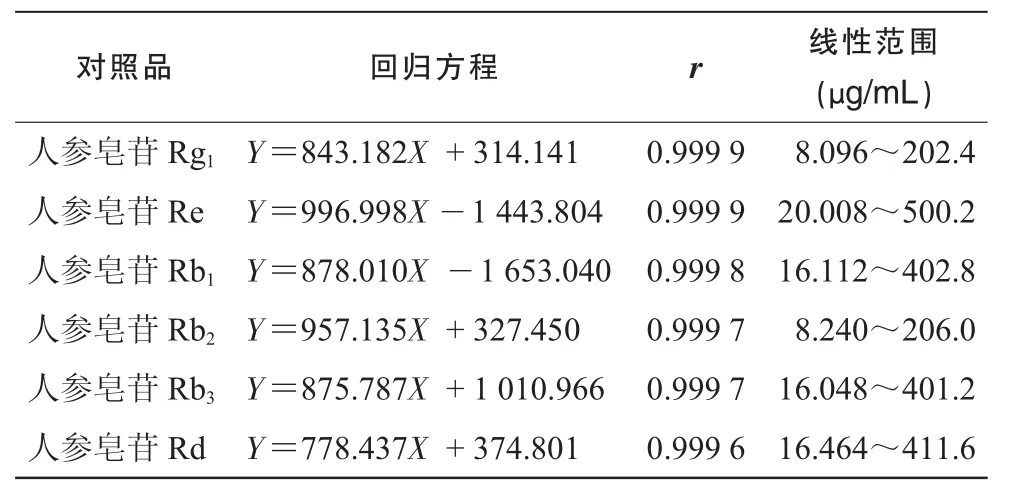
表2 6种人参皂苷的回归方程
2.3.2精密度试验精密吸取对照品溶液 1 μL,重复进样5次。结果,人参皂苷Rg1、人参皂苷Re、人参皂苷 Rb1、人参皂苷 Rb2、人参皂苷 Rb3和人参皂苷Rd峰面积的RSD分别为0.52%,0.91%,0.45%,0.63%,0.52%和0.92%(n=5),表明本试验方法的精密度良好。
2.3.3溶液稳定性试验精密吸取同一供试品溶液 (批号:151106)1 μL,分别于0,2,8,12,24 h进样,测定峰面积。结果,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rb3和人参皂苷Rd峰面积的RSD分别为0.60%,0.71%和0.93%,0.97%,0.54%和1.02%,表明供试品溶液在24 h内稳定。
2.3.4重复性试验取同一批样品(批号:151106)适量,共5份,按“2.2.2”项下方法制备,每份测定3次。结果,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rb3和人参皂苷Rd的平均含量分别为每袋0.19,0.34,0.17,0.15,0.27,0.34 mg,RSD分别为1.12%,1.03%,0.80%,0.43,0.59%和0.66%,表明本法重复性良好。
2.3.5加样回收率试验取已知含量的样品(批号:151106)适量,研细,精密称取4 g,分别精密加入人参皂苷 Rg1、人参皂苷 Re、人参皂苷 Rb1、人参皂苷Rb2、人参皂苷Rb3和人参皂苷Rd对照品适量,按“2.2.2”项下方法制备供试品溶液,共6份,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表3。
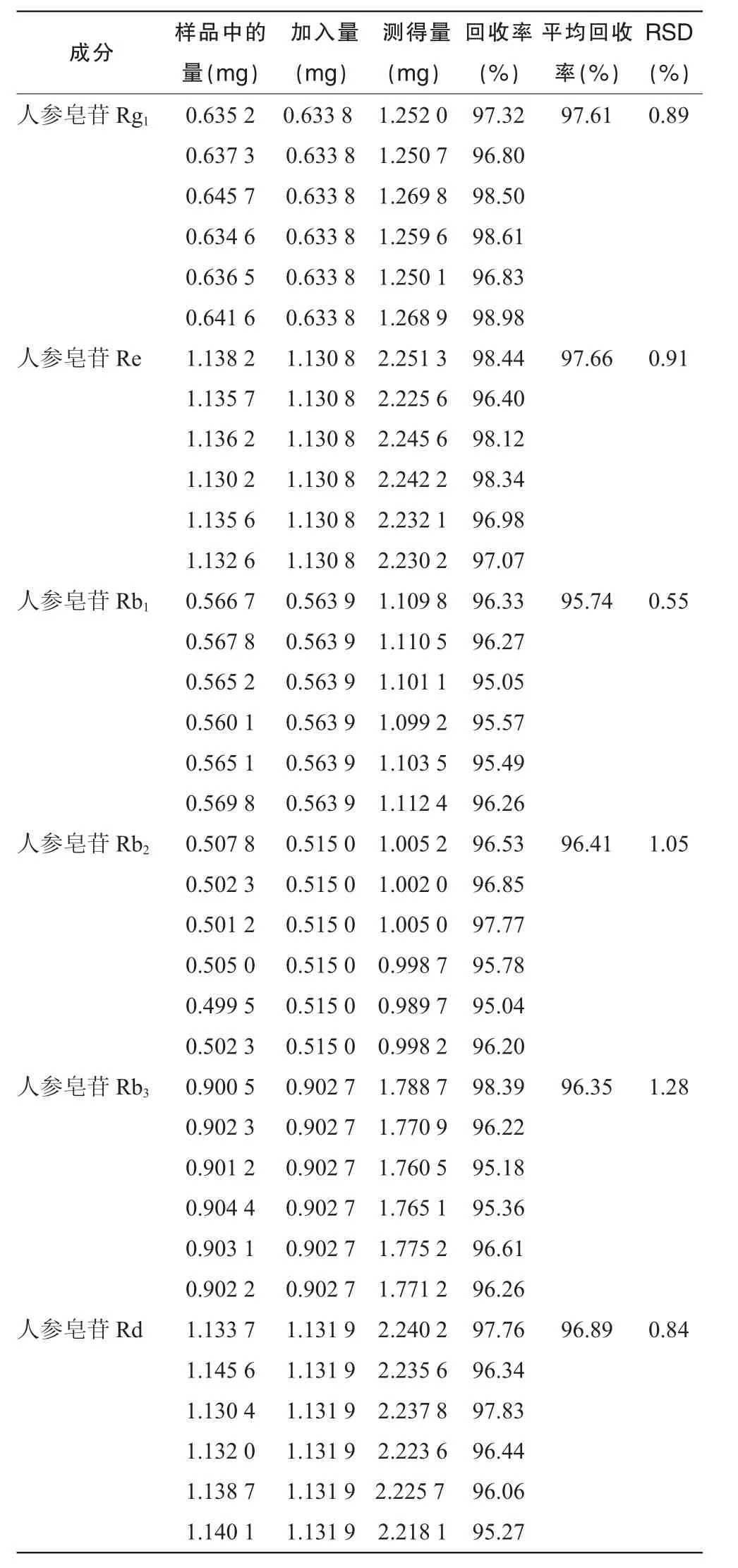
表3 加样回收率试验结果
2.4样品测定的结果
取3批样品,按“2.2.2”项下方法制备供试品溶液,每批制备3份,每份测定2次,取两份的平均值,见表4。

表4 样品测定结果 (mg/袋)
3 讨论
3.1人参总皂苷纯化方法的选择
脑安颗粒为多组分组成的中成药,成分复杂,若提取不完全杂质较多,影响人参皂苷的测定。因此采用溶剂萃取法对人参皂苷进行纯化,除去大部分杂质。参考文献[6-8],先用甲醇超声提取,与原标准[1]中的索氏提取相比时间缩短、收率提高、温度降低;用二氯甲烷去除大部分杂质;再用水饱和正丁醇萃取样品中人参皂苷,最后用正丁醇饱和水去除样品中过量的杂质。文献[9-10]报道采用D-101大孔吸附树脂进行纯化,虽效果较好,但需对大孔树脂进行预处理、装柱、洗柱等步骤,方法繁琐、耗时;而溶剂萃取法相对简便、用时少,通过上述萃取方法可去除大部分杂质。所以,本实验采用溶剂萃取法对人参中的人参皂苷进行分离纯化。
3.2洗脱梯度的选择
本实验建立了同时测定脑安颗粒中6种人参皂苷含量的方法,参照文献[11-15]报道,通过探索不同的洗脱体系,不同的梯度洗脱程序,最终得到了优化洗脱系统,使 6种重要的人参皂苷类成分获得完全的分离。选用乙腈-水梯度洗脱,其中,0~ 9 min时,乙腈占18~ 22,在18~ 26 min之间,乙腈占52~ 18,可使样品中人参皂苷 Rg1与人参皂苷Re、人参皂苷Rb2与人参皂苷Rb3的分离度最佳(R≥1.5),该色谱条件可用于6种人参皂苷的含量测定。用超高效液相色谱法同时测定脑安颗粒中6种人参皂苷,改进了原标准中的含量测定方法,该方法更加准确、快速、可靠,同时增加了脑安颗粒的检测项目,可作为脑安颗粒的质量控制方法。
本实验采用UPLC同时测定了脑安颗粒中6种人参皂苷类成分,增加了原标准对人参的检测指标,又改进了原标准的方法,且该方法更加准确、快速、可靠。
[1]国家药典委员会.国家食品药品监督管理局药品标准.新药转正标准第 34册[S].国家食品药品监督管理局,WS3-208(Z-208)-2002(Z),34-73.
[2]鞠保顺.脑安颗粒治疗血管性头痛30例临床分析[J].临床医学研究与实践,2016,1(11):23-25.
[3]吴敏,邵敏,沈志华,等.枣仁安神颗粒结合脑安颗粒治疗老年神经衰弱的超声评估观察[J].中华中医药学刊,2015,33(2):360-361.
[4]张会秋.个性化护理结合脑安颗粒治疗老年神经衰弱的超声评估观察[J].中国医药指南,2016,14(7):275.
[5]吴立蓉,王秀凤,高卫东,等.超高效液相色谱(UPLC)在药物分析领域中的应用[J].药物分析杂志,2008,28(11):1976-1981.
[6]张崇禧,郑友兰,张春红,等.不同方法提取人参总皂苷工艺的优化研究[J].人参研究,2003,15(4):5-8.
[7]张春红,张连学,李向高,等.人参皂苷常规水提取法和新提取方法的比较研究[J].中药材,2006,29(10):1040-1042.
[8]信小娟,陈旸,丛建华,等.不同提取方法对人参皂苷收率的影响[J].中国林副特产,2015,135(1):34-35.
[9]桂双英,周亚球.比色法测定人参中人参总皂苷的含量[J].安徽中医学院学报,2003,22(4):51-52.
[10]蔡一新,黄宗锈,苏必桔,等.保健食品中人参总皂苷含量的测定[J].海峡预防医学杂志,2001,7(6):35.
[11]孙英英,郭玉海,林华庆,等.UPLC测定丹七片中三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量[J].中国生化药物杂志,2005,35(1):148-150.
[12]李慧,许亮,温美佳,等.不同产地人参皂苷成分含量UPLC法测定及质量评价[J].中华中医药杂志,2015,30(6):1963-1968.
[13]林苏娜,余楚钦,林华庆,等.UPLC测定参麦注射液中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1的含量[J].中国实验方剂学杂志,2014,20(8):48-50.
[14]逄世峰,曲正义,李亚丽,等.UPLC法同时测定人参糖中 7种人参皂苷[J].特产研究,2014,(3):53-56.
[15]吴立蓉,王秀凤,高卫东,等.超高效液相色谱法快速测定复方丹参片中皂苷类成分的含量[J].广东药学院学报,2016,32(1):32-35.
Simultaneous Determination of Contents Six Kinds of Ginsenosides in Naoan Granules by UPLC
Hu Ziyan,Sun Xiarong,Shi Da,Zhu Ying,Jiang Jian(1 Nanjing Institute for Food and Drug Control,Jiangsu Nanjing 210000,China)
Objective:To develop a ultra performance liquid chromatography(UPLC)method for simultaneous determination of contents of six kinds of ginsenosides in Naoan granules.Methods:ACQUITY BEH C18column(2.1 mm×100 mm,1.7 μm)was used with a mobile phase consisting of acetonitrile(A)-water(B)by gradient elution at a flow rate of 0.45 mL/min.The wavelength for detection was 203 nm while the column temperature was 35℃.Results:The contents of ginsenosides Rg1,Re,Rb1,Rb2,Rb3and Rd within the range of 8.096~ 202.4,20.008~ 500.2,16.112~ 402.8,8.24~ 206,16.048~ 401.2 and 16.048~ 401.2 μg/mL showed good linear relationship to the corresponding peak areas,respectively.The average recoveries of the six kinds of ginsenosides were 98.92%,98.78%,97.91%,98.00%,98.13%and 98.10%,with RSDs of 0.46%,0.43%,0.26%,0.70%,0.62%and 0.76%,respectively.Conclusion:The UPLC method showed good separation effect and reproducibility,which was rapid,simple,and might be used for the quality control of naoan granules.
Ultra Performance Liquid Chromatography(UPLC);Naoan Granules;Ginsenoside;Content Determination
10.3969/j.issn.1672-5433.2016.12.006
胡紫艳,女,硕士,主管药师。研究方向:药物分析。通讯作者E-mail:huzy0903@163.com
(2016-09-29)

