膨润土/硫复合材料在锂硫电池中的应用*
宁超凡,潘俊安,程 豪,袁国龙,谢淑红
(1. 湘潭大学 材料科学与工程学院,薄膜材料及器件湖南省重点实验室,湖南 湘潭 411105;2. 湘潭大学 低维材料及其应用技术教育部重点实验室,湖南 湘潭 411105)
膨润土/硫复合材料在锂硫电池中的应用*
宁超凡1,潘俊安1,程 豪1,袁国龙1,谢淑红2
(1. 湘潭大学 材料科学与工程学院,薄膜材料及器件湖南省重点实验室,湖南 湘潭 411105;2. 湘潭大学 低维材料及其应用技术教育部重点实验室,湖南 湘潭 411105)
以膨润土作为单质硫的载体,热处理得到含硫50%(质量分数)的膨润土/硫复合材料,采用X射线衍射、扫描电镜、透射电镜和比表面分析仪对复合材料进行结构、形貌和孔径分析,通过充放电性能测试和交流阻抗对锂硫电池进行电化学性能分析。电化学测试结果表明,在1.0~3.0 V电压范围内,以0.2、0.5 C大小的电流密度对电池进行充放电性能测试,首次放电比容量分别为795.6和586.0 mAh/g,100次循环后对应的放电比容量分别为488.5和421.5 mAh/g,容量保持率分别为61.3%和71.8%。
膨润土/硫复合材料;锂硫电池;电化学性能
0 引 言
锂离子电池广泛用于便携式电子设备、电动汽车、混合动力汽车等领域,随着经济社会的迅猛发展,它们对电池的性能提出了越来越高的要求[1-3]。锂硫电池是正极采用硫,单质硫的理论比容量为1 675 mAh/g[4],1 C的电流密度是1 675 mA/g。负极采用锂的新型锂离子二次电池,具有耐过充能力[5],且硫资源丰富,价格便宜,环境友好,因此锂硫电池具有广阔的应用前景。
目前锂硫电池存在的问题包括:在充放电反应过程中生成的高聚态多硫化物易溶于电解液,使活性物质减少,电解液粘度增加,电阻增大[6];溶解的高聚态多硫化物扩散到负极与金属锂发生副反应,生成低聚态的多硫化锂,部分低聚态的多硫化锂扩散回正极,氧化生成高聚态的多硫化锂,形成“飞梭效应”造成库伦效率降低[7]。
为解决上述问题,可在硫正极中添加介孔二氧化硅[8],Mg0.6Ni0.4O[9-10], TiO2[11-13],利用纳米氧化物的吸附性有效抑制多硫化物溶解,从而提高锂硫电池的性能。但上述纳米氧化物存在制备工艺复杂和成本高的缺点,限制了其实际应用。
膨润土是一种具有吸附性的片层结构的材料,具有较大的比表面积。同时也是一种以蒙脱石为主的含水粘土矿,具有良好的机械、热、化学稳定性和离子交换性能,但粘土本身的导电性能很差。研究结果表明[14],蒙脱石的层间物质表现为强烈的非电活性,并且指出超过离子交换容量的被吸附物质才是电活性的。膨润土的端面带有正电荷,可以吸附多硫化物,抑制多硫化物的溶解,提高电池的性能。此外,我国膨润土资源储量预测在80亿吨以上,位居世界首位,这一资源优势有利于膨润土在锂硫电池中的应用。
本文作者将膨润土用作锂硫电池正极基质材料,通过简单的热处理得到膨润土/硫复合材料,材料易得,制备方法简单,并且提高了锂硫电池的性能。
1 实 验
1.1 膨润土/硫正极材料的制备
将膨润土和硫按质量比1∶1的比例研磨均匀混合,放入密封小烧杯中并称重,再放入真空干燥箱中在105 ℃保温3 h,冷却后取出再称重,即得到膨润土/硫复合材料。由于前后两次质量变化很小,故膨润土/硫复合材料大约含硫50%。因注硫之后的膨润土/硫复合材料容易出现结块现象,需要对其进行研磨。
1.2 材料结构和形貌表征
使用日本Rigaku公司的Minflex型X射线衍射仪对粉末材料的结构进行分析。测试条件为:Cu Kα靶,管电压40 kV,管电流40 mA,扫描速度为5°/min,扫描角度2θ范围5~90°。使用日本Hitachi公司S4800型扫描电子显微镜(SEM)对样品的表面形貌进行分析。使用日本JEM-2100透射电子显微镜(TEM)对样品的结构进行分析。使用北京精微高博公司生产的JW-BK122W型比表面积测试仪对样品的比表面积和孔径进行分析。
1.3 电化学性能测试
将制备好的膨润土/硫复合材料,乙炔黑和PVDF粘结剂以质量比7∶2∶1混合,分散在N-甲基吡咯烷酮(NMP)中,充分搅拌得到均匀混合的浆料。把浆料均匀地涂在铝箔上,置于60 ℃真空烘箱中干燥12 h,然后轧制成正极片。以制备好的极片作为正极,金属锂片作为负极,Celgard 2400多孔聚乙烯为隔膜,1 mol/L LiTFSI/V(DOL)∶V(DME)=1∶1为电解液,在充满氩气的手套箱(Mikrouna)内将制备的材料组装成2016型扣式电池。使用电池测试系统(深圳新威)在室温下恒流进行循环性能、倍率性能测试,充放电电压范围为1.0~3.0 V,使用CHI660D电化学工作站(上海辰华)进行交流阻抗测试。
2 结果与讨论
图1为膨润土和膨润土/硫复合材料的XRD图。从图1可知,膨润土主要由蒙脱石、碳酸钙、石英和钠长石组成,同时还含有一定量的结晶水,课题组已发表的文章[15]中证明去掉结晶水后电化学性能变差,说明在电化学反应过程中结晶水起到了积极作用。而膨润土/硫复合材料的衍射峰表明单质硫和膨润土已经复合,由于硫的含量较高,结晶性好,使得复合后衍射峰的强度明显增大。
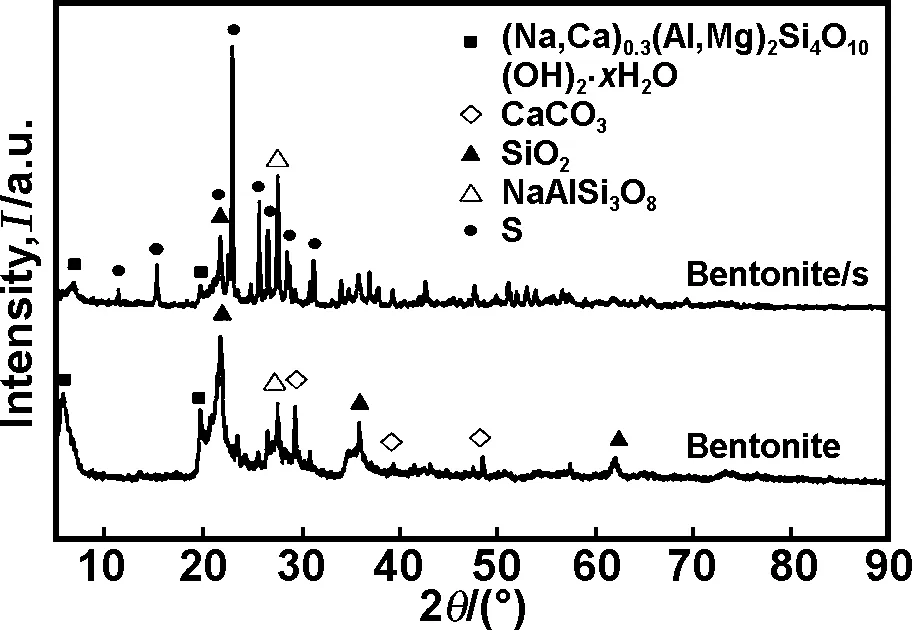
图1 膨润土和膨润土/硫复合粉末的XRD图谱
Fig 1 XRD patterns of bentonite and bentonite/S composite powders
图2为膨润土和膨润土/硫复合材料的SEM、TEM图。图2(a)为膨润土的SEM图,从图中可看出膨润土粉末粒径大小在2~20 μm,尺寸分布不均匀;图2(a)右上角的插图为膨润土的TEM形貌图,从图中可看出膨润土是由不规则的片状结构重叠在一起。图2(b)为经过研磨后的膨润土/硫复合材料的SEM图,粉末粒径大小在2~10 μm,由于载硫量较高,部分硫团聚吸附在膨润土表面。
图3为膨润土和膨润土/硫复合材料的吸脱附曲线和孔径分布图。从图3(a)中可以得出膨润土的比表面积为46.34 m2/g,孔容为0.10 cm3/g,载硫后膨润土/硫复合材料的比表面积减小为5.57 m2/g,孔容减小为0.017 cm3/g,表明硫吸附在膨润土表面,降低了膨润土的孔隙率。从图3(b)得出膨润土主要孔径分布范围为3~4 nm的介孔,载硫后得到的膨润土/硫复合材料的平均孔径变小,约为2 nm,但孔的尺寸分布更均匀。在实验中膨润土/硫复合材料含硫量越多,则平均孔径越小。这是由于随着含硫量逐渐增加,电解液与活性硫接触更加充分,电化学反应面积也增大,所以电荷传递电阻较小;但如果含硫量过多,导致溶解于电解液中的多硫化物更多,“穿梭效应”更明显,电解液的粘度更大,不利于锂离子的传输。

图2 粉末样品的SEM、TEM图

图3 (a)膨润土和膨润土/硫复合粉末吸脱附图, (b) 膨润土和膨润土/硫复合粉末孔径分布图
Fig 3 (a) N2adsorption-desorption isotherms at 77 K, and (b) BJH pore size distribution curves for bentonite and bentonite/S composite powders
图4为膨润土/硫复合材料在0.2 C倍率下的充放电曲线图。从图中可以看出第1,30,50,100次循环对应的放电比容量分别是795.6,618.4,569.2和494.4 mAh/g。在2.3和2.0 V左右有2个明显的放电平台,在2.4 V左右有1个充电平台。在2.3 V左右的高放电平台,对应着环状硫得到电子生成系列的长链多硫化物(Li2Sx,4≤x≤8)[16-17],在2.0 V左右的低放电平台,对应着长链的多硫化物进一步还原生成短链的多硫化物(Li2Sx,1≤x≤4),在2.4 V左右的充电平台对应Li2S和Li2S2先氧化为短链的多硫化物,最后转变为长链的多硫化物[18]。

图4 膨润土/硫复合材料的充放电曲线
Fig 4 Galvanostatic charge-discharge curves of bentonite/S composite
图5(a)为膨润土/硫复合材料在不同倍率下的前100次循环性能图。

图5 (a) 膨润土/硫复合材料的循环性能和库伦效率, (b) 膨润土/硫复合材料的倍率性能
Fig 5 (a) Cycling performance and the corresonding coulombic efficiency of bentonite/S composite and (b) rate capability under different discharge rate
以0.2 C电流密度放电,首次放电比容量为795.6 mAh/g,低于其理论容量,这是因为膨润土/硫复合材料的电子导电性差,不利于硫的活化。100次循环后放电比容量为488.5 mAh/g,为首次循环的61.3%。库伦效率始终保持在95%以上,这是因为膨润土的吸附作用能够有效地抑制多硫化物的溶解。以0.5 C电流密度放电,首次放电比容量为586.0 mAh/g,100次循环后放电比容量为421.5 mAh/g,为首次循环的71.8%,库伦效率始终保持在94%以上,说明膨润土/硫复合材料具有较好的循环稳定性。图 5(b)为膨润土/硫复合材料的倍率性能图。在0.1 C的电流密度下,首次放电比容量是933.5 mAh/g,10次循环后的放电比容量是866.7 mAh/g,将电流密度逐步增大到0.2,0.5和1.0 C,对应的放电比容量分别为708.8,427.3和340.5 mAh/g。再将电流密度降至0.1 C,放电比容量又上升至835.4 mAh/g,说明膨润土/硫复合材料具有较好的循环可逆性。
图6为膨润土/硫复合材料进行充放电循环1次和100次后的交流阻抗图。阻抗谱高频区的半圆体现电极的相间电接触阻抗及对应的电容[19],说明循环100次后电极的相间电接触阻抗增大。中频区的半圆体现电荷转移阻抗及对应的电容[20],循环100次后中频区的半圆明显小于循环1次的半圆,这说明循环100次后电荷转移阻抗变小,这可能是由于电解液的充分浸润有利于电荷转移和电化学反应进行。

图6 膨润土/硫复合材料的交流阻抗图
Fig 6 EIS curves of the bentonite/S composite after the first cycle and 100 cycles
3 结 论
采用简单的热处理方法制备了含硫50%的膨润土/硫复合材料,膨润土/硫复合材料为正极组装的电池具有稳定的充放电平台和良好的循环、倍率性能。以0.2 C电流密度放电,首次放电比容量为795.6 mAh/g,经过100次循环之后,放电比容量为488.5 mAh/g,容量保持率为61.3%;以0.5 C电流密度放电,首次放电比容量为586.0 mAh/g,经过100次循环之后,放电比容量为421.5 mAh/g,容量保持率为71.8%,在整个循环测试过程中库伦效率都在94%以上。
[1] Armand M, Tarascon J M. Building better batteries[J]. Nature, 2008, 451(7179): 652-657.
[2] Yang P, Yu S X, Jiang F, et al. Prepation and electrochemical performance of Gd3+doping SnO2nanocrystals as anode material for lithium ion batteries[J]. Journal of Xiangtan University,2014,01:26-32.
杨 萍,余随淅,蒋 峰,等. Gd3+掺杂纳米SnO2锂离子电池负极材料的制备与电化学性能研究[J]. 湘潭大学自然科学学报,2014,01:26-32.
[3] Li J G, Li W, Lei W, et al. Synthesis and characterization of Li(Li0.23Mn0.47Fe0.2Ni0.1)O2cathode material for Li-ion batteries[J]. J Power Sources, 2013, 244: 652-657.
[4] Ji X L, Lee K T, Nazar L F. A highly ordered nanostructured carbon-sulphur cathode for lithium-sulphur batteries[J]. Nat Mater, 2009, 8(6): 500-506.
[5] Hassoun J, Scrosati B. A high-performance polymer tin sulfur lithium ion battery[J]. Angew Chem Int Ed, 2010, 49(13): 2371-2374.
[6] Rauh R D, Abraham K M, Pearson G F, et al. A lithium/dissolved sulfur battery with an organic electrolyte[J]. J Electrochem Soc, 1979, 126(4): 523-527.
[7] Walus S, Barchasz C, Colin J F, et al. New insight into the working mechanism of lithium-sulfur batteries: in situ and operando X-ray diffraction characterization[J]. Chem Commun, 2013, 49(72): 7899-7901.
[8] Ji X L, Evers S, Black R, et al. Stabilizing lithium-sulphur cathodes using polysulphide reservoirs[J]. Nat Commun, 2011, 2(5): 325-331.
[9] Zhang Y, Bakenov Z, Zhao Y, et al. Effect of nanosized Mg0.6Ni0.4O prepared by self-propagating high temperature synthesis on sulfur cathode performance in Li/S batteries[J]. Powder Technol, 2013, 235: 248-255.
[10] Zhang Y, Zhao Y, Yermukhambetova A, et al. Ternary sulfur/polyacrylonitrile/Mg0.6Ni0.4O composite cathodes for high performance lithium/sulfur batteries[J]. J Mater Chem A, 2013, 1(2): 295-301.
[11] Wu H, Yu G H, Pan L J, et al. Stable Li-ion battery anodes by in-situ polymerization of conducting hydrogel to conformally coat silicon nanoparticles[J]. Nat Commun, 2013, 4: 1941-1943.
[12] Li Q, Zhang Z, Zhang K, et al. Synthesis and electrochemical performance of TiO2-sulfur composite cathode materials for lithium-sulfur batteries[J]. J Solid State Electrochem, 2013, 17(11): 2959-2965.
[13] Ding B, Shen L, Xu G, et al. Encapsulating sulfur into mesoporous TiO2host as a high performance cathode for lithium-sulfur battery[J]. Electrochim Acta, 2013, 107: 78-84.

杨卫华. 自组装膜修饰悬汞电极的制备及电化学性能研究;聚苯胺/膨润土(Pan/Ben)修饰电极电化学性能探究[D]. 河北: 河北师范大学,2000.46-50.
[15] Pan J A, Wu C, Cheng J J, et al. Sepiolite-sulfur as a high-capacity, high-rate performance, and lowcost cathode material for lithium-sulfur batteries[J]. J Power Sources, 2015, 293:527-532.
[16] Li Y J, Zhan H, Liu S Q, et al. Electrochemical properties of the soluble reduction products in rechargeable Li/S battery[J]. J Power Sources, 2010, 195(9): 2945-2949.
[17] Jung Y, Kim S. New approaches to improve cycle life characteristics of lithium-sulfur cells[J]. Electrochem Commun, 2007, 9(2): 249-254.
[18] Barchasz C, Molton F, Duboc C, et al. Lithium/sulfur cell discharge mechanism: an original approach for intermediate species identification[J]. Anal Chem, 2012, 84(9): 3973-3980.
[19] Atebamba J M, Moskon J, Pejovnik S, et al. On the interpretation of measured impedance spectra of insertion cathodes for lithium-ion batteries[J]. J Electrochem Soc, 2010, 157(11): A1218-A1228.
[20] Chen J J, Jia X, Shen Q J, et al. The preparation of nano-sulfur/MWCNTs and its electrochemical performance[J]. Electrochimica Acta, 2010, 55(27): 8062-8066.
Application of bentonite/S composite for lithium-sulfur batteries
NING Chaofan1, PAN Junan1, CHENG Hao1, YUAN Guolong1, XIE Shuhong2
(1. School of Materials Science and Engineering, and Hunan Provincial Key Laboratory of Thin Film Materials and Devices, Xiangtan University, Xiangtan 411105 China;2. Key Laboratory of Low Dimensional Materials and Application Technology of Ministry of Education,Xiangtan University, Xiangtan 411105 China)
Bentonite/S composite with 50% sulfur for lithium-sulfur batteries is obtained by heat treatment with bentonite as carrier of element sulfur. The structure, morphology and pore size of the composite are characterized by X-ray diffraction (XRD), scanning electron microscope (SEM), transmission electron microscope (TEM) and Brunauer Emme-Teller (BET) techniques. The electrochemical properties of lithium-sulfur batteries are analyzed by charge-discharge and electrochemical impedance spectroscopy tests. It is shown that the first specific discharge capacity of bentonite-sulfur cathode is about 795.6 mAh/g at 0.2 C current rate in the voltage range of 1.0-3.0 V, and it remains 488.5 mAh/g after 100 cycles, which is 61.3% of the initial cycle. Under 0.5 C current density, the first discharge capacity is 586.0 mAh/g, and maintains 421.5 mAh/g after 100 cycles, corresponding to 71.8% of the initial cycle.
bentonite/S composite; lithium-sulfur battery; electrochemical properties
1001-9731(2016)11-11087-04
国家自然科学基金面上资助项目(11472236);国家级大学生创新创业训练计划资助项目(201510530004);湖南省科技计划资助项目(2015JC3092)
2015-09-14
2016-01-22 通讯作者:谢淑红,E-mail: shxie@xtu.edu.cn
宁超凡 (1987-),男,湖南娄底人,在读硕士,师承谢淑红教授,从事锂硫电池正极材料研究。
TM910.4
A
10.3969/j.issn.1001-9731.2016.11.017

