冷沉淀制备过程质控及其临床应用效果探讨
蒋永红
吉林省珲春市无偿献血中心采制科,吉林珲春 133300
冷沉淀制备过程质控及其临床应用效果探讨
蒋永红
吉林省珲春市无偿献血中心采制科,吉林珲春 133300
目的 探讨冷沉淀制备全程中的质量控制方法及在严格质控条件下去冷沉淀血浆可达到的临床应用效果。方法 回顾性分析该站2014年全年2 062份冷沉淀制备成功率,并总结出一套冷沉淀全程质控方案,将实施后2015年全年2 271份冷沉淀制备成功率与实施前2014数据进行对比,分析质控方案效果。采取同一血样分为3份,分别制备为新鲜冷冻血浆、普通冷冻血浆以及去冷沉淀血浆;分别测定3样本中的凝血因子FV、FⅦ、FⅧ、FⅨ,纤维蛋白原及总蛋白数值并进行对比分析。结果 质控组冷沉淀制备合格率为99.91%,对照组冷沉淀制备合格率为75.02%,质控组冷沉淀制备合格率为99.91%,显著高于对照组,P<0.01;新鲜冷冻血浆中FⅧ (64.3± 11.2)%、FⅨ(83.9±9.6)%、纤维蛋白原(2.8±0.9)g/L及总蛋白(59.8±5.7)g/L均明显高于去冷沉淀血浆,P<0.05,普通冷冻血浆中FⅧ(59.6±15.2)%、FⅨ(80.3±11.5)%纤维蛋白原(2.6±0.7)g/L及总蛋白(58.6±4.8)g/L均明显高于去冷沉淀血浆,P<0.05。 结论 冷沉淀制备过程全程严格质量控制可有效提高制备合格率,去冷沉淀血浆与新鲜冷冻血浆、普通冷冻血浆中的凝血因子FV、FⅦ、FⅧ、FⅨ,纤维蛋白原及总蛋白数值差异较大,因此去冷沉淀血浆在临床应用中无法达到新鲜冷冻血浆、普通冷冻血浆的临床效果,临床上应根据具体情况选择应用。
冷沉淀;全程质控;去冷沉淀血浆
冷沉淀是临床中一种常见的血液制品,主要含有凝血因子FV、FⅦ、FⅧ、FⅨ,纤维蛋白原五项成分[1]。主要用于先天或继发性的甲型血友病、手术与创伤后凝血功能障碍以及部分低纤维蛋白原血症患者的临床治疗当中[2]。现将该院2014年1月—2015年12月间的冷沉淀制备数据进行具体分析,现报道如下。
1 资料与方法
1.1 一般资料
以该站2014年全年进行的2062份冷沉淀制备样本作为对照组,总结2014年冷沉淀制备经验后制定出一套全程质控方案,实施1年后以2015年全年进行的2 271份冷沉淀制备样本作为质控组,对比两组制备的冷沉淀制备成功率。同时随机抽取45份符合《献血者健康检查要求》的全血样本[3],样本每份300 mL,全部样本采集过程顺畅无污染,采集后以血液保存液Ⅱ行抗凝处理,采集后6 h内完成该次研究的全部后续操作。
1.2 设备试剂
凝血因子系列检测使用CA-1 500全自动型凝血仪及专用试剂进行检测,蛋白检测使用NSA-400全自动型生化仪及专用试剂检测,低温融化设备使用科瑞特Cyto Therm CT-4 T的6℃低温融化箱;新鲜冷冻血浆使用血浆速冻机制备,普通冷冻血浆使用低温冰箱制备。
1.3 质控制备方法
确保全程冷链系统完备,样本采集后置于2~6℃冰箱内储存,需运输的使用降温后的血液专用保温冷藏箱保存。于6 h内分离200 mL新鲜血浆,再取2份15 mL样本,其中1份置入血浆速冻机内速冻至-50℃制备为新鲜冷冻血浆样本,第2份置于4℃的低温冰箱之中制备为普通冷冻血浆样本,全过程中尽量避免或缩短样本暴露时间。次日将200 mL新鲜冷冻血浆置入1~6℃的Cyto Therm CT-4T低温融化箱中快速融化,以离心法进行血浆平衡离心。融化过程控制在99~120 min,观察血浆融化至直径2~3 cm左右、厚度约为1 cm左右冰块时取出样本,于4℃离心温度下以4 000 r/离心15 min,分离取得上清去冷沉淀血浆,取20 mL白色沉淀物即为冷沉淀,迅速置入血浆速冻机冷冻,同时取15 mL去冷沉淀血浆样本置入零下20℃冰箱内储存。检测新鲜冷冻血浆、普通冷冻血浆、去冷沉淀血浆中的凝血因子FV、FⅦ、FⅧ、FⅨ,纤维蛋白原及总蛋白含量,同时检测冷沉淀当中的FⅧ及纤维蛋白数值。
1.4 质量标准
遵照GB18469-2012《全血及成分血质量要求》中冷沉淀凝血因子之相关质量标准执行,制备的每200 mL冷沉淀中FⅧ水平≥80 IU,纤维蛋白原水平≥150 mg,容量为标示量mL的±10%。
1.5 统计方法
使用SPSS 18.0统计学软件进行数据计算,全部数据中计数资料采取χ2检验,用[n(%)]表示,计量资料采取均数t检验,用(±s)表示。P<0.05为差异有统计学意义。
2 结果
2.1 质控方案实施前后对比
实施全程质控方案后质控组冷沉淀制备合格率为99.91%,实施前的对照组冷沉淀制备合格率为75.02%,质控组冷沉淀制备合格率显著高于对照组,P<0.01,差异有高度统计学意义。见表1。
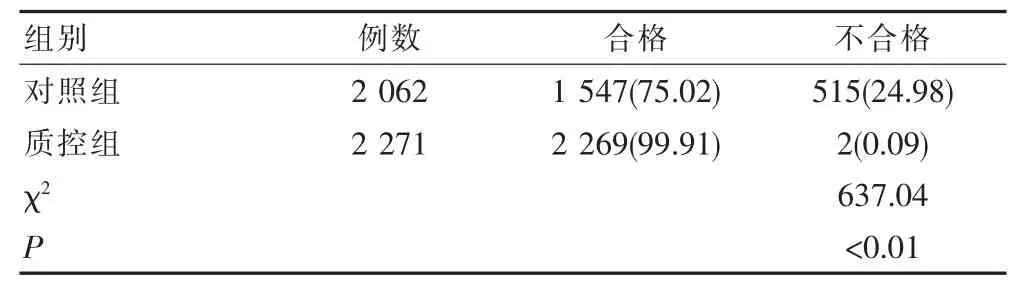
表1 质控方案实施前后冷沉淀制备合格率统计对比[n(%)]
表2 3种血浆标本各项指标统计对比(±s)
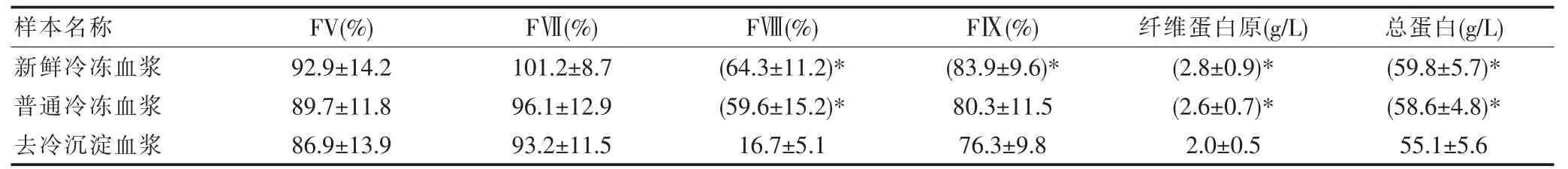
表2 3种血浆标本各项指标统计对比(±s)
注:去冷沉淀血浆分别与其它两种样本对比,*为P<0.05。
普通冷冻血浆去冷沉淀血浆89.7±11.8 86.9±13.9 96.1±12.9 93.2±11.5 (59.6±15.2)* 16.7±5.1 80.3±11.5 76.3±9.8 (2.6±0.7)* 2.0±0.5 (58.6±4.8)* 55.1±5.6
2.2 3种血浆标本各项指标统计对比
经测定新鲜冷冻血浆中FⅧ、FⅨ、纤维蛋白原及总蛋白含量明显高于去冷沉淀血浆,P<0.05,差异有统计学意义;普通冷冻血浆中FⅧ、纤维蛋白原及总蛋白含量均明显高于去冷沉淀血浆,P<0.05,差异有统计学意义。具体数据见表2。
2.3 冷沉淀检测
经测定冷沉淀当中的FⅧ含量为(394.2±72.8)%,纤维蛋白原含量为(6.8±0.8)g/L。
3 讨论
冷沉淀于二十世纪六十年代时被美国科学家Pool首先发现,当时主要应用于血友病的临床治疗当中[5]。近些年来冷沉淀的临床应用已不再局限于纤维蛋白原与凝血因子缺乏导致的出血类疾病、传统的甲型血友病等,在术后创伤、肿瘤手术、多发外伤、自发性气胸、弥散性血管内凝血DIC、黏膜与皮肤病、糖尿病足以及深度烧伤等的临床中也被广泛应用,且应用效果理想[6]。冷沉淀是临床上维持患者生命力不可或缺的一项治疗手段[7]。冷沉淀当中的FⅧ因子十分不稳定,FⅧ在体内的生物半衰期具有较大变化,通常约为8~12 h,活性极易丧失。新鲜冷冻血浆融化后12 h内FⅧ活性可逐渐丧失42%,24 h后则可丧失44%[8]。冷沉淀正被越来越广泛的应用于临床治疗当中[9],因此冷沉淀的制备质量也越来越突显其重要性。冷沉淀的制备过程中须进行严格质量把控。全血采集后应立即置于2~6℃条件下冷藏。新鲜血浆袋的容量应控制在<250 mL范围内并统一容量,避免因容量不同使融化时间及速冻效果产生差异。采集后6 h内冰冻。低温融化箱与离心机均应严格控制温度,应于使用前达到要求温度。
该次研究中新鲜冷冻血浆中FⅧ(64.3±11.2)%、FⅨ(83.9±9.6)%、纤维蛋白原(2.8±0.9)g/L及总蛋白(59.8±5.7)g/L均明显高于去冷沉淀血浆,P<0.05,普通冷冻血浆中FⅧ(59.6±15.2)%、纤维蛋白原(2.6± 0.7)g/L及总蛋白(58.6±4.8)g/L均明显高于去冷沉淀血浆,P<0.05。说明冷沉淀血浆中各项指标的含量与新鲜冷冻血浆、普通冷冻血浆差异较大。黎美君等[10]在相关研究中指出去冷沉淀血浆中FⅧ水平为(16.0± 5.3%、FⅨ水平为(75.5±9.9)%、纤维蛋白原为(2.1±0.3)g/L、总蛋白为(55.4±4.7)g/L,与该次研究结果去冷沉淀血浆中 FⅧ水平为(16.7±5.1)%、FⅨ水平为(76.3± 9.8)%、纤维蛋白原为(2.0±0.5)g/L、总蛋白为(55.1± 5.6)g/L相符。因此在临床治疗中如需补充FⅧ、FⅨ、纤维蛋白原及总蛋白时使用去冷沉淀血浆则无法达到治疗效果,应用将去冷沉淀血浆与普通冰冻血浆区别标识,在临床应用时区别使用。
综上所述,在冷沉淀制备过程中可导致制备结果差异的环节很多,应严格执行操作规程及质量控制要求。有鉴于去冷沉淀血浆中各项指标与新血冷冻血浆的差异较大,应将不同血浆区别标识,临床应用时应根据血浆内各项指标的含量特点区别应用,以提高临床疗效。
[1]曹鸿霖,刘咏梅,陈秀娟,等.冷沉淀制备过程中的关键因素探讨[J].临床输血与检验,2015,17(2):172-173.
[2]张湘.冷沉淀制备方法的改进[J].吉林医药学院学报,2012, 33(4):256-257.
[3]袁小玲,吴杰敏,林桂芳,等.冷沉淀制备技术改进与临床应用情况的研究[J].实验与检验医学,2014,32(3):350-352.
[4]苏红,谭爱玲,许少英,等.冷沉淀制备的关键控制环节[J].中国医学创新,2012,10(10):144-145.
[5]郭博,陈丽,管政.冷沉淀的临床应用[J].蚌埠医学院学报, 2011,36(7):765-766,769.
[6]魏晓娟.冷沉淀在临床中的应用[J].检验医学与临床, 2013,10(2):255-256.
[7]熊荣.冷沉淀的临床应用分析[J].齐齐哈尔医学院学报, 2014,35(19):2893-2894.
[8]王万仲,张雪,王艳.冷沉淀制备技术在血液成分制备中的临床应用效果浅析[J].中国实用医药,2013,8(3):268-269.
[9]王光敏,任思嫡,马怡然,等.冷沉淀在心脏外科手术中的作用[J].血栓与止血学,2011,17(6):269-271.
[10]黎美君,马姗姗,夏代全,等.冷沉淀制备过程的质量控制和去冷沉淀血浆的临床应用价值探讨[J].检验医学与临床,2015,12(6):819-820.
Quality Control of Preparation Process of Cold Precipitation and its Clinical Application Effect
JIANG Yong-hong
The Center and the Department of Blood Donors in Jilin City of Hunchun,Jilin Province,Hunchun,Jilin Province,133300 China
Objective To investigate the effect of cryoprecipitate preparation and clinical application of the quality control method of the whole.Methods A retrospective analysis of 2 062 cold precipitation for the year 2014 production success rate,and summed up a set of cryoprecipitate quality control scheme.Will be implemented after 2015,the year of 2 271 cold precipitation comparing with 2014 data prior to the preparation and implementation success rate,analysis quality control plan.Take the same blood sample was divided into three parts,respectively,for the preparation of fresh frozen plasma.The common cold and frozen plasma to precipitate plasma;three samples of coagulation factor FV,were measured by the FⅤ,FⅦ,FⅧ,FIX,fibrinogen and total protein values were compared and analyzed.Results The control group of cryoprecipitate preparation qualified rate is 99.91%,the control group cold precipitation preparation qualified rate is 75.02%,the control group,cryoprecipitate preparation qualified rate was significantly higher than the control group,P<0.01;In fresh frozen plasma FⅧ(64.3±11.2)%,FⅨ (83.9±9.6),fibrinogen(2.8±0.9)%g/L,and total protein (59.8±5.7)g/L were significantly higher than last year precipitation cold plasma,P<0.05,normal frozen plasma FⅧ(59.6±15.2)%,FⅨ(80.3±11.5)%fibrinogen(2.6±0.7)g/L and total protein(58.6±4.8)g/L content Were significantly higher than those in plasma cryoprecipitate.The conclusion of the P<0.05.Conclusion of cryoprecipitate preparation process of strict quality control can effectively improve the qualified rate,cryoprecipitate plasma and fresh
Cold sediment;Total quality control;Cold plasma;Plasma
R47
A
2096-1782(2016)11-0022-03
蒋永红(1971.9-),朝鲜族,女,吉林珲春人,中专,主管护师,主要从事采血成分制备工作。
2016-08-15)
10.19368/j.cnki.2096-1782.2016.11.022
frozen plasma,ordinary frozen plasma coagulation factor FV,FVII,FⅧ,FIX,protein fiber and total protein numerical differences larger,and therefore to plasma cryoprecipitate in clinical application to fresh frozen plasma.The clinical effect of ordinary frozen plasma,clinical should be chosen according to the specific circumstances.

