氯化苯丙胺盐法全自动化检测微量总蛋白存在重大的方法学缺陷
庄小青,罗士来,杨 露,夏前凤,薛 梦
(1.泗阳仁慈医院检验科,江苏宿迁 223700;2.泗阳县中医院检验科,江苏宿迁 223700)
·经验交流·
氯化苯丙胺盐法全自动化检测微量总蛋白存在重大的方法学缺陷
庄小青1,罗士来2,杨 露1,夏前凤2,薛 梦2
(1.泗阳仁慈医院检验科,江苏宿迁 223700;2.泗阳县中医院检验科,江苏宿迁 223700)
目的 探讨氯化苯丙胺盐法全自动化检测脑脊液或尿液中微量总蛋白发生严重差错的原因。方法 将定值总蛋白采用连续递减稀释法获得35例标本(总蛋白质量浓度0~30 g/L),然后在贝克曼DXC800生化分析仪上采用氯化苯丙胺盐法检测。结果 (1)当总蛋白质量浓度为0~3 g/L时检测值呈线性增加,与理论值一致。(2)当总蛋白质量浓度为3~9 g/L时检测值递减,在0.5~2.5 g/L之间。当总蛋白质量浓度大于9 g/L时检测值趋于0.5 g/L左右。结论 该法不能满足全自动化检测的单区间要求,即检测值存在二元性,故不宜单独采用全自动生化分析仪检测。
生物化学/仪器和设备; 自动化; 血蛋白质类; 氯化苯丙胺盐
氯化苯丙胺盐与脑脊液或尿液中微量总蛋白结合产生稳定的浊度,通过浊度变化确定微量蛋白质的质量浓度。据文献报道,该方法稳定性好、灵敏度高、线性范围宽、抗干扰能力强[1]。2014年7月至2015年5月作者使用该法试剂盒在全自动生化分析仪上检测微量总蛋白共计120例,其中结果出现严重偏差5例,与临床诊断不符。经实验研究表明,该法存在重大方法学缺陷,即对高质量浓度标本无反应饱和点,无法进行纠正与监测,导致检测值存在二元性,易误诊病理性高值,现报道如下。
1 材料与方法
1.1 材料 美国贝克曼定值血清(总蛋白质量浓度30 g/L)。
1.2 仪器与试剂 美国贝克曼全自动生化分析仪 Dxc 800及其配套试剂、校准品;氯化苯丙胺盐法脑脊液及尿蛋白检测试剂盒(检测线性0~3 g/L),配套标准品及质控品(国产)。
1.3 方法 确认按照试剂盒说明书设置检测参数并定标,连续检测质控品20个工作日,确认试剂稳定、测量状态在控;确认检测人员已熟练掌握仪器与试剂盒使用方法。采用生理盐水将贝克曼定值血清按约1 g/L质量浓度递减连续稀释获得30份标本,再将第30号标本(总蛋白质量浓度为0.9 g/L)按倍比稀释法获取5份标本,见表1。将35份标本编号后按1~35号和35~1号次序测量2次,取均值。
1.4 数据处理 应用Excel2003软件进行数据分析、计算、绘图与制表等。
2 结 果
总蛋白质量浓度大于3 g/L时检测值不是趋于饱和而是下降,造成检测值二元性,不能满足全自动化检测的单区间要求。35份标本检测结果见表2。
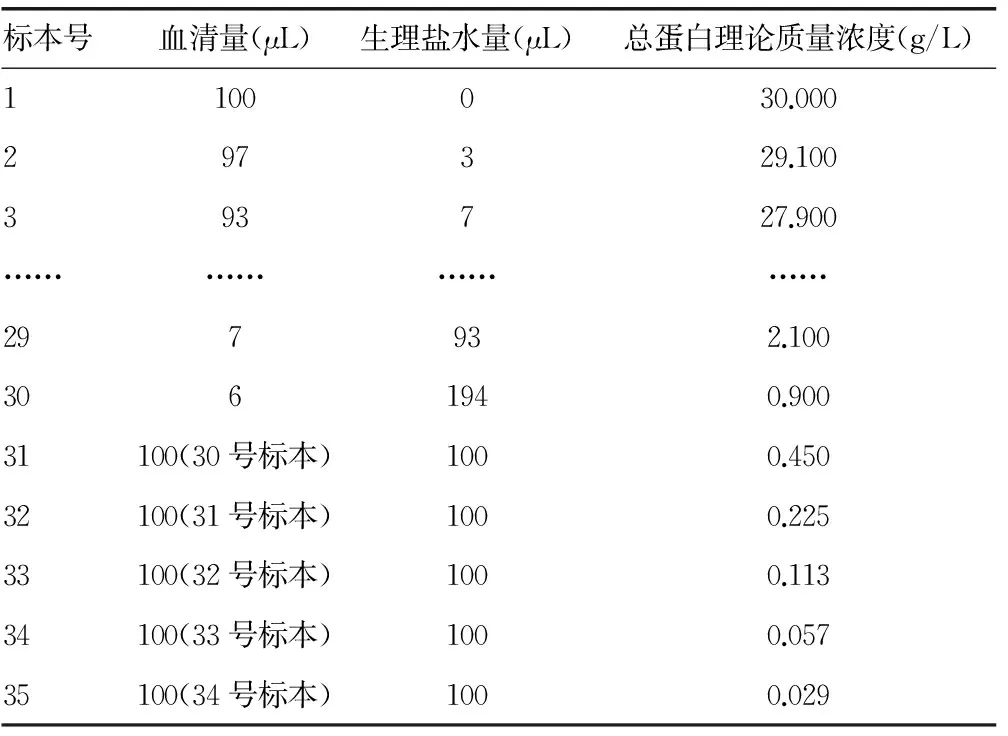
表1 定值血清稀释后质量浓度(g/L)

表2 35份标本检测结果
3 讨 论
在微量总蛋白检测方法中磺基水杨酸比色法需要自配试剂、操作繁琐、易产生凝块造成误差且标准液不统一、精密度较低。染料结合法和邻苯三酚红钼络合法对清蛋白的灵敏度高于球蛋白,且染料易污染比色杯。干化学法测定线性宽、速度快,但成本很高。据文献报道氯化苯丙胺盐法是较理想的方法[2-8]。
作者在使用该法时发现会出现严重误差并据此进行深入探讨。对35份标本的检测结果与理论值绘制成散点图,见图1。当总蛋白质量浓度为0.029~3 g/L时检测结果与理论值相关性好,其散点图呈直线型(Ⅰ区);3~6.9 g/L时图形呈快速下降趋势(Ⅱ区);8.1~30 g/L时其散点图呈低吸光度平缓趋势(Ⅲ区)。很直观地表明采用该法检测高质量浓度标本时其检测值不成饱和状态,反而快速、无规律下降(是形成大小不一的凝块所致),造成所有结果均存在二元性。即使采用定性方法确定送检标本为病理性,需进行稀释测定,但也绝对不知如何稀释才能确保稀释标本待测质量浓度在该法检测线性范围内,否则检测结果仍为二元性,说明该法存在重大方法学缺陷。

图1 35份标本检测值与理论值配对散点图
通过对35份标本检测过程进行连续监测,根据图1的3个不同区域选择代表性标本绘制检测反应曲线图,见图2。曲线1、2、3总蛋白质量浓度在该法检测范围内并逐渐增加,由图2可见,随着总蛋白质量浓度增加,测量吸光度亦逐渐增加,对每一个标本而言,在整个反应过程中吸光度是稳定逐渐增加的。曲线4、5、6总蛋白质量浓度大于该法检测范围并逐渐增加,但其最大吸光度、测量吸光度、反应速度及反应过程均无固定规律并与曲线1、2、3重叠交叉,说明该法方法学缺陷是无法在全自动生化分析仪上设置参数进行监测与纠正[9-11]。

图2 典型检测反应曲线图
综上所述,采用全自动生化分析仪应用氯化苯丙胺盐法检测微量总蛋白会因方法学存在缺陷造成所有测量结果均在其检测线性范围之内,需人工对检测值甄别避免高值误诊,故不宜单独采用全自动生化分析仪检测。
[1]唐晓霞.氯化苯丙胺盐比浊法检测脑脊液蛋白质方法学评价[J].检验医学与临床,2013,10(12):1553-1554.
[2]叶应妩,王毓三,申子瑜.全国临床检验操作规程[M].3版.南京:东南大学出版社,2006:342.
[3]张文英,赵毓祥,沈广虎.脑脊液蛋白检测方法学评价[J].国际检验医学杂志,2010,31(11):1334-1335.
[4]陈新宽.伊红Y染料结合法测定脑脊液蛋白在全自动生化分析仪上的应用[J].检验医学与临床,2012,9(3):335-336.
[5]胡志斌.两种脑脊液及尿蛋白定量方法的比较[J].检验医学与临床,2012,9(10):1251-1252.
[6]殷舟,陈屹一,蒋朱秀,等.脑脊液微量总蛋白检测体系最低检出限的非参数评估方案[J].医学研究杂志,2013,42(7):70-73.
[7]胡盈莹,胡望平,周长邵,等.尿液与脑脊液总蛋白测定方法研究[J].医学研究杂志,2007,36(3):56-57.
[8]黄小燕,李宇雄,戴小波.苄索氯铵比浊法测定脑脊液蛋白质的方法学评价[J].检验医学与临床,2008,5(15):902-903.
[9]徐国宾,蒋琳.临床生物化学常规定量方法的分析性能评价[J].中华检验医学杂志,2007,30(6):718-720.
[10]罗梅,贺岩,张晓宇.全自动生化分析仪参数设置与应用[J].国际检验医学杂志,2012,33(2):222-223.
[11]肖玉鹏,吴卫平.自动生化分析仪定量测定脑脊液总蛋白[J].检验医学与临床,2007,4(2):116-117.
10.3969/j.issn.1673-4130.2016.02.063
B
1673-4130(2016)02-0275-03
2015-07-09)

