儿童肺炎支原体感染及耐药检测与分析*
刘调侠 张晓瓒 李延琴
(铜川市妇幼保健院 1.儿科;2.检验科, 陕西 铜川 727007)
·论著·
儿童肺炎支原体感染及耐药检测与分析*
刘调侠1张晓瓒2李延琴1
(铜川市妇幼保健院 1.儿科;2.检验科, 陕西 铜川 727007)
目的 分析肺炎患儿中肺炎支原体(MP)的感染及耐药情况,并探讨其临床特点及基因分型特征,为临床合理选择抗生素提供理论依据。方法 收集2015年1月至2015年12月铜川市妇幼保健院儿科以发热、咳嗽等呼吸道症状首诊确定MP感染的住院患儿120例。通过肺炎支原体抗体检测、体外培养及核酸检测了解肺炎支原体感染状况,测定多种抗菌药物的最低抑菌浓度(MIC值),分离出耐药菌株。根据药敏试验鉴定结果分为耐药组(n=98)和非耐药组(n=22),比较耐药组与非耐药组患儿临床特征;将耐药组98例患儿依据初选抗生素种类分为初选阿奇霉素或红霉素组(n=78)和初选头孢或青霉素类(n=20),比较两组患儿的临床特点。将耐药菌株的23SrRNA基因序列与标准珠相比对,研究耐药菌株的23SrRNA基因突变位点。结果 120例经临床诊断为MP肺炎的患儿中,98例体外药敏试验结果提示为耐药支原体肺炎,对大环内酯类药物高度耐药。耐药组发热时间、住院时间及给予大环内酯类药物(阿奇霉素)后发热时间均较非耐药组长(P<0.05),两组间年龄、呼吸道症状时间、白细胞计数(WBC)、中性粒细胞比例、C反应蛋白(CRP)、血沉(ESR)、影像所见好转时间、大环内酯类抗生素(ML)总疗程比较差异均无统计学意义(均P>0.05)。耐药组与非耐药组之间预后比较差异有统计学意义(P<0.05),其中非耐药组痊愈患儿比例高于耐药组。98例耐药支原体肺炎中初选头孢或青霉素类抗生素组20例,治疗中更改为大环内酯类抗生素的平均时间为病程第(5.2±1.8)天。初选不同治疗药物两组在呼吸道症状持续时间、使用大环内酯类抗生素后发热时间、白细胞计数等指标差异有统计学意义(P<0.05)。肺炎支原体核糖体23S rRNA全序列分析:其中约90%耐药MP株发生了2063位A→G(A2063G)的突变,少数MP耐药株发生了 A2064G(约5%)、A2063C、C2617G/A 的突变。结论 铜川地区2015年支原体肺炎患儿对大环内酯类抗生素耐药现象严重,其耐药机制主要与2063位A→G(A2063G)的点突变有关。非耐药组患儿预后好于耐药组。MP快速鉴定培养与直接药敏试验方法标本获取容易,检测技术操作简单,检测结果可为临床诊疗提供科学依据。
肺炎支原体; 感染; 儿童; 耐药机制
肺炎支原体(mycoplasma pneumoniae,MP)是患儿急性上、下呼吸道感染的常见病原体之一。研究表明,肺炎支原体肺炎具有年龄分布特征和季节性,不同国家和地区的发病率差别较大。儿童MP感染主要以大环内酯类药物治疗为主;近年来关于MP耐药现象的报道较多[1]。本研究通过对铜川地区住院肺炎患儿肺炎支原体感染及耐药检测与分析,以期对临床MP肺炎的诊治提供依据。
1 资料与方法
1.1 一般资料 收集本院2015年1月至2015年12月以发热、咳嗽等呼吸道症状首诊确定MP感染的住院患儿120例,其中男性患儿64例(53.33%),女性患儿56例(46.67%)。MP肺炎诊断标准依据《诸福棠实用儿科学》第7版诊断标准,有发热、持续剧烈咳嗽、肺部啰音等呼吸道症状及体征,伴胸部影像学单侧或双侧异常改变,酶联免疫吸附法(ELISA)检测肺炎支原体抗原阳性,青霉素或头孢类抗生素治疗无效,病程初期未发现其他病原感染的证据。排除标准:①体液和细胞免疫异常。②正在接受免疫抑制剂治疗。③既往患支气管哮喘、反复呼吸道感染、先天性或继发性免疫抑制或缺陷、肾脏或肝脏疾病、心血管疾病及结缔组织疾病等,既往1个月内接受住院治疗。④既往有重症肺炎病史仍未痊愈。⑤病历资料不完整。纳入本研究的病例均已获患儿家属知情同意。依据是否耐药分为耐药组(n=98)和非耐药组(n=22);依据98例耐药支原体肺炎按初选抗生素种类分为初选阿奇霉素或红霉素组(n=78)及初选头孢或青霉素类抗生素组(n=20)。
1.2 方法
1.2.1 主要仪器及试剂 TGL-16G型台式高速离心机、Bio-rad公司Opticon 2 PCR扩增仪、GeneAmp PCR System9600、HB-100型电热恒温水槽、ELX-800酶标仪、Milli-Q纯水系统、DNP-9052型电热恒温培养箱、PCR扩增试剂、MP-IgM检测试剂盒、DNA提取试剂盒、MP快速液体培养基、MP标准株MP-129。
1.2.2 标本采集 所有患儿在入院后24 h内完成标本的采集,抽取外周血2 ml用于ELISA法检MP-IgM抗体,用无菌生理盐水浸湿的无菌咽拭子适度用力刮拭患儿咽后壁,标记后行MP培养和MP-PCR检测。
1.2.3 检测方法 ①酶联免疫吸附法试验(ELISA)检测MP-IgM抗体:按照深圳博卡生物有限公司提供的试剂盒说明书进行操作及结果的判定。②MP快速液体培养法:液体培养基在使用前置于4 ℃保存,用时移至室温待培养基融化后使用。应注意MP对热和干燥敏感,取材后应立即接种,若置于转运培养基中,4 ℃能保存72 h。 所有患儿采取标本前用温水漱口,然后用无菌生理盐水浸湿的咽拭子在患儿口腔咽后壁捻转数次,60 min内送至实验室,小心取出棉拭子,置于含培养基的小瓶中,揽动棉拭子数次,再把棉拭子对着瓶壁,尽量挤压出其中液体,取出棉拭子弃至医疗垃圾桶中。盖上瓶塞,置37 ℃恒温箱中培养24~48 h即可观察结果,待培养基颜色由红转黄且无明显沉淀物时,判断为肺炎支原体培养阳性。利用九种抗生素的高低浓度在体外对微生物生长的抑制作用,对微生物作耐药性进行分析,采用珠海市银科医学工程股份有限公司生产的MP 培养药敏试剂盒,严格按说明书进行操作。③肺炎支原体PCR检测:向咽拭子中加入4倍体积的生理盐水,用1 ml移液器反复吹打后置4 ℃冰箱。用移液器混匀后吸取1~1.5 ml离心管中。12 000 rpm离心5 min后弃上清;在沉淀中加入50 μL的DNA提取液充分混均。100 ℃恒温处理10 min;12 000 rpm离心5min后保存于-20 ℃冰箱中备用。2×缓冲液10.0 μL,10.0 μmol/L 的引物 P3 1.0 μL,10.0 μmol/L 引物 P4 1.0 μL,模板DNA 1.0 μL,ddH2O 7.0 μL。反应条件及循环:93 ℃变性2 min;95 ℃ 1 min,50 ℃ 1 min,72 ℃ 1 min,35个循环;75 ℃延伸5 min。荧光测定PCR产物采用胶回收试剂盒回收,采用T Easy载体连接体系克隆,4 ℃连接过夜。转化感受态细胞,蓝白斑筛选。采用Blast功能进行序列分析,挑选测序结果一致的克隆提取质粒备用。巢式PCR:2×缓冲液10.0 μL,40×Assay Mix(含P3,P4,T3和T4各0.5 μL),DNA模板1.0 μL,ddH2O 7.0 μL,总体积20.0 μL。反应条件及循环:95 ℃ 1 min,92 ℃ 15 s;60 ℃ 1 min,40个循环。收集扩增前,扩增时,扩增后荧光信号,采用SDS 软件获得标准曲线。④肺炎支原体核糖体23s全序列分析:利用外引物MN23SDVF、MN23SDVR和巢式引物MN23SF1812、MN23SR2152进行扩增,PCR产物采用双向测序。测得序列与NCBI已登录的MP标准珠MP129 23SrRNA基因相比对。产物由华大基因科技有限公司进行测序。采用DNAstar软件与肺炎支原体M129(GenBank Accession No.X68422)进行序列比对分析。
1.3 观察指标
1.3.1 记录患儿的一般临床资料 性别、年龄、住院天数、发热时间、呼吸道症状持续时间、初起选择抗生素的种类、病程中更换为大环内酯类抗生素的时间,使用大环内酯类抗生素后发热时间、大环内酯类抗生素的使用时间等。
1.3.2 记录相关辅助检查结果 白细胞总数、中性粒细胞比例、C反应蛋白、血沉、肺炎支原体抗体结果、咽拭子肺炎支原体PCR结果、肺炎支原体培养结果及MIC值等,胸部影像学表现及影像学指标好转时间。
1.3.3 疗效判断 疗效分痊愈,显效,进步,无效4级。痊愈:初始治疗2周内体温、呼吸道症状及体征正常,实验室检查血象、CRP均恢复正常;显效:体温呈下降趋势,但呼吸道症状、体征,实验室检查均未完全恢复正常;进步:体温不退,但呼吸道症状、体征、实验室检查中至少有一项改善;无效:体温不降,呼吸道症状体征、实验室检查无改善,或一度改善又恶化。
1.4 统计学方法 应用SPSS 17.0统计软件进行数据处理。计数资料采用2检验,计量资料用t检验,组间比较采用独立样本t检验,非正态分布资料采用非参数检验。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 120例经临床诊断为MP肺炎的患儿中,血清MP-IgM抗体检测均为阳性。113例咽拭子肺炎支原体PCR检测阳性;其余7例PCR检测阴性,PCR检测阴性者咽分泌物支原体培养阳性。咽分泌物支原体培养阳性者为101例。98例体外药敏试验结果提示为耐药支原体肺炎,对大环内酯类药物高度耐药。体外药敏实验结果见表1。

表1 120例MP肺炎患儿感染样本的药敏试验结果(MIC值,mg/L)
2.2 MP肺炎耐药组与非耐药组临床特点比较 两组患儿的临床表现及检验结果显示,耐药组发热时间、住院时间及给予大环内酯类药物(阿奇霉素)后发热时间均较非耐药组长(P<0.05);两组间年龄、呼吸道症状时间、白细胞计数(WBC)、中性粒细胞比例、C反应蛋白(CRP)、血沉(ESR)、影像所见好转时间、大环内酯类抗生素(ML)总疗程比较均差异无统计学意义(P>0.05),见表2。
2.3 初选阿奇霉素或红霉素组和初选头孢或青霉素类抗生素组临床特点比较 初选头孢或青霉素类抗生素组20例,治疗中更改为大环内酯类抗生素药物的平均时间为病程第(5.2±1.8) d。两组比较后发现在呼吸道症状持续时间、使用大环内酯类抗生素后发热时间、白细胞计数等指标差异有统计学意义(P<0.05),见表3。
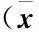
Table 2 Clinical features of resistant group and non-resistant group

临床指标 耐药组(n=98)非耐药组(n=22)P年龄(岁)8±37±40.518发热时间(d)11±48±50.007呼吸道症状时间(d)18±516±40.085WBC(×109/L)7±48±40.176中性粒细胞比例0.68±0.740.61±0.830.457CRP(mg/L)11.01±18.2313.0±20.610.972ESR(mm/h)25±1322±140.682胸部影像所见好转时间(d)14±313±50.661住院时间(d)12±38±40.001ML总疗程10±39±50.438用ML后发热时间(d)8±36±40.042
2.4 耐药组与非耐药组患儿预后比较 耐药组与非耐药组之间预后的比较有统计学意义(P<0.05),其中非耐药组痊愈患儿比例高于耐药组(P<0.05),见表4。
Table 3 Clinical characteristics of children with different antibiotics resistance of mycoplasma pneumonia primaries
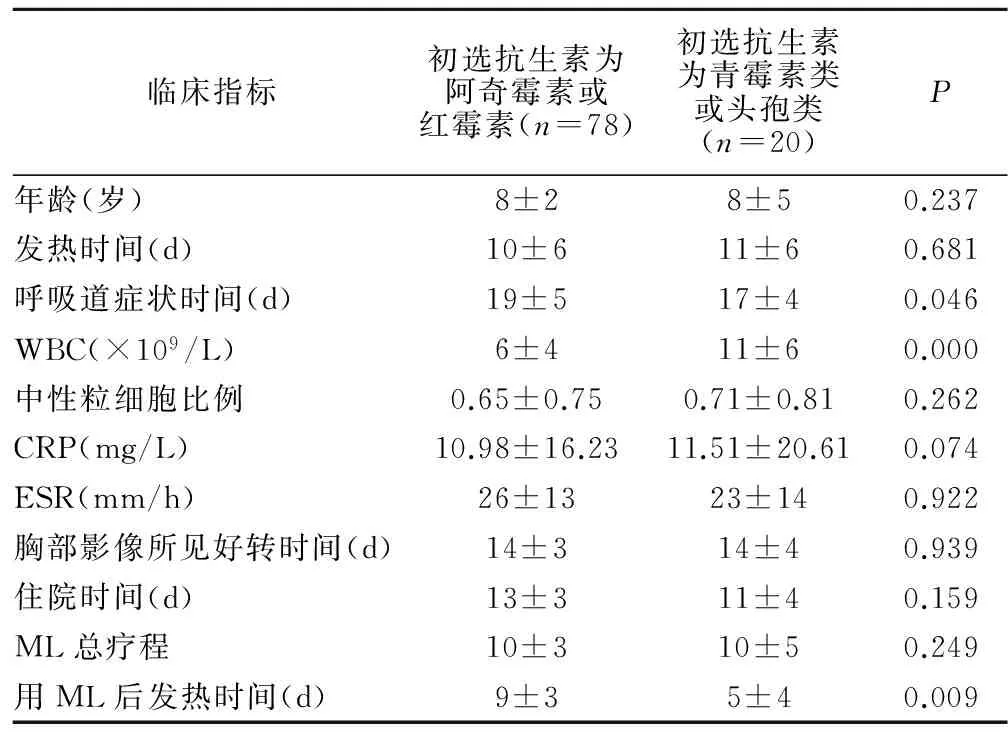
临床指标初选抗生素为阿奇霉素或红霉素(n=78)初选抗生素为青霉素类或头孢类(n=20)P年龄(岁)8±28±50.237发热时间(d)10±611±60.681呼吸道症状时间(d)19±517±40.046WBC(×109/L)6±411±60.000中性粒细胞比例0.65±0.750.71±0.810.262CRP(mg/L)10.98±16.2311.51±20.610.074ESR(mm/h)26±1323±140.922胸部影像所见好转时间(d)14±314±40.939住院时间(d)13±311±40.159ML总疗程10±310±50.249用ML后发热时间(d)9±35±40.009
表4 耐药组与非耐药组患儿预后比较
Table 4 prognosis of resistance group and non-resistant group
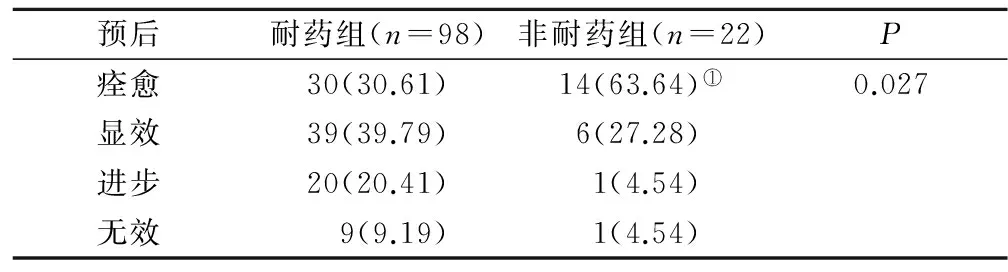
预后耐药组(n=98)非耐药组(n=22)P痊愈30(30.61)14(63.64)①0.027显效39(39.79)6(27.28)进步20(20.41)1(4.54)无效9(9.19)1(4.54)
注:与耐药组比较,P<0.05
2.5 肺炎支原体核糖体23S rRNA全序列分析 约90%耐药MP株发生了2063位A→G(A2063G)的突变,少数MP耐药株发生了 A2064G(约5%)、A2063C、C2617G/A 的突变,而且A2063G/C和 A2064G 的突变能引起 MP 对红霉素产生高水平耐药,并对其他大环内酯类发生交叉耐药。
3 讨论
肺炎支原体(MP)是介于细菌与病毒之间,无细胞壁的一类原核细胞型生物,其已成为儿童社区获得性肺炎的常见病原体之一。因为缺乏细胞壁结构,对β-内酞胺类、糖肽类和磺胺类等抗生素固有耐药[2]。既往认为肺炎支原体对大环内酯类药物敏感性高,无耐药性产生。2000年Okazaki等[3]首次在儿童患者体内分离到对大环内酯类抗生素耐药的MP。随后国内外相继报道了在临床标本中尤其儿童患者中分离得到对大环内酯类抗生素耐药的MP[4-7]。德国报道MP的耐药率为3%[8];我国北京地区报道儿童MP的耐药率>80%[9]。本研究中支原体肺炎患儿耐药率为81.67%(98/120),可见本地区支原体耐药现象亦十分严重。
引起微生物对大环内酯类抗生素耐药的主要机制是:①靶位改变: 基因突变或甲基化。②主动外排。③药物灭活。基因点突变导致的靶点改变是肺炎支原体对大环内酯类耐药的最重要原因。23S rRNA 结构域V区和II区与抗生素直接结合的碱基点突变可导致抗生素与核糖体亲和力下降而引起耐药[10-15]。既往文献报道的基因突变集中在23SrRNA V区2063或2064位点基因颠换或转换,主要表现为A2063G、A2063C和A2064G发生点突变,以A2063G最为常见[16-18]。本研究中约90%耐药MP株发生了2063位A→G(A2063G)的突变,少数MP耐药株发生了 A2064G(约5%)、A2063C、C2617G/A 的突变,而且A2063G/C和 A2064G 的突变能引起 MP 对红霉素产生高水平耐药,并对其他大环内酯类发生交叉耐药。可见核糖体23S rRNA A2063G核苷酸点突变仍是引起肺炎支原体对红霉素耐药的主要机制。
本研究显示耐药组发热时间和给予大环内酯类药物(阿奇霉素)后发热时间均较非耐药组长,提示耐药组患儿病情相对更严重,发热时间更长。两组间年龄、呼吸道症状时间、白细胞计数、中性粒细胞比例、C反应蛋白、血沉、影像所见好转时间、大环内酯类药物总疗程等方面比较并无差异。耐药组住院时间明显延长,考虑与耐药组患者病程中发热时间及使用大环内酯类药物后发热时间均较非耐药组患儿延长有关。
在病程初期,在白细胞计数较正常升高的病例治疗上,医生往往更易选择头孢或青霉素类抗生素,因此大环内酯类药物的初始给药时间较晚。初选头孢及青霉素类药物组,比初选大环内酯类抗生素的患儿用大环内酯类药物后发热时间较短,差异有统计学意义,提示初选头孢及青霉素类药物对耐药支原体肺炎患儿的发热程度影响并不明显。病程初期使用非有效抗生素(头孢或青霉素类)者住院时间无明显延长,提示其对治疗效果的影响不明显。本研究提示非耐药组患儿预后好于耐药组,而耐药组治疗无效病例高于耐药组,但并无统计学意义,此部分病例为重症耐药支原体肺炎,其研究还有待于进一步完善。目前支原体肺炎耐药率较高,对于是否可继续使用大环内酯类抗生素治疗仍有争议[19]。目前国内外治疗选择仍以阿奇霉素和红霉素为主,必要时予肾上腺皮质激素等免疫治疗。
在耐药支原体感染十分严重的现状下,支原体肺炎治疗过程中应尽早使用不同的诊断方法,及时判断病情程度,以减轻患儿组织器官的损害,缩短病程,尽量避免肺内外并发症的发生[20]。MP快速鉴定培养与直接药敏试验方法标本获取容易,检测技术操作简单,检测结果可为临床诊疗提供科学依据。针对耐药支原体感染的病原学和发病机制以及有效的治疗仍有待于进一步研究。
4 结论
铜川地区2015年支原体肺炎患儿对大环内酯类抗生素耐药现象严重,其耐药机制主要与2063位A→G(A2063G)的点突变有关。非耐药组患儿预后好于耐药组。MP快速鉴定培养与直接药敏试验方法标本获取容易,检测技术操作简单,检测结果可为临床诊疗提供科学依据,应在临床推广应用。
[1]Zhao F, Liu LY, Tao XX,etal. Culture-Independent Detection and Genotyping of Mycoplasma pneumoniae in Clinical Specimens from Beijing, China[J]. PLoS One, 2015,59(2): 10481-051.
[2]Yang E,Altes T, Anupindi SA.Early Mycoplasma pneumoniae infection presenting as multiple pulmonary masses: an unusual presentation in a child[J].Pediatr Radiol,2008,38(4):477-480.
[3]Okazaki N,Narita M,Yamada S,etal.Characteristics of macrolide-resistant Mycoplasmapneumoniae strains isolated from patients and induced with erythromycinin vitro[J]. Micro Immune, 2001, 45(12):617-620.
[4]Cao B, Zhao CJ, Yin YD,etal. High prevalence of macrolide resistance in Mycoplasma pneumoniae isolates from adult and adolescent patients with respiratory tract infection in China[J]. Clin Infect Dis, 2010, 51(7):189-194.
[5]Dumke R, von Baum H, Luck PC,etal. Occurrence of macrolideresistant Mycoplasma pneumoniae strain in Germany[J]. Clin Microbiol Infect, 2010, 16(10):613-616.
[6]姜越, 刘禧杰,秦选光,等. 2011年北京地区儿童肺炎支原体耐药情况及其耐药机制研究[J]. 中国全科医学,2013, 11(16):3778-3782.
[7]韩旭, 辛德莉. 肺炎支原体对大环内酯类抗生素的耐药机制[J].实用儿科临床杂志, 2006, 21(16): 1101-1103.
[8]Peuchant O,Menard A,Renaudin H,etal.Increased macrolide resistance ofMycoplasma pneumoniae in France directly detected in clinical specimens byreal-time PGR and meltingcurve analysis[J].Antimicrob Chemother,2009,64 (1):52-58.
[9]Roger Dumke, Enno Jacobs. Evaluation of Five Real-Time PCR Assays for Detection of Mycoplasma pneumoniae[J]. J Clin Microbiol, 2014,52(11): 4078-4081.
[10] 付玲, 谭继权. 小儿呼吸道感染快速肺炎支原体鉴定及药敏检测对指导临床抗生素应用的价值[J].医学临床研究, 2015, 32(2): 304-306.
[11] 孙红妹, 薛冠华,闫超,等. 2010-2012年北京地区儿童肺炎支原体流行基因型监测[J]. 中华微生物学和免疫学杂志, 2012, 32(11): 939-943.
[12] 叶芸, 李苏亮,姜萍,等. 肺炎支原体23SrRNA基因突变位点与耐药表型的分析[J]. 检验医学, 2013, 28(1): 11-16.
[13] 汪小五, 曾宪聪,陈伟,等. 肺炎支原体P1蛋白的制备及其应用的初步研究[J]. 安徽医科大学学报, 2014, 49(12): 1709-1713.
[14] 李东, 范丽萍,孙惠泉,等. 肺炎支原体流行株基因分型研究[J]. 临床儿科杂志, 2015(4): 338-341.
[15] 陈岳明, 张卫英,余道军,等. 肺炎支原体耐大环内酯类抗菌药物分子机制的初步研究[J]. 中华医院感染学杂志, 2009,19(8): 877-879, 895.
[16] 廖嘉仪, 张涛. 13 198 例急性呼吸道感染住院患儿肺炎支原体、肺炎衣原体及嗜肺军团菌分布特点分析[J].中国当代儿科杂志,2016,18(7):607-613.
[17] Piedra PA, Mansbach JM, Jewell AM,etal. Bordetella pertussis is an uncommon pathogen in children hospitalized with bronchiolitis during the winter season[J]. Pediatr Infect Dis J,2015,34(6):566-570.
[18] Metaxas EI, Balis E, Papaparaskevas J,etal. Bronchiectasis exacerbations: The role of atypical bacteria, respiratory syncytial virus and pulmonary function tests[J]. Can Respir J,2015,22(3):163-166.
[19] Simmons WL, Dybvig K. Catalase Enhances Growth and Biofilm Production of Mycoplasma pneumoniae[J]. Curr Micro-biol,2015,71(2):190-194.
[20] Zhou Z, Li X, Chen X,etal. Comparison of P1 and 16S rRNA genes for detection of Mycoplasma pneumoniae by nested PCR in adults in Zhejiang, China[J]. J Infect Dev Ctries,2015,9(3):244-253.
(收稿: 2016-05-16; 修回: 2016-08-08; 编辑: 张文秀)
The infection of mycoplasma pneumoniae, detection and analysis of drug resistance in children
LIU Diaoxia1, ZHANG Xiaozan2, LI Yanqin1
(1.DepartmentofPediatrics,TongchuanMaternalandChildHealthCareCenter,Tongchuan727007,Shanxi,China;2.ClinicalLaboratory,TongchuanMaternalandChildHealthCareCenter,Tongchuan727007,Shanxi,China)
Objective To analyze the infection and drug resistance of mycoplasma pneumoniae in children, explore its clinical characteristics and genotyping feature, and provide a theoretical basis for the selection of antibiotic. Methods 120 children of mycoplasma pneumoniae pneumonia were enrolled. The infection of mycoplasma pneumoniae was explored by detection of mycoplasma pneumoniae antibody and nucleic acid. The MIC value of multiple antimicrobial drugs was tested. The drug-resistant strains was isolated. The children were divided into drug resistance group and non- drug resistance group by drug-resistant results. The clinical features drug resistance group and non- drug resistance group were compared. The gene sequence of 23SrRNA of drug-resistant strains and non- drug resistance group were detected.Results 98 cases were drug-resistant pneumonia according to susceptibility test results in vitro, which were highly resistant to macrolides .The time of fever and hospitalization in drug resistance group were longer than that of non-drug resistance group (P<0.05). The age, duration of symptoms of respiratory tract, white blood cell count (WBC), neutrophil percentage, C-reactive protein (CRP), erythrocyte sedimentation rate (ESR), the image seen better times, period of treatment with macrolides (ML) showed no statistical significance between the two groups. The prognosis was statistically significant (P<0.05) between drug resistance group and non-drug resistance group. The proportion of healed cases in non-drug resistance group was higher than that of the drug resistance group. The time of change the treatment with macrolide antibiotics was (5.2±1.8) d. The duration of respiratory symptoms, time of fever, white blood cell counts and other indicators were statistically significant in groups of different treatment. There were 90% of mutations occurred A2063G in drug-resistant strains and 5% occurred A2064G, A2063C and C2617G/A.Conclusion MP is widely prevalent in children and its resistance to MLs is serious in the region of Tongchuan of the year of 2015. Its principal mechanism of resistance were 2063 A→G (A2063G) of point mutations. Non-drug resistance group of children has a better prognosis than drug resistance groups. Rapid culture identification of MP and drug susceptibility testing meet clinical requires of easy collection and simple handling and provide scientific rationals for clinical diagnosis and treatment.
Mycoplasma pneumoniae; Infection; Children; Mechanism of drug resistance
陕西省科技攻关课题(CX14A016)
R 735+.2;R 725.6
A
10.3969/j.issn.1672-3511.2016.11.031

