剂量调整B-NHL-BFM95方案治疗儿童非霍奇金淋巴瘤临床研究
陈宁斌,吴 晖,陈 英,杨 瑜,何鸿鸣,陈道光,林剑扬,郑艳彬,邹思平,王杰松,陈秀容
(福建省肿瘤医院、福建省肿瘤转化重点实验室、福建医科大学教学医院,福建 福州 350014)
剂量调整B-NHL-BFM95方案治疗儿童非霍奇金淋巴瘤临床研究
陈宁斌,吴 晖,陈 英,杨 瑜,何鸿鸣,陈道光,林剑扬,郑艳彬,邹思平,王杰松,陈秀容
(福建省肿瘤医院、福建省肿瘤转化重点实验室、福建医科大学教学医院,福建 福州 350014)
目的 探讨改良B-NHL-BFM95方案治疗儿童非霍奇金淋巴瘤的临床疗效和毒副反应。方法 入组20例经病理确诊的14岁以下非霍奇金淋巴瘤患者,均接受改良B-NHL-BFM95方案治疗,未行放疗。结果 近期疗效:18例(90.0%)CR,2例(10.0%)PD。治疗期间大部分患者出现Ⅲ、Ⅳ度骨髓抑制,经对症处理恢复正常,不影响下一步治疗。中位随访55个月,全组3 a无事件生存率80.0%,Ⅰ~Ⅱ期100.0%,Ⅲ~Ⅳ期60.0%;低危组100.0%,中危组85.7%,高危组50.0%。结论 改良B-NHL-BFM-95方案治疗儿童非霍奇金淋巴瘤,特别是低、中危儿童非霍奇金淋巴瘤疗效显著,毒副反应可耐受。
改良B-NHL-BFM95方案;非霍奇金淋巴瘤;疗效;毒副反应
儿童成熟B细胞淋巴瘤,包括Burkitt型和大淋巴细胞型,恶性度高,进展快,容易出现骨髓和中枢侵犯,死亡率高[1]。单用CHOP方案生存率大约在30%~40%[2-3]。目前欧美国家淋巴母细胞淋巴瘤/白血病采用治疗方案包括诱导-强化-巩固-再强化和维持治疗;而其他类型的侵袭性和高度侵袭性淋巴瘤采用短程、高强度、多药联合和中枢预防的治疗方案治疗,使儿童侵袭性和高度侵袭性巴瘤生存率超过80%。德国学者采用B-NHL-BFM95方案治疗,全组患者3 a无事件生存89%,低中危患者为94%,高危患者为81%[4]。我科自2010年3月至2014年7月采用改良B-NHL-BFM-95方案治疗儿童非霍奇金淋巴瘤,取得显著疗效,现报道如下。
1 资料与方法
1.1 临床资料 入组20例经病理确诊的14岁以下非霍奇金淋巴瘤患者(伯基特淋巴瘤13例、灰区淋巴瘤5例、弥漫大B细胞淋巴瘤2例),年龄4~14岁,中位年龄10岁;男15例,女5例;所有患者均行详细影像学检查(包括胸腹盆及病灶部位CT或MR检查)及骨髓穿刺检查;Ann Arbor分期:Ⅰ期3例(15.0%),Ⅱ期7例(35.0%)Ⅲ期4例(20.0%),Ⅳ期6例(30.0%),其中Ⅲ~Ⅳ期患者占50.0%。肿瘤主要侵犯:淋巴结、肠、骨、肾上腺、肾、骨髓、鼻咽、上颌窦、脑膜、椎管、肺等部位。全组患者乳酸脱氢酶(LDH)中位水平216(114~2 065)IU·L-1,15例≤500 IU·L-1,1例760 IU·L-1,4例>1 000 IU·L-1。
1.2 治疗方法 所有患者采用改良B-NHL-BFM-95方案,根据患者Ann Arbor分期、LDH水平及是否完整切除分为低危、中危、高危,其中低危组7例、中危组7例、高危组6例。低危组接受A-B或A-B-A-B方案;中危组接受V-A-B-A-B-A-B方案;高危组接受V-AA-BB方案治疗后评价如果达CR或CRu,则继续AA-BB-AA-BB方案共6周期,如果未达CR或CRu则予CC-AA-BB-CC方案共6周期。A、B方案中MTX静滴4 h; AA、BB方案中MTX予10%的剂量静滴30 min,剩余剂量静滴23.5 h。CF于MTX结束后12 h开始解救30 mg·m-2q6 h至血MTX浓度降至1×107mol·L-1。MTX治疗期间予以水化碱化。见表1~3。

表1 危险度分级及治疗
1.3 疗效评价 疗效评定按照国际淋巴瘤工作组制定非霍奇金淋巴瘤治疗反应标准,分为完全缓解(CR)、不确定的完全缓解(CRu)、部分缓解(PR)、稳定(SD)和进展(PD),以CR+CRu计算CR率,以CR+CRu+PR计算总有效率。

表2 所有患者的化疗方案

表3 鞘内注射剂量
1.4 毒副反应评价 按照WHO抗肿瘤药物毒副反应分度标准分为Ⅰ~Ⅳ度。
1.5 随访 随访截止至2015年11月。失访患者生存期计算至末次随访时间。
1.6 统计学处理 采用SPSS 22.0进行统计,采用Kaplan-Meier方法对生存资料进行分析,采用log rank检验对生存资料进行检验,检验水准α=0.05。
2 结果
2.1 疗效 20例患者均可评价疗效,其中18例(90.0%)CR,2例(10.0%)PD。治疗期间大部分患者出现Ⅲ、Ⅳ度骨髓抑制,经对症处理恢复正常,不影响下一步治疗。中位随访55(4~70)个月,全组3 a无事件生存率80.0%,低危组100.0%,中危组85.7%,高危组50.0%;Ⅰ~Ⅱ期100.0%,Ⅲ~Ⅳ期60.0%。见图1、2。
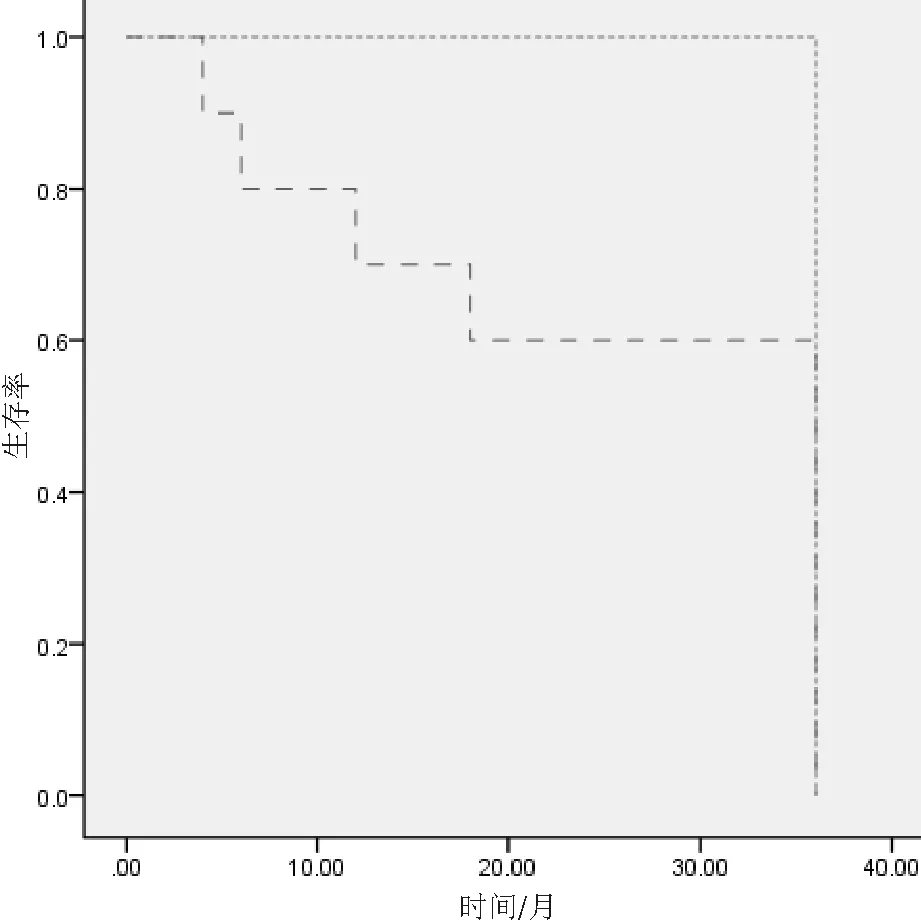
图2 不同分期患者的3 a无事件生存率比较
2.2 毒副反应 主要毒副反应为血液学毒性,所有患者治疗期间予G-CSF预防性升白细胞治疗,Ⅳ度骨髓抑制在A、B、AA、BB、CC方案中分别为51.6%、3.2%、100.0%、25.0%、33.3%,经治疗后可恢复。非血液学毒性主要为轻度黏膜炎,发生于AA、BB方案,考虑予大剂量MTX持续24 h输注有关,不影响下周期化疗,未发生Ⅲ、Ⅳ度黏膜炎。全组未发生治疗相关死亡。
3 讨论
儿童非霍奇金淋巴瘤为儿童常见恶性肿瘤,约占儿童恶性肿瘤的10%[5],主要类型包括伯基特淋巴瘤、弥漫大B细胞淋巴瘤、间变大细胞淋巴瘤和前B和前T淋巴母细胞淋巴瘤。常规CHOP方案疗效差,对于非前B和前T淋巴母细胞淋巴瘤治疗,近20 a欧美国家采用短程、高强度、多药联合方案和中枢预防方案治疗,疗效已显著提高。中山大学附属肿瘤医院对31例儿童青少年伯基特淋巴瘤采用B-NHL-BFM90方案和策略治疗,全组3 a无事件生存率为86%,其中Ⅰ~Ⅱ期100%,Ⅲ~Ⅳ期为82.1%[6]。
既往研究显示B-NHL-BFM90方案疗效显著,长期生存在90%左右,但由于大剂量MTX 24 h持续静滴毒反应较重,尤其口腔黏膜炎,部分患者难以耐受。目前研究方向逐渐转向在保证疗效的情况下减轻化疗毒副反应。MTX毒副反应与药物剂量和静滴的持续时间有关。德国B-NHL-BFM95方案[4]在B-NHL-BFM90基础上对MTX进行剂量和用法的调整,低、中危组将大剂量MTX由5 000 mg·m-2下调至1 000 mg·m-2,持续静滴时间由24 h改为4 h,结果显示毒副反应显著降低,疗效与B-NHL-BFM90方案相似,低、中危组3 a无事件生存率分别为(94±4)%、(94±2)%。我们于2010年3月开始应用B-NHL-BFM-95方案治疗非前B和前T淋巴母细胞淋巴瘤,低、中危组获得相似疗效,3 a无事件生存率分别为100.0%和85.7%。
既往研究显示Ⅲ~Ⅳ期和高危患者B-NHL-BFM95方案中将MTX 5 000 mg·m-2持续静滴24 h改为持续静滴4 h,疗效显著降低(静滴24 h 1 a无事件生存率和静滴4 h的3 a无事件生存率分别为91%和75%[7])。因此,高危患者缩短MTX静滴时间需慎重。但由于MTX 5 000 mg·m-2持续24 h静滴毒副反应重,为减轻化疗毒副反应,我们在高危组将MTX剂量减为3 000 mg·m-2,结果疗效显著低于B-NHL-BFM95方案,高危组分别为50%和81%[4],进一步分层分析发现B-NHL-BFM95组纵隔大B细胞淋巴瘤3 a无事件生存率53%,较其他病理类型明显下降;并在本研究中高危患者6例中病理类型为灰区淋巴瘤占5例,我们知道灰区淋巴瘤的预后较其他病理类型更差,并且因为本研究病历数较少,降低MTX剂量是否会影响高危患者疗效需进一步研究。
该化疗方案主要毒副反应为骨髓抑制,在G-CSF预防性升白细胞治疗基础上,仍有大部分患者发生IV度骨髓抑制,特别是A和AA方案时,经积极支持对症治疗后均可恢复正常,未发生治疗延迟及减量。MTX易引起口腔黏膜炎,予CF漱口同时按计划予CF解救,未发生Ⅲ度以上黏膜炎。为减轻大剂量MTX毒副反应,在化疗期间积极水化和碱化尿液,按时予CF解救并根据血MTX浓度调整解救剂量。全组未发生治疗相关死亡。
本组研究表明对于低、中危的儿童非霍奇金淋巴瘤,剂量调整的B-NHL-BFM95方案具有很好疗效并毒副反应可耐受;高危患者剂量调整的B-NHL-BFM95方案毒副反应可耐受,尚需进一步研究。
[1] 符仁义,刘玉峰.儿童血液与肿瘤疾病[M].郑州:河南科学技术出版社,2005:324.
[2] Anderson JR,Jenkin RD,Wilson JF,et al.Long-term follow-up of patients treated with COMP or LSA2L2 therapy for childhood non-Hodgkin's lymphoma: a report of CCG-551 from the Childrens Cancer Group[J].J Clin Oncol,1993,11(6):1024-1032.
[3] Hvizdala EV,Berard C,Callihan T,et al.Nonlymphoblastic lymphoma in children--histology and stage-related response to therapy: a Pediatric Oncology Group study[J].J Clin Oncol,1991,9(7):1189-1195.
[4] Woessmann W,Seidemann K,Mann G,et al.The impact of the methotrexate administration schedule and dose in the treatment of children and adolescents with B-cell neoplasms: a report of the BFM Group Study NHL-BFM95[J].Blood,2005,105(3):948-958.
[5] 张永红.儿童淋巴瘤[M].北京:人民卫生出版,2009:79.
[6] 孙晓非,甄子俊,刘冬耕,等.改良B-NHL-BFM-90方案治疗儿童青少年伯基特淋巴瘤的疗效分析[J].癌症,2007,26(12):1339-1343.
[7] Asselin BL,Devidas M,Chen L,et al.Cardioprotection and Safety of Dexrazoxane in Patients Treated for Newly Diagnosed T-Cell Acute Lymphoblastic Leukemia or Advanced-Stage Lymphoblastic Non-Hodgkin Lymphoma: A Report of the Children's Oncology Group Randomized Trial Pediatric Oncology Group 9404[J].J Clin Oncol,2016,34(8):854-862.
Clinical Study of Modified B-NHL-BFM95 Regimen in the Treatment of Non-Hodgkin Lymphoma in Children
Chen Ningbin,Wu Hui,Chen Ying,Yang Yu,He Hongming,Chen Daoguan,Lin Jianyang,Zheng Yanbin,Zhou Shiping,Wang Jiesong,Chen Xiurong
(FujianTumorHospital,Fuzhou350014,China)
Objective To evaluate the efficacy and toxicities of modified B-NHL-BFM95 regimen in the treatment of non-Hodgkin lymphoma in children.Methods Twenty patients with untreated non-Hodgkin lymphoma aged less than 14 were enrolled,and received modified B-NHL-BFM95 regimen.Results The short-term efficacy: 18 patients(90.0%) achieved CR,2 patients(10.0%) had PD.Grade Ⅲ and Ⅳ myelosuppression occurred in most patients,were recovered by active support care and did not affect the next course of chemotherapy.At a median follow-up of 55 months,the 3-year event-free survival rate was 80.0% for all the patients,with 100.0% for stage Ⅰ-Ⅱ and 60.0% for stage Ⅲ-Ⅳ patients; 100.0% for the low risk group,85.7% for the moderate risk group and 50.0% for the high risk group.Conclusion Modified B-NHL-BFM-95 regimen can improve the responses and survival of low-moderate risk non-Hodgkin lymphoma in children with tolerable toxicities.
B-NHL-BFM95 regimen; non-Hodgkin lymphoma; efficacy; toxicity
国家临床重点专科建设项目
陈宁斌(1977-),男,主治医师,主要从事淋巴瘤化疗工作。E-mail:chen_nb227@hotmail.com
吴晖(1964-),女,主任医师,主要从事淋巴瘤化疗工作。E-mail:kkwff123@163.com
10.3969/j.issn.1673-5412.2016.05.004
R733.1;R730.53
A
1673-5412(2016)05-0380-04
2016-05-22)

