Ferricyanide/RGO/PDDA纳米复合物的制备及其对抗坏血酸的电催化
焦守峰, 金 晶, 王 伦
(1.淮北职业技术学院,安徽 淮北 235000;2.安徽师范大学,安徽 芜湖 241000)
Ferricyanide/RGO/PDDA纳米复合物的制备及其对抗坏血酸的电催化
焦守峰1, 金 晶2, 王 伦2
(1.淮北职业技术学院,安徽 淮北 235000;2.安徽师范大学,安徽 芜湖 241000)
通过静电作用将带负电并具有电活性的铁氰酸根离子固定到预先制备好的RCO/PDDA纳米复合物修饰玻碳电极上.继而研究了该修饰电极的电化学性质,发现铁氰酸根离子作为电子媒介体,对抗坏血酸有良好的电催化作用.而且氧化电位只有0.08V,远远低于其它类型的电化学传感器.在优化后的pH条件下将其应用于实际样品的分析检测,有很好的重现性和快速的电流效应.
电化学传感器;石墨烯;纳米复合物;电催化氧化;生物传感器;电子媒介体
抗坏血酸,也称维生素C, 是一种水溶性维生素,广泛存在于生物体系,特别是新鲜的水果和绿色蔬菜中.作为抗氧化剂,它在人体的新陈代谢中起着重要的作用,同时它还能清除自由基,有助于避免自由基引起的疾病[1].目前测量抗坏血酸的方法很多,如化学发光、光谱、色谱法等[2-4].抗坏血酸是电活性化合物,因为电化学方法灵敏度高、易操作、价格低廉,所以电化学测定是一个很好的方法.但是电化学方法测存在的问题是,抗坏血酸通常和多巴胺、尿酸共存,在传统的固体电极上,这三种物质的氧化电位靠的太近,可能会发生重叠,造成测量上的互相干扰.并且在氧化过程中的产物会聚集到电极表面,引起污染,导致选择性和敏感度降低[5].因此,抗坏血酸检测选择性的提高是研制新型传感器要解决的一个重要问题.
本文把铁氰酸根离子固定到石墨烯上,充分利用二者优良性能制备一种具备催化活性的电化学传感器.首先用聚二烯丙基二甲基氯化铵(PDDA)还原氧化石墨烯成为PDDA包裹的石墨烯滴涂到玻碳电极上,然后采用自组装的方法,利用PDDA的正电性,通过静电作用把铁氰酸根离子固定在电极表面.制备的石墨烯-铁氰酸根/PDDA纳米复合物修饰到玻碳电极上,发现对抗坏血酸有着良好的电催化效果.该电化学传感器选择性高,检测范围广,并且对多巴胺、尿素等抗干扰性很强.用于实际样品中的测定,结果令人满意,这将为食品、医学上抗坏血酸的检测提供一个简单、快速、选择性高的电化学传感方法.
1 实验部分
1.1 药品与仪器
药品:氧化石墨烯;聚二烯丙基二甲基氯化铵(PDDA);抗坏血酸;铁氰化钾、磷酸盐等其它所有药品均为分析纯.仪器:CHI 660C电化学工作站(中国上海辰华),使用三电极系统,饱和甘汞电极作为参比电极,铂丝作为对电极,修饰和未修饰过的玻碳电极(3mm内径,天津兰力科科技股份有限公司)作为工作电极,原子力显微镜(美国Veeco公司Multimode Nanoscope IIIa controllor).
1.2 Ferricyanide/RGO/PDDA纳米复合物及其修饰电极制备
将60mL 0.5mg mL-1GO水溶液超声10min,然后加入600μL 20wt% PDDA,强力搅拌30min.之后加热至90℃并回流12h,在此过程中溶液的颜色由黄棕色转变为黑色.最后将产物放入离心机中10000rpm离心5min,然后加入二次水清洗后再离心,这样重复两次除去产物中剩余的PDDA.最后将最终产物再次分散在水中以获得胶状的石墨烯/PDDA悬浮液.
在修饰玻碳电极前,依次用0.3和0.5μm的三氧化二铝研磨液对玻碳电极进行抛光处理,然后再在二次水和乙醇中进行超声,最后再用氮气吹干.将前面石墨烯/PDDA悬浮液分散在水中超声2min得到稳定的黑色悬浮液,取5μL均匀地滴加到玻碳电极上,将其置于室温下干燥备用.最后将制备好的石墨烯/PDDA修饰电极浸泡在0.1 mM铁氰化钾溶液1 h,取出晾干.
2 结果与讨论
2.1 Ferricyanide/RGO/PDDA纳米复合物的形貌表征
通过原子力显微镜(AFM)对氧化石墨烯、PDDA/石墨烯、Ferricyanide/RGO/PDDA纳米复合物的形貌进行了表征.通过图1(A)可以看出,氧化石墨烯的厚度只有1纳米左右,说明氧化石墨烯是单层碳原子构成.图1(B)为经PDDA还原和包裹的石墨烯,其厚度明显增加了大约0.5nM,证明PDDA已经均匀覆盖到了表面.图1(C)是铁氰化钾离子通过自组装到石墨烯/PDDA纳米复合物表面的形貌,显然厚度继续增大,说明静电吸附已然发挥作用把铁氰酸根离子吸附到了表面.
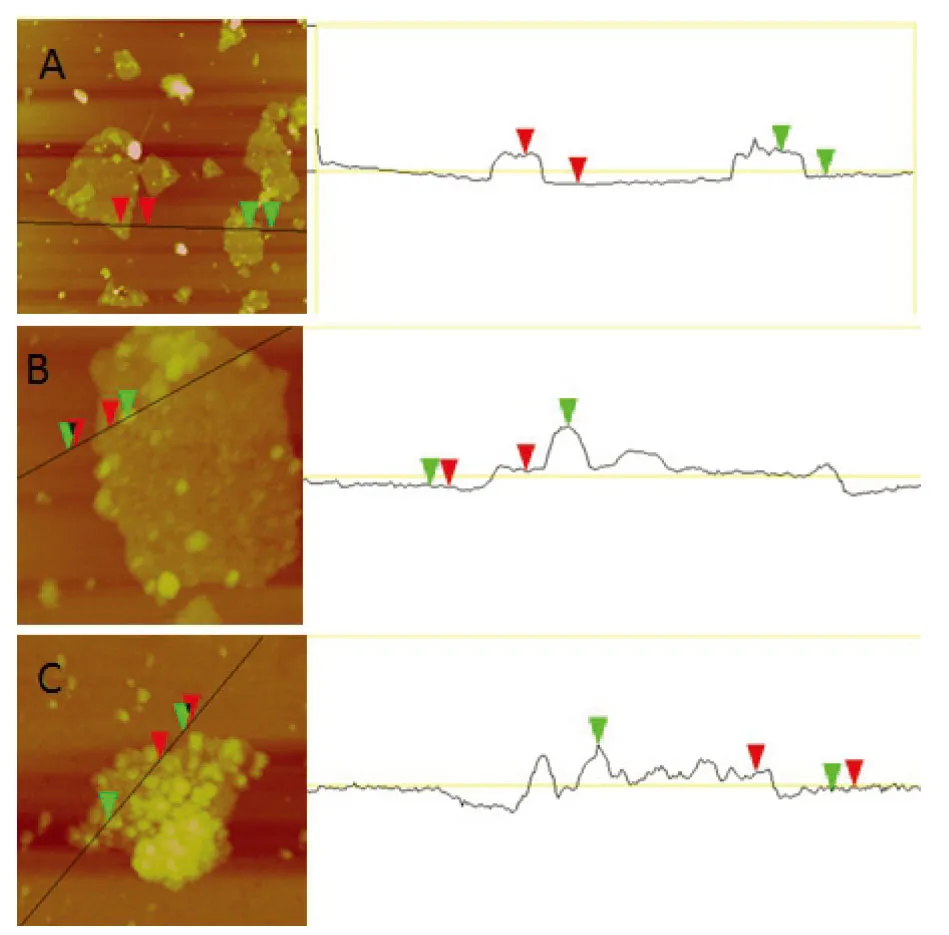
图1 原子力显微镜示意图:(a) GO, (b) PDDA/RGO 和(c) Ferricyanide /PDDA/RGO.

图2 抗坏血酸的循环伏安图:(a)裸电极0μMAA;(b)裸电极200μM;(c)修饰电极0μMAA;(d)修饰电极200μM AA.
2.2 Ferricyanide/RGO/PDDA纳米复合物修饰电极对抗坏血酸的电催化作用
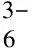
(1)
(2)
在此催化过程中,抗坏血酸首先被电极表面的铁氰化钾离子氧化成脱氢抗坏血酸,本身被还原亚铁氰化钾离子(方程1),随后又被电已化为铁氰化钾离子(方程2)参加第一个反应.
2.3 PH值和电压对传感器的影响
图3考察的是PH值对修饰电极电催化的影响,PH的变化范围为5.0-9.0.如图所示,氧化峰电流从5.0-7.0逐渐增大,PH7.0时达到最大值,然而7.0到9.0时逐渐减小,这与文献报道相类似[6].所观察到的PH值对电流的影响可以理解是PDDA大约在7.0附近质子化程度最大,这时带的正电荷最多.PH过大或过小都会影响带正电的PDDA和铁氰酸根离子之间的静电作用所使.
进一步研究电压对峰电流的影响,在不同的电压下峰电流的变化,结果表明所加电压对抗坏血酸的电流有着很大的影响,在大约0.08V时达到了最大值.所以就选择0.08V作为测定抗坏血酸的理想电压.
2.4 Ferricyanide/RGO/PDDA纳米复合物修饰电极对抗坏血酸的计时电流测定
在0.1M磷酸盐缓冲溶液中(pH 7.0),随着抗坏血酸的连续加入,修饰电极的计时电流相应如图4所示.在0.08 V电压下,抗坏血酸浓度增大,氧化峰电流也随着线性稳定增长,其线性关系如图5所示.加入浓度在1.0×10-6-2.5×10-3M之间,电流和浓度的线性方程为Ipa(μA) =-4.8634C(mM)-0.6874,R2=0.9996(n=19),检测限为6.0×10-7M(信噪比为3).

图3 PH值和电压对传感器的影响
2.5 干扰测定
为了考察一些常见干扰物对抗坏血酸测定的影响,选择0.08V电压下0.1M磷酸盐缓冲溶液中(pH 7.0)加入多巴胺、尿酸、葡萄糖、氯化钾的混合溶液,它们的浓度分别是抗坏血酸的40倍.结果发现如图6所示,它们的加入几乎对电流没有造成影响,这说明Ferricyanide/RGO/PDDA纳米复合物修饰电极对抗坏血酸的测定具有极高的选择性.
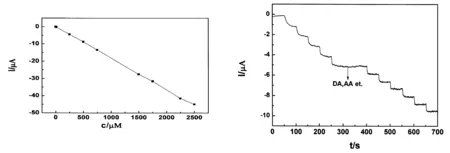
图5 电流与浓度线性关系示意图
2.6 传感器的再现性和稳定性
修饰电极的再现性和稳定性通过计时电流方法考察,10次连续测量2μM抗坏血酸其相对标准偏差为3.1%,同时5根不同的修饰电极测量同一种溶液相对标准偏差为4.3%,这些都说明修饰电极的再现性良好.把修饰电极保存在pH7.0的0.1M 磷酸盐缓冲溶液中10天,取出来测量已知溶液,电流强度能够保持原来的93%,这足以说明制备的修饰电极具有很好的稳定性.从上述结果可以看出,此修饰电极能够满足常规分析中的应用.
2.7 实际样品测定
为了考察Ferricyanide/RGO/PDDA纳米复合物修饰电极在实际样品中的应用,我们对市场上销售的维生素C片剂中含有的抗坏血酸进行了测定(如表1).首先把维生素C片剂溶于pH7.0的0.1M磷酸盐缓冲溶液中,然后采取标准加入法添加已知浓度的抗坏血酸到被检测液中.三组样品的回收率范围是99.4-102.4%,同时相对标准偏差结果也令人满意.这些表明制备的抗坏血酸电化学传感器具有很好的准确度,适合实际样品的测定.

表1 实际样品测定
3 结论
本文利用聚二烯丙基二甲基氯化铵(PDDA)的还原性和表面带有正电荷的性质,首先把氧化石墨烯转变为PDDA包裹的还原石墨烯,然后将其滴涂到玻碳电极上,再通过自组装方法利用静电作用把带负电荷的铁氰酸根离子固定在电极表面,成功地制备了Ferricyanide/RGO/PDDA/GCE.同时把制得的纳米复合物修饰电极上进行了电化学表征,发现该修饰电极极其稳定,并且对抗坏血酸表现出良好的电催化作用.作为测定抗坏血酸的电化学传感器,选择性非常好,一些易干扰的物质如多巴胺、尿酸、葡萄糖等不会造成干扰.此传感器制备简单,检测范围广,检测限低,对实际样品的检测效果良好,有望在日常抗坏血酸的测定中得到应用.
[1] ROBERT B R, STEINBERG, FRANCENE. Encyclopedia of biological chemistry[J]. University of California, 2004,4:367-371.
[2] ZHANG Z, QIN W. Chemiluminescence flow sensor for the determination of ascorbic acid with immobilized reagents[J]. Talanta,1996,43:119-124.
[3] BIURRUN M Y, ROMER R C, BARRERA P B. Indirect flow-injection determination of ascorbic acid by flame atomic absorption[J]. Spectrometry Microchim Acta, 1997,126:53-58.
[4] YEBRA M C, CESPE R M, CID A M. Automatic determination of ascorbicacid by flame atomic absorption spectrometry[J]. Anal Chim Acta, 2001,448:157-164.
[5] ZEN J M, CHEN P J. A selective voltammetric method for uric acid and dopaminedetection using clay-modified electrodes[J]. Anal Chem, 1997,69:5087-5093.
[6] LAVIRON E, BARD A J. Electroanalytical chemistry[M]. New York:Marcel Dekker, 1982:53-157.
Preparation of Ferricyanide/RGO/PDDA Nanocomposites and Its Catalysis for Ascorbic Acid
JIAO Shou-feng1, JIN Jing2, WANG Lun2
(1.Huaibei Vocational & Technical College, Huaibei 235000, China; 2.Anhui Normal University, Wuhu 241000, China)
A novel electro-active material was successfully prepared with ferricyanide ions loaded by electrostatic interaction onto the layer of prepared RCO-PDDA. Further, an electrochemical sensor for use in ascorbic acid (AA) detection was constructed with the use of the above electro-active materials Ferricyanide/PDDA/RCOmatrixasanelectronmediator.TheelectrocatalyticoxidationofAAbyferricyanidewasobservedatthepotentialof0.08V,whichwasnegativeshiftcomparedwiththatbydirectelectrochemicaloxidationofAAonaglassycarbonelectrode.Theexperimentalparameters,includingthepHvalueoftestingsolutionandtheappliedpotentialfordetectionofAA,wereoptimized.Thecurrentelectrochemicalsensornotonlyexhibitedagoodreproducibilityandstoragestability,butalsoshowedafastamperometricresponsetoAA.
electrochemical sensors; graphene; nanocomposites; electrocatalytic oxidation; biosensor; electron mediator
2016-01-10
焦守峰(1974-),安徽淮北市人,讲师;通讯作者:王伦(1956-),安徽省长丰县人,教授.
国家自然科学基金(21075002);安徽省教育厅高校自然科学研究项目(KJ2014A652).
10.14182/J.cnki.1001-2443.2016.05.008
O657.1
A
1001-2443(2016)05-0441-04

