聚吡咯/尼龙6纳米纤维膜对Pb2+固相萃取的吸附效能研究
刘静静 李晓晴 崔梦晶 戎 非 许 茜*,
1(东南大学公共卫生学院,南京 210009) 2(东南大学环境医学工程教育部重点实验室,南京 210009)
聚吡咯/尼龙6纳米纤维膜对Pb2+固相萃取的吸附效能研究
刘静静1,2李晓晴1,2崔梦晶1,2戎 非3许 茜*1,2,3
1(东南大学公共卫生学院,南京 210009)2(东南大学环境医学工程教育部重点实验室,南京 210009)
3(东南大学苏州市环境与生物安全重点实验室,南京 215123)
以电纺尼龙6纳米纤维膜为基底,原位氧化聚合制得聚吡咯/尼龙6纳米纤维膜(PPy/Nylon 6-NFsM)。通过静态和动态吸附实验考察PPy/Nylon 6-NFsM对Pb2+的吸附行为,探究其作为固相萃取介质富集水中痕量Pb2+的可行性。结果表明:298 K,pH=10时,PPy/Nylon 6-NFsM对Pb2+的静态饱和吸附量达542 mg/g;吸附动力学和吸附等温线分别符合准二级动力学模型和Freundlich模型;优化了PPy/Nylon 6-NFsM的固相萃取条件,采用火焰原子吸收光谱法检测实际水样中的Pb2+,检出限为1.2 μg/L(信噪比为3计), 10 μg/L加标水平加标回收率为95.3%~100.4%,相对标准偏差(RSD)为1.6%(n=3),可实现实际水样中痕量Pb2+的准确、灵敏的检测。
聚吡咯/尼龙6纳米纤维膜; 铅; 吸附; 固相萃取
1 引 言
我国生活饮用水卫生标准(GB5749-2006)规定,饮用水中Pb2+含量不得超过0.01 mg/L。而近年来,随着工业化进程的加快,环境水体中的Pb2+含量逐渐增加,对人类健康、居住环境和生态系统造成了严重的危害。因此,监测环境水体中Pb2+的浓度具有重要意义。由于环境水体中的Pb2+浓度极低,共存污染物成分复杂,因此在检测前必须对样品进行预处理,其中固相萃取法具有样品体积需要量小,有机溶剂用量少,操作简单等优势,其技术核心是吸附介质[1]。
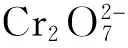
静电纺丝法(Electrospinning),简称电纺,是制备纳米纤维/NFsM的有效方法[6]。因PPy难溶难熔,难以直接电纺制得NFsM,一般需选择适合的模板材料以静电纺丝法先行制备纳米纤维基底膜,之后再对基底膜进行PPy修饰。尼龙6 (Nylon 6)良好的力学性能、耐热性、耐磨损性、耐化学药品性等,满足模板材料的要求。本研究以电纺Nylon 6-NFsM为基底,对其进行原位氧化聚合制得PPy/Nylon 6-NFsM,研究其作为水样中Pb2+的固相萃取介质的吸附行为,在此基础上建立基于PPy/Nylon 6-NFsM的固相萃取,结合火焰原子吸收光谱法测定水中痕量Pb2+的方法,并考察方法实际应用的可行性。
2 实验部分
2.1 仪器与试剂
AA-7000原子火焰分光光度计(日本岛津公司);AT-250型精密分析天平(瑞士Mettler公司);DZF-6020型真空干燥箱(上海一恒科技有限公司);iS10 红外光谱仪(美国Thermo公司);X射线电子能谱(美国 Thermo公司);Hitachi S-3000N扫描电子显微镜(日本日立公司);JEM-1011透射电子显微镜(日本日立公司);DW-P403-1AC高压直流电源(天津市东文高压电源厂);TCI-Ⅱ型注射泵(北京思路高科技发展有限公司)。
分析纯Pb(NO3)2、HNO3、吡咯、间甲基苯酚、 FeCl3·6H2O、 色谱纯无水乙醇、甲醇(国药集团化学试剂有限公司); 甲酸(分析纯,上海金山亭新化工试剂厂); NaOH(分析纯, 上海凌峰化学试剂有限公司);Nylon 6原料(分子量16000,张家港港荣国际贸易公司)。
2.2 标准溶液的配制
准确称取0.1599 g Pb(NO3)2于烧杯中,加入10 mL 0.1 mol/L HNO3,完全溶解后,用0.1 mol/L HNO3稀释至100 mL,摇匀,即得1000 mg/L Pb2+储备液。取5.0 mL Pb2+贮备液,用0.1 mol/L HNO3稀释至100 mL,配制成50 mg/L Pb2+标准液,并用去离子水逐级稀释至实验中所需浓度。
2.3 Pb2+检测条件
原子吸收光谱参数: 测定波长为283.3 nm,狭缝宽为0.7 nm,灯电流为10 mA; 燃烧器高度为7.0 mm,空气/乙炔火焰,空气流量为2.0 L/min,乙炔流量为15.0 L/min; 进样速度为3.0 mL/min。
2.4 PPy/Nylon 6-NFsM的制备
依照文献[7]制备Nylon 6-NFsM,将制得的Nylon 6-NFsM放入50 mL吡咯浓度为0.1 mol/L的乙醇溶液中,室温下静置1 h后,加入氧化剂FeCl3·6H2O氧化聚合12 h。用乙醇、甲醇、水分别对膜进行超声清洗1 min,重复清洗3次,至洗涤液无色,自然晾干即得。
2.5 静态吸附实验
2.5.1 吸附动力学 准确称取50 mg PPy/Nylon 6-NFsM,置于100 mL 50 mg/L Pb2+溶液中,在室温(298 K)下,静置吸附,分别在设定时刻(0, 10, 20, 30, 45, 60, 120, 180, 210, 240, 270, 300, 330, 360和540 min)吸取400 μL溶液,并用0.1 mol/L HNO3稀释至4 mL,测定其中Pb2+浓度,每次吸取溶液后补充同温度同体积的空白溶剂(pH=10去离子水)。
按式(1)和式(2)分别计算Pb2+溶液的去除率(Removal rate, RR)和t时刻PPy/Nylon 6-NFsM对Pb2+的吸附容量(Qt):
(1)
(2)
式中,C0为溶液Pb2+的初始浓度(mg/L);Ce为吸附平衡时溶液中剩余Pb2+的浓度(mg/L);Ct为时刻t溶液Pb2+的浓度(mg/L)。V为Pb2+溶液的体积(mL);m为PPy/Nylon 6-NFsM质量(mg);Qt为吸附时间t时刻的吸附量(mg/g)。
2.5.2 吸附等温线 准确称取50 mg PPy/Nylon 6-NFsM,置于100 mL不同浓度(1.0, 5.0, 30, 50, 100, 150和200 mg/L) Pb2+溶液中,分别在298, 308和318 K条件静置吸附,待至吸附平衡后,测定溶液中Pb2+的浓度,计算吸附容量Qe。
(3)
式中:C0为Pb2+溶液的初始浓度(mg/L);Ce为吸附平衡时溶液中剩余Pb2+的浓度(mg/L);V为Pb2+溶液的体积(mL);m为PPy/Nylon 6-NFsM质量(mg);Qe为平衡吸附容量(mg/g)。
2.6 动态吸附实验 采用实验室自制的膜盘式固相萃取装置[8]:将PPy/Nylon 6-NFsM裁剪成直径约为1 cm的圆形膜,称取3 mg置于过滤器中,过滤器上方接样品管,下方接收集器,连接于固相萃取仪。取10 mL样品溶液,抽真空使其以一定流速通过PPy/Nylon 6-NFsM(以400 μL水先行活化),随后用400 μL洗脱溶剂洗脱,将收集到的洗脱液用0.1 mol/L HNO3稀释到4 mL,以原子吸收火焰法测定其中Pb2+浓度,按式(4)计算回收率(R)。
(4)
式中,C0为Pb2+溶液的初始浓度(mg/L);Cx为洗脱液中Pb2+的浓度(mg/L)。
3 结果与讨论
3.1 PPy/Nylon 6-NFsM的表征
3.1.1 扫描电镜分析 Nylon 6-NFsM和PPy/Nylon 6-NFsM的扫描电镜(Scanning electron microscope,SEM)表征结果如图1所示,右图为左图的放大图。结果显示:模板Nylon 6-NFsM(图1a)粗细均匀、表面光滑、无颗粒,修饰后的PPy/Nylon 6-NFsM(图1b)表面变得粗糙,可见少量PPy颗粒,且由于PPy在Nylon 6-NFsM表面的沉积和包裹,纤维直径增加,平均直径为460 nm。
本研究组前期研究中发现,Nylon 6-NFsM含有的酰胺基在pH≤3可部分质子化,纤维间容易发生粘连,造成纤维的结构和形貌的改变[9];但如图1c所示,将PPy/Nylon 6-NFsM置于HNO3溶液(pH=2)中浸泡12 h后,纤维结构和形貌并未发生变化,提示PPy完全均匀地包裹在Nylon 6-NFsM表面,形成了PPy/Nylon 6-NFsM,表现出良好的耐酸性。

图1 Nylon 6-NFsM(a),PPy/Nylon 6-NFsM(b)和在HNO3水溶液中PPy/Nylon 6-NFsM(c)的SEM 照片Fig.1 SEM images of (a)Nylon 6-nano-fabers mat (NFsM),(b)Polypyrrole (PPy)/Nylon 6-NFsM and (c) PPy/Nylon 6-NFsM in HNO3 solution


图2 Nylon 6-NFsM(a)和PPy/Nylon 6-NFsM(b)的红外光谱图Fig.2 XPS spectra of Nylon 6-NFsM(a)and PPy/Nylon 6-NFsM(b)

3.1.4 吸附效能表征 本实验进行了PPy/Nylon 6-NFsM与Nylon 6-NFsM对Pb2+吸附效能比较。分别准确称取50 mg PPy/Nylon 6-NFsM和Nylon 6-NFsM,分别置于100 mL 50 mg/L Pb2+溶液中,室温(298 K),静置4 h,测定溶液中Pb2+浓度,按式(1)计算去除率。结果表明,Nylon 6-NFsM对Pb2+去除率为5.9%±7.2%(n=3),PPy/Nylon 6-NFsM对Pb2+去除率可达26.4%±5.1%(n=3),PPy/ Nylon 6-NFsM对Pb2+的吸附效能有明显增加。
3.2 静态吸附性能考察
3.2.1 吸附条件优化 (1) PPy/Nylon 6-NFsM用量 在100 mL 50 mg/L Pb2+溶液中,加入不同质量的PPy/Nylon 6-NFsM(30~100 mg),在室温(298 K)下,静置至吸附平衡后,测定溶液中Pb2+浓度,按式(1)计算去除率。结果显示,在30~100 mg范围内,去除率随着PPy/Nylon 6-NFsM的用量增加而逐渐增大;但当用量高于50 mg时,去除率保持在80.2%~83.5%之间(RSD 2.2%~9.7%(n=3))不再上升。因此,本实验PPy/Nylon 6-NFsM的用量为50 mg。(2)溶液pH值的影响 准确称取50mg PPy/Nylon 6-NFsM,置于100 mL 50 mg/L Pb2+溶液中,在室温(298 K)下,以10 mol/L NaOH溶液和0.1 mol/L HNO3溶液调节溶液pH,分别得到pH为3, 5, 7, 9, 10, 11的溶液,静置吸附至平衡后,测定溶液Pb2+浓度,按式(1)计算去除率。结果表明,PPy/Nylon 6-NFsM在碱性条件下对Pb2+的吸附去除明显优于酸性条件,并在pH=10可达最佳吸附,此时的去除率为82.1%±4.5%(n=3)。因此,溶液pH=10作为优化吸附条件。
3.2.2 吸附动力学考察 准确称取3份50 mg PPy/Nylon 6-NFsM,分别置于100 mL浓度为1.0, 5.0和50 mg/L的Pb2+溶液中,在室温(298 K)下,静置进行吸附,分别在设定时刻(0, 10, 20, 30, 45, 60, 120, 180, 210, 240, 270, 300, 330, 360和540 min)吸取400 μL溶液,并用0.1mol/L HNO3稀释至4 mL,测定其中Pb2+浓度,每次吸取溶液后补充同温度同体积的空白溶剂(pH=10去离子水),按式(1)计算去除率。结果表明,起始浓度为1.0, 5.0和50 mg/L的吸附平衡时间分别为180, 240和360 min,即在PPy/Nylon 6-NFsM用量一定的情况下,吸附平衡时间的长短与溶液的浓度大小呈正相关。
3.2.3 吸附动力学 研究探讨吸附过程的动力学规律,分别用准一级动力学方程和准二级动力学方程对实验数据进行拟合。
方程如式(5)和式(6)所示:准一级方程:
(5)
准二级方程:
(6)
其中,K1和K2为准一级和准二级动力学方程的速率常数;qt为当吸附时间为t时的吸附容量(mg/g);qe为当达到吸附平衡时的吸附量(mg/g)。
方程拟合结果表明准二级动力学方程(R2=0.977)相比准一级动力学方程(R2=0.807)更合适描述PPy/Nylon 6-NFsM对Pb2+吸附,因此吸附过程为化学吸附,且受到Pb2+浓度和PPy/Nylon 6-NFsM上吸附位点数量的影响。
3.2.4 吸附等温线 研究吸附过程分别用Langmuir和Freundlich方程进行拟合,二者的表达式如式(7)和式(8):
Langmuir方程
(8)
Freundlich方程
(9)
其中,Qmax是最大吸附量(mg/g);Qe是平衡吸附量(mg/g);Ce(mg/L)是吸附平衡时Pb2+浓度;KL(L/mg)为吸附平衡常数;KF为吸附系数,n为表征吸附强度的参数。
由表1可见,各温度下,Freundlich模型的R2均大于Langmuir模型,表明Freundlich模型更适于描述PPy/Nylon 6-NFsM对Pb2+的吸附行为。Freundlich模型中的K和n值均大于l,表明PPy/Nylon 6-NFsM对Pb2+有较强的亲和吸附能力,且n值随着温度升高而递增,提示吸附是一个吸热过程。3.2.5 PPy/Nylon 6-NFsM的静态重复使用 可重复使用次数是评价吸附剂优越性的重要指标。在100 mL 50 mg/L Pb2+溶液中,加入50 mg PPy/Nylon 6-NFsM,在室温(298 K),pH=10条件下,静置吸附6 h至平衡后,测定其Pb2+浓度,按上述式(1)计算去除率。用蒸馏水清洗PPy/Nylon 6-NFsM后置于100 mL 0.1 mol/L HNO3溶液中解吸附6 h,以蒸馏水清洗去除膜上残留的HNO3,重复上述吸附/解吸附操作5次。结果表明PPy/Nylon 6-NFsM经过5次吸附/解吸附循环实验,去除率为80.5%~81.7%,RSD为3.4%~6.3%(n=3),显现良好的可再生性能,表明PPy/Nylon 6-NFsM是一种可循环利用的高效吸附介质。
3.2.6 与现有Pb2+吸附剂的比较 在优化的条件下,准确称取50mg PPy/Nylon 6-NFsM,分别置于100 mL不同浓度(50~500 mg/L)的Pb2+溶液中,在室温(298 K),静置吸附48 h后,测定其Pb2+浓度,按式(3)计算最大吸附量。结果表明,随着Pb2+浓度增大,吸附容量也逐渐增大,当初始浓度达到400 mg/L时,PPy/Nylon 6-NFsM对Pb2+的吸附已经饱和,最大吸附量在温度为298 K时可达542.1 mg/g。
表1 吸附等温模型的参数
Table 1 Parameters of isothermal adsorption model for adsorption of lead ions

温度Temperature(K)LangmuirKLQmax(mg/g)R21FreundlichKFnR222980.024350.9297.621.180.9963080.043570.75514.71.410.9893180.053700.81124.51.610.993
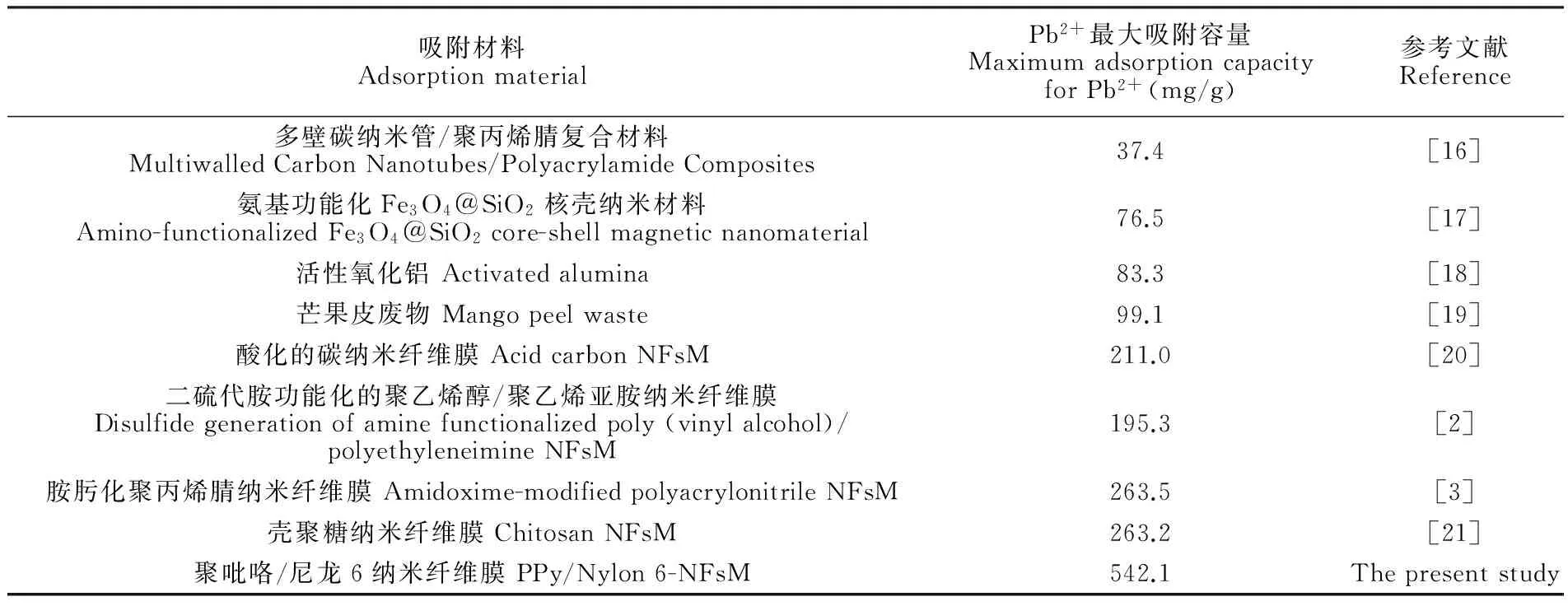
近年来文献报道的Pb2+的吸附剂与本实验采用的PPy/Nylon 6-NFsM进行比较。结果见表2,可见PPy/Nylon 6-NFsM的吸附容量明显更高,具有实现规模化水处理实际应用的潜力。
3.3 动态吸附性能考察
3.3.1 吸附条件优化 (1)洗脱剂及用量 合适的洗脱剂及用量可将吸附在PPy/Nylon 6-NFsM上的目标物完全洗脱下来。静态重复使用考察中采用HNO3解吸,因此,此处对HNO3洗脱浓度和体积进行优化。如2.6节操作,上样溶液的浓度1.0 μg/mL,以回收率为指标,考察不同浓度(0.001~0.5 mol/L)、体积(200~400 μL)HNO3溶液的洗脱效果。结果表明,HNO3对Pb2+的洗脱效率随着HNO3浓度增大而升高,当HNO3浓度为0.1 mol/L时,回收率稳定在96.3%±1.5%。洗脱剂体积在200 μL时,Pb2+的回收率仅75.2%±5.5%;当增加到400 μL时,Pb2+的回收率保持在96.2%±1.7%以上。因而,采用400 μL 浓度为0.1 mol/L HNO3作为洗脱条件。(2)PPy/Nylon 6-NFsM用量 如2.6节操作,上样Pb2+溶液的浓度1.0 μg/mL,以回收率为指标,考察不同膜用量(2~5 mg)对Pb2+的吸附效果。实验结果表明,膜用量对Pb2+的回收率几乎没有影响,均大于95.8%±6.5%(n=3)。考虑到膜质量过轻易导致过样时膜发生破裂,本文将动态吸附实验PPy/Nylon 6-NFsM用量定为3 mg。(3)过样速度 过样速度的快慢影响PPy/Nylon 6-NFsM与目标物的接触时间,从而影响对目标物的吸附。如2.6节操作,膜用量3 mg,上样样品为10 mL 1.0 mg/L Pb2+溶液,以回收率为指标,考察不同过样速度(0.3~3.0 mL/min)的洗脱效果。结果表明, 在过样速度低于0.7 mL/min时,回收率可保持在95.5%±4.7%(n=3)以上。因此后续实验的过样速度定为0.7 mL/min。
表2 不同的吸附材料对Pb2+吸附容量的比较
Table 2 Comparison of different adsorption materials on adsorption capacity of lead ions
吸附材料AdsorptionmaterialPb2+最大吸附容量MaximumadsorptioncapacityforPb2+(mg/g)参考文献Reference多壁碳纳米管/聚丙烯腈复合材料MultiwalledCarbonNanotubes/PolyacrylamideComposites37.4[16]氨基功能化Fe3O4@SiO2核壳纳米材料Amino-functionalizedFe3O4@SiO2core-shellmagneticnanomaterial76.5[17]活性氧化铝Activatedalumina83.3[18]芒果皮废物Mangopeelwaste99.1[19]酸化的碳纳米纤维膜AcidcarbonNFsM211.0[20]二硫代胺功能化的聚乙烯醇/聚乙烯亚胺纳米纤维膜Disulfidegenerationofaminefunctionalizedpoly(vinylalcohol)/polyethyleneimineNFsM195.3[2]胺肟化聚丙烯腈纳米纤维膜Amidoxime-modifiedpolyacrylonitrileNFsM263.5[3]壳聚糖纳米纤维膜ChitosanNFsM263.2[21]聚吡咯/尼龙6纳米纤维膜PPy/Nylon6-NFsM542.1Thepresentstudy
3.3.2 PPy/Nylon 6-NFsM动态重复使用 实验中每次完成固相萃取操作后,用2 mL浓度为0.1 mol/L HNO3对NFsM上可能残留的目标物进行清洗,再进行下一次动态吸附实验,上样样品为10 mL 1.0 mg/L的Pb2+溶液。结果表明PPy/Nylon 6-NFsM可高效重复使用5次,回收率为95.4%~96.8%,RSD为1.5%~5.6%(n=3)。
3.4 方法学评价
在经动态吸附实验优化的固相萃取条件下(400 μL水活化,上样溶液pH=10,400 μL 0.1 mol/L HNO3洗脱),以空白自来水水样作为基底,进行加标实验(加标水平为10 μg/L),按2.6节操作,采用原子火焰吸收法检测Pb2+含量,以浓度C(μg/L)为横坐标,吸光度A为纵坐标绘制工作曲线,对方法的线性范围、检出限、回收率等指标进行评价。
结果表明,在8~500 μg/ L范围内,所得Pb2+的回归方程为y=0.01875x+0.0077,R2=0.999,呈良好的线性关系,方法检出限为 1.2 μg/L(信噪比为3计),加标回收率为95.6%-101.3%,RSD为1.5%(n=3)。与我国生活饮用水检测方法(GB5750.6-2006)中火焰原子吸收法的线性范围(25~300 μg/L)和检出限(25 μg/L)相比更优,更适用于水中痕量Pb2+的检测,且本文方法的最低检测浓度(8 μg/L)低于我国生活饮用水标准(GB5749-2006)中Pb2+的限值(0.01 mg/L),能满足于实际水样中痕量Pb2+灵敏、准确的定量要求。
实际水样是一种存在多种重金属离子的混合体系,为说明本方法用于实际水样中Pb2+的吸附的可行性,本研究考察了Cu2+, Zn2+和Hg2+共存时Pb2+的回收率。以空白自来水水样作为基底制备模拟水样,Cu2+, Zn2+, Hg2+和Pb2+加标水平均为10 μg/L,按2.6节操作,采用原子火焰吸收法检测Pb2+含量,计算得方法回收率为95.1%±6.8%(n=3)。实验结果表明,在其它离子共存时PPy/Nylon 6-NFsM仍表现对Pb2+的高效吸附。
1 Cui Y, Hu Z J, Yang J X,Gao H W.MicrochimicaActa. 2011, 176(3-4): 359-366
2 ZHANG Qian, XIA Ke, LIU Li, LIU You-Chang,ZHANG Cui, LIU Xuan, XU Yuan, CHEN Shi-Jin, CHEN Ji-Da.Chem.J.ChineseUniversities, 2013, 34(11): 2667-2673
张 谦, 夏 柯, 刘 丽, 刘又畅, 张 翠, 刘 璇, 徐 缓, 陈世金, 陈际达. 高等学校化学学报, 2013, 34(11): 2667-2673
3 Saeed K, Haider S, Oh T J,Park S Y.JournalofMembraneScience, 2008, 322(2): 400-405
4 Tian T, Deng J, Xie Z, Zhao Y, Feng Z, Kang X,Gu Z.Analyst, 2012, 137(8): 1846-1852
5 Wang J Q, Luo C, Qi G G, Pan K,Cao B.AppliedSurfaceScience, 2014, 316: 245-250
6 Teo W E, Ramakrishna S.Nanotechnology, 2006, 17(14): R89-R106
7 YIN Xue-Yan, XU Qian, WU Shu-Yan, WANG Min, GU Zhong-Ze.Chem.J.ChineseUniversities, 2010, 31(4): 690-695
殷雪琰, 许 茜, 吴淑燕, 王 敏, 顾忠泽. 高等学校化学学报, 2010, 31(4): 690-695
8 Xu Q, Zhang N, Yin X, Wang M, Shen Y, Xu S, Zhang L,Gu Z.J.Chromatogr.B, 2010, 878(26): 2403-2408
9 Xu Q, Wu S Y, Wang M, Yin X Y, Wen Z Y, Ge W N,Gu Z Z.Chromatographia, 2009, 71(5-6): 487-492
10 Bhaumik M, McCrindle R,Maity A.Chem.Engineer.J., 2013, 228: 506-515
11 Wu Q J, Liu X H,Berglund L A.Polymer, 2002, 43(8): 2445-2449
12 Nair S, Natarajan S,Kim S H.MacromolecularRapidCommunications, 2005, 26(20): 1599-1603
13 Saoudi B, Jammul N, Chehimi M M, Jaubert A S, Arkam C,Delamar M.Spectroscopy-anInternationalJournal, 2004, 18(4): 519-535
14 FENG Yuan.NorthEnvironment, 2013, (3): 87-93
冯 源. 北方环境, 2013, (3): 87-93
15 Zhang X,Bai R B.Langmuir, 2003, 19(26): 10703-10709
16 Yang S, Hu J, Chen C, Shao D,Wang X.Environ.Sci.Technol., 2011, 45(8): 3621-3627
17 Wang J, Zheng S, Shao Y, Liu J, Xu Z,Zhu D.JColloidInterfaceSci., 2010, 349(1): 293-299
18 Naiya T K, Bhattacharya A K,Das S K.JColloidInterfaceSci., 2009, 333(1): 14-26
19 Iqbal M, Saeed A, Zafar S I.J.HazardMater, 2009, 164(1): 161-171
20 Faghihian H, Kooravand M, Atarodi H.KoreanJournalofChemicalEngineering, 2013, 30(2): 357-363
21 Haider S,Park S Y.J.MembraneSci., 2009, 328(1-2): 90-96
(Received 15 July 2015; accepted 4 November 2015)
This work was supported by the National Natural Science Foundation of China (Nos. 81172721, 81473019)
Research on Adsorption of Pb2+from Aqueous Solutions Using Polypyrrole/Nylon 6 Nanofibers Mat
LIU Jing-Jing1,2, LI Xiao-Qing1,2, CUI Meng-Jing1,2, RONG Fei3, XU Qian*1,2,3
1(SchoolofPublicHealth,SoutheastUniversity,Nanjing210009,China)2(KeyLaboratoryEnvironmentalMedicineEngineering,MinistryofEducation,SoutheastUniversity,Nanjing210009,China)3(SuzhouKeyLaboratoryofEnvironmentalandBiosafety,SoutheastUniversity,Nanjing215123,China)
Polypyrrole/Nylon 6 core-shell Nanofibers mat (PPy/Nylon 6-NFSM), prepared via situ polymerization on nylon6 electrospun nanofibers mat template, was used as an adsorbent to remove Pb2+from aqueous solutions. To study the adsorption characteristics of PPy/Nylon 6-NFSM on Pb2+, the work focused on two parts, dynamic adsorption and static adsorption. The investigation explored the possibility of PPy/Nylon 6-NFSM as an efficient solid phase extraction (SPE) adsorbent for the separation and enrichment of trace Pb2+in water samples. The experiment results showed that the maximum static adsorption capacity of PPy/Nylon 6-NFSM for Pb2+was 542.1 mg/g at 298 K in pH=10 solution. The adsorption process could be well fitted with the pseudo-second-order kinetic model, the adsorption equilibrium data accorded with Freundlich isotherm model. Under the optimum conditions, PPy/Nylon 6-NFSM was used as adsorbent in SPE coupled with Flame atomic spectrophotometer (AA-7000) for the determination of Pb2+in water samples. The limits of detection of the method were 1.2 μg/L (S/N=3), the recoveries of spiked water samples at concentration of 10 μg/L were 95.3%-100.4% with RSD of 1.6%. The method is accurate and sensitive in detection of trace concentrations of Pb2+in water sample.
Polypyrrole/Nylon 6-nanofibers mat; Lead; Adsorption; Solid phase extraction
10.11895/j.issn.0253-3820.150785
本文系国家自然科学基金项目(Nos.81172721,81473019)和苏州市纳米技术专项项目(No.ZXG2013026)资助
2015-07-15收稿;2015-11-04接受
* E-mail: q_xu68@163.com

