同位素稀释超高效液相色谱串联质谱测定尿液中苯系物和三氯乙烯代谢产物
朱 婧 李 妍 雍 莉 郑 波 邹晓莉* 刘 珍
1(四川大学华西公共卫生学院卫生检验教研室,成都 610041)2(四川省疾病预防控制中心,成都 610041) 3(四川大学华西第二医院出生缺陷中心,成都 610041)
同位素稀释超高效液相色谱串联质谱测定尿液中苯系物和三氯乙烯代谢产物
朱 婧1李 妍1雍 莉2郑 波1邹晓莉*1刘 珍3
1(四川大学华西公共卫生学院卫生检验教研室,成都 610041)2(四川省疾病预防控制中心,成都 610041)3(四川大学华西第二医院出生缺陷中心,成都 610041)
建立同位素内标稀释,超高效液相色谱串联质谱(Ultra performance liquid chromatography-tandem mass sepctrometry, UPLC-MS/MS)同时测定尿中苯系物和三氯乙烯代谢产物的方法,并用于孕妇尿样的分析。尿样过经含同位素内标的醋酸铵缓冲液稀释10倍后,过滤,取滤液进样分析。采用C18色谱柱,梯度洗脱进行UPLC分离,电喷雾负离子扫描多反应监测(Multiple reaction monitoring,MRM) 模式检测。方法检出限在0.0350~1.75 μg/L之间,方法的日内和日间精密度分别为1.2%~9.1%和2.0%~9.7%;用所建立的方法测定了650个孕妇尿液样品,并统计分析了其地区差异,加标回收率为85.0%~104%。所建立的方法快速灵敏,适合尿液样品的批量分析。
同位素稀释; 超高效液相色谱串联质谱; 苯系物; 三氯乙烯; 代谢物; 尿液
1 引 言
苯系物主要包括苯、甲苯、二甲苯、乙苯和苯乙烯等物质,在化工、建筑等领域应用广泛,主要对人体皮肤粘膜、中枢神经、造血功能等造成损害。其中,苯已经被世界卫生组织确定为强致癌物。三氯乙烯(Trichloroethylene,TCE)是一种优良的溶剂,广泛用于金属清洗、干洗剂、杀虫剂和萃取剂等。三氯乙烯对中枢神经系统有麻醉作用,亦可引起肝、肾、心脏等损害[1]。近年来,苯系物和三氯乙烯的污染问题受到人们的广泛关注。特别是孕期接触苯系物、三氯乙烯的孕妇,自然流产及发生先天畸形的危险性增高[2]。在对这些物质进行环境监测的同时,生物监测也十分必要,通过对生物监测指标的测定,可以在一定程度上说明人体对有害物质的接触水平。
苯系物的生物监测指标各不相同,苯、甲苯、二甲苯、苯乙烯和乙苯的生物监测指标通常分别为苯巯基尿酸(苯酚、反式-反式粘糠酸)、马尿酸、甲基马尿酸(Methylhippuric acid,MHA)、苯乙醛酸 (Phenylglyoxylic acid,PGA)和苯乙醇酸(Mandelic acid,MA)。三氯乙烯的生物监测指标为三氯乙酸(Trichloroacetic acid,TCA)。其中,因在评价低浓度苯接触时,苯巯基尿酸(S-phenylmercapturic acid,SPMA)个体差异影响较小,用于生物监测具有较为明显的优势[3,4],因此实验选择了苯巯基尿酸作为苯的监测指标。此外,马尿酸是甲苯的非特异产物,2013年美国政府工业卫生家协会(American Conference of Governmental Industrial Hygienists,ACGIH)已经取消其作为甲苯的生物监测指标,因此实验采用了它的特异性产物N-乙酰基-S-苯基-L-半胱氨酸(N-acetyl-S-(benzyl)-L-cysteine, BMA)作为监测对象;三氯乙酸亦非是三氯乙烯的特异性产物,因此增加检测了它的特异性代谢产物N-乙酰基-S-(1,2-二氯乙烯基)-L-半胱氨酸(N-acetyl-S-(1,2-dichlorovinyl)-L-cysteine,1,2-DCVMA、N-乙酰基-S-(2,2-二氯乙烯基)-L-半胱氨酸(N-acetyl-S-(2,2-dichlorovinyl)-L-cysteine,2,2-DCVMA)。
目前,我国职业卫生标准中,这些生物监测指标都是分别进行检测,多用高效液相色谱法[5~7]、气相色谱法[8~10]和分光光度法[11],但生物样品基质通常较为复杂,用这些方法进行检测,样品基质干扰会造成准确度和灵敏度的下降。 结合UPLC的高分离效率和快速及串联质谱检测的高特异性的UPLC-MS/MS在痕量测定领域得到了广泛应用,极大地提高代谢产物测定的灵敏度和准确度。
为了同时测定尿样中苯系物和三氯乙酸的代谢物,且适应尿中基体复杂、含量低的特点,本实验采用超高效液相色谱-串联质谱法,以同位素内标进行基质效应校正,建立简单快速同时测定尿样中苯系物和三氯乙酸代谢物的方法,与文献[5~11]相比,检出限降低2~3个数量级,更有利于痕量分析,为暴露人群的生物监测提供了有力的检测手段。将所建立的方法用于各地孕妇尿样的检测,初步分析了不同地区孕妇的暴露水平差异。
2 实验部分
2.1 仪器与试剂
Acquity超高液相色谱仪(UPLC,美国Waters公司),3200Q TRAP联用质谱仪(LC/MS/MS System,美国AB SCIEX公司)。
标准品(纯度≥98%):苯巯基尿酸(S-phenylmercapturic acid,SPMA,购自东京化成工业株式会社);N-乙酰基-S-苯基-L-半胱氨酸(N-acetyl-S-(benzyl)-L-cysteine, BMA)、N-乙酰基-S-(1,2-二氯乙烯基)-L-半胱氨酸(N-acetyl-S-(1,2-dichlorovinyl)-L-cysteine,1,2-DCVMA)、N-乙酰基-S-(2,2-二氯乙烯基)-L-半胱氨酸(N-acetyl-S-(2,2-dichlorovinyl)-L-cysteine,2,2-DCVMA),购自Toronto Research Chemicals公司;苯乙醛酸(Phenylglyoxylic acid,PGA)、苯乙醇酸(Mandelic acid,MA),购自Aladdin Chemistry公司;三氯乙酸(Trichloroacetic acid,TCA)、甲基马尿酸(Methylhippuric acid,MHA,)、三氟乙酸(Trifluoroacetic acid,TFA),均购于Sigma公司。
同位素内标:DL-S-phenylmercapturic-3,3-d2Acid(SPMA-d2,CDN Isotopes公司);N-acetyl-S-(1,2-dichlorovinyl)-L-cysteine-13C,d3(1,2-DCVMA-13C,d3)、N-acetyl-S-(2,2-dichlorovinyl)-L-cysteine-13C,d3(2,2-DCVMA-13C,d3)、N-acetyl-S-(benzyl-13C6)-L-cysteine (BMA-13C6),均购于Toronto Research Chemicals公司。
甲醇、乙腈均为色谱纯;醋酸铵(优级纯)。实验用水为超纯水(由Millipore Synergy 185超纯水机制得,18.2 MΩ·cm)。标准溶液配制:分别准确称取适量的各标准品,用甲醇溶解SPMA,MA,DCVMA和BMA; 水溶解MHA,PGA和TCA,配制成1.0 mg/mL 的标准储备溶液。取上述标准储备液适量,用15 mmol/L醋酸铵缓冲液稀释成适合浓度的混合标准中间应用液,测定前,用15 mmol/L醋酸铵缓冲液(含内标物质)稀释成混合标准系列溶液(见2.2.3节)。
表1 色谱梯度洗脱程序
Table 1 Gradient elution program of UPLC

时间Time(min)流速Flowrate(μL/min)15mmol/L醋酸铵缓冲液15mmol/Lammoniumacetatebuffer(%)乙腈Acetonitrile(%)02509822300955330090105300703063006040730080207.5300901083009829250982
2.2 实验方法
2.2.1 色谱条件 C18柱(50 mm×2.1 mm,1.7 μm,美国Waters公司),柱温40℃,进样体积10 μL。流动相为15 mmol/L醋酸铵缓冲液和乙腈,梯度洗脱,流动相和流速的洗脱程序见表1。
2.2.2 质谱条件 负离子模式;多反应模式(Multiple reaction monitoring mode ,MRM);离子源电压-4400 V;离子源温度400℃;雾化气345 kPa;辅助雾化气310 kPa;气帘气207 kPa;进口电压-10 V;出口电压-10 V;驻留时间100 ms。待测物和内标物质谱条件及其母/子离子见表2。2.2.3 标准曲线的绘制 用15 mmol/L醋酸铵缓冲液(内含各内标物质浓度为10~100 ng/mL)将上述混合标准中间应用液分别稀释为SPMA, PGA, TCA, BMA, DCVMA浓度为0.1, 0.2, 0.5, 1, 5, 10, 20, 50, 100, 200和500 ng/mL,以及MA, MHA浓度为5, 20, 50, 100, 200, 300, 400, 500, 600, 800和1000 ng/mL的混合标准系列溶液,进样10 μL分析。以各待测物的浓度作为横坐标,待测物峰面积和内标物峰面积的比值或待测物峰面积为纵坐标,绘制标准曲线,求得回归方程和相关系数。
表2 待测物和内标物质谱条件及其母/子离子
Table 2 Mass spectrometric parameters for target compounds and their internal standards
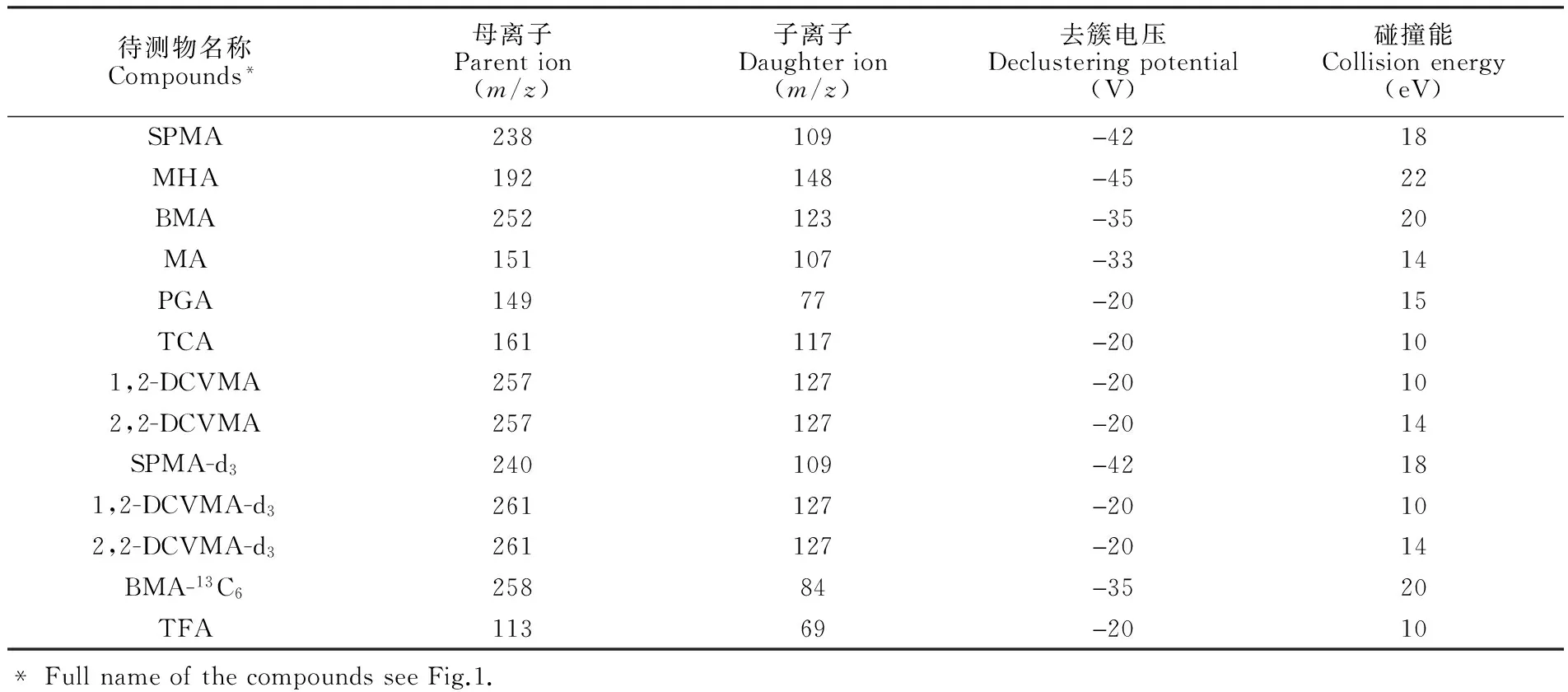
待测物名称Compounds*母离子Parention(m/z)子离子Daughterion(m/z)去簇电压Declusteringpotential(V)碰撞能Collisionenergy(eV)SPMA238109-4218MHA192148-4522BMA252123-3520MA151107-3314PGA14977-2015TCA161117-20101,2-DCVMA257127-20102,2-DCVMA257127-2014SPMA-d3240109-42181,2-DCVMA-d3261127-20102,2-DCVMA-d3261127-2014BMA-13C625884-3520TFA11369-2010*FullnameofthecompoundsseeFig.1.
2.2.4 样品的采集与处理 尿样采集后立即放入冷冻小瓶,-70℃贮存。
取尿样解冻,用HPLC方法测定肌酐浓度(WS/T98-1996),肌酐浓度超过0.3~3.0 g/L的范围,尿样舍弃,符合此浓度范围,用于检测,测定结果同时进行肌酐校正。
尿样经15000 r/min离心5 min,取上清液,以15 mmol/L醋酸铵缓冲液稀释10倍(缓冲液中含待测物同位素内标),过滤,取滤液上样测定。
2.2.5 空白尿液样品 分别称取氯化钠、磷酸氰二胺、硫酸钾、尿素、肌酐试剂12.5, 4.05, 1.74, 25.0和1.20 g,溶于1000 mL纯水,配制成模拟空白尿样[12]。按照2.2.4节进行样品前处理后进行UPLC/MS/MS分析,用于基质效应的评价。
3 结果与讨论
3.1 质谱条件的确定
分别配制浓度为 100 μg/mL 的标准溶液和内标溶液,采用全扫描方式,利用针泵以 20.0 μL/min 流速进样,循环10次后,分别确定其母离子。在优化的最佳锥孔电压和碰撞能量条件下,进行子离子的选择。MSM方式下选择用于分析的母离子和子离子见表2。
3.2 色谱条件的确定
实验考察了甲醇-甲酸、乙腈-甲酸、甲醇-醋酸铵、乙腈-醋酸铵4种流动相体系下,各待测物质的色谱响应。结果表明,各待测物质以乙腈-醋酸铵作为流动相时分离更好,响应更高。
固定乙腈-醋酸铵体积比为20∶80,流速为300 μL/min,实验在5~20 mmol/L范围内研究了流动相中醋酸铵浓度的影响,结果表明,在流动相中加入适量的醋酸铵能提高待测物的离子化效率,利于待测物的分子离子化,从而改善了色谱峰的峰形,提高了灵敏度。当醋酸铵浓度为15 mmol/L时,响应值较高且稳定。实验选择乙腈-15 mmol/L醋酸铵为流动相,并考察流动相比例,乙腈-醋酸铵体积比为20∶80时,DCVMA保留时间已经大于30 min,而TFA保留时间小于0.5 min,因此采用梯度洗脱以得到合适的分析时间,优化梯度洗脱条件,程序见表1。在选定色谱和质谱条件下得到的标准溶液色谱图见图1。
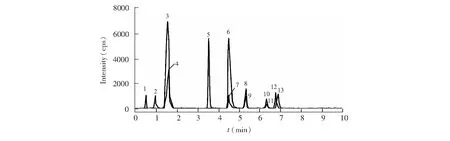
图1 混合标准溶液色谱图Fig.1 Chromatogram of mixed standard solution1. 三氟乙酸(Trifluoroacetic acid,TFA); 2. 苯乙醇酸(Mandelic acid,MA); 3. 苯乙醛酸(Phenylglyoxylic acid,PGA); 4. 三氯乙酸(Trichloroacetic acid, TCA); 5. 甲基马尿酸(Methylhippuric acid,MHA); 6. 苯巯基尿酸(S-phenylmercapturic acid, SPMA); 7. 苯巯基尿酸-d2(DL-S-phenylmercapturic-3,3-d2 Acid,SPMA-d2); 8. N-乙酰基-S-苯基-L-半胱氨酸(N-acetyl-S-(benzyl)-L-cysteine, BMA); 9. N-乙酰基-S-苯基-L-半胱氨酸-13C6(N-acetyl-S-(benzyl-13C6)-L-cysteine,BMA-13C6); 10. N-乙酰基-S-(1,2-二氯乙烯基)-L-半胱氨酸(N-acetyl-S-(1,2-dichlorovinyl)-L-cysteine,1,2-DCVMA);11. N-乙酰基-S-(1,2-二氯乙烯基)-L-半胱氨酸-13C,d3(N-acetyl-S-(1,2-dichlorovinyl)-L-cysteine-13C, d3(1,2-DCVMA-13C,d3); 12. N-乙酰基-S-(2,2-二氯乙烯基)-L-半胱氨酸(N-acetyl-S-(2,2-dichlorovinyl)-L-cysteine,2,2-DCVMA);13. N-乙酰基-S-(2,2-二氯乙烯基)-L-半胱氨酸-13C,d3(N-acetyl-S-(2,2-dichlorovinyl)-L-cysteine-13C,d3(2,2-DCVMA-13C,d3)
3.3 样品前处理
为减少饮水量和排汗量的影响,采样后需尽快测定尿肌酐含量。肌酐浓度超过0.3~3.0 g/L的范围,尿样舍弃,符合此浓度范围,用于待测物检测。
在实验所建立的方法下,各待测物质的检出限在0.035~1.75 μg/L之间,其灵敏度满足了暴露人群的接触水平的检测。实验平衡了方法灵敏度与大批量分析检测的实际工作要求,同时为了最大限度保证同时测定大批量尿样的准确度,采用了稀释进样的样品处理方式代替浓缩的样品处理方式。结果表明,10倍的稀释能够获得最小的离子抑制, 并且保持合适的灵敏度,此外,少于2%的样品在分析过程中出现了离子抑制的现象,继续稀释能够解决此问题,同时得到更优的分析结果。稀释液用15 mmol/L 醋酸铵缓冲液最佳,在其中即便加少量的甲醇也会使得测定灵敏度下降,峰形展宽且拖尾,这对出峰靠前的待测物影响尤为显著。
据文献[13]报道,苯系物的代谢产物前体 pre-SPMA在酸性条件下能转化成 SPMA,但实验发现,采用强酸水解尿样,会使SPMA以外的分析物的稳定性降低,故省略了此步骤。
因此,尿样经肌酐校正后,15000 r/min 离心5 min,取上清液用15 mmol/L醋酸铵缓冲液稀释10倍后,直接进样分析。
3.4 基质效应
为检测基质效应,将6 份模拟空白尿样品按2.2.5 节处理后,加入50 ng/mL混合标准溶液,进样分析。与用15 mmol/L 醋酸铵缓冲液配制的同样浓度的混合标准溶液测定的信号强度比较,计算各待测物的基质效应因子(Matrix factor,MF)[14],其中MHA、MA、PGA的基质效应较小,MF在95%~105%范围内,而TCA、SPMA、BMA和DCVMA的基质效应对定量结果有显著影响,主要表现为使测定结果偏低,MF在30%~40%范围内,为了获得更为准确的定量测定结果,实验对 SPMA、BMA 和 DCVMA 采用了同位素内标进行基质效应的校正(TCA同位素内标纯度达不到要求,仅为97%,实验采用三氟乙酸 (Trifluoroacetic acid,TFA)作为其内标物进行基质效应的校正),通过内标校正,MF可控制在90%~110%范围内。
3.5 方法指标
3.5.1 线性范围和检出限 用15 mmol/L醋酸铵缓冲液配制成混合标准系列应用液,按照2.2.3节绘制标准曲线。实验结果表明,待测物SPMA, PGA, TCA, BMA和DCVMA分别在0.1~500 ng/mL浓度范围内,MA、MHA在5~1000 ng/mL浓度范围内,线性良好,相关系数≥0.997。以3倍基线噪声所对应的浓度计算检出限,尿样稀释10倍处理,各待测物的方法检出限在0.035~1.75 μg/L范围内。
3.5.2 精密度 在本实验条件下,使用5 ng/mL混合标准溶液在同一天内重复进样6次和连续6 d进样测定,内标校正计算其响应值的RSD考察仪器的日内和日间精密度,测定结果分别为1.3%~5.9%和2.1%~6.4%。
3.5.3 加标回收率和精密度 在方法的线性范围内,于相同的尿样中分别加入低、中、高3个浓度的混合标准溶液,分别计算加标回收率,结果如表3所示,方法的回收率为85.0%~104%。样品的日内和日间精密度(RSDs,n=5)分别为1.2%~9.1%和2.0%~9.7%。
表3 加标回收率(n=5)
Table 3 Recoveries of spiked samples (n=5)
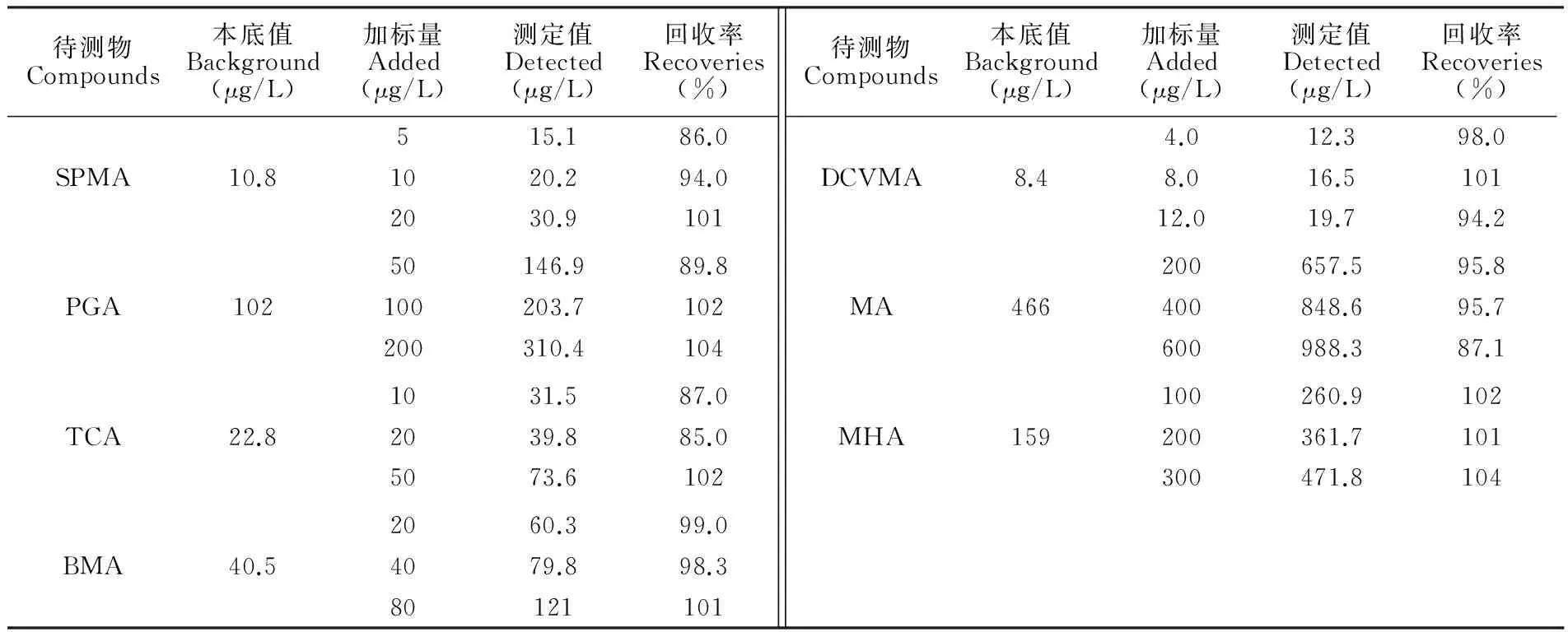
待测物Compounds本底值Background(μg/L)加标量Added(μg/L)测定值Detected(μg/L)回收率Recoveries(%)SPMA10.8PGA102TCA22.8BMA40.5515.186.01020.294.02030.910150146.989.8100203.7102200310.41041031.587.02039.885.05073.61022060.399.04079.898.380121101待测物Compounds本底值Background(μg/L)加标量Added(μg/L)测定值Detected(μg/L)回收率Recoveries(%)DCVMA8.4MA466MHA1594.012.398.08.016.510112.019.794.2200657.595.8400848.695.7600988.387.1100260.9102200361.7101300471.8104
3.6 实际样品分析
随机采集各地医院的孕妇尿样,用所建立的方法测定了深圳、南宁、成都、福州、石家庄、西安等地区650例孕妇尿样中苯系物和三氯乙烯代谢物的含量,并对测定值进行统计分析。通过正态性检验,p<0.05, 说明各样本所代表的总体不满足正态分布,故采用非参数检验-Bonferroni校正的两两比较法。首先进行各指标的总体比较,各地区的各指标中位数和统计结果如表4所示。当p>0.05,尚不能认为各地区孕妇尿样中相应指标具有差异;当p<0.05,可以认为各地区孕妇尿样中相应指标具有差异,经成对比较得出两地区间的差异。
表4 各地区孕妇尿样中苯系物和三氯乙烯代谢物的中位值和p值
Table 4 Statistic analysis of urine samples of pregnant women in different regional
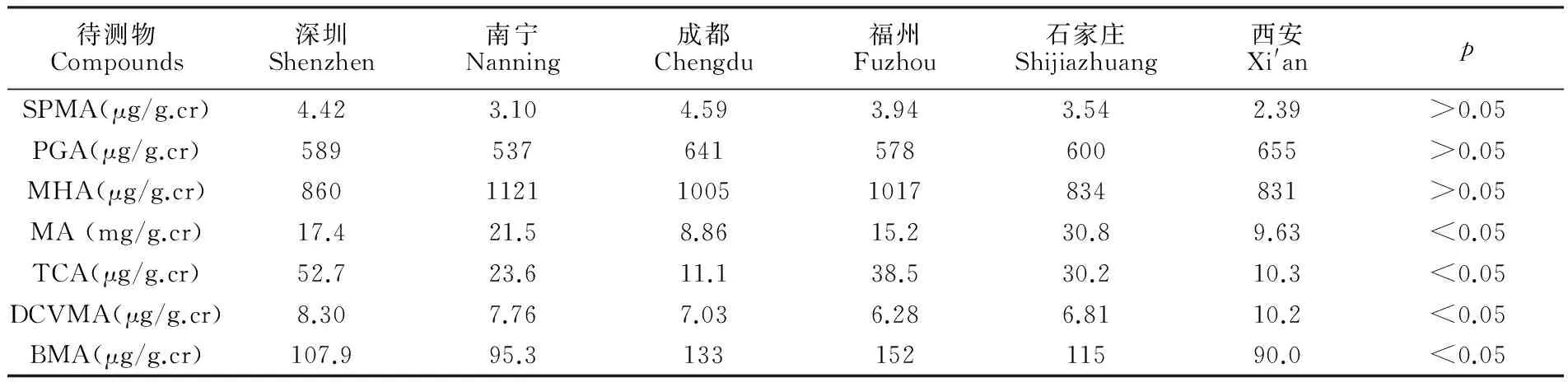
待测物Compounds深圳Shenzhen南宁Nanning成都Chengdu福州Fuzhou石家庄Shijiazhuang西安Xi'anpSPMA(μg/g.cr)4.423.104.593.943.542.39>0.05PGA(μg/g.cr)589537641578600655>0.05MHA(μg/g.cr)860112110051017834831>0.05MA(mg/g.cr)17.421.58.8615.230.89.63<0.05TCA(μg/g.cr)52.723.611.138.530.210.3<0.05DCVMA(μg/g.cr)8.307.767.036.286.8110.2<0.05BMA(μg/g.cr)107.995.313315211590.0<0.05
经成对比较,得出石家庄地区孕妇尿样中MA值分别与深圳、西宁、成都、福州、西安地区有明显差异,石家庄地区孕妇尿样中的MA值明显高于上述5个地区;深圳地区孕妇尿样中MA含量高于西安地区孕妇尿样中MA含量。
深圳地区孕妇尿样中TCA值分别与西宁、成都、福州、石家庄、西安有明显差异,深圳地区孕妇尿样中的TCA值明显高于以上地区;此外,福州地区孕妇尿样中TCA含量高于西宁、成都、西安地区孕妇尿样中TCA含量。
福州地区孕妇尿样中DCVMA值分别与深圳、西宁、西安地区有明显差异,福州地区孕妇尿样中的DCVMA值低于以上3个地区; 石家庄地区孕妇尿样中DCVMA含量低于深圳、西安地区孕妇尿样中DCVMA含量。
福州地区孕妇尿样中BMA值分别与深圳、西宁地区有明显差异,福州地区孕妇尿样中的BMA值高于以上2个地区。
综上,在各地区孕妇尿样中苯系物和三氯乙酸的代谢产物含量差异比较中,尚不能认为各地区孕妇尿样中SPMA、PGA、MHA值具有差异;各地区之间孕妇尿样中MA、TCA、DCVMA、BMA含量分别具有一定的差异,其中福州、石家庄、深圳地区含量较高,可能与其城市的工业发展状况、城市环境污染有一定的关系。
1 CHEN Wen, XU Lei, DENG Li-Xia, LI Fang-Hong, YANG Xing-Fen, ZHENG Chang-Liang, CHEN Gang.Chin.Occup.Med., 2000, 27(5): 9-11
陈 雯, 徐 雷, 邓丽霞, 李方红, 杨杏芬, 郑创亮, 陈 刚. 中国职业医学, 2000, 27(5): 9-11
2 LI Xing-Hu, WANG Jin-Feng, ZHENG Xiao-Ying, ZHANG Ke-Li.Chin.J.PublicHealth, 2005, 21(10): 1158-1160
李新虎, 王劲峰, 郑晓瑛, 张科利. 中国公共卫生, 2005, 21(10): 1158-1160
3 Boogarrd P J, Van Sittert N J.Environ.HealthPerspect, 1996, 104(6): 1151-1157
4 Qu Q, Melikian A A, Li G, Shore R, Chen L, Cohen B, Yin S, Kagan M R, Li H, Meng M, Jin X, Winnik W, Li Y, Mu R, Li K.Am.J.Ind.Med., 2000, 37(5): 522-531
5 Inoue O,Kanno E, Yusa T, Kakizaki M, Watanabe T, Higashikawa K, Ikeda M.Biomarkers, 2001, 6(3): 190-203
6 Laffon B, Lema M, Mendez J.J.Chromatogr.B, 2001, 753(2): 385-393
7 Schad H, Schafer F, Weber L, Seidel H J.J.Chromatogr.A, 1992, 593(1-2): 147-151
8 LIU Yun-Fu, TAN Guang-Hui.ChineseJournalofHealthLaboratoryTechnology, 2013, 23(3): 625-627
刘云富, 谭广辉. 中国卫生检验杂志, 2013, 23(3): 625-627
9 DU Hong, KONG Yu-Mei, WANG Ping, DU Guang-Yu.TheAdministrationandTechniqueofEnvironmentalMonitoring, 2000, 12(6): 33-34
杜 宏, 孔玉梅, 王 平, 杜广玉. 环境监测管理与技术, 2000, 12(6): 33-34
10 LIU Ming-Ren, YANG Xue-Yu, WANG Li, ZHANG Zhao-Liang.EnvironmentalScienceandTechnology, 2011, 34(11): 135-138
刘明仁, 杨学雨, 王 力, 张昭良. 环境科学与技术, 2011, 34(11): 135-138
11 LIU Wen-Jun, DUAN Ai-Ling, GAO Lan-Zhen.GansuEnvironmentalStudyandMonitoring, 2000, 13(4): 195-197
刘文君, 段爱玲, 高兰珍. 甘肃环境研究与监测, 2000, 13(4): 195-197
12 SUN Chen-Jun.BiomaterialsInspection, Beijing: People′s Medical Publishing House, 2006: 193
孙成均主编. 生物材料检验, 北京: 人民卫生出版社, 2006: 193
13 Sterz K, Kohler D, Schettgen T, Scherer G.J.Chromatogr.B, 2010, 878(27): 2502-2505
14 van Eeckhaut A, Lanckmans K, Sarre S, Smolders I, Michotte Y.J.Chromatogr.B, 2009, 877(23): 2198-2207
(Received 17 June 2015; accepted 21 October 2015)
This work was supported by the State Key Development Program for Basic Research of China (No.2010CB529502)
Determination of Metabolites of Benzene Compounds and Trichloroethylene in Urinary by Isotope Dilution-Ultra Performance Liquid Chromatography-Tandem Mass Spectrometry
ZHU Jing1, LI Yan1, YONG Li2, ZHENG Bo1, ZOU Xiao-Li*1, LIU Zhen3
1(DepartmentofLaboratoryTechnologyandScienceofPublicHealth,WestChinaSchoolofPublicHealth,SichuanUniversity,Chengdu610041,China)2(CenterforDiseaseControlandPreventionofSichuanProvince,Chengdu610041,China)3(NationalCenterforBirthDefectMonitoring,WestChinaSecondUniversityHospital,SichuanUniversity,Chengdu610041,China)
A method for simultaneous determination of metabolites of benzene compounds and trichloroethylene in pregnant urine by isotope dilution-ultra performance liquid chromatography-tandem mass spectrometry was established. Urine samples were diluted 10 times with ammonium acetate buffer containing working mixed internal standard and the filtrate was injected into UPLC/MS/MS for analysis. UPLC-MS/MS was performed on Waters C18column and the gradient elution was used for separation. The negative electrospray ionization (ESI) source under the multiple reaction monitoring (MRM) mode was used for quantitative analysis. The limits of detection (LOD) ranged from 0.0350 μg/L to 1.75 μg/L. The inter-day and intra-day precisions of method were 1.2%-9.1% and 2.0%-9.7%, respectively. The proposed method was applied on detecting 650 urine samples of pregnant women in different region and the results were analyzed by statistical method. The spiked recoveries were in the range of 85.0%-104%. The method was quick, sensitive and suitable for batch analysis of urine samples.
Isotope dilution; Ultra performance liquid chromatography-tandem mass spectrometry; Benzene compounds; Trichloroethylene; Metabolite; Urinary
10.11895/j.issn.0253-3820.150497
本文系国家重点基础研究发展计划(No.2010CB529502)资助
2015-06-17投稿;2015-10-21接受
* E-mail:zouxl_1113@163.com

