人源抗EV71病毒中和表位SP70 的Fab抗体研制
余艳琼,翁育伟,严延生
人源抗EV71病毒中和表位SP70 的Fab抗体研制
余艳琼1,翁育伟2,3,严延生2,3
目的 构建人源抗EV71病毒Fab噬菌体抗体库,筛选具有中和活性的人源单克隆抗体,为EV71感染引起的手足口病临床诊断及治疗奠定基础。方法 从成人志愿者抗凝血中分离外周淋巴细胞,提取总RNA并逆转录为cDNA。以cDNA为模板,用人源IgG Fab段基因引物扩增轻链及重链Fd区基因,分步克隆至pComb3载体,构建Fab噬菌体抗体库。以SP70为抗原对Fab噬菌体抗体库进行富集筛选,将获得的重组噬菌体感染XL1-Blue菌并诱导表达,用SP70对诱导表达的菌上清进行筛选。结果 共获得3株轻、重链基因组合序列不同的克隆,且这3株Fab抗体可特异性结合SP70多肽。结论 成功构建人源抗EV71病毒Fab噬菌体抗体库,并从中筛选出3株针对EV71病毒结构蛋白VP1上中和线性表位SP70的特异性人源Fab抗体,为研发新的手足口病诊断和治疗工具奠定基础。
EV71病毒;手足口病;噬菌体展示技术;人源化抗体;抗体Fab段;SP70
肠道病毒71型(Enterovirus 71,EV71)是一类单正链无包膜RNA病毒,属于小RNA病毒科肠道病毒A属成员[1]。近年来,由EV71病毒引起的手足口病对婴幼儿和儿童的健康成长造成了严重威胁,特别是EV71感染造成的重症和死亡病例高居不下,已成为我国的重要公共卫生问题之一[2-5]。虽然已经研发了EV71疫苗,且临床试验证实疫苗安全、有效[6-7],但尚无市售商品化疫苗问世[8];此外,对于EV71病毒引起的手足口病仍然缺乏有效防治措施[9]。
单克隆抗体因具有性质纯、效价高、特异性强、少或无血清交叉反应等特点,已被广泛应用于肿瘤、自身免疫性疾病、感染性疾病等疾病治疗[10-12]。因此,抗EV71单克隆抗体是一种潜在的、具有重要临床应用前景的侯选药物,或可应用于EV71感染引起手足口病的临床治疗,降低重症及死亡。SP70是EV71病毒VP1结构蛋白上具有中和活性的肽段[1]。研究表明,应用合成SP70多肽免疫小鼠,产生的鼠源性单克隆抗体对EV71病毒具有明显的中和活性[13]。但鼠源抗体对人体免疫系统具有较强的免疫原性,可诱发人抗鼠抗体反应,同时鼠源抗体不能有效激活人体免疫系统的生物效应功能[14],从而限制了其临床应用。本研究采用噬菌体表面展示技术,构建人源抗EV71病毒Fab抗体库,从中筛选针对EV71病毒结构蛋白VP1上中和线性表位SP70的特异性人源Fab抗体,从而为EV71病毒引起的手足口病诊断和治疗工具研发奠定基础。
1 材料与方法
1.1 材料
1.1.1 病毒、细胞、菌株及载体 EV71病毒分离株(2010FJLY008),C4a亚型,Gene Bank No.HQ426649,由福建省疾病预防控制中心病毒科分离;人横纹肌肉瘤RD细胞、大肠埃希菌(E.coli) XL1-Blue株、噬菌体载体pComb3由福建省疾病预防控制中心病毒科保存。
1.1.2 多肽及单抗 SP70多肽(氨基酸序列为:YPTFGEHKQEKDLEY)由上海生工公司合成,纯度≥95%;人源抗狂犬病毒Fab单克隆抗体由中国疾病预防控制中心病毒病所出血热室提供。
1.1.3 主要试剂 人淋巴细胞分离液购自天津灏洋生物制品公司;TRIzol○RLS Reagent及cDNA合成试剂盒购自Invitrogen公司;HRP-抗人IgG(Fab)抗体、抗人 IgG(Fab)抗体及FITC-抗人IgG(Fab)抗体购自Sigma公司;FITC-抗鼠抗体购自Dako公司;内切酶及T4 DNA 连接酶购自New England Biolabs公司产品;鼠源抗EV71病毒单克隆抗体购自Merck Millipore公司;其他试剂均为实验室常规试剂。
1.2 方法
1.2.1 淋巴细胞供体筛选 采集16名成人志愿者外周血3 mL,分离血清,以EV71病毒LY008分离株为抗原,通过免疫荧光试验(IFA)检测血清抗体,并进一步检测血清中针对EV71病毒的特异性中和抗体滴度,筛选出EV71病毒感染者。中和抗体滴度检测方法参照《手足口病防治手册》[19]。再将SP70(200 ng/孔)包被于高吸附96孔板中,采用ELISA法,检测其SP70多肽结合活性。
1.2.2 噬菌体抗体库的构建 从上述抗EV71病毒中和抗体阳性成人志愿者外周血中分离淋巴细胞,提取总RNA并反转录为cDNA。以人源抗体IgG Fab段基因引物[20]扩增重链Fd区基因、Kappa和Lambda轻链基因,PCR条件为:95 ℃预变性 5 min,94 ℃变性 1 min,52 ℃退火 1 min,72 ℃延伸 1 min,35个循环后,72 ℃延伸 10 min。利用XbaI/SacI、XhoI/SpeI内切酶将扩增出的人源抗体轻链片段及重链Fd区片段分步克隆至pComb3载体,电转至E.coliXLI-Blue,加入辅助噬菌体VCSM13进行感染,最终形成Fab噬菌体抗体菌库。将梯度稀释后的抗体库溶液感染XLI-Blue菌后均匀涂至含有氨苄青霉素的LB平皿,次日随机挑选单菌落,快提质粒后XbaI/SacI双酶切验证轻链插入率,XhoI/SpeI双酶切验证重链插入率,以检测转化效率;计算菌落数,按每mL轻链或重链抗体库所含的克隆数计算库容。
1.2.3 噬菌体抗体库的富集筛选 采用高吸附96孔板包被多肽抗原SP70,进行3轮富集筛选,3轮SP70包被量分别为2 μg/孔、500 ng/孔和100ng/孔。第1轮用0.1 mol/L NaHCO3包被液(pH 8.6)将合成多肽SP70包被于高吸附96孔板,4 ℃过夜;次日洗去未结合的抗原,并用B-MPBST(PBST 加入1%脱脂奶及1%BSA,新鲜配制使用)于37 ℃中封闭1 h后,加入100 μL预先活化的Fab噬菌体抗体库,37 ℃孵育2 h,用PBS-T( PBS 加入0.1%Tween-20)反复洗20遍,再用PBS洗2遍,最后每孔用100 μL甘氨酸盐酸洗脱液(pH 2.2)洗脱,再用适量的2 mol/L Tris液中和洗脱下的噬菌体;再次感染A600=0.5左右的XLI-Blue菌液,经辅助噬菌体VCSM13感染后进入下一轮富集筛选,重复上述步骤,对抗体库共进行3轮富集筛选。
1.2.4 Fab阳性克隆诱导表达及筛选鉴定 随机挑选经3轮富集筛选后的单菌落,过夜培养并利用IPTG诱导剂,30 ℃诱导表达过夜;次日离心后吸取菌上清用于ELISA检测,分别用多肽抗原SP70及抗人Fab抗体包被高吸附96孔板,加入待测样品菌上清,用HRP酶标的抗人Fab二抗检测 Fab活性及抗原结合活性。
1.2.5 Fab阳性克隆基因序列分析 对筛选获得的阳性菌克隆提取质粒后,检测Fab段轻、重链基因序列,并用DNA star软件对测序结果进行分析处理,获得其氨基酸序列分析结果,结合Internet V-Base基因库中的IgG家族序列,确定阳性克隆的抗体轻、重链。
2 结 果
2.1 EV71病毒感染者筛选 对16例成人志愿者血清进行EV71抗体IFA及EV71病毒中和抗体滴度检测,选出IFA反应阳性(图1),且抗EV71中和抗体滴度最高的血清,其血清滴度为1∶128。进一步对该血清进行SP70多肽结合活性ELISA检测,结果发现该名志愿者血清具有SP70多肽结合活性。抽取该患者外周血50 mL,置于肝素瓶中备用。
2.2 人源抗EV71病毒Fab噬菌体抗体库的构建 分离供体外周血淋巴细胞,提取总RNA,逆转录为cDNA,用人IgG Fab基因引物扩增了IgG重链Fd区基因和轻链基因(图2)。合并轻链PCR纯化产物,经XbaI/SacI双酶切后克隆入pComb3载体,电转感受态细胞,建立轻链库(pComb3-L)。再将重链Fd段PCR纯化产物及pComb3-L载体分别进行XhoI/SpeI双酶切,纯化酶切产物经T4连接酶连接后,电转感受态细胞,构建噬菌体Fab抗体库。双酶切验证轻、重链基因插入率,结果显示轻链、重链的插入率均接近100%,且轻、重链抗体库的平均库容量均可达到108。

图1 人血清EV71病毒免疫荧光分析Fig.1 Immunofluorescence assay of EV71 in human serum

M:100 bp DNA marker;1-5:κappa基因PCR产物;6-13:lamda基因PCR产物;14-21:Fd基因PCR产物. M: 100 bp DNA marker; 1-5: PCR products of κappa chain genes; 6-13: PCR products of lambda chain genes; 14-21: PCR products of Fd chain genes.图2 人源抗体Fd、κappa及lamda基因PCR产物Fig.2 PCR products of Fd,κappa and lamda chain genes
2.3 人源抗EV71病毒Fab噬菌体抗体库的富集筛选 经过3轮富集筛选后随机挑选800个克隆,诱导表达后,用抗人Fab抗体(1∶1 000)及纯化的SP70为抗原包被高吸附96孔板,分别加入待测样品菌上清,用HRP标记的抗人Fab二抗(1∶1 000)进行ELISA检测。结果共获得51个既有Fab抗体表达的同时也具有与多肽抗原SP70结合活性的克隆,阳性克隆与SP70多肽抗原特异性结合活性及与人源Fab表达活性ELISA检测结果见图3、4。

图3 ELISA 检测Fab抗体与SP70多肽抗原的特异性结合Fig.3 Specific binding of Fab antibody to SP70 antigen detected using ELISA

图4 ELISA检测人源Fab抗体表达Fig.4 Expression of Fab antibodies detected by ELISA
2.4 人源抗EV71病毒Fab抗体序列 将上述51个阳性菌克隆提取质粒后,通过序列测定确定其基因序列,与Internet V-Base基因库比对确定IgG家族,与IMGT/V-QUEST数据库比对,确定51个阳性克隆的抗体轻、重链型别,其中有15个克隆为同一抗体基因序列,本文将其命名为antiEV71-Fab1;有24个克隆为同一抗体基因序列,将其命名为antiEV71-Fab2;其余12个克隆抗体基因序列相同,将其命名为antiEV71-Fab3。即共获得3株具有不同抗体轻、重链基因组合序列的Fab抗体,其重链可变区主要分布在IgG VH1、VH3及VH4家族,轻链可变区主要分布在IgG VK3和Vλ1家族。这3株Fab抗体的互补决定区重链、轻链基因的氨基酸序列见表1、2。
表1 人源抗EV71病毒Fab抗体重链可变区基因的氨基酸序列
Tab 1 Deduced amino acid sequences of heavy chain V regions of humanized Fab antibody against EV71

FabcloneVHCDR1CDR2CDR3AntiEV71-Fab1VH1GQTFSSYAIIPIWGTFARSYGSSWTAGGFQHAntiEV71-Fab2VH3GFTSSQHYIPWNFGSAARYQSGWRAGDHAntiEV71-Fab3VH4GQSIFSGTYAIYASGYTARDKPGLHWFALGGFHP
表2 抗EV71病毒人源Fab抗体轻链可变区基因的氨基酸序列
Tab 2 Deduced amino acid sequences of light chain V regions of humanized Fab antibody against EV71
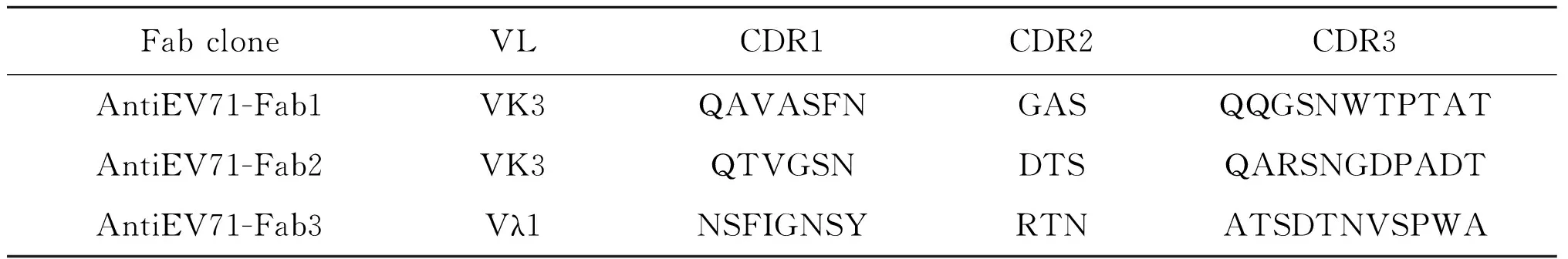
FabcloneVLCDR1CDR2CDR3AntiEV71-Fab1VK3QAVASFNGASQQGSNWTPTATAntiEV71-Fab2VK3QTVGSNDTSQARSNGDPADTAntiEV71-Fab3Vλ1NSFIGNSYRTNATSDTNVSPWA
3 讨 论
本研究采用噬菌体展示技术[16]从EV71感染的成人志愿者抗凝血中分离外周淋巴细胞,构建人源抗EV71病毒Fab噬菌体抗体库,并选择SP70为抗原对Fab噬菌体抗体库进行富集筛选。其中有51个克隆具有与多肽抗原SP70特异性结合活性,对其进行序列分析,获得的氨基酸序列比对显示,共有3株具有不同抗体轻、重链基因组合序列的Fab抗体,分别命名为antiEV71-Fab1、antiEV71-Fab2、antiEV71-Fab3。
虽然EV71感染后主要在婴幼儿及学龄前儿童发病[1],但婴幼儿体内EV71病毒保护性抗体水平非常低[17]。研究表明[18],在EV71病毒引起的脑膜脑炎患儿体内,其中和抗体水平与正常儿童无明显差异。造成这样现象的原因可能是:婴幼儿免疫应答机制不成熟,而且体内淋巴细胞仍处于动态变化中、功能尚不完善,所以合成抗体能力也较差[19]。因此,选择恢复期EV71感染患儿外周血作为人源性EV71病毒中和抗体的供体,可能无法获得高中和效价的中和抗体。本研究采用既往感染的成人外周淋巴细胞作为中和抗体来源,在一定程度上更有利于获得高效价抗病毒中和抗体。
抗原是决定特异性抗体筛选的关键,直接关系到抗体库筛选的有效性[21]。完整的EV71病毒颗粒虽然保留了所有天然抗原表位,有利于筛选到多种具有天然抗原结合活性的特异性中和抗体,但由于病毒颗粒制备步骤繁琐,且不易提纯,不利于抗体库的筛选。相比之下,合成多肽具有制备简单,纯度高,且特异性强,适合用于抗体库的筛选。综合考虑成本-效益后,本研究选用EV71病毒结构蛋白VP1上中和线性表位SP70作为筛选抗原。EV71抗体表位主要位于VP1结构蛋白上,而SP70是位于VP1结构蛋白上208~222位氨基酸的肽段[1]。Foo等[22]证实 SP70免疫小鼠产生的中和抗体效价与以完整病毒作为免疫源所产生的抗体效价一致,且SP70的氨基酸残基序列分析显示,在不同亚型病毒间SP70呈现高度保守性。Li等[13]用SP70免疫小鼠后获得的鼠单克隆抗体,经与EV71病毒进行中和实验后发现该株鼠单抗具有中和活性,进一步证明了SP70作为中和性线性表位的重要性。基于SP70多肽的诸多优势,我们合成了SP70的裸肽蛋白,以其作为抗体库筛选所需的抗原,经过3轮“吸附-洗脱-扩增”后,成功筛选出了3株SP70线性表位特异性的人源Fab单克隆抗体。这3株克隆的重链可变区主要分布在IgG VH1、VH3及VH4家族,轻链可变区主要分布在IgG VK3和Vλ1家族,造成所获得的Fab抗体的重、轻链基因家族的多样性有限的原因可能有:1)在构建噬菌体抗体库时,由于样本来源有限,我们只选取了1名曾感染过EV71病毒的成人志愿者外周血,这可能对抗体库的多样性有一定程度的影响;2)本研究选择的Fab基因扩增引物,更多的针对人体内所占比例较高的IgG1的抗体基因,利用其进行人抗体基因的扩增时,也可能会导致某些遗传信息的丢失;3)不同个体间抗体基因的使用频率差异也可能造成抗体的多样性下降,Davidkova等[23]就曾运用原位杂交的方法,发现各健康个体之间VH基因家族的使用频率存在很大差异;4)抗体库构建过程中因操作和方法等因素的影响也可能导致多样性降低。所以在本次研究过程中,不可避免的存在抗体库多样性受限的情况。此外,鉴于SP70仅是EV71病毒中由14个氨基酸组成的多肽,而不是完整的病毒颗粒[1],故这3株特异性单克隆抗体是否具有针对EV71完整病毒颗粒的中和活性,还有待进一步研究。然而,由于线性多肽在抗体库筛选中具有简单、快速的优势,如进一步采用多种线性多肽作为筛选抗原,则可能可以筛选出多价抗病毒中和抗体。
综上,本研究成功构建了人源抗EV71病毒Fab噬菌体抗体库,并从中筛选出3株针对EV71病毒结构蛋白VP1上中和线性表位SP70的特异性人源Fab抗体,为研发新的手足口病诊断和治疗工具奠定了基础。
[1] Wang SM, Liu CC. Enterovirus 71: epidemiology, pathogenesis and management[J]. Expert Rev Anti Infect Ther, 2009, 7(6): 735-472. DOI: 10.1586/eri.09.45
[2] Xing W, Liao Q, Viboud C, et al. Hand, foot, and mouth disease in China, 2008-12: an epidemiological study[J]. Lancet Infect Dis, 2014, 14(4): 308-318. DOI:10.1016/S1473-3099(13)70342-6
[3] Wang C, Li X, Zhang Y, et al. Spatiotemporal cluster patterns of hand, foot, and mouth disease at the county level in mainland China, 2008-2012[J]. PLoS One, 2016, 11(1): e0147532. DOI: 10.1371/journal.pone.0147532
[4] Zhuang ZC, Kou ZQ, Bai YJ, et al. Epidemiological research on hand, foot, and mouth disease in mainland China[J]. Viruses, 2015, 7(12): 6400-6411.DOI: 10.3390/v7122947
[5] Liu MY, Liu W, Luo J, et al. Characterization of an outbreak of hand, foot, and mouth disease in Nanchang, China in 2010[J]. PLoS One, 2011, 6(9): e25287. DOI: 10.1371/journal.pone.0025287
[6] Li R, Liu L, Mo Z, et al. An inactivated enterovirus 71 vaccine in healthy children[J]. N Engl J Med, 2014, 370(9): 829-837. DOI: 10.1056/NEJMoa1303224
[7] Zhu F, Xu W, Xia J, et al. Efficacy, safety, and immunogenicity of an enterovirus 71 vaccine in China[J]. N Engl J Med, 2014, 370(9): 818-828.DOI:10.1056/NEJMoa1304923
[8] Chong P, Liu CC, Chow YH, et al. Review of enterovirus 71 vaccines[J]. Clin Infect Dis, 2015, 60(5): 797-803. DOI:10.1093/cid/ciu852
[9] Wong SS, Yip CC, Lau SK, et al. Human enterovirus 71 and hand, foot and mouth disease[J]. Epidemiol Infect, 2010, 138(8): 1071-1089. DOI: org/10.1017/S0950268809991555
[10] Weiner GJ. Building better monoclonal antibody-based therapeutics[J]. Nat Rev Cancer, 2015, 15(6): 361-370. DOI: 10.1038/nrc3930
[11] Racadot DE, Wendling D, Rumbach L, et al. Current concepts in the treatment of autoimmune diseases with monoclonal antibodies[J]. Clin Immun, 1994, 1(3): 199-208. DOI: 10.1007/BF03258506
[12] Ter Meulen J. Monoclonal antibodies in infectious diseases: clinical pipeline in 2011[J]. Infect Dis Clin North Am, 2011, 25(4): 789-802. DOI: 10.1016/j.idc.2011.07.006
[13] Li X, Mao C, Ma S, et al. Generation of neutralizing monoclonal antibodies against Enterovirus 71 using synthetic peptides[J]. Biochem Biophys Res Commun, 2009, 390(4): 1126-1128. DOI: 10.1016/j.bbrc.2009.09.103
[14] Ge Y. Development strategy analysis and application of humanized antibody[J]. International Journal of Immunology, 2004, 27(5): 271-274. (in Chinese)
葛彦. 人源化抗体研制策略分析及应用研究[J]. 国际免疫学杂志, 2004, 27(5): 271-274.
[15] Wang ZC. Hand, foot, and mouth disease prevention manual[M]. Suzhou: Suzhou University Press[M]. Suzhou:Suzhou Univerity press 2008:57-61.(in Chinese)
王忠灿.手足口病防治手册[M]. 苏州:苏州大学出版社,2008:57-61.
[16] Zhang ZD, Cheng J, Zhang SL. Phage display technology and application[J]. World Chinese Journal of Digestology , 2003, 11(4): 459-461.(in Chinese)
张忠东, 成军, 张树林. 噬菌体展示技术的原理及应用[J].世界华人消化杂志, 2003, 11(4): 459-461.
[17] Zhang Y, Liu H, Wang L, et al. Comparative study of the cytokine/chemokine response in children with differing disease severity in enterovirus 71-induced hand, foot, and mouth disease[J]. PLoS One, 2013, 8(6): e67430. DOI: 10.1371/annotation/f582a7ef-3b3e-4e95-9522-23f0f3f77cde
[18] Yang KD, Yang MY, Li CC, et al. Altered cellular but not humoral reactions in children with complicated enterovirus 71 infections in Taiwan[J]. J Infect Dis, 2001, 183(6): 850-856. DOI: 10.1086/319255
[19] Zhang HY, Han YY. Study of cell immunity and humoral immunity in HFMD infants with EV71 infection[J]. China Modern Doctor, 2013, 51(9): 28-30.(in Chinese)
张海瑛,韩宜姚. EV71感染手足口病患儿细胞及体液免疫功能研究[J]. 中国现代医生, 2013, 51(9): 28-30.
[20] Hust M, Toleikis L, Du-bel S. Antibody phage display[M].In: Handbook of therapeutic antibodies. Weinheim;Wiley-VCH,2007,45-68.
[21] Gou LT, Yang JL. Advances of technology and strategy of antibody library[J].Letters In Etters In Biotechnology, 2009, 20(6): 859-864.(in Chinese)
勾蓝图,杨金亮. 抗体库技术与策略进展[J]. 生物技术通讯, 2009, 20(6): 859-864.
[22] Foo DG, Alonso S, Phoon MC, et al. Identification of neutralizing linear epitopes from the VP1 capsid protein of Enterovirus 71 using synthetic peptides[J]. Virus Res, 2007, 125(1): 61-68. DOI:10.1016/j.virusres.2006.12.005
[23] Davidkova G, Pettersson S, Holmberg D, et al. Selective usage of VH genes in adult human B lymphocyte repertoires[J]. Scand J Immunol,1997, 45: 62-73. DOI:10.1046/j.1365-3083.1997.d01-376.x
Yan Yan-sheng, Email:yysh@publ.fz.fj.cn
Development of a humanized Fab antibody against the neutralizing SP70 epitope of EV71
YU Yan-qiong1, WENG Yu-wei2,3, YAN Yan-sheng2,3
(1.HuliDistrictCenterforDiseaseControlandPrevention,Xiamen361000,China;2.SchoolofPublicHealth,FujianMedicalUniversity,Fuzhou350001,China;3.FujianCenterforDiseaseControlandPrevention,Fuzhou350001,China)
We developed a humanized Fab phage-display library against EV71, and screened humanized monoclonal antibody with a neutralization activity, so as to provide a basis for clinical diagnosis and treatment of hand, foot and mouth disease induced by EV71 infection. Peripheral blood lymphocytes were isolated from anticoagulated blood specimens of adult volunteers infected with EV71. Total RNA was extracted from lymphocytes, and transcribed reversely into cDNA. The light-chain and heavy-chain Fd fragments were amplified using cDNA as a template, and cloned into the vector pComb3 to construct Fab phage-display library. SP70, a neutralizing linear epitope from the VP1 structural protein of EV71, was used as an antigen for enrichment and screening of Fab phage antibody library, and the yielded recombinant phage was used to infectE.coliXL1-Blue. Then, the supernatant ofE.coliXL1-Blue following induced expression was screened using SP70. A total of 3 light- and heavy-chain clones with various sequences were yielded, which bound specifically to SP70 polypeptide. A humanized anti-EV71 Fab phage antibody library is successful constructed, and 3 specific humanized Fab antibodies are screened that target the neutralizing linear epitope SP70, which provide new insights into the development of novel diagnostics and therapeutics for hand, foot, and mouth disease.
Enterovirus 71 (EV-71); hand, foot and mouth disease; phage display technology; humanized antibody; Fab fragment; SP70
国家高技术研究发展计划(863计划)(No.2011AA02A114);福建省自然科学基金(No.2010J01115)联合资助
严延生,Email:yysh@publ.fz.fj.cn
1.福建省厦门市湖里区疾病预防控制中心,厦门 361000;
2.福建医科大学公共卫生学院,福州 350001;
10.3969/j.issn.1002-2694.2016.08.001
R373
A
1002-2694(2016)08-0683-06
2016-03-20;
2016-04-18
3.福建省疾病预防控制中心,福州 350001
Supported by the National High-tech R & D Program of China (No. 2011AA02A114) ,and the Natural Science Foundation of
Fujian Province (No. 2010J01115).

