Ag/BiOCl复合材料合成及光催化杀菌活性研究
魏 黛, 刘向宇, 吕 中
(武汉工程大学 化工与制药学院, 武汉 430074)
Ag/BiOCl复合材料合成及光催化杀菌活性研究
魏 黛, 刘向宇, 吕 中*
(武汉工程大学 化工与制药学院, 武汉 430074)
通过沉积法直接将纳米银颗粒负载到BiOCl上,合成Ag/BiOCl二元复合纳米材料,通过X射线粉末衍射、扫描电子显微镜、能量色散X射线光谱仪和紫外可见漫反射光谱等多种表征方法对纳米复合物的组成、形貌、光学性质进行表征. 研究其在可见光下对金黄色葡萄球菌 (S.aureus) 的杀菌活性,并探讨杀菌机理. 结果发现,BiOCl负载纳米银后,由于银的表面等离子体效应,将BiOCl对光的吸收范围从紫外光区拓展到可见光区. 在可见光下Ag/BiOCl能将浓度为1×106cfu·mL-1的S.aureus在6 h内完全杀灭,优于单纯的BiOCl以及纳米Ag在可见光下对S.aureus的杀菌效果. 通过荧光光谱和电化学阻抗对BiOCl和Ag/BiOCl内电子的激发、迁移与消耗过程进行分析,发现Ag/BiOCl二元复合材料光生电子和空穴的复合率低于单纯的BiOCl. 通过捕获剂实验初步确定杀菌过程中的主要活性物种是电子、空穴和H2O2. 该研究首次报道了Ag/BiOCl在可见光下对S.aureus的光催化杀菌活性.
可见光催化杀菌; Ag/BiOCl; 杀菌机理; 活性物种
随着我国生物、医药、食品等行业的飞速发展,大量含微生物废水的肆意排放对环境造成的污染程度日趋严重. 细菌感染最直接普遍的途径就是通过污染与人类息息相关的饮用水. 目前使用的饮用水消毒方式主要有物理消毒、化学消毒和光化学消毒等. 然而,随着水质污染加剧、抗生素的广泛使用和微生物的抵抗性及毒性的增强,很多传统的消毒方法不能有效去除水体中的有害微生物,有些方法甚至会产生致癌的有毒副产物[1-3]. 1985年Matsunaga等人[4]首次报道TiO2光催化杀菌作用,其对环境污染小,不会产生对人体有害的副产物,同时还能用于治理环境中有机物降解,因而基于半导体的光催化杀菌性能研究受到了广大学者的关注[5]. 目前大多数的报道是基于TiO2光催化杀菌研究,然而,TiO2属于宽带隙半导体,只能在紫外光下被激发,但紫外光在自然光中只占大约4%,对光能的利用率低是限制TiO2被广泛应用的主要原因[6-7].因此寻求在可见光下能有效杀菌的光催化剂具有重要意义.
铋元素位于元素周期表中金属与非金属交界处,具有特殊的理化性质,对有机体毒性小,是一种无毒的“绿色”金属. 近年来,含铋无机半导体材料被发现具有较好的光、热、电转化性能,有望在非均相催化领域得到进一步的应用[8-9]. 其中,BiOCl因其独特的层状结构,使其具有良好的光生载流子流动性能与高的光生电子与空穴分离效率,在水解制氢、太阳能电池、燃料电池及有机污染物降解等领域的研究被广泛报道[10-11]. 但是单体BiOCl带隙值较大,直接的价带到导带的光跃迁只能利用太阳光谱中仅占4%的紫外光,因此其作为光催化剂在实际的应用中受到很大的局限. 通过贵金属负载是提高半导体催化活性的有效手段之一,其中纳米Ag因为其价格相对低廉,对可见光有强烈响应,以及在半导体上能产生表面等离子体效应,被认为是非常具有应用前景的改性材料之一[12]. 目前关于Ag/BiOCl二元复合纳米材料的研究集中在光催化降解有机染料[13-14],在光催化杀菌领域的研究未见报道. 鉴于此,本文通过直接沉积法,将合成好的纳米Ag颗粒沉积到片状BiOCl上,合成出Ag/BiOCl二元复合纳米材料,探讨其光催化杀菌活性及机理.
1 实验部分
1.1材料与仪器
五水合硝酸铋 (Bi(NO3)3·5H2O),重铬酸钾 (K2Cr2O7),草酸钠 (Na2C2O4),Aldrich;氯化钾 (KCl),一缩二乙二醇 (DEG),异丙醇 (Isopropanol),国药集团化学试剂有限公司;EDTA-Fe (II), AJAX化学试剂有限公司. 实验所用菌种为金黄色葡萄球菌 (S.aureus, ATCC 9118) 由华中师范大学生命科学学院提供.
样品的组分和形貌通过X射线粉末衍射 (XRD, Bruker axs D8 Discover,CuKα=1.5406 Å)、扫描电子显微镜 (SEM, Hitachi S4800)与X 射线能谱 (EDX);利用紫外可见分光光度计 (DRS, Shimadzu UV-2550) 对样品进行紫外-可见光吸收光谱测试; 利用电化学阻抗 (EIS, 上海辰华CHI 660E)和荧光光谱 (PL, Htiachi F-4600)对Ag/BiOCl内电子的激发、迁移与消耗过程进行分析.
1.2实验方法1.2.1BiOCl和纳米Ag的合成 将 0.970 g Bi(NO3)3·5H2O (2 mmol) 溶解至40 mL DEG,得溶液A. 将0.150 g KCl溶解到 20 mL 去离子水中得溶液B. 然后将溶液B缓慢滴加到溶液A中,得白色沉淀. 将所得溶液静置15 min后,离心、洗涤并收集样品. 所得样品在60oC 烘箱中干燥24 h后待用,编号S1. 纳米Ag的合成:参见本课题组的合成方法[15],粒径为 2~10 nm.
1.2.2Ag/BiOCl的合成 称取0.1 g上述合成的BiOCl (S1) 粉末,将其分散在1 mL上述配好的纳米Ag溶液(1 mg/mL)中,在磁力搅拌器下搅拌4 h后,离心、洗涤并收集样品. 所得样品在60oC 的烘箱中干燥24 h后待用,编号S2.
1.2.3光催化杀菌实验 实验所用光源为带有紫外光滤光片 (λ≥400 nm) 的500 W氙灯提供的可见光. 实验过程中所用到的玻璃仪器均在121oC下高温高压灭菌20 min以确保无菌. 具体实验步骤如下:将细菌用0.9 %的无菌生理盐水稀释成浓度约为1×106cfu·mL-1的菌悬液,取20 mL菌液并加入2 mg的Ag/BiOCl催化剂,使体系中催化剂浓度为100 mg·L-1. 实验温度控制在25oC左右,反应过程中每隔1 h取0.5 mL的菌液,用0.9 % 的生理盐水稀释后倒平板,在37oC恒温箱中培养24 h后,通过菌落计数法确定反应体系中存活的细菌浓度.
1.2.4光电测试 采用标准三电极系统,铂丝作为对电极,甘汞电极作为参比电极,0.5 mol/L 铁氰化钾/亚铁氰化钾溶液为电解质.工作电极制作过程如下:将 20 mg 所合成样品分散到由 1 mL DMF 和 0.01 mL nafion 溶液 (5%, DuPont) 组成的混合溶液,取 0.1 mL将其均匀滴涂到 10 mm × 10 mm的铟锡氧化物 (ITO) 导电玻璃电极上,控制平均样品涂覆量为2 mg/cm2. 浆液自然风干后,将导电玻璃转移到80 °C的真空干燥箱中干燥4 h以除去残存的DMF液体.在开路电压下测试,实验过程中以样品通过滴涂的方法涂覆到玻碳电极上,作为工作电极使用.测试过程中交流扰动电压设置为5 mV ,扫描频率范围为0.5~105Hz.
1.2.5捕获剂实验 在20 mL 1×106cfu·mL-1的S.aureus与100 mg·L-1Ag/BiOCl的混合溶液中,分别采用了0.5 mmol/L Na2C2O4作为空穴 (h+) 的捕获剂,5 mmol/L Isopropanol作为羟基自由基 (·OH) 的捕获剂,0.05 mmol/L K2Cr2O7作为电子 (e-) 的捕获剂,0.1 mmol/L EDTA-Fe (II) 作为H2O2的捕获剂.活性物种捕获实验过程与上述光催化杀菌活性测试的过程一致.
2 结果与讨论
2.1样品的表征分析
图1为所合成样品的XRD表征结果. 样品S1的所有特征衍射峰都能与正方晶系的BiOCl (JCPDS卡片编号06-0249) 完全对应,没有出现杂峰,说明合成样品S1是BiOCl,且纯度高. 样品S2中同样能观察到BiOCl的所有特征衍射峰,但是没有明显观察到单质Ag的特征衍射峰,这可能与银的负载量太低有关.
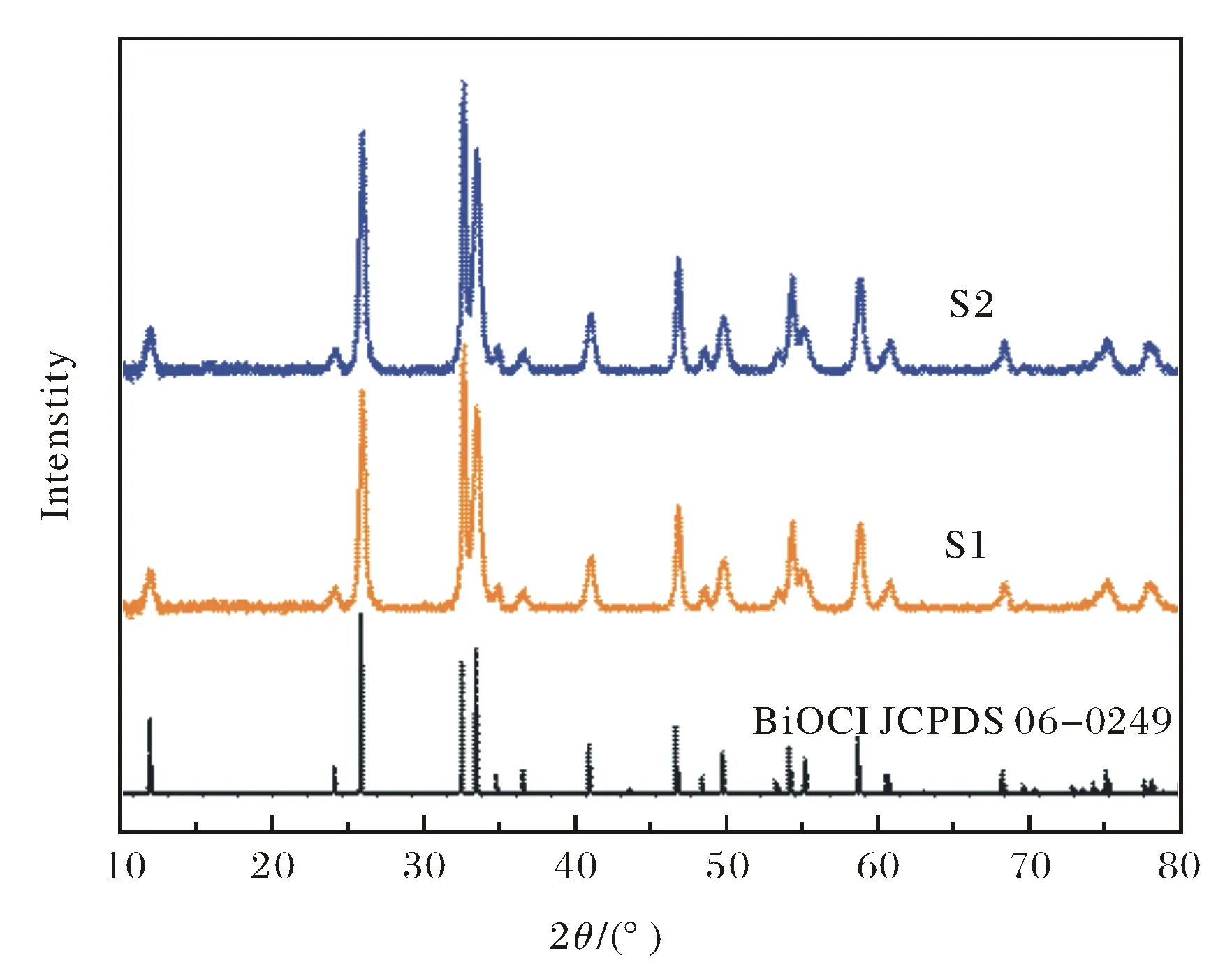
图1 样品S1和S2的XRD图谱Fig.1 XRD patterns of S1and S2
样品的SEM分析如图2所示,图2 (a) 和图2(b) 分别是样品S1和S2的扫描图,从图2中可以看出,负载前后样品形貌没有发生明显变化,都是平均直径在50 nm,厚度在10 nm的片状结构;从图2 (b) 中可以观察到有小颗粒分散在纳米片上.

图2 样品S1 (a) 和S2 (b) 的SEMFig.2 SEM of S1 (a) and S2 (b)
图 3 是样品S2的EDX分析,图谱中出现了Ag、Cl、O、Bi、C、Al的峰,其中C和Al为样品在测试中使用的基底材料,这说明样品S2中含有元素Ag、Cl、O、Bi. 虽然从XRD图谱中没有观察到样品S2中出现单质Ag的特征衍射峰,但是结合样品S1和S2的SEM和EDX图分析可知,样品S1为纯的BiOCl,样品S2为Ag/BiOCl二元复合纳米材料.
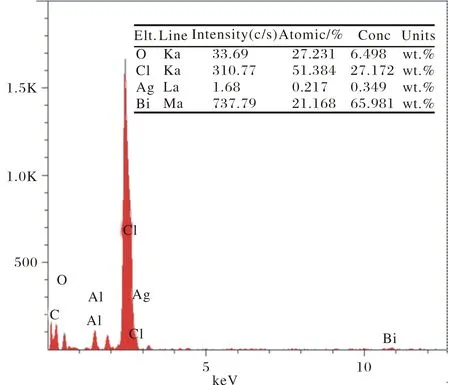
图3 样品S2的EDXFig.3 EDX of S2
纯的BiOCl、Ag/BiOCl二元复合材料和合成的纳米银颗粒的紫外漫反射光谱如图4所示. 单纯的BiOCl属于宽带隙半导体材料,对光的吸收主要集中在紫外光区域,在可见光区基本没有吸收,纳米Ag颗粒在可见光区 (400 nm左右) 表现出对光强烈的吸收. 当在BiOCl上负载Ag后,二元复合物对光的吸收范围从紫外区拓展到可见光区,从图中可以明显观察到在400~500 nm 对光的吸收增强,这说明纳米Ag的表面等离子效应有利于复合材料的光吸收范围向可见光区延展,提升材料对可见光的利用率.
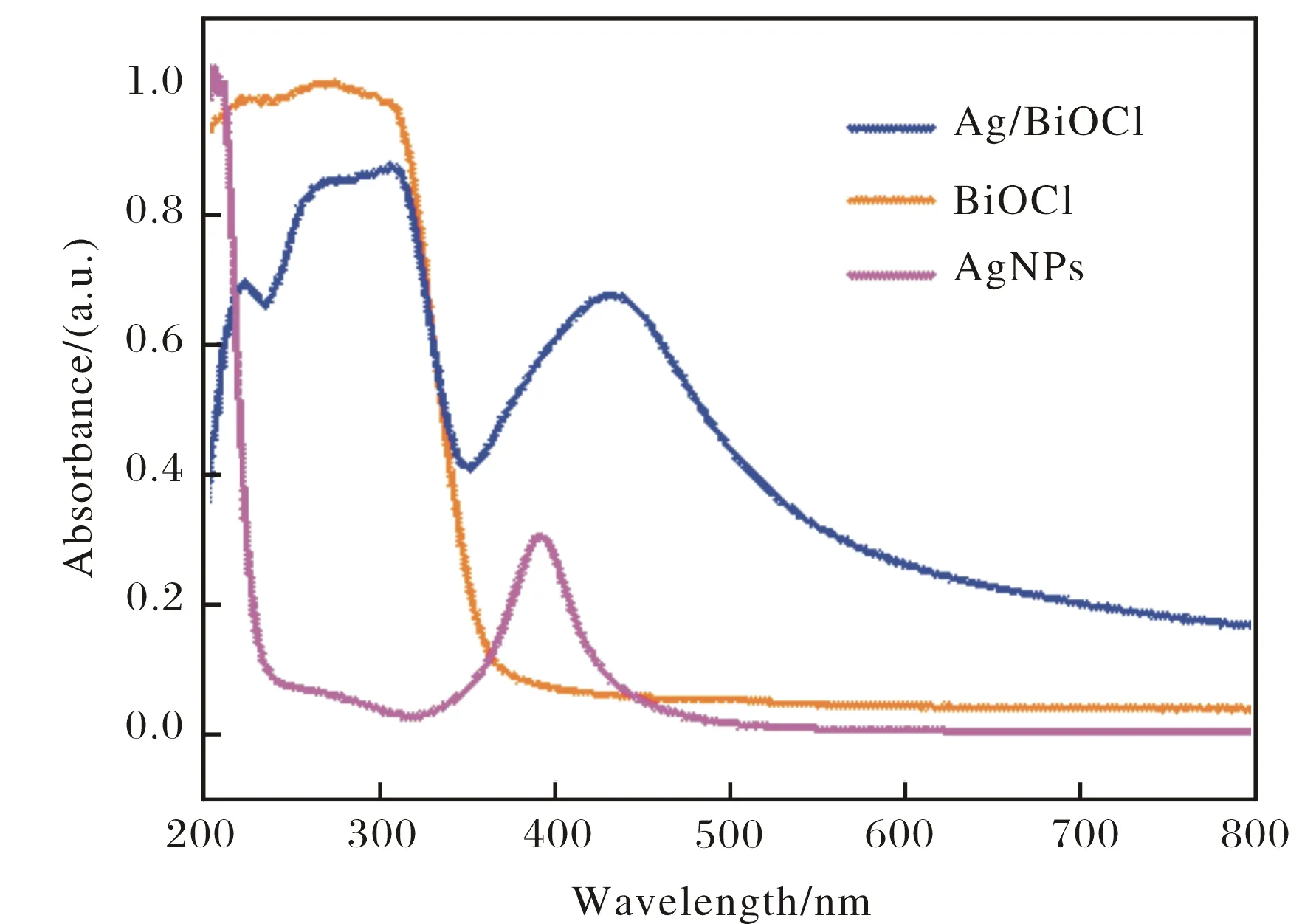
图4 BiOCl、纳米银和Ag/BiOCl的紫外-可见光漫反射光谱图Fig.4 UV-vis diffuse reflectance spectra of BiOCl, Ag nanoparticles and Ag/BiOCl
2.2Ag/BiOCl的可见光催化杀菌活性研究
Ag/BiOCl二元复合材料在可见光下对S.aureus的光催化杀菌活性见图5. 在空白实验 (Light control) 中显示,S.aureus在没有催化剂存在条件下,在可见光下照射6 h后,细菌浓度基本没有变化,说明在实验条件下的光照不会对细菌造成损伤. 当只有催化剂Ag/BiOCl存在而没有可见光照射条件下 (Dark control),细菌浓度在6 h内也基本没有变化,这说明催化剂Ag/BiOCl本身对细菌是无毒无害的. 在可见光照射下,单纯的BiOCl对S.aureus的杀菌能力很低,在6 h后的灭活率只有0.71-log,当催化剂为Ag/BiOCl二元复合体系时,其光催化杀菌活性有了很大程度的提升,在6 h内能将细菌完全杀灭. 已有文献报道纳米Ag对细菌有抗菌作用[16-18],为了研究Ag/BiOCl的杀菌效果是否是由于负载在BiOCl上的单质Ag发挥杀菌作用,将纳米Ag (理论负载浓度10 mg·L-1)作为催化剂,发现其在可见光下,6 h内对S.aureus的杀菌效率仅有1.9-log,远低于Ag/BiOCl二元复合材料对S.aureus的杀菌活性. 这些结果说明,Ag/BiOCl二元复合材料的光催化杀菌活性提高,主要不是因为纳米Ag的杀菌效果,可能是负载Ag后材料的光催化活性改变,从而影响其杀菌活性.
2.3Ag/BiOCl的可见光催化杀菌机理探讨
为探究Ag负载后样品的光催化杀菌性能提升机制,通过材料的EIS及PL对材料内电子的激发,迁移与消耗过程进行分析,结果如图6.图6 (a) 是BiOCl和Ag/BiOCl的EIS Nyquist图谱,Ag/BiOCl表现出比单纯BiOCl更小的半圆弧,说明复合材料内电子和空穴的迁移效果更好,更有利于电子与空穴的分离.光生电子与空穴的复合过程通过PL进行研究.材料的PL是材料内处于激发态电子以光能形式释放能量回到基态的过程,因此,荧光强度越强说明材料内光生电子与空穴的复合机率越大.图6 (b) 为BiOCl和Ag/BiOCl的光致荧光谱图,从图中可以得知,Ag/BiOCl表现出更低的荧光强度,说明负载纳米银后,光生载流子的复合率降低.综上所述,在BiOCl上负载纳米Ag能有效促进光生电子和空穴的分离,从而提高Ag/BiOCl的光催化活性.
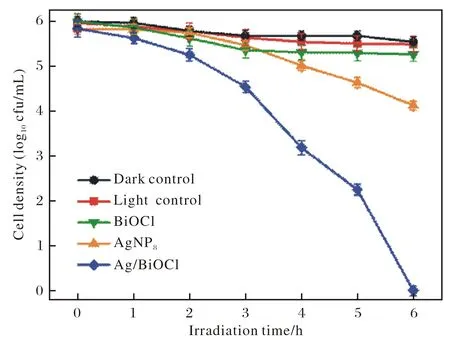
图5 不同催化剂在可见光下对S.aureus的光催化杀菌活性Fig.5 Photocatalytic inactivation efficiency of S.aureus under visible light irradiation using different catalysts
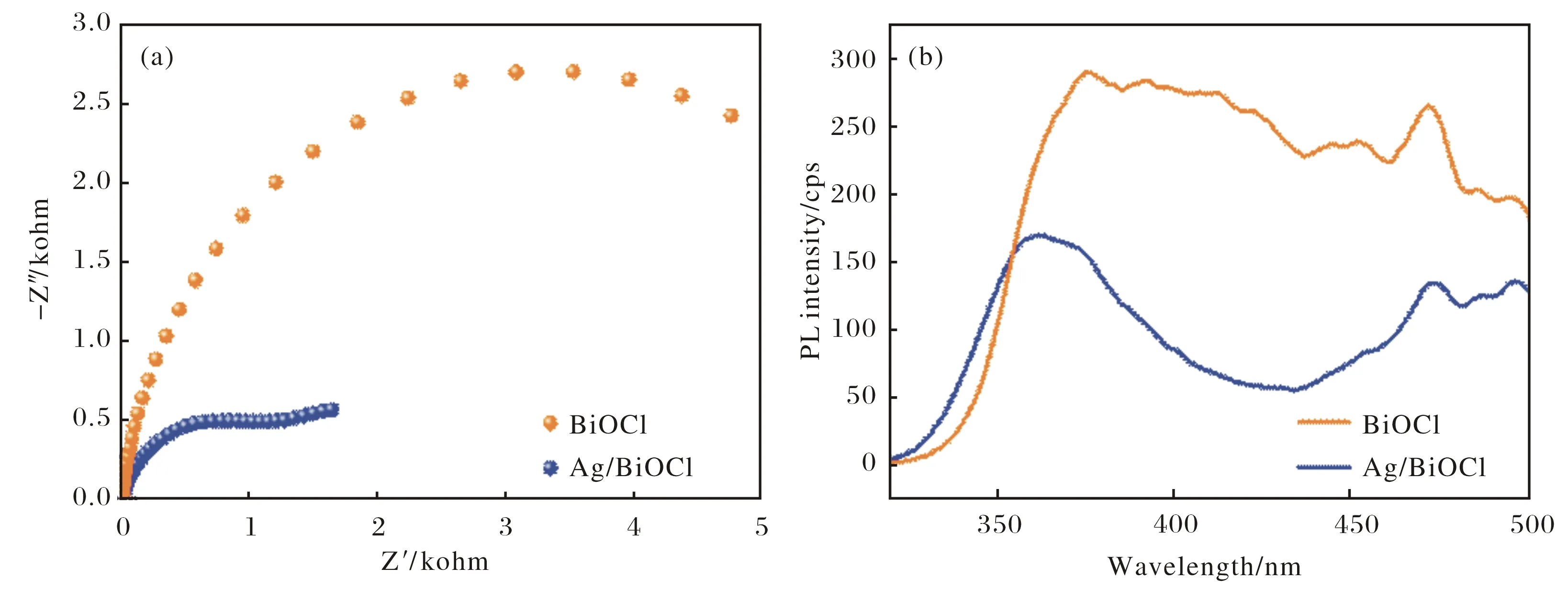
图6 BiOCl和Ag/BiOCl的交流阻抗谱 (a) 以及荧光光谱图 (b)Fig.6 (a) Electrochemical impedance spectroscopy and (b) photoluminescence spectra of BiOCl and Ag/BiOCl
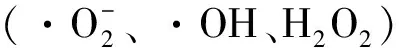
3 结论
通过简单的沉积法成功合成纳米Ag颗粒分布较均一的Ag/BiOCl二元复合材料,在可见光下Ag/BiOCl表现出优于BiOCl和纳米Ag颗粒对S.aureus的光催化杀菌活性. 可能的杀菌机理是在可见光照射下,由于纳米Ag的表面等离子体效应,使材料表面产生e-和h+,而BiOCl的层状结构能够有效的转移电子,促进光生载流子的分离,从而提高复合材料的光催化活性.生成的e-和h+能与反应体系中的H2O或O2发生反应,生成H2O2,氧化细菌细胞壁,或进入细胞氧化细胞内的生物大分子,从而导致细菌灭亡.

图7 不同捕获剂对S.aureus的可见光催化杀菌活性图(a)在没有Ag/BiOCl存在下;(b)存在Ag/BiOCl时Fig.7 (a) Photocatalytic disinfection efficiency of S.aureus in absence of Ag/BiOCl with different scavengers under visible light irradiation (b) Photocatalytic disinfection efficiency of S.aureus in the presence of Ag/BiOCl with different scavengers under visible light irradiation.
[1] PARK S K, HU J Y. Assessment of the extent of bacterial growth in reverse osmosis system for improving drinking water quality[J]. J Environ Sci, Health Part A, 2010, 45(8): 968-977.
[2] KULAKOV L A, MCALISTER M B, OGDEN K L, et al. Analysis of bacteria contaminating ultrapure water in industrial systems[J]. Appl Environ Microb, 2002, 68(4): 1548-1555.
[3] SRINIVASAN S, HARRINGTON G W, XAGORARAKI I, et al. Factors affecting bulk to total bacteria ratio in drinking water distribution systems[J]. Water Res, 2008, 42(13): 3393-3404.
[4] MATSUNAGA T, TOMODA R, NAKAJIMA T, et al. Photoelectrochemical sterilization of microbial cells by semiconductor powders[J]. Fems Microbiol Lett, 1985, 29(1-2): 211-214.
[6] TONG T Z, ZHANG J L, TIAN B Z, et al. Preparation of Fe3+-doped TiO2catalysts by controlled hydrolysis of titanium alkoxide and study on their photocatalytic activity for methyl orange degradation[J]. J Hazard Mater, 2008, 155(3): 572-579.
[7] RIZZO L, SANNINO D, VAIANO V, et al. Effect of solar simulated N-doped TiO2photocatalysis on the inactivation and antibiotic resistance of anE.colistrain in biologically treated urban wastewater[J]. Appl Catal B-Environ, 2014, 144: 369-378.
[8] ZHOU Y, VUILLE K, HEEL A, et al. An inorganic hydrothermal route to photocatalytically active bismuth vanadate[J]. Appl Catal A-gen, 2010, 375(1): 140-148.
[9] ZHOU Y, KRUMEICH F, HEEL A, et al. One-step hydrothermal coating approach to photocatalytically active oxide composites[J]. Dalton Trans, 2010, 39(26): 6043-6048.
[10] ZHAO H P, ZHANG Y F, LI G F, et al. Rhodamine B-sensitized BiOCl hierarchical nanostructure for methyl orange photodegradation[J]. RSC Adv, 2016, 6(10): 7772-7779.
[11] XIONG J Y, CHENG G, LI G F, et al. Well-crystallized square-like 2D BiOCl nanoplates: mannitol-assisted hydrothermal synthesis and improved visible-light-driven photocatalytic performance[J]. RSC Adv, 2011, 1(8): 1542-1553.
[12] MCEVOY J G, ZHANG Z S. Antimicrobial and photocatalytic disinfection mechanisms in silver-modified photocatalysts under dark and light conditions[J]. J Photochem Photobiol C-Photochem Rev, 2014, 19: 62-75.
[13] GAO Y P, WANG L, LI Z, et al. Microwave-assisted synthesis of flower-like Ag-BiOCl nanocomposite with enhanced visible-light photocatalytic activity[J]. Mater Lett, 2014, 136: 295-7.
[14] ZHANG Z, ZHOU Y, YU S, et al. Ag-BiOCl nanocomposites prepared by the oxygen vacancy induced photodeposition method with improved visible light photocatalytic activity[J]. Mater Lett, 2015, 150: 97-100.
[15] LI J, RONG K F, ZHAO H P, et al. Highly selective antibacterial activities of silver nanoparticles against Bacillus subtilis[J]. J Nanosci Nanotechnol, 2013, 13(10): 6806-6813.
[16] LI W R, XIE X B, SHI Q S, et al. Antibacterial activity and mechanism of silver nanoparticles on Escherichia coli[J]. Appl Microbiol Biot, 2010, 85(4): 1115-1122.
[17] KORA A J, Arunachalam J. Assessment of antibacterial activity of silver nanoparticles on Pseudomonas aeruginosa and its mechanism of action[J]. World J Microb Biot, 2011, 27(5): 1209-1216.
[18] LI W R, XIE X B, SHI Q S, et al. Antibacterial effect of silver nanoparticles on Staphylococcus aureus[J]. Biometals, 2011, 24(1): 135-141.
[19] SCHNEIDER J, MATSUOKA M, TAKEUCHI M, et al. Understanding TiO2photocatalysis: mechanisms and materials[J]. Chem Rev, 2014, 114(19): 9919-9986.
[20] RANJIT K T, WILLNER I, BOSSMANN S H, et al. Lanthanide oxide-doped titanium dioxide photocatalysts: Novel photocatalysts for the enhanced degradation of p-chlorophenoxyacetic acid[J]. Environ Sci Technol, 2001, 35(7): 1544-1549.
[21] KIKUCHI Y, SUNADA K, IYODA T, et al. Photocatalytic bactericidal effect of TiO2 thin films: Dynamic view of the active oxygen species responsible for the effect[J]. J Photoch Photobio A, 1997, 106(1-3): 51-56.
[22] CHANG F, XIE Y, ZHANG J, et al. Construction of exfoliated g-C3N4 nanosheets-BiOCl hybrids with enhanced photocatalytic performance[J]. RSC Adv, 2014, 4(54): 28519-28528.
[23] CHEN S, LIU Y, CHEN J. Heterogeneous electron transfer at nanoscopic electrodes: importance of electronic structures and electric double layers[J]. Chem Soc Rev, 2014, 43(15): 5372-5386.
[24] LI H, ZHANG L. Oxygen vacancy induced selective silver deposition on the {001} facets of BiOCl single-crystalline nanosheets for enhanced Cr(VI) and sodium pentachlorophenate removal under visible light[J]. Nanoscale, 2014, 6(14): 7805-7810.
Synthesis and photocatalytic disinfection efficiency of Ag/BiOCl composite
WEI Dai, LIU Xiangyu, LYU Zhong
(School of Chemical Engineering and Pharmacy, Wuhan Institute of Technology, Wuhan 430074)
The Ag/BiOCl binary nanocomposites were synthesized by depositing silver nanoparticles to BiOCl directly. The composition,morphology and optical properties of the obtained sample were characterized by X-ray diffraction, scanning electron microscopy, energy dispersive X-ray spectra and UV-vis diffuse reflectance spectra. The photocatalytic disinfection efficiency and its mechanism of Ag/BiOCl forS.aureuswere investigated. It was found that owning to the surface plasmonic resonance of silver, the light absorption band of Ag/BiOCl extended from ultraviolet to visible light area. The results of photocatalytic disinfection showed that 1×106cfu·mL-1ofS.aureuswere completely inactivated within 6 h by Ag/BiOCl under visible light irradiation, exceeding those of pure BiOCl and Ag nanoparticles. The electronic excitation, migration and consumption process of BiOCl and Ag/BiOCl were analyzed by photoluminescence spectra and electrochemical impedance spectroscopy experiments. Ag/BiOCl binary composites exhibited the lower recombination of electron-hole pair compared to that of pure BiOCl, which thereby improved photocatalytic performance. The scavenger experiments indicated that the e-, h+and H2O2were the major reactive species for bacterial inactivation. This study is the first report on photocatalytic bactericidal activity of Ag/BiOCl under visible light.
visible-light-driven photocatalytic disinfection; Ag/BiOCl; bactericidal mechanism; reactive species
2016-04-13.
国家自然科学基金项目(21371139).
1000-1190(2016)04-0559-06
Q505
A
*通讯联系人. E-mail: zhonglu@wit.edu.cn.

