水飞蓟宾防晒霜安全性评价
吴 迪 祁永华 张 宁 李艳微 张春蕾 徐艳明 李建民
黑龙江中医药大学佳木斯学院中药系,黑龙江佳木斯154007
水飞蓟宾防晒霜安全性评价
吴 迪 祁永华 张 宁 李艳微 张春蕾 徐艳明 李建民
黑龙江中医药大学佳木斯学院中药系,黑龙江佳木斯154007
目的评价水飞蓟宾防晒霜外用安全性。方法与3种市售知名品牌化妆品和阴性对照品比较,以豚鼠为试验对象,将水飞蓟宾防晒霜、3种知名品牌、阴性对照品和阳性对照品涂抹在豚鼠背部脱毛区,进行急性经皮毒性试验和皮肤变态反应试验,观察皮肤变化情况,记录动物死亡情况,并进行血象和脏器系数检测与比较,评价水飞蓟宾防晒霜外用安全性。结果水飞蓟宾防晒霜急性经皮毒性试验豚鼠无死亡和行动异常现象,血象和脏器系数检测结果与3种知名品牌和阴性对照品比较差异无统计学意义(P>0.05);皮肤变态反应试验未产生皮肤致敏现象。结论水飞蓟宾防晒霜外用安全。
水飞蓟宾;经皮毒性试验;刺激性试验;安全评价
近年来,由于国内外屡次出现的化妆品事故,其中不乏皮肤永久性损伤,让广大爱美消费者对上市或即将上市化妆品的安全性和功效性产生了质疑,化妆品新产品上市的安全性及已上市产品日常监测备受消费者关注[1-4]。经皮毒性试验和皮肤刺激性试验是化妆品安全性评价最基本的方法,可以用来评价和检测化妆品使用的可靠性[5]。水飞蓟宾防晒霜是由黑龙江中医药大学(以下简称“我校”)汇集中医名师研制而成,具有明显抗光老化、延缓衰老的作用,具有很高的市场价值,可依托我校附属企业佳木斯红杏生物技术开发有限公司生产与销售。为使这一成果给更多人带去福音,应对其安全性进行评估,做好应用准备。
1 料与方法
1.1 材料
1.1.1 试剂与动物水飞蓟宾防晒霜(自制,批号:20150601);3种市售知名品牌化妆品(以下简称“知名品牌”,购于黑龙江市化妆品商店,批号分别为20141207、20150120、20140701);脱毛膏(广州有喜化妆品有限公司,批号:20141107);2,4-二硝基氯代苯(化学纯,天津市光复精细化工研究所,批号:150102);丙酮(分析纯,天津市光复精细化工研究所,批号:140801);戊巴比妥钠(化学纯,上海哈灵生物科技有限公司,批号:20140711),用生理盐水制成体积分数2%的无菌溶液;500 U/mL肝素钠生理盐水注射液(化学药品,南京生物化学制药厂,批号:150303);豚鼠[普通级健康7周龄,雌雄各半,体重300~400 g,由长春市亿斯试验动物技术责任有限公司提供,合格证号:SCXK-(吉)2014-0002]。
1.1.2 仪器设备全自动生化分析仪(URIT-8021A,迈瑞生物医疗电子股份有限公司);全自动血细胞分析仪(Bc2600,迈瑞生物医疗电子股份有限公司);电子天平(BSA124S,德国赛多利斯)。
1.2 方法
1.2.1 实验动物分组与处理实验动物共分6组,标记为:Ⅰ、Ⅱ、Ⅲ、IV、Ⅴ、Ⅵ组,Ⅰ~IV组统称为给药组,即给水飞蓟宾防晒霜为Ⅰ组,给知名品牌Ⅰ为Ⅱ组,给知名品牌Ⅱ为Ⅲ组,给知名品牌Ⅲ为IV组,阴性对照组(生理盐水)为Ⅴ组,阳性对照组(0.1%与1%的2,4-二硝基氯代苯丙酮溶液)为Ⅵ组,所有试验动物在给药前24 h进行脱毛。
1.2.2 急性经皮毒性试验取健康豚鼠50只,雌雄各半,按照“1.2.1”项下分组,取Ⅰ~Ⅴ组,于试验前24 h去除躯干背部毛,<40 cm2,试验前记录体重。涂抹药物与阴性对照物时只设一个高剂量,即>2180mg/kg,每只试验动物用药1 g。将水飞蓟宾防晒霜、知名品牌Ⅰ~Ⅲ和生理盐水涂抹于背部脱毛区,用医用纱布和胶带覆盖固定,每只试验动物分开饲养,24 h后用温开水去除试验药物,并在第7、14天称量体重,观察受试动物是否出现异常症状和死亡,试验结束进行采血和尸检,检测主要器官生理生化指标,按照《化妆品卫生规范》中“皮肤毒性分级标准”对试验结果进行评定[6-12]。剧毒:半数致死量(LD50)<5 mg/kg;高毒:5 mg/kg<LD50<45 mg/kg;中等毒,45 mg/kg<LD50<350 mg/kg;低毒,350 mg/kg<LD50<2180 mg/kg;微毒,LD50>2180 mg/kg。
1.2.3 皮肤变态反应试验取健康豚鼠60只,按照“1.2.1”项下分组,每组10只。实验前24 h右侧背部去毛<5 m2,用蒸馏水清洗。将水飞蓟宾防晒霜0.3 g、知名品牌Ⅰ~Ⅲ、阴性对照物生理盐水0.3 mL及阳性对照物1%的2,4-二硝基氯代苯丙酮溶液0.3 mL均匀涂抹于豚鼠右侧脱毛区,覆盖两层纱布及一层硫酸纸,外部用无刺激医用胶布固定6 h,第7、14天以相同的方法重复一次。将末次诱导后14 d的豚鼠左侧脱毛<5 m2,涂抹相应的受试药物、阴性对照物及阳性对照物0.1%的2,4-二硝基氯代苯丙酮溶液,用量及外部处理与第一次相同,激发24 h和48 h观察皮肤反应并记录,判断致敏性[13-16]。

皮肤致敏强度评级标准:无致敏性,0%~8%;轻度致敏性,9%~28%;中毒致敏性,29%~64%;高度致敏性,65%~80%;极度致敏性,81%~100%。皮肤过敏反应评分标准见表1。

表1 皮肤过敏反应评分标准
1.2.4 统计学方法采用SPSS 20.0软件对试验结果进行统计学分析,两组间采用方差分析,以P<0.05为差异有统计学意义。
2 果
2.1 急性经皮毒性试验结果
各组试验动物在观察期内表现活泼,未见死亡、震颤、抽搐、流涎、腹泻、嗜睡和昏迷症状,觅食、呼吸、生理活动正常;毛色光滑,试验处皮肤未见水肿、红斑现象,评价刺激指数为“0”,刺激性强度为无刺激性。各组试验动物体重均有所增加,水飞蓟宾防晒霜组增加幅度与知名品牌组、阴性对照组比较差异无统计学意义(P>0.05),增加幅度各组别比较差异无统计学意义(P>0.05)。对各组实验动物进行尸检及病理学检查,水飞蓟宾防晒霜组试验动物的血、肝、肾功能检查结果与知名品牌组、阴性对照组比较差异无统计学意义(P>0.05),水飞蓟宾防晒霜组脏器系数与知名品牌组、阴性对照组比较差异无统计学意义(P>0.05)。试验结果提示,水飞蓟宾防晒霜与知名品牌化妆品无急性经皮毒性反应。结果见表2~4。
2.2 皮肤变态反应试验结果
按照中华人民共和国卫生部《化妆品卫生规范》有关规定对水飞蓟宾防晒霜、知名品牌及阴性对照物进行皮肤刺激反应评分和致敏强度分级评价[17]。各组试验动物中,水飞蓟宾防晒霜、知名品牌及阴性对照物均未引起豚鼠皮肤产生红斑和水肿反应,致敏率为“0”;阳性对照物2,4-二硝基氯代苯丙酮溶液有明显激发红斑和水肿反应明显,致敏率为70%,具有极强的致敏性。试验结果提示,水飞蓟宾防晒霜、知名品牌均无皮肤致敏性。结果见表5。
3 论
皮肤衰老主要分为自然老化和光老化两种形式。光老化是指皮肤暴露在紫外线(UA)下,受到的损伤逐渐积累,无规则的色素沉着,表皮角化出现不良反应,真皮弹性纤维变性以及降解产物蓄积等各种生理变化,独自或叠加在皮肤上的表现[18]。光老化主要是日光中的中波紫外线(UVB)和长波紫外线(UVA)引起的,光老化的机制主要包括两种:一种是UV照射使皮肤产生活性氧簇等自由基,使DNA受到氧化性损伤,进而影响蛋白质的正常合成而损伤皮肤;另一种是UV照射使血管周围的巨噬细胞和肥大细胞活性被激发,产生并释放细胞因子和致炎介质,激发真皮炎性反应,同时释放组织溶解酶,从而导致真皮基质成分降解,引发炎性反应,形成皮肤弹性衰退、皱纹数增加、色素沉着等[19-21]皮肤衰老表现。皮肤衰老变现为皮肤红斑和延迟性色素沉着,皮肤变粗、皱纹增多、角质增厚等。
表2 水飞蓟宾日霜、市售化妆品及阴性对照品对豚鼠急性经皮毒性试验结果
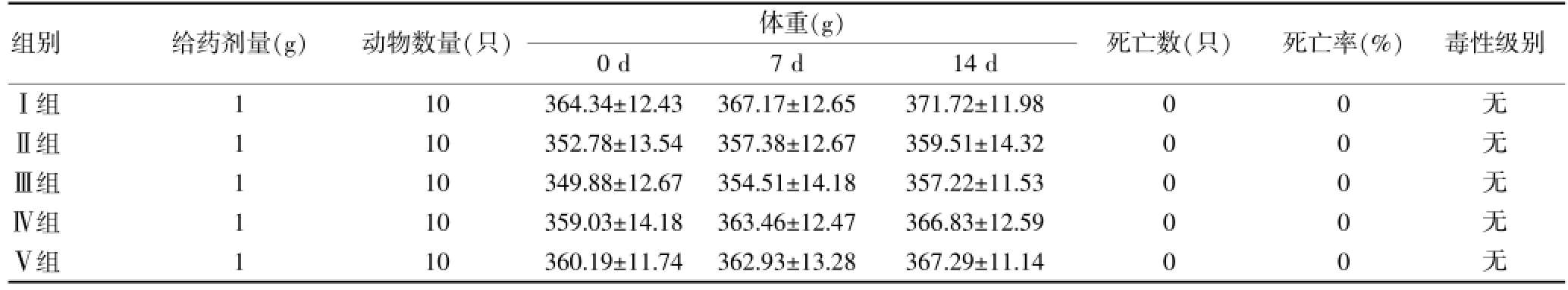
表2 水飞蓟宾日霜、市售化妆品及阴性对照品对豚鼠急性经皮毒性试验结果
组别给药剂量(g)动物数量(只)死亡数(只)死亡率(%)毒性级别体重(g)0 d 7 d 14 dⅠ组Ⅱ组Ⅲ组Ⅳ组Ⅴ组11111 10 10 10 10 10 364.34±12.43 352.78±13.54 349.88±12.67 359.03±14.18 360.19±11.74 367.17±12.65 357.38±12.67 354.51±14.18 363.46±12.47 362.93±13.28 371.72±11.98 359.51±14.32 357.22±11.53 366.83±12.59 367.29±11.14 00000 00000无无无无无
表3 豚鼠经皮毒性试验的血、肝、肾功能检查结果
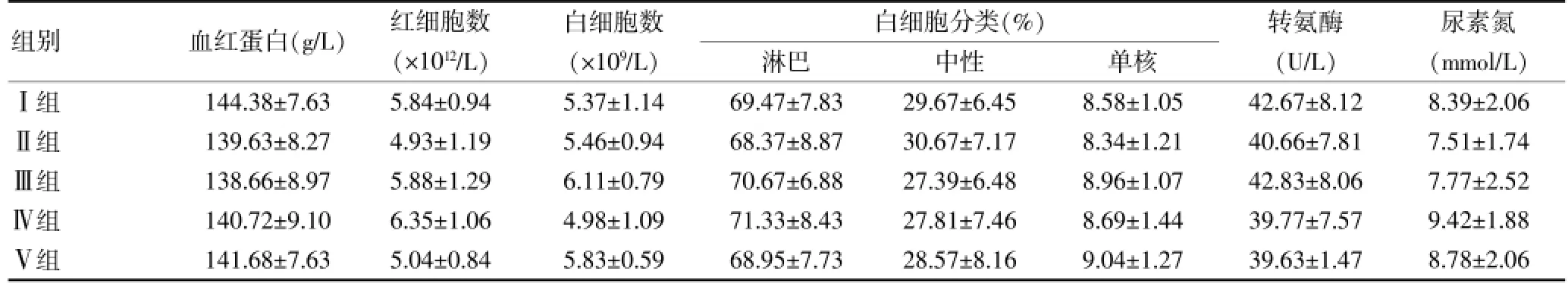
表3 豚鼠经皮毒性试验的血、肝、肾功能检查结果
组别血红蛋白(g/L)红细胞数(×1012/L)白细胞数(×109/L)白细胞分类(%)淋巴中性单核转氨酶(U/L)尿素氮(mmol/L)Ⅰ组Ⅱ组Ⅲ组Ⅳ组Ⅴ组144.38±7.63 139.63±8.27 138.66±8.97 140.72±9.10 141.68±7.63 5.84±0.94 4.93±1.19 5.88±1.29 6.35±1.06 5.04±0.84 5.37±1.14 5.46±0.94 6.11±0.79 4.98±1.09 5.83±0.59 69.47±7.83 68.37±8.87 70.67±6.88 71.33±8.43 68.95±7.73 29.67±6.45 30.67±7.17 27.39±6.48 27.81±7.46 28.57±8.16 8.58±1.05 8.34±1.21 8.96±1.07 8.69±1.44 9.04±1.27 42.67±8.12 40.66±7.81 42.83±8.06 39.77±7.57 39.63±1.47 8.39±2.06 7.51±1.74 7.77±2.52 9.42±1.88 8.78±2.06
表4 豚鼠急性经皮毒性试验主要脏器系数结果

表4 豚鼠急性经皮毒性试验主要脏器系数结果
组别心肝脾肺肾Ⅰ组Ⅱ组Ⅲ组Ⅳ组Ⅴ组0.403±0.032 0.410±0.031 0.415±0.018 0.408±0.009 0.411±0.021 3.75±0.27 3.82±0.30 3.85±0.32 3.79±0.29 3.81±0.33 0.212±0.019 0.209±0.020 0.205±0.028 0.211±0.021 0.207±0.030 0.642±0.081 0.658±0.072 0.651±0.079 0.639±0.088 0.647±0.094 0.895±0.101 0.912±0.082 0.889±0.105 0.904±0.093 0.907±0.097
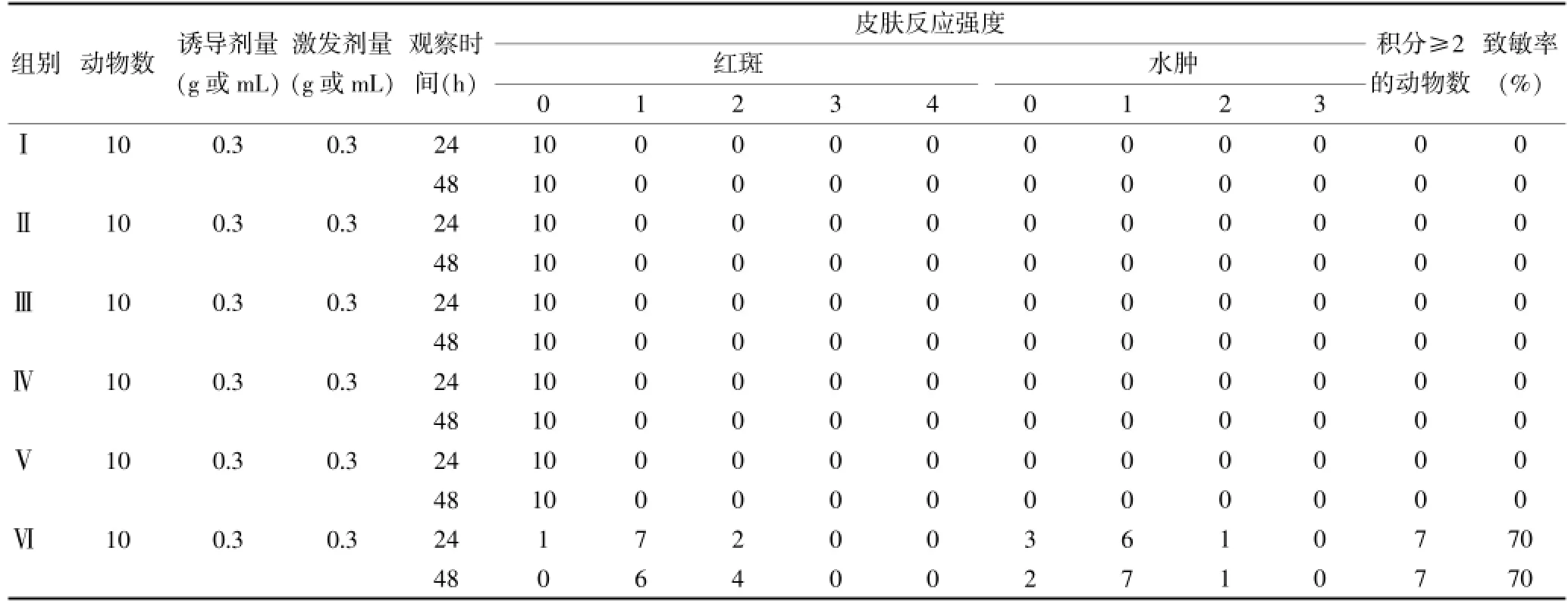
表5 水飞蓟宾防晒霜、市售化妆品对豚鼠皮肤变态反应试验结果(只)
水飞蓟宾是从菊科药用植物提取出的有效成分最多的一种水飞蓟素,其作用也最强,具有抗氧化、抗炎症、免疫调节、促进肝细胞再生等作用。水飞蓟宾的抗氧化作用是通过消除氧自由基,抑制脂质过氧化及5-脂氧酶活性来降低被损伤机体组织中丙二醛以及白三烯的含量。在此过程中,最主要的是提升超氧化歧化酶含量,抑制脂质过氧化反应,保护、维持细胞膜的流动性[22]。水飞蓟宾常用于肝脏功能的调节、抗病毒、抗肿瘤[23-24]。随着近年来研究发现[25-26],水飞蓟宾在抗皮肤光老化有较好的作用,并有广阔的开发前景。其抗光老化机制为:通过调节细胞外基质成分的合成与降解、抑制炎症因子对肝星状细胞的活化,使UV所致的角质形成(HaCaT)细胞的脂质过氧化损伤程度得以降低,控制HaCaT细胞乳酸脱氧酶活力,减少炎性因子的释放等途径以及UA所致细胞的不可逆损害,维持表皮角质形成细胞、真皮成纤维细胞正常功能。本研究将水飞蓟宾制备成化妆品,改变其给药方式,以化妆品日常护理的形式对抗UV所引起的损害,将其直接涂敷于皮肤表面,直接渗透到皮肤细胞中,维持和保护机体细胞的生理功能,开发出一款具有应用灵活、拥有无限未来的应用产品。
化妆品安全性风险评估是保证化妆品安全的重要手段,可降低避免出现安全隐患,保证产品上市安全可靠。试验方法主要包括急性经皮毒性试验、皮肤刺激性试验、眼部刺激性试验、皮肤变态反应试验和皮肤光毒性试验。安全性评价主要采用实验动物来进行,多以豚鼠、SD大鼠、裸鼠及家兔为实验动物,主要针对眼部和脱毛背部进行接触性试验,可以直观地反映被试化妆品的安全性。目前由于欧盟禁止在其范围内销售的化妆品采用动物进行安全性测试,因此出现了一些代替试验,如人工皮肤、离体细胞等[27-28],但因其重复性、关联性的局限,无法得到有力证据验证方法的可靠性,因此动物实验仍然是化妆品安全评价的主要方法。
本试验通过急性经皮试验和皮肤变态试验评估水飞蓟宾防晒霜的安全性,急性经皮毒性试验无豚鼠死亡现象,血象、各内脏主要器官功能以及脏器系数与知名品牌和阴性对照品比较,差异无统计学意义;皮肤变态试验时,与阳性对照比较,皮肤完好,无红斑和水肿现象,不会引起豚鼠皮肤过敏反应,与阴性对照和知名品牌评价结果相同[29-30]。试验结果提示,水飞蓟宾防晒霜安全性评价结果与已上市的知名品牌相同,无毒性和致敏性反应,符合《化妆品卫生规范》合格产品要求,可以放心应用。
[1]李霁云,李向阳.关注化妆品质量安全[J].日用化学品科学,2014,37(11):17-20.
[2]张亚晗.浅析化妆品与人体健康[J].学术探讨,2015,(2):295.
[3]王昊天.我国食品安全监管体系现状分析及对策[J].市场研究,2014,12(2):4.
[4]付小凤,陆贞玉,陈雯,等.2014年桂林市18份化妆品卫生监测情况分析[J].中国校医,2014,28(12):898-899.
[5]萧惠来.国际化妆品监管合作组织化妆品安全性评价原则介绍[J].香料香精化妆品,2012,8(4):54-56.
[6]郏自明,岳苗苗,郑艳华,等.兔经皮肤给药防蚴灵防护剂长期毒性实验[J].中国血吸虫病防治杂志,2015,27(1):26-31.
[7]李时恩,郭艳,周舫,等.0.5%溴鼠灵母药急性毒性、眼和皮肤刺激及皮肤致敏试验[J].毒理学杂志,2014,28(6):480-483.
[8]李烨,张晶璇,田璐,等.乙酰地蒽酚软膏在小型猪皮肤的急性毒性研究[J].中国现代药物应用,2015,9(7):265-268.
[9]吴霓,徐晓娇,江天久,等.抑食金球藻对卤虫和鼠的急性毒性及对兔皮肤和眼的刺激作用[J].水产学报,2014,38(3):444-448.
[10]朱文娟.钩藤碱对痴呆模型小白鼠学习记忆的干预作用研究[J].中国现代医生,2016,54(6):12-18.
[11]赵景云,王振宇,宋京风,等.荷芩止痒搽剂对家兔主要脏器的毒性实验研究[J].昆明医科大学学报,2015,36(11):25-30.
[12]王林,彭蔷,曾怡,等.农药百草枯的急性毒性评价[J].预防医学情报杂志,2014,30(11):898-903.
[13]路孝兵,聂奎,肖蓉,等.中药“连蒲”透皮剂的稳定性、刺激性和安全性试验[J].四川畜牧兽医,2014(2):34-36.
[14]曲婷丽,李芸,布紫云,等.一种创伤用纳米银抗菌凝胶预防创伤感染与皮肤刺激性试验研究[J].中国消毒学杂志,2014,31(4):344-348.
[15]杨沫银,宋广莹.消肿九味散、消肿九味散(无草乌)及瑞香狼毒对皮肤刺激性和致敏性的实验研究[J].中国民族医药杂志,2014(11):52-53.
[16]黄锦威,吴其当,黎丽,等.瑶药透骨消痛膏皮肤刺激性实验研究[J].亚太传统医学,2014,10(16):11-12.
[17]中华人民共和国卫生部.化妆品卫生规范[S].2007.
[18]来吉祥,何聪芬,董银卯,等.皮肤衰老机制及延缓衰老化妆品的研究进展[J].中国美容医学,2009,18(8):1208-1212.
[19]曾丽,胡晗菲,谢红炬,等.果酸治疗光老化皮肤临床疗效观察[J].中国美容医学,2015,24(13):57-59.
[20]陈默,赵亚,孙懿.杜仲预防UVB致人成纤维细胞光老化的作用及基因水平的机制探讨[J].日用化学工业,2016,46(1):36-38.
[21]王璐,杜沛,陈高敏,等.中药抗皮肤光老化实验研究十年进展[J].中医文献杂志,2015,(2):62-68.
[22]刘敏,肖颖,左爱仁,等.槲皮素、根皮素、水飞蓟宾清除自由基和抑制脂质过氧化活性研究[J].中成药,2012,34(4):753-756.
[23]李青权,周强,牛俊奇,等.水飞蓟素药理机制新进展及临床价值再探讨[J].临床肝胆病杂志,2015,31(2):315-317.
[24]王小记,郎美琦.水飞蓟宾的作用机制及临床应用[J].山西中医,2014,30(7):58-59.
[25]石玉生,吴鹏程,张艳.水飞蓟宾对UVA致人表皮角质形成细胞光老化保护作用的研究[J].中医药信息,2014,31(3):20-21.
[26]周玮婷,张壮壮,康伟,等.水飞蓟素及其脱氢衍生物的抗氧化活性研究[J].北方药学,2014,11(8):82.
[27]程树军,潘芳.体外皮肤刺激模型的生物标志研究进展[J].中国比较医学杂志,2010,20(3):65-68.
[28]李中良,伍津津,杨桂红,等.用于替代皮肤刺激试验的组织工程表皮模型的构建研究[J].中国修复重建外科杂志,2011,25:129-132.
[29]张宏伟.化妆品的毒理学安全性评价概况[J].环境与健康杂志,2008,25(10):927.
[30]张继恩,莫云杰,张永容,等.重组溶葡萄球菌酶的刺激性和皮肤变态反应试验[J].实验动物比较医学,2008,28(4):255-258.
Safety evaluation of Silybin Sunscreen
WU Di QIYonghua ZHANGNing LIYanwei ZHANGChunlei XU Yanming LIJianmin
Department of Traditional Chinese Medicine,Jiamusi College,Heilongjiang University of Chinese Medicine,Heilongjiang Province,Jiamusi 154007,China
Objective To evaluate the external use security of Silybin Sunscreen.M ethods Compared with three kinds of famous brand cosmetics and negative reference,cavy was experiment subject,cavy's hair removal back area was smeared silybin screen,three kinds of famous brand cosmetics,negative reference and positive reference,acute dermal toxicity test and skin allergic reaction experiments were conducted,skin change phenomenon was observed,animal dead phenomenon was recorded,blood picture and viscera coefficient test were conducted and compared in order to evaluate the external use security of silybin sunscreen.Results In Silybin sunscreen acute dermal toxicity test,therewas no sign for cavy's death and abnormal phenomenon;there was no significant difference for blood picture and viscera coefficient test and three kinds of famous brand cosmetics,negative reference and positive reference(P>0.05).There was no skin sensitization phenomenon in skin allergic reaction test.Conclusion The external use of silybin sunscreen is safe.
Silybin;Dermal toxicity test;Irritation test;Safety evaluation
R965.3
A
1673-7210(2016)05(c)-0135-04
2016-01-01本文编辑:赵鲁枫)
黑龙江省应用技术研究与开发计划项目(PC13S15)。
吴迪(1982.1-),男,硕士;研究方向:药物缓释控释及靶向研究。
李建民(1964.10-),男,硕士,教授,硕士生导师;研究方向:中药药效物质基础研究。

