羊耳蒜属植物化学成分及药理作用的研究进展
郑叶子 张智宽 马宏文 卜亚恒 黄 帅
西南交通大学生命科学与工程学院,四川成都610031
羊耳蒜属植物化学成分及药理作用的研究进展
郑叶子 张智宽 马宏文 卜亚恒 黄 帅▲
西南交通大学生命科学与工程学院,四川成都610031
通过查阅国内外相关文献,进行归纳、分析,对兰科羊耳蒜属植物的化学成分和药理作用进行综述,结果显示该属植物主要化学成分为生物碱、黄酮及其苷类、甾醇及其苷类,酚酸及其苷类。现代药理研究表明,羊耳蒜属植物具有抗炎、止血、抗菌、抗氧化等多种生物活性。羊耳蒜属植物的现代研究尽管取得了一定的进展,但仍存在一些问题,需要进一步探讨。
羊耳蒜属;植物资源;化学成分;药理作用
羊耳蒜属(Liparis L.C.Rich)为兰科植物,我国有45种,<有19种产自台湾,其余以西南为最多[1]。其中多种植物如羊耳蒜、见血青、小花羊耳蒜、大花羊耳蒜等在历代本草中都有记载,民间应用时多以全草入药,具有清热解毒、止血活性、消肿止痛,怯风除湿之功效,通常用于治疗肺热咯血、肠风下血、疮疡肿毒、毒蛇咬伤、跌打损伤等症[2]。该属植物的主要化学成分为生物碱、酚酸、黄酮及苷类、萜类、甾醇类等。本文在查阅相关国内外文献基础之上,对该属植物的植物资源、主要化学成分、药理作用方面进行综述,以期为将来羊耳蒜属植物的开发利用提供参考。
1 学成分
1.1 挥发油
刘杰书等[3-4]采用气相-质谱联用法对羊耳蒜乙醇和乙醚提取物中的挥发性成分进行分析,鉴定的化合物主要是生物碱、脂肪酸及酚性物质。胡少南等[5]将见血青干燥全草粉碎后用70%乙醇回流提取,得到的浸膏依次用极性分段,采用气相-质谱联用分析鉴定,主要为有机酸类、有机醇类、酚类、醛酮类以及酯类化合物、含氮的有机化合物和2个萜类化合物。
1.2 生物碱类化合物
羊耳蒜属植物中生物碱的结构类型主要为吡咯里西啶类,目前从中共发现19种。见表1。化合物结构见图1。

表1 羊耳蒜属植物的生物碱成分
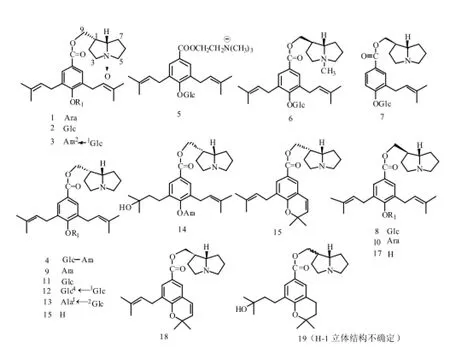
图1 羊耳蒜属植物的生物碱类成分结构
1.3 黄酮及其苷类
目前该属植物中的黄酮类化合物结构式、名称和植物来源见图2、表2。

表2 羊耳蒜属植物的黄酮类成分
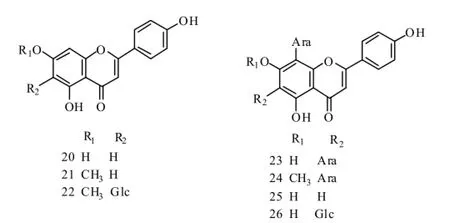
图2 羊耳蒜属植物的黄酮类成分结构
1.4 酚酸及其苷类
目前,从羊耳蒜属植物中分离出24种酚酸及其苷类,化合物名称及来源见表3、图3。

表3 羊耳蒜属植物的酚酸类成分

图3 羊耳蒜属植物的酚酸类成分结构
1.5 甾醇及其苷
目前,从该属植物中分离到了3种甾醇及其苷类化合物,见表4、图4。

表4 羊耳蒜属植物的甾醇类及其苷成分

图4 羊耳蒜属植物的甾醇类成分结构
1.6 香豆素类
目前,从该属植物中分离到了4个香豆素类化合物,名称和植物来源见表5、图5。
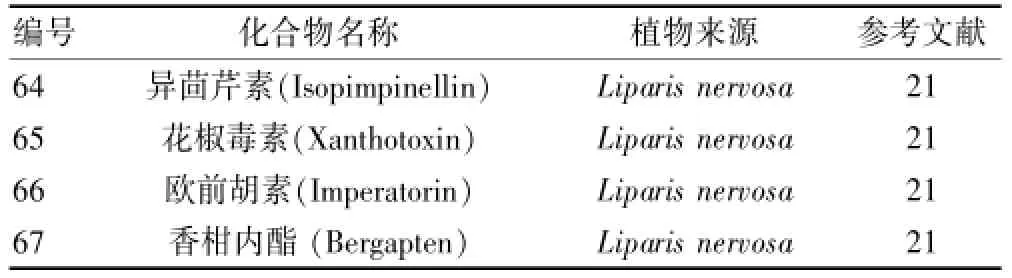
表5 羊耳蒜属植物的香豆素类成分
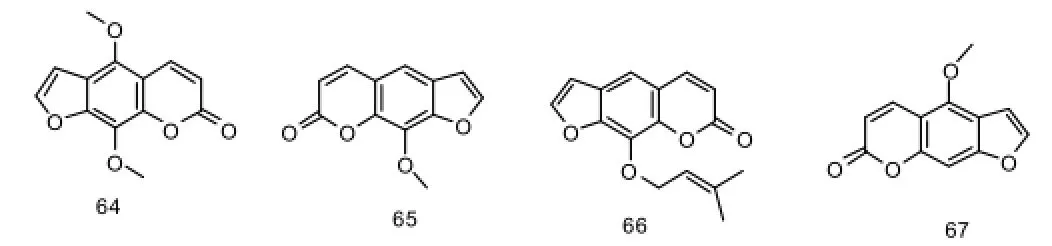
图5 羊耳蒜属植物的香豆素成分结构
1.7 芪类
目前,从该属植物中分离到了5个芪类化合物,化合物名称和植物来源见表6、图6。

表6 羊耳蒜属植物的芪类成分
1.8 其他
其他类成分及来源见表7。
2 理作用
2.1 抗炎作用
黄帅等[9]见血青中吡咯里西啶类生物碱抑制LPS诱导的RAW264.7巨噬细胞产生NO作用。Piao等[6]发现见血青中酚苷类化合物也具有抑制LPS诱导的RAW264.7巨噬细胞产生NO作用。

图6 羊耳蒜属植物的芪类成分结构
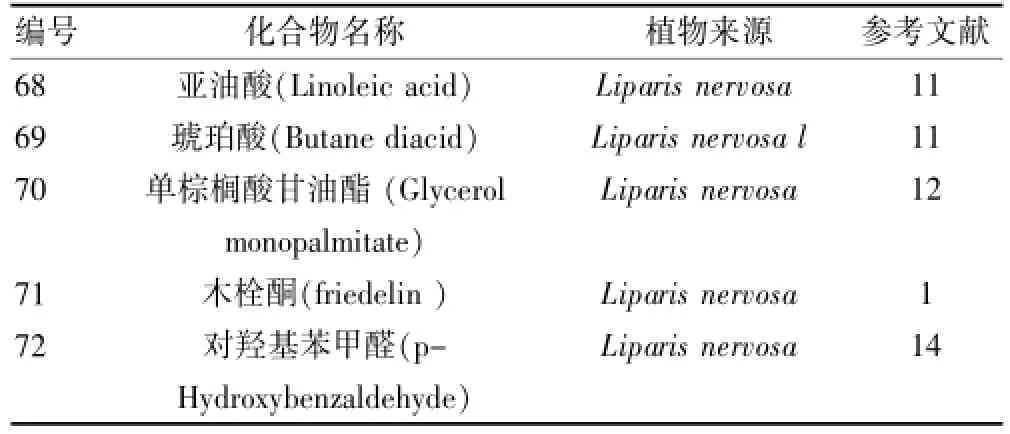
表7 羊耳蒜属植物的其他类成分
2.2 止血作用
宋琴等[22]对见血青醇提物乙醚、乙酸乙酯、正丁醇及水部位,分别检测大鼠的凝血活性,结果显示见血青具有一定的止血作用。赵颖等[23]研究制备了见血青的水提取物及不同极性部位提取物,考察其止血活性,推断二氯甲烷部位是见血青止血作用的有效部位。Piao等[6]发现见血青中3个新的吡咯里西啶类生物碱具有一定的凝血作用。
2.3 抗氧化作用
曾春涵等[24]研究见血青总皂苷体外抗氧化活性,结果表明见血青皂苷具有一定的抗氧化作用。董艳芳等[25-26]测定见血青总生物碱和多糖清除自由基能力,结果表明见血青总生物碱和多糖均具有较强的抗氧化作用。
2.4 抑菌活性
董艳芳等[26]采用滤纸片法,以12种细菌和4种真菌为试供菌种,对见血青中生物碱进行体外抑菌活性实验结果表明,见血青总生物碱对16种微生物的生长均有很强的抑制性。
3 语与展望
羊耳蒜属植物资源丰富,其中多种植物药用历史悠久。目前,仅对香花羊耳蒜、见血青、尾唇羊耳蒜、玉簪羊耳蒜、细茎羊耳蒜进行了化学成分及生物活性研究,都还不全面。因此,需要对羊耳蒜属的化学成分及生物活性进行系统的研究,结合临床功效阐明其药效物质基础及作用机制,为该属植物的质量控制、临床应用及合理开发提供重要的科学依据。
[1]中国科学院中国植物志编委会.中国植物志(第18卷第2分册)[M].北京:科学出版社,1999:54,73-74.
[2]华应熊,刘诗发,杨振球,等.中华本草[M].上海:上海科学技术出社,1999,24:734-737.
[3]刘杰书,李泳锋,刘金龙.国际濒危植物羊耳蒜中化学成分的气相色谱-质谱联用分析[J].中国民族医药杂志,2009,15(6):50-51.
[4]刘杰书,李泳锋,刘金龙.羊耳蒜中化学成分的气相色谱-质谱联用分析比较[J].时珍国医国药,2010,21(3):529-530.
[5]胡少南,赵颖,郑一敏,等.见血青的气相色谱-质谱联用分析[J].重庆理工大学学报:自然科学版,2014,28(2):54-58.
[6]Jiang P,Liu H,Xu X,et al.Three new alkaloids and three new phenolic glycosides from Liparis odorata[J].Fitoterapia,2015,107:63-68.
[7]Nishikawa K,Hirata Y.Chemotaxonomical alkaloid studies I.Structure ofnervosine[J].Tetrahedron Let,1967,27:2591-2596.
[8]Nishikawa K,Miyamura M,Hirata Y.Chemotaxonomical alkaloid studies structures of Liparis alkaloids[J].Tetrahedron,1969,25:2723-2741.
[9]Huang S,Zhou X,Wang C,et al.Pyrrolizidine alkaloids from Liparis nervosawith inhibitory activities against LPS-induced NO production in RAW 264.7 macrophages[J]. Phytochemistry,2013,93:154-161.
[10]Huang S,Zhong DX,Shan LH,etal.Threenew pyrrolizidine alkaloids derivatives from Liparis nervosa[J].Chinese Chemical Letters,2016.
[11]赵颖,胡少南,王昌华,等.见血青化学成分研究[J].中草药,2013,44(21):2955-2959.
[12]赵颖,胡少南,王昌华,等.兰科药用植物见血青乙酸乙酯部位化学成分研究[J].中国实验方剂学杂志,2013,19(22):111-113.
[13]SlapetováT,Smejkal K,Innocenti G,et al.Glycosylated nervogenic acid derivatives from Liparis condylobulbon(Reichb.f.)leaves[J].Carbohydrate research,2009,344(13):1770-1774.
[14]黄帅.四种药用植物的化学成分及生物活性研究[D].成都:西南交通大学,2013:13-56.
[15]Huang S,Zhou X L,Wang CJ,et al.New nervogenic acid derivatives from Liparis nervosa[J].Planta medica,2013,79(3-4):281-287.
[16]Huang S,Pan MF,Zhou XL,et al.Five new nervogenic acid derivatives from Liparis nervosa[J].Chinese Chemical Letters,2013,24(8):734-736.
[17]Li B,Liu H,Zhang D,et al.Three new bioactive phenolic glycosides from Liparis odorata[J].Natural product research,2014,28(8):522-529.
[18]Xie Y,Yu S,Liu H,et al.Anti-inflammatory phenolic glycosides from Liparis odorata[J].Medicinal Chemistry Research,2015,24(1):356-361.
[19]Kuo WL,Huang YL,Shen CC,et al.Prenylated benzoic acids and phenanthrenes from Liparis nakaharai[J]. Journal of the Chinese Chemical Society,2007,54(5):1359-1362.
[20]Song Q,Shou Q,Goun X,etal.A new nervogenic acid glycosidewith pro-coagulantactivity from Liparisnervosa[J]. Natural product communications,2013,8(8):1115-1116.
[21]刘量,殷启蒙,李佳,等.见血清石油醚部位化学成分研究[J].世界科学技术—中医药现代化,2013,15(7):1552-1556.
[22]宋琴,刘芳,苟小军,等.见血清有效部位的止血作用及机制研究[J].中药材,2014,37(10):1849-1852.
[23]赵颖,胡少南,郑一敏,等.见血青提取物止血作用的实验研究[J].中国药房,2013,24(31):2884-2886.
[24]曾春菡,刘小波,曹弈璘,等.见血青总皂苷体外溶血与抗氧化活性研究[J].四川大学学报:自然科学版,2015,52(15):1141-1144.
[25]董艳芳,陈法志,郭彩霞,等.见血青多糖的抑菌活性与抗氧化性[J],湖北农业科学,2012,51(12):2570-2573.
[26]董艳芳,李伟阳,《睿超,等.见血青总生物碱的抑菌活性和抗氧化性研究[J].四川大学学报:自然科学版,2010,47(3),669-673.
Advances on chem ical constituents and bioactivities of genus lipairs
ZHENG Yezi ZHANG Zhikuan MA Hongwen BU Yaheng HUANG Shuai▲
School of Life Science and Engineering,Southwest Jiaotong University,Sichuan Province,Chengdu 610031,China
By reviewing and analyzing domestic and foreign researches on chemical constituents and bioactivities of Liparis L.C.Rich.Alkaloids,flavonoids and glycosides,sterols,phenolic acid and other compounds have been isolated from Liparis L.C.Rich.Modern pharmacological researches indicates that it posses the efficacy of anti-inflammatory,hemostasis,antioxidant and antibiosis.Although much progress has been made in modern research of Liparis L.C. Rich,there are still some problems for the further exploration.
Liparis Rich;Plant resources;Chemical constituents;Pharmacological effects
R284;R285.5
A
1673-7210(2016)05(c)-0044-04
2016-01-22本文编辑:赵鲁枫)
国家自然科学基金资助项目(81402803);国家大学生科研训练计划项目(201510613065)。
▲通讯作者

