钒酸铜纳米棒的合成及其光催化特性*
方 燕,程燕丽,林 楠,王蒙蒙,吴其辉,刘 鑫,裴立宅
(安徽工业大学 材料科学与工程学院,安徽 马鞍山 243002)
钒酸铜纳米棒的合成及其光催化特性*
方 燕,程燕丽,林 楠,王蒙蒙,吴其辉,刘 鑫,裴立宅
(安徽工业大学 材料科学与工程学院,安徽 马鞍山243002)
以聚乙烯吡咯烷酮(PVP)作为表面活性剂,通过水热过程制备出了钒酸铜纳米棒。X-射线衍射(XRD)分析表明钒酸铜纳米棒由单斜Cu5V2O10晶相构成,扫描电子显微镜(SEM)观察表明纳米棒的直径和长度分别为50~300nm和3μm。PVP浓度、水热温度和保温时间对于钒酸铜纳米棒的形成及尺寸具有重要作用,采用PVP辅助的水热核化与晶体生长过程解释了钒酸铜纳米棒的形成与生长。采用龙胆紫(GV)评估了太阳光照射下钒酸铜纳米棒的光催化活性。随着光照时间、钒酸铜纳米棒含量的增加,GV溶液的浓度明显降低。采用10mg钒酸铜纳米棒作为光催化剂,在太阳光照射4h后,龙胆紫溶液可以完全脱色降解。在太阳光照射下,钒酸铜纳米棒对于龙胆紫具有良好的光催化降解活性。
钒酸铜纳米棒;水热合成;扫描电子显微镜;光催化;龙胆紫
1 引言
在水处理领域中去除污水中的有机染料等有机污染物引起了人们的研究兴趣[1]。龙胆紫(GV)是一种典型的有机染料,被广泛应用于造纸工业和织物染色等工业领域[2]。然而,由于GV在生物体内的积累容易影响环境,污水中的GV会引起污水的有色化及影响人体健康[3]。因此,发展高效率、廉价的染料废水处理方法具有较重要的研究意义。
吸附技术由于具有高的有机污染物去除效率及稳定性,所以被用于去除污水中的GV等有机污染物。然而,吸附技术不能降解有机污染物,只是将有机污染物转移至吸附剂上。光催化技术属于一种经济及环境友好的方法去除有机污染物。以二氧化钛作为催化剂,在紫外(UV)光及氧存在下可以高效光催化去除GV[2]。然而,二氧化钛属于宽禁带半导体,只能吸收紫外光[4]。因此,探索可见光光催化的新型光催化剂来处理有机污染物具有较重要的研究意义。
钒酸盐纳米材料由于禁带宽度窄[5],被认为在光催化处理有机污染物方面具有广泛的应用前景。在这些钒酸盐纳米材料中,钒酸铜纳米棒作为一种窄禁带的半导体材料,可以吸收可见光,引起了人们的广泛关注。然而,钒酸铜的制备通常要求高温[6-7],所以发展简单的制备方法来合成特殊结构的钒酸铜纳米棒具有重要的研究意义。水热方法是合成低维纳米材料的有效方法[8-9],本文以聚乙烯吡咯烷酮(PVP)作为表面活性剂,通过简单的水热过程合成了钒酸铜纳米棒。根据基于不同水热条件下所得产物的结果,分析了钒酸铜纳米棒的形成过程。采用PVP辅助的水热核化与晶体生长过程解释了钒酸铜纳米棒的形成过程。通过太阳光光催化降解GV分析了钒酸铜纳米棒的光催化特性,详细研究了光照时间、钒酸铜纳米棒的含量及GV浓度对光催化降解GV的影响。
2 实验
钒酸钠(AR级,纯度≥99.9%)、乙酸铜(AR级,纯度≥99.9%)及PVP(AR级)分别购买于中国阿拉丁试剂有限公司和国药试剂有限公司。所有原料使用前没有进一步纯化处理。合成过程中,首先将钒酸钠、乙酸铜及一定浓度的PVP溶解于60mL蒸馏水中,其中乙酸铜与钒酸钠的摩尔比为1∶2,于是将混合溶液放置于体积100mL的反应釜内。将反应釜加热至80~180℃、保温0.5~24h,随后将反应釜自然冷却至室温。将釜内黄色的絮状沉积物用蒸馏水和乙醇清洗数次并过滤,在空气中于60℃干燥,最后获得了黄色的钒酸铜纳米棒。
采用Bruker AXS D8 X-射线衍射(XRD)仪分析了样品的结构,Cu靶Kα辐射,波长0.15406nm,扫描范围为20°~80°,扫描速率是0.05°/s。将样品在蒸馏水内通过超声波处理约15min,然后滴于尺寸约1cm×1cm清洁的铜片表面,在空气中自然凉干。采用日本JEOL公司的Nova nanoSEM FEI 430型高分辨场发射扫描电子显微镜分析样品的形貌。
通过太阳光照射下光催化降解GV评估了钒酸铜纳米棒的光催化活性。GV为分析纯,购于中国国药试剂有限公司。将2.5~20mg钒酸铜纳米棒放置于10mL浓度为2.5~20mgL-1的GV溶液中,实施了光催化反应。在太阳光照射前,将含有钒酸铜纳米棒和GV的混合物放于暗处20min,持续搅拌以保持GV分子在钒酸铜纳米棒表面吸附平衡。所有实验均在空气内于室温下实施。将处理后的GV溶液通过离心过程与钒酸铜纳米棒分离,然后采用UV756紫外—可见光分光光度计(上海佑科有限责任公司)分析了样品的紫外—可见光谱。通过测量GV溶液的紫外—可见光吸收光谱在581nm的强度确定了GV溶液的初始浓度(C0)和处理后的GV溶液浓度(C)。C/C0比率是被用于评估了钒酸铜纳米棒的光催化活性。
3 结果与讨论
图1所示为以乙酸铜、钒酸钠和3wt.%的PVP作为原料,180℃、保温24h的水热条件下所得产物的XRD衍射图谱。经检索(JCPDS卡,PDF卡号:33-0504)可知,样品的所有XRD衍射峰对应于单斜Cu5V2O10晶相。产物中没有观察到其它杂质相,说明产物中只有单斜Cu5V2O10晶相的钒酸铜形成。Hu等[10]报道了以V(IV)O(acac)2和硝酸铜作为原料,PVP作为表面活性剂,通过简单的软化学方法合成了单斜ε-Cu0.95V2O5中空微球。以乙酸铜、五氧化二钒和双氧水作为原料,通过水热过程合成了四方CuV2O6晶相的钒酸铜纳米带[11]。本文所得钒酸铜纳米棒的单斜Cu5V2O10晶相与以不同钒源和铜源作为原料,通过水热过程所得钒酸铜纳米带及中空微球的晶相是明显不同的。

图1 采用3wt.%的PVP作为表面活性剂,180℃,保温24h所得钒酸铜纳米棒的XRD衍射图谱
图2所示为以3wt.%的PVP作为表面活性剂,180℃、保温24h的水热条件下所得产物的SEM图像,所得产物完全由棒状形貌构成,图2(a)。更高倍数的SEM图像显示所得钒酸铜纳米棒的长度和直径分别为3μm和50~300nm,图2(b)。本文所得钒酸铜纳米棒的形貌与采用不同原料及相似的水热过程所得纳米棒[19-20]的形貌是相似的。

图2 钒酸铜纳米棒不同放大倍数的SEM图像
水热合成参数,例如PVP浓度、水热温度和保温时间对于钒酸铜产物的形貌的形成有着重要影响。相似于PVP对于不同成分的纳米棒的形成作用[12-13],PVP对于钒酸铜纳米棒的形成有着重要影响。图3所示为以不同浓度的PVP作为表面活性剂,于180℃、保温24h所得产物SEM图像。从图中可以看到当实验中没有加入PVP时,所得产物完全由微米级和亚微米级尺寸的颗粒构成如图3(a)。当PVP浓度为0.1wt.%时,所得产物由微棒和圆形颗粒构成如图3(b),钒酸铜微棒的直径和长度分别为150~750nm和3μm,圆形颗粒被认为是形成钒酸铜纳米棒的晶核,这也被随后的保温时间实验结果所证实。随着PVP浓度增加到1wt.%,产物中颗粒的数量明显减少如图3(c),微棒的直径减少到100~400nm,长度为3μm。随着PVP浓度增加到3wt.%,产物中的颗粒消失(见图2),钒酸铜纳米棒的直径为50~300nm。随着PVP浓度增加到5wt.%,纳米棒的直径进一步减少到了40~150nm如图3(d)。进一步增加PVP的用量,例如PVP浓度增加到10wt.%,所得纳米棒的直径进一步降低至30~100nm。以上结果表明PVP浓度对于钒酸铜纳米棒形成的影响结果显示PVP对于钒酸铜纳米棒的形成具有本质作用,随着PVP浓度的增加,钒酸铜纳米棒的直径明显减少,而纳米棒的长度相似,长度为3μm。

图3 添加不同浓度的PVP,180℃,保温24h所得产物的SEM图像
图4所示为以3wt.% PVP作为表面活性剂,于180℃、保温不同时间所得产物的SEM图像。当保温时间为0.5h时,所得产物由纳米棒及一些圆形及无规则颗粒构成如图4(a),纳米棒被认为是由于颗粒形成的。随着保温时间增加到6h,颗粒数量明显减少如图4(b)。随着保温时间增加到12h,产物全部由钒酸铜纳米棒构成如图4(c)。此结果表明保温时间对于钒酸铜纳米棒的形成具有重要作用。图5所示为以3wt.% PVP作为表面活性剂,于不同温度、保温24h所得产物的SEM图像。80℃、保温24h所得产物主要由尺寸小于100nm的颗粒构成如图5(a),然而,从SEM图像中也观察到了少量长度1.5μm的纳米棒。随着水热温度增加到120℃,所得产物主要由直径和长度分别为30~120nm和1.5μm的纳米棒构成如图5(b)。此结果进一步表明钒酸铜纳米棒起源于直径小于100nm的颗粒,水热温度对于钒酸铜纳米棒的形成具有本质作用。
根据水热生长条件对于钒酸铜纳米棒形成的分析结果,说明PVP对于钒酸铜纳米棒的形成具有本质作用。有报道表明PVP可以诱导一维纳米材料的形成[14-15]。因此,提出了PVP辅助核化与晶体生长过程解释了钒酸铜纳米棒的形成与生长。在初始的水热反应阶段,通过乙酸铜与钒酸钠的反应形成了钒酸铜。钒酸铜在水热溶液中达到超饱和状态后,从水热溶液中析出形成了钒酸铜纳米团簇。钒酸铜纳米团簇可以作为形成纳米棒的晶核,这也被水热温度和保温时间对钒酸铜纳米棒形成的影响结果所证实。PVP吸附于钒酸铜晶核的表面,诱导了钒酸铜纳米棒的形成。随着水热温度和保温时间的增加,最终形成了钒酸铜纳米棒。

图4 采用浓度为3wt.%的PVP,于180℃,保温不同时间所得产物的SEM图像

图5 不同水热温度,保温24h所得产物的SEM图像
图6所示为以3wt.% PVP作为表面活性剂,于180℃、保温24h所得钒酸铜纳米棒的固体紫外—可见光(UV-vis)漫反射光谱。通过固体UV-vis漫反射光谱可以计算钒酸铜纳米棒的禁带宽度,其吸收边为550nm,对应钒酸铜纳米棒的禁带宽度为2.25eV。Nemade等[16]报道了氧化铜纳米颗粒的禁带宽度为4.2eV。与禁带宽度为4.2eV的氧化铜纳米颗粒相比较,钒酸铜纳米棒的吸收边明显出现了红移,增强了其在可见光区域的光吸收能力。钒酸铜纳米棒的吸收边为550nm,表明钒酸铜纳米棒在可见光区域具有良好的可见光吸收能力。

图6 钒酸铜纳米棒的固体UV-vis漫反射光谱
GV是一种重要的有机染料,难于被降解。因此,GV通常被用于作为一种模型污染物来分析光催化剂的光催化性能。作为对比,在未采用可见光、仅以钒酸铜纳米棒作为光催化剂,以及仅采用可见光照射,未添加钒酸铜纳米棒的两种光催化条件下分析了光催化降解GV的光催化特性。图7(a)所示为以钒酸铜纳米棒作为光催化剂,经太阳光照射不同时间后GV溶液的紫外—可见光(UV-vis)吸收光谱。GV溶液的初始浓度和钒酸铜纳米棒的含量分别为10mgL-1和10mg/10mL GV溶液。随着太阳光照射时间的增加,UV-vis吸收光谱在581nm位置处的吸收峰的强度明显减少。经太阳光照射4h后,GV浓度减少到了0mgL-1,GV溶液的颜色由紫色转变为了无色。图7(b)所示为在不同的实验条件下,经不同的光照时间前后GV溶液的浓度变化比率。GV溶液浓度变化比率(C/Co)与光照时间曲线(图7(b))显示GV溶液未经可见光照射,钒酸铜纳米棒对于GV溶液没有光催化能力。另外,仅经可见光照射,而未添加钒酸铜纳米棒,GV溶液也不能被降解。经太阳光照射4h后,GV溶液可以被完全降解。Saquib等[2]报道了以二氧化钛作为光催化剂,采用125W汞灯,在紫外光照射GV也能够被降解。不同于紫外光照射光催化降解GV,钒酸铜纳米棒在太阳光照射下,对于GV具有良好的光催化活性。
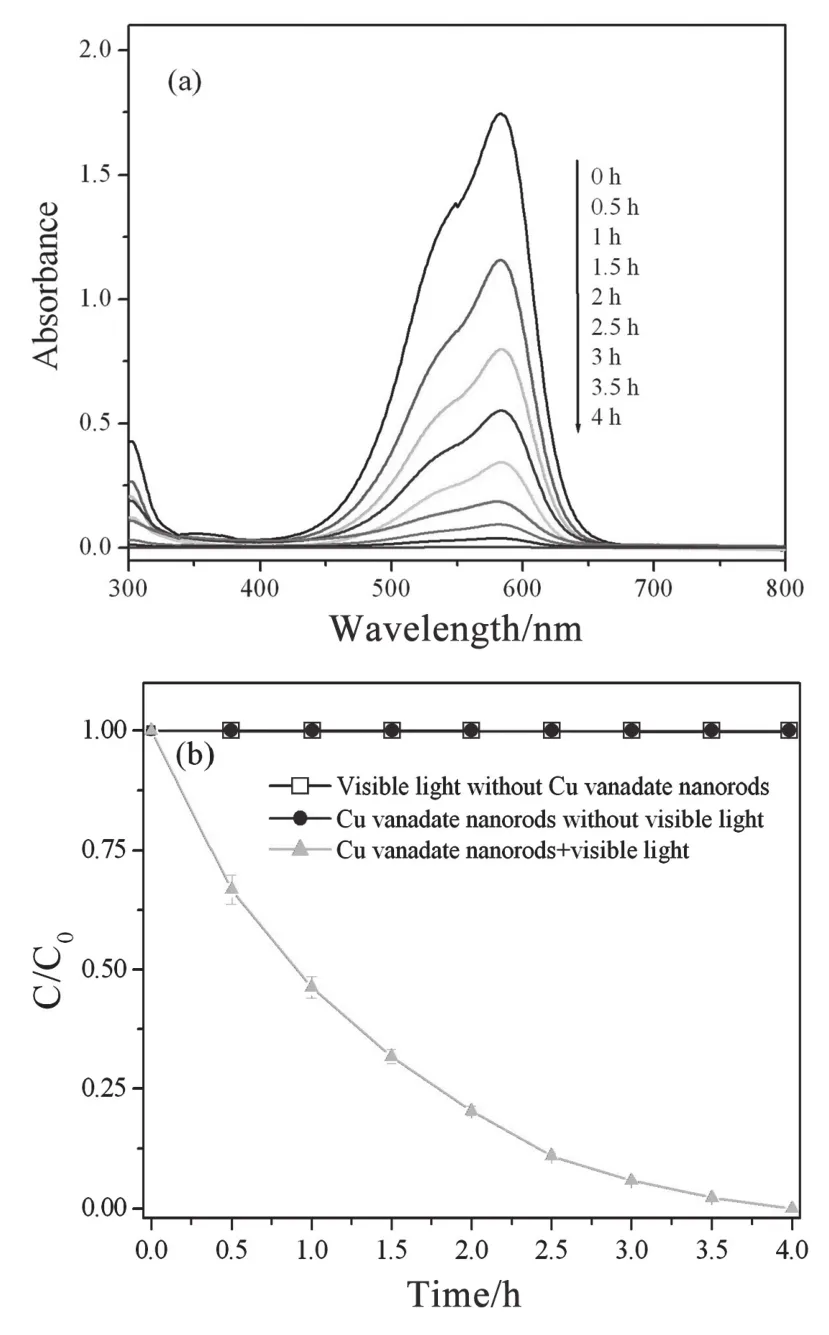
图7 在10mLGV溶液内经太阳光照射不同时间后GV溶液的UV-vis光谱(a)及GV降解比率与光照时间的关系曲线(b)。钒酸铜纳米棒用量,10mg;GV浓度,10mgL-1
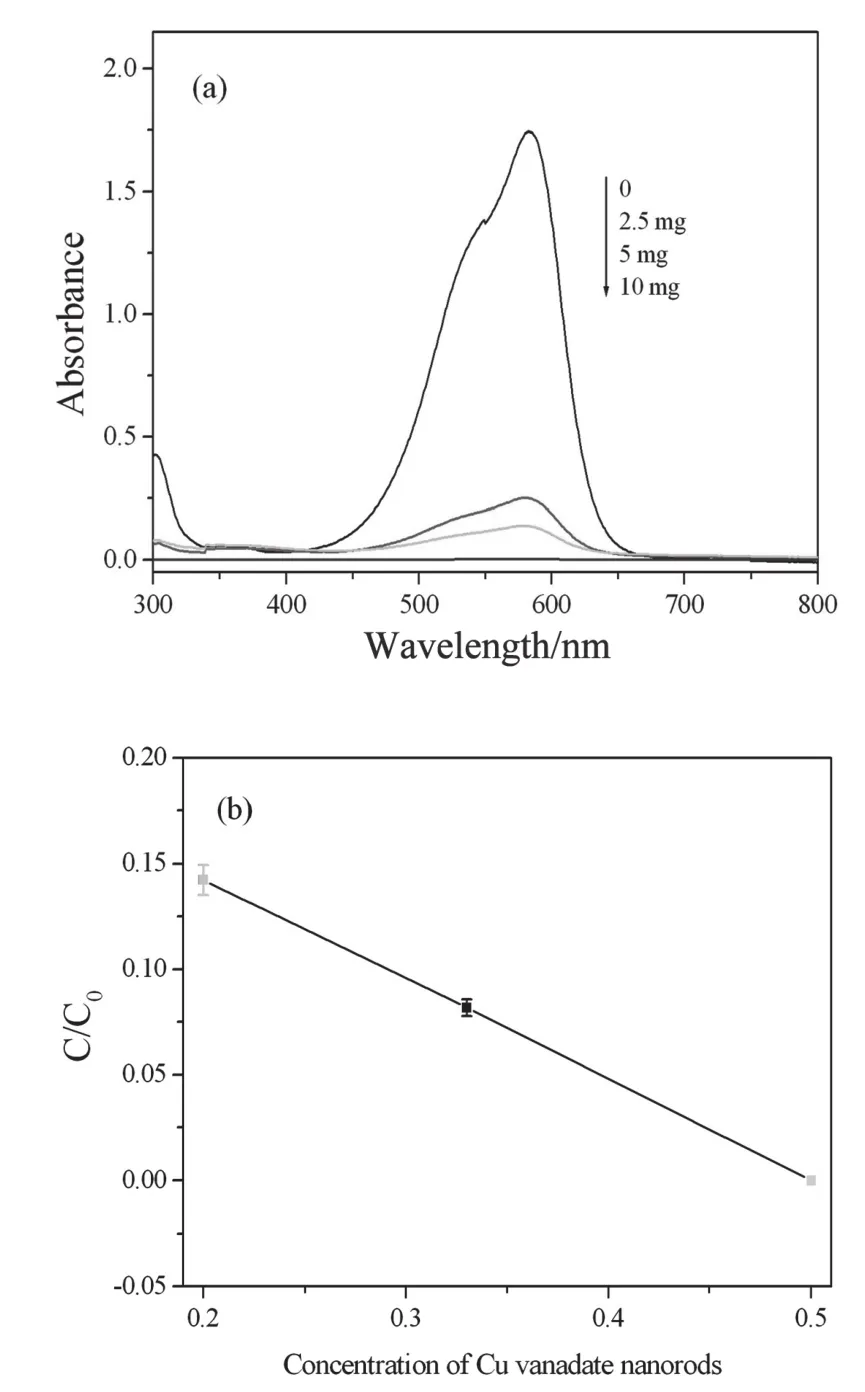
图8 在10mLGV溶液中,以不同用量的钒酸铜纳米棒光催化处理GV溶液前后的UV-vis吸收光谱(a)和GV浓度变化比率(b)。光照时间4h;GV浓度,10mgL-1
光催化剂的光催化活性与光催化剂的禁带宽度、形貌和表面积密切相关,其光催化活性随着禁带宽度的降低和表面积的增加而增加[17-18]。钒酸铜纳米棒的禁带宽度小,可以吸收可见光。当钒酸铜纳米棒吸收高于2.25eV的能量时,光生电子即可从价态转移至导带。水由价态中带正电荷的空穴所氧化,当电荷载流子扩散至钒酸铜纳米棒的表面时,GV分子吸收了太阳光的能量,处于激发态,带正电荷[19],带正电荷的GV分子与氢氧基离子反应形成了·OH自由基,·OH自由基氧化了GV分子,使得GV溶液由紫色转变为了无色,从而在太阳光照射下GV被降解。
钒酸铜纳米棒的用量对于光催化降解GV分子具有一定的作用,所以分析了不同钒酸铜纳米棒用量对光催化降解GV的影响,太阳光照射时间和GV浓度分别为4h和10mgL-1。图8所示为采用不同用量的钒酸铜纳米棒,光催化降解后GV溶液的UV-vis吸收光谱及光催化处理前后GV浓度变化比率。随着钒酸铜纳米棒用量的增加,GV溶液的UV-vis吸收峰的强度明显降低,见图8(a)。随着钒酸铜纳米棒的用量减少至20wt.%(2.5mg/10mL GV溶液),GV降解比率减少到了85.77%,见图8(b)。
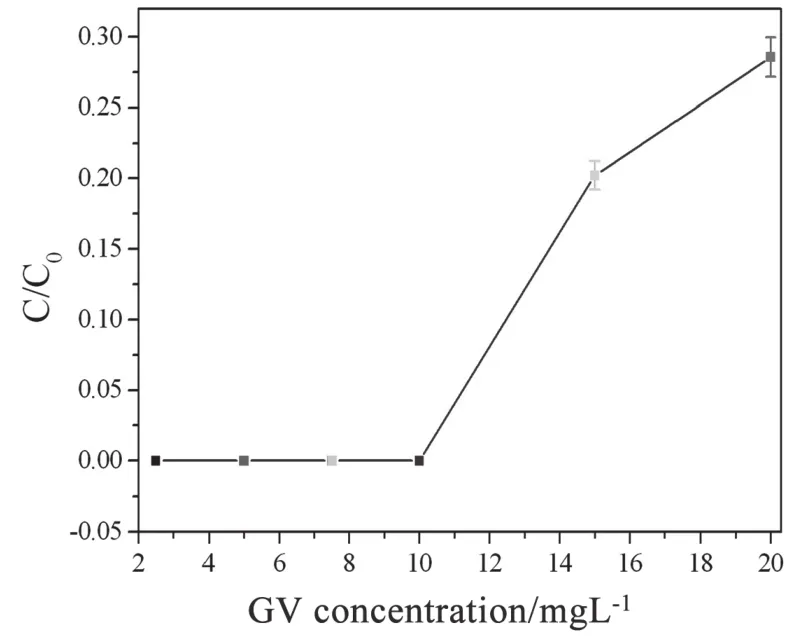
图9 光催化处理前后GV溶液的浓度变化比率与GV浓度的关系曲线。钒酸铜纳米棒的用量,10mg,光照时间,4h
GV浓度对于钒酸铜纳米棒光催化降解GV也具有重要作用。图9所示为GV浓度范围为2.5到20mgL-1时,GV溶液处理前后的GV浓度变化比率与GV浓度的关系曲线。从图中可以看出GV浓度低于10mgL-1时,GV可以被完全降解。然而,随着GV溶液浓度的增加,GV溶液的降解率明显降低。随着GV溶液的浓度增加到20mgL-1,GV降解率减少到了71.42%,这可能时由于GV分子的高浓度使得光穿透溶液的能力降低,能够参与光催化反应的光子数减少引起的[20-21]。
4 结论
以PVP作为表面活性剂,通过简单的水热过程制备出了单斜Cu5V2O10晶相的钒酸铜纳米棒。钒酸铜纳米棒的直径和长度分别为50~300nm和3μm。PVP浓度、水热温度和保温时间对于钒酸铜纳米棒的形成与尺寸具有重要影响。随着PVP浓度从0.5wt.%增加到5wt.%,钒酸铜纳米棒的直径由150~750nm减少到了40~150nm。采用PVP辅助的核化与晶体生长过程解释了钒酸铜纳米棒的形成与生长。固体紫外—可见漫反射光谱分析表明钒酸铜纳米棒的禁带宽度为2.25eV,可以吸收可见光。随着光照时间、钒酸铜纳米棒的用量的增加,GV溶液的浓度明显降低。以10mg钒酸铜纳米棒作为光催化剂,在太阳光照射4h后,10mgL-1的GV溶液可以被完全降解。钒酸铜纳米棒在可见光光催化降解有机污染物方面具有良好的应用潜力。
[1]杨硕, 裴立宅, 余意, 等. 三元铜铁硫去除铬酸和罗丹明B的研究 [J].铜业工程, 2015(3):23-26.
[2]Saquib M, Muneer M. TiO2-mediated photocatalytic degradation of triphenylmethane dye (gentian violet), in aqueous suspensions [J]. Dyes Pigments, 2003, 56:37-49.
[3]He H A, Yang S G, Yu K, et al. Microwave induced catalytic degradation of crystal violet in nano-nickel dioxide suspensions [J]. J Hazard Mater,2010, 173:393-400.
[4]Xu S H, Shangguan W F, Yuan J, et al. Photocatalytic properties of bismuth titanate Bi12TiO20 prepared by co-precipitation processing [J]. Mater Sci Eng B, 2007, 137:108-111.
[5]Pei L Z, Xie Y K, Pei Y Q, et al.l Hydrothermal synthesis of Mn vanadate nanosheets and visible-light photocatalytic performance for the degradation of methyl blue [J]. Mater Res Bull, 2013, 48(3):2 557-2 565.
[6]Cao X Y, Xie J G, Zhan H, et al. Synthesis of CuV2O6 as a cathode material for rechargeable lithium batteries from V2O5 gel [J]. Mater Chem Phys, 2006, 98(1):71-75.
[7]Wei Y J, Nam K W, Chen G, et al. Synthesis and structural properties of stoichiometric and oxygen deficient CuV2O6 prepared via coprecipitation method [J]. Solid State Ionics, 2005, 176(29-30):2 243-2 249.
[8]魏天, 马健, 余素春, 等. 钒酸钙纳米棒的生长调控及其电化学特性[J]. 铜业工程, 2014(6):38-43.
[9]Pei L Z, Yang Y, Pei Y Q, et al. Cd2Ge2O6 nanowires grown by a simple hydrothermal route [J]. Cryst Res Technol, 2011, 46(5):480-484.
[10]Hu W, Du X C, Wu Y M, et al. Novel ε-Cu0.95V2O5hollow microspheres and α-CuV2O6nanograins: Facile synthesis and application in lithiumion batteries [J]. J Power Sources, 2013, 237: 112-118.
[11]Li G C, Wu W Z, Zhang C Q, et al. Synthesis of ultra-long single crystalline CuV2O6 nanobelts [J]. Mater Lett, 2010, 64(7):820-823.
[12]Pei L Z, Wei T, Lin N, et al. Synthesis of zinc oxide and titanium dioxide composite nanorods and their photocatalytic properties [J]. Adv Compos Lett, 2016, 25(1):9-15.
[13]李晓倩, 王永生, 梁婷, 等. 锌掺杂锗酸锶纳米棒及其光催化特性[J]. 铜业工程, 2015(6):39-43.
[14]Du X W, Chu Y, Xing S X, et al. Hydrothermal synthesis of calcium hydroxyapatite nanorods in the presence of PVP [J]. J Mater Sci, 2009,44:6 273-6 279.
[15] Reddy C V S, Jr E H W, Sr S A W, et al. Characterization of MoO3nanorods for lithium battery using PVP as a surfactant [J]. J Solid State Electrochem, 2009, 13: 1945-1949.
[16]Nemade K R, Waghuley S A. Study of optical band gap of CuO using Fermi's Golden Rule [J]. J Phys:Conf Ser, 2012, 365: 012018.
[17]Pei L Z, Wang S, Lin N, et al. Vanadium doping of stronium germanate and their visible photocatalytic properties [J]. RSC Adv, 2014, 4(89):48 144-48 149.
[18]Chine M K, Sediri F, Gharbi N. Solvothermal synthesis of V4O9 flakelike morphology and its photocatalytic application in the degradation of methylene blue [J]. Mater Res Bull, 2012, 47:3 422-3 426.
[19]Ameta J, Kumar A, Ameta R, et al. Synthesis and characterization of CeFeO3photocatalyst used in photocatalytic bleaching of gentian violet[J]. J Iran Chem Soc, 2009, 6:293-299.
[20]Liu T H, Li Y H, Du Q J, et al. Adsorption of methylene blue from aqueous solution by graphene [J]. Colloids Surf B, 2012, 90(2):197-203.
[21]Pei L Z, Lin N, Wei T, et al. Synthesis of manganese vanadate nanobelts and their visible light photocatalytic activity for methylene blue[J]. J Experi Nanosci, 2016, 11(3):197-214.
Synthesis of Copper Vanadate Nanorods and Photocatalytic Properties
FANG Yan, CHENG Yan-Li, LIN Nan, WANG Meng-meng, WU Qi-hui, LIU Xin, PEI Li-zhai
(School of Materials Science and Engineering, Anhui University of Technology, Ma'anshan 243002, Anhui, China)
copper vanadate nanorods were synthesized via the hydrothermal process by using polymer polyvinyl pyrrolidone (PVP)as the surfactant. X-ray diffraction (XRD) showed that the nanorods were composed of monoclinic Cu5V2O10 phase. Scanning electron microscopy (SEM) observation showed that the diameter and length of the nanorods were 50-300 nm and 3 μm, respectively. PVP concentration, hydrothermal temperature and duration time play essential roles in the formation and sizes of the Cu vanadate nanorods. PVP-assisted nucleation and crystalline growth process was proposed to explain the formation of the Cu vanadate nanorods. Gentian violet (GV) was used to evaluate the photocatalytic activites of the Cu vanadate nanorods under solar light. GV concentration was decreased obviously with the increase of the irradiation time and content of the Cu vanadate nanorods. GV solution with the concentration of 10 mgL-1 can be totally degraded under solar light irradiation for 4 h using 10 mg Cu vanadate nanorods. The Cu vanadate nanorods have good photocatalytic activities for the degradation of GV under solar light.
copper vanadate nanorods;hydrothermal synthesis;scanning electron microscopy;photocatalysis;gentian violet
TN305.3
A
1009-3842(2016)04-0031-06
2016-05-26
安徽工业大学大学生创新创业训练计划SRTP项目(2015015Z);安徽省科技厅自然科学基金资助项目(1208085QE98)
方燕(1994-),女,安徽寿县人,工学学士,主要从事低维纳米材料的研究。E-mail: 1033296434@qq.com

