调强放疗治疗原发性肝癌合并脾功能亢进1例
杨梅健, 赵建国
(内蒙古医科大学附属医院放疗科, 呼和浩特 010000; *通讯作者,E-mail:suli1012@163.com)
调强放疗治疗原发性肝癌合并脾功能亢进1例
杨梅健, 赵建国*
(内蒙古医科大学附属医院放疗科, 呼和浩特010000;*通讯作者,E-mail:suli1012@163.com)
原发性肝癌;脾亢;调强放疗
脾功能亢进是肝硬化和肝癌的常见并发症之一,可导致脾脏增大及外周血细胞减少, 从而引发贫血、感染、出血等并发症。目前临床上治疗脾亢的主要方式有手术切除、介入治疗和放射治疗。手术切除和介入治疗因有较高并发症而存在局限性,而放射治疗作为一种无创治疗手段,因靶区分布更为均匀、对病灶治疗更为精准而应用于临床。因此,我们使用调强放疗治疗1例原发性肝癌合并脾功能亢进,现报道如下。
1 临床资料
1.1病例资料
患者,男,52岁,因确诊原发性肝癌1年余于2016年4月12日入院。患者于2014年4月因烫伤就诊当地医院化验发现HBsAg阳性,给予抗病毒、保肝等对症治疗。2014年7月就诊于解放军302医院,于2014年7月2日在CT引导下穿刺,病理回报:(肝脏穿刺1、2、3、4)穿刺组织内见肝细胞癌,高-中分化。2014年7月4日和8月14日患者于解放军302医院行肝动脉造影及栓塞术治疗及口服索拉非尼抗肿瘤治疗。于第3次介入治疗时发现胸壁转移,考虑穿刺种植转移,遂于内蒙古自治区医院行胸壁种植转移病灶放射治疗,拟照射剂量36 Gy(3 Gy×12次),因放疗过程中出现血小板(PLT 24×109/L)过低暂停放疗,故实际照射剂量30 Gy(3 Gy×10次)。2016年1月患者再次于解放军302医院行介入治疗,后因胸壁疼痛无缓解就诊我科。患者入院后血常规(2016年4月13日)提示PLT 22×109/L,WBC 2.58×109/L,Hb 140 g/L,凝血功能正常,因血小板、白细胞过低而暂不能行胸壁转移灶放疗,同时影像资料显示患者脾脏增大,考虑原发性肝癌合并脾功能亢进(hypersplenism,以下简称脾亢),患者目前明确诊断为:①原发性肝癌(T2N0M1Ⅳ期) 脾功能亢进,左胸壁种植转移;②乙型肝炎肝硬化失代偿期。经全科讨论及与患者及其家属沟通决定先行脾区调强放疗缓解脾亢。具体放疗方案如下:患者体膜固定后, 在CT模拟机下定位, 将CT定位影像资料传入治疗计划系统后勾画靶区,GTV为全脾,PGTV为GTV外扩5 mm,PTV为PGTV外扩5 mm,靶区由两位主任医师审核后交由物理师做计划,计划完成后由两位主任医师和一位物理师共同审核计划,审核后将计划传至加速器进行治疗。脾脏放疗剂量为:PGTV 30 Gy(2 Gy×15次),常规分割,同时给予肝脏、胃、小肠等危及器官保护。患者于2016年4月26日开始放疗, 5月28日放疗结束,放疗期间密切监测患者血象。
1.2治疗效果
1.2.1脾脏大小的变化在放疗结束后10 d患者脾脏大小已有略微缩小(见图1)。
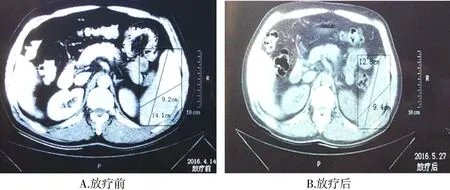
图1 放疗前后脾脏大小变化
1.2.2外周血象的变化患者于内蒙古自治区医院放疗期间,2015年9月23日血象提示PLT为23×109/L,于当日输血小板2 U,9月24日PLT为35×109/L,9月25日PLT下降到30×109/L,PLT仅上升1 d后就开始下降。在本次放疗中,由表1可以看出,虽然放疗期间WBC、PLT出现了下降,但总体是处于上升的趋势。2016年5月24日患者出现低烧,WBC升高,考虑是肠道炎症造成低热,使用头孢呋辛钠、昂丹司琼静点3 d后,患者体温正常,无明显胃肠道不适。患者在脾区放疗结束后因继续行原发灶及转移灶区域的放疗,WBC受抑制,但PLT仍处于上升趋势,可见放疗对抑制脾亢还具有后续疗效。
1.2.3不良反应患者在脾脏放疗期间无明显不适,无发热、放射部位疼痛,在放疗结束后出现轻度消化道症状伴低烧,经药物止吐处理后症状消失。
表1放疗期间外周血象变化
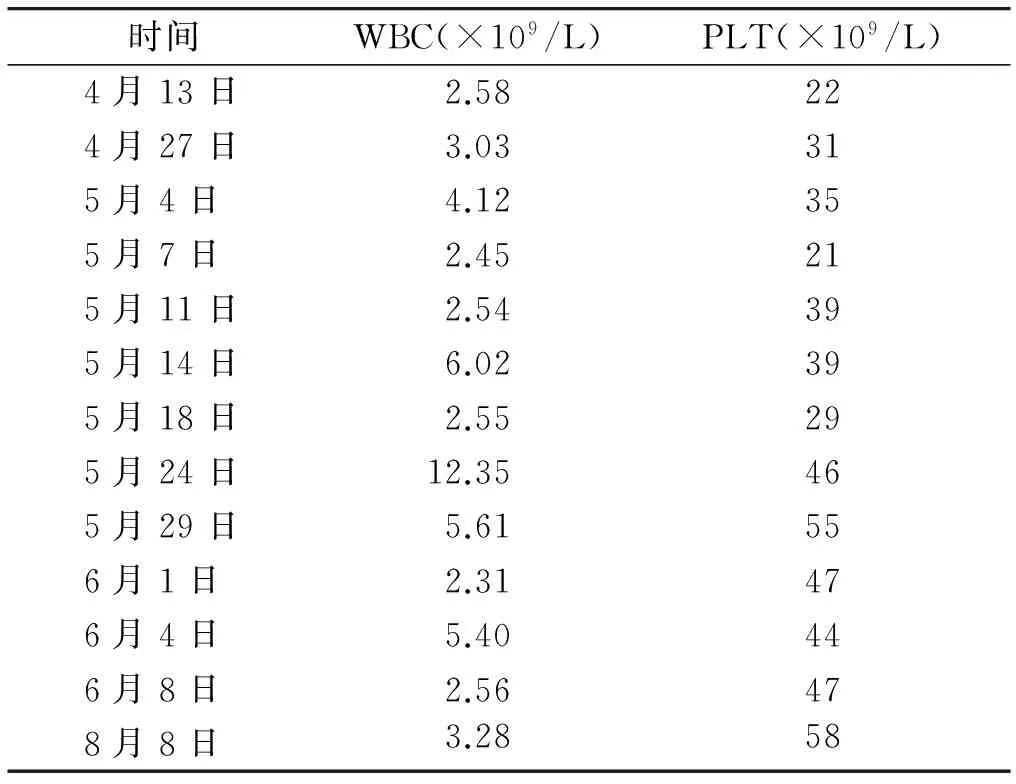
时间WBC(×109/L)PLT(×109/L)4月13日2.58224月27日3.03315月4日4.12355月7日2.45215月11日2.54395月14日6.02395月18日2.55295月24日12.35465月29日5.61556月1日2.31476月4日5.40446月8日2.56478月8日3.2858
2 讨论
肝硬化失代偿期和肝癌患者门静脉高压症的典型症状为脾脏增大,同时血细胞过度损伤,晚期可发展为脾亢[1], 主要表现为白细胞、血小板和红细胞计数减少。目前临床上治疗脾亢的主要方式有手术切除、介入治疗和放射治疗。手术是治疗脾亢的传统手段,通过将脾脏切除而减轻巨脾造成的多种或单种血细胞降低、上腹不适等症状,达到防止出血和止血的目的[2],手术是一种有创性的治疗手段,其适应证和术中风险都存在局限性[3],同时脾脏作为人体的一个重要器官,当被切除后人体免疫力会下降,进而增加感染风险[3],有报道显示脾脏切除术后门静脉血栓的发生率高达29%-35%[4];尽管现在介入治疗脾亢被认为是一种既安全又可取得良好效果的治疗手段[5],但其具有较高的术后并发症[6],Zhu等[7]的研究表明介入术后几乎所有的患者都出现了凝固性坏死吸收导致的发热、穿刺部位皮肤的损伤、脾区疼痛等并发症,部分患者还会出现胸腔积液;目前调强放疗(intensity modulated radiation therapy,IMRT)是一种精确放疗手段,在本例中,患者采用的就是IMRT,因脾脏对放射线敏感,同时,IMRT通过增加子野数可最大程度地减少计划的靶区体积,这也可达到减少周围正常组织和器官射线受量的目的。刘丽霞等[8]和王丽娜等[2]的研究显示,放疗结束4周后脾脏大小会有明显缩小。王丽娜等[2]的一项研究中表明放射治疗脾亢和介入治疗脾亢可以取得相同效果(P>0.05),但放疗不同于介入,它可以显著减少发热和疼痛(P<0.05),Kriz等[9]和Shrimali等[10]也得到相同结论。刘丽霞等[8]的一项35例脾亢患者行三维适形放疗疗效观察的研究中,期间也有4例患者出现了血象下降的现象。在本例中,患者也仅照射了30 Gy的剂量便达到了不错的效果。患者于2015-05-20~2016-06-08于我科行原发灶及转移灶的放疗。目前,该患者的放疗全部结束,我们也对患者进行了随访,患者放疗结束后一般状态佳,无明显胃肠道反应,转移灶部位疼痛也明显缓解,2016年8月8日血象提示PLT上升至58×109/L,WBC也处于上升状态。可见,本例中使用调强放疗治疗原发性肝癌合并脾亢达到了不错效果。我们还会继续密切监测患者血象,进一步评估调强放疗治疗原发性肝癌合并脾功能亢进的疗效。
[1]Xu RH,Gao W,Wang C,etal.RETRACTED ARTICLE:Systematic evaluation of percutaneous radiofrequency ablation versus percutaneous ethanol injection for the treatment of small hepatocellular carcinoma:a meta-analysis[J].Eur J Med Res,2014,19(9):76-81.
[2]王丽娜,何津祥,靳炘,等.放射治疗与介入治疗肝源性脾亢75例[J].世界华人消化杂志,2012,(24):2296-2301.
[3]Di Sabatino A,Carsetti R,Corazza GR.Post-splenectomy and hyposplenic states[J].Lancet,2011,378(9785):86-97.
[4]Ushitora Y,Tashiro H,Takahashi S,etal.Splenectomy in chronic hepatic disorders:portal vein thrombosis and improvement of liver function[J].Dig Surg,2011,28(1):9-14.
[5]Gerstein HC,Bosch J,Dagenais GR,etal.Basal insulin and cardiovascular and other outcomes in dysglycemia[J].N Engl J Med,2012,367(4):319-328.
[6]Abdella HM,Abd-El-Moez AT,El-Maaty MEA,etal.Role of partial splenic arterial embolization for hypersplenism in patients with liver cirrhosis and thrombocytopenia[J].Indian J Gastroenterol,2010,29(2):59-61.
[7]Zhu K,Meng X,Qian J,etal.Partial splenic embolization for hypersplenism in cirrhosis:a long-term outcome in 62 patients[J].Dig Liver Dis,2009,41(6):411-416.
[8]刘丽霞,崔德广,牛智祥,等.脾功能亢进三维适形放疗34例疗效观察[J].临床医学,2013,33(10):18-21.
[9]Kriz J,Micke O,Bruns F,etal.Radiotherapy of splenomegaly:a palliative treatment option for a benign phenomenon in malignant diseases[J].Strahlenther Onkol,2011,187(4):221-224.
[10]Shrimali RK,Correa PD,O’Rourke N.Low-dose palliative splenic irradiation in haematolymphoid malignancy[J].J Med Imaging Radiat Oncol,2008,52(3):297-302.
杨梅健,女,1990-10生,在读硕士,住院医师,E-mail:ymeijianhb@163.com
2016-07-26
R735.7
B
1007-6611(2016)10-0950-03DOI:10.13753/j.issn.1007-6611.2016.10.017

