双核水杨醛缩乙二胺合铜的合成、结构和性能研究
桑雅丽,潘淑娟,张耀华,张 潇,刘少博,尹 亮
(赤峰学院 化学化工学院,内蒙古 赤峰 024000)
双核水杨醛缩乙二胺合铜的合成、结构和性能研究
桑雅丽,潘淑娟,张耀华,张潇,刘少博,尹亮
(赤峰学院化学化工学院,内蒙古赤峰024000)
以水杨醛缩乙二胺为配体,与醋酸铜在甲醇溶液中反应,制备了一个双核水杨醛缩乙二胺合铜配合物,通过测定熔点和红外光谱对其进行了初步表征,进一步通过X-ray测试了配合物的晶体结构,并对其热性能和荧光性能进行了研究.
水杨醛缩乙二胺;铜配合物;晶体结构;热性能;荧光性能
1 前言
Schiff碱化合物通常是由醛或酮与含有氨基(-NH2)的化合物发生缩合反应而得到的含有-C=N基团的化合物,由于—C=N上的N原子能够提供一对孤对电子,Schiff碱化合物能与金属离子发生配位作用,形成结构新颖、性能优异的单核、多核配合物[1-3].这些配合物在生物化学、医药、催化、电化学等方面表现出许多新颖的性能[4-6],可作为光致变色材料、热致变色材料、非线性光学材料等.因此,长期以来,Schiff碱化合物一直是科研工作者们的研究热点[7-10].
本文通过实验制备了水杨醛缩乙二胺,并以其为配体,在甲醇溶剂中合成了双核水杨醛缩乙二胺合铜配合物,并对配合物进行了X-ray单晶结构解析,同时对配合物的热性能和荧光性能进行了研究.
2 实验部分
2.1仪器及试剂
TJ270-30A型红外光谱仪(KBr压片)(美国Nicolet公司);Bruker Smart-1000 CCD单晶衍射仪(德国Bruker公司);热重分析仪TG(德国耐驰仪器制造有限公司);样品的固态荧光光谱用日立F-7000型荧光光谱仪在室温下测定,激发狭缝和发射狭缝均为2.5nm,扫描速率1200nm/min,扫描电压700V.所用试剂均为市售分析纯,使用前未进一步纯化.
2.2水杨醛缩乙二胺的合成
反应原理
乙二胺中带有孤电子对的氮原子进攻水杨醛羰基基团上带有正电荷的碳原子,脱去两分子水,完成亲核加成反应.

图1 水杨醛缩乙二胺的合成路线
实验合成
在分析天平上称取1.202g(0.02moL)乙二胺溶于10mL无水乙醇中,将该溶液滴加到10mL含有4.8848g(0.04moL)水杨醛的乙醇溶液中,搅拌,得到亮黄色固体.减压过滤,用无水乙醇洗涤.干燥,得到亮黄色片状固体,产量3.1526g,产率58.82%.熔点:120~122℃.
2.3水杨醛缩乙二胺铜配合物的合成
实验合成
将水杨醛缩乙二胺(2.7mg,0.1mmoL)的甲醇溶液(5mL)加入到Cu(Ac)2(2.0mg,0.1 mmoL)的甲醇溶液(4mL)中,再加入5滴水.将得到的绿色混合溶液搅拌均匀过滤,滤液静置于暗处,两星期后有墨绿色片状单晶生成,该晶体在空气中稳定.熔点:140~143℃.
2.4红外光谱
采用KBr压片法在400~4000cm-1范围内测得水杨醛缩乙二胺配体和配合物的红外光谱,配合物的红外图谱与配体相比,某些吸收峰发生了明显的位移,强度也有较大的改变,初步说明金属盐与配体发生了反应.

图2 水杨醛缩乙二胺的红外光谱图

图3 水杨醛缩乙二胺合铜的红外光谱图
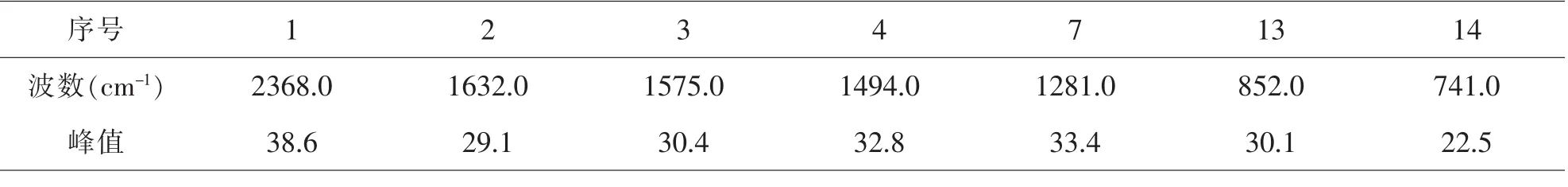
表1 水杨醛缩乙二胺的红外光谱数据

表2 水杨醛缩乙二胺合铜的红外光谱数据
表1、表2分别为水杨醛缩乙二胺与水杨醛缩乙二胺合铜的红外光谱数据.如图2、图3所示,配体水杨醛缩乙二胺在1632cm-1处的吸收峰可指派为v(C=N)伸缩振动峰,表明Schiff碱的形成,1281cm-1处为苯环的伸缩振动峰.形成铜双核配合物后,苯环的伸缩振动向高波数移动168cm-1,表明羟基参与了配位.v(C=N)的伸缩振动向高波数移动,表明C=N的N原子参与配位,从而证实了配合物的生成.
3 X射线衍射实验与晶体结构
选取大小为0.22mm×0.20mm×0.20mm的配合物单晶,293(2)K下在Bruker Smart-1000CCD衍射仪上,用石墨单色器单色化的Mo Ka射线(λ=0.071073Å),在2.05<θ<26.37°范围内(h:-31~33,k:-8~6,l:-18~18),以ω扫描方式,共收集到独立的衍射点9702个,其中I>2σ(I)的点为2789个.结构分析表明,该配合物晶体属单斜晶系,C2/c空间群.晶胞参数a=2.66433(8)Å,b=0.69832(71)Å,c=1.4714221(21)Å,V=2714.25Å3,Dc=1.765g/cm3,Z=4,F(000)=1352,μ=1.61mm-1.衍射数据经Lp因子校正后,采用直接法初步解出各原子位置坐标,继而经差值Fourier合成及最小二乘法修正和各向异性温度因子校正,结构参数190个.最终偏离因子R1=0.0406,wR2=0.0885.所有的计算均使用SHELXL-97程序包[11].
3.1水杨醛缩乙二胺合铜的晶体结构
配合物的有关键长及键角数据列于表3和表4,水杨醛缩乙二胺合铜(Ⅱ)的单晶结构见图4,晶胞堆积见图5.

图4 水杨醛缩乙二胺合铜的单晶结构
如图4所示,水杨醛缩乙二胺合铜(Ⅱ)为双核铜配合物,每个配合物结构单元中包含有两个水杨醛缩乙二胺配体分子和两个铜原子,其中,每个水杨醛缩乙二胺配体分子中的两个N原子和两个O原子均参与配位.中心铜原子除了与其中一个配体分子中的两个N原子和两个O原子结合外,还与另一个配体分子中的O原子结合,通过Cu-O-Cu氧桥键将两个水杨醛缩乙二胺配体连接起来,形成了以两个铜原子为中心的双核铜配合物.在这个配合物中,两个铜原子均为五配位,其中,Cu(1)-O(2)与Cu(1A)-O(2A)的键长相等,均为1.9450Å,Cu(1)-O(2A)和Cu(1A)-O(2)的键长也相等,均为2.4142Å,因此,两个铜原子和两个桥联氧原子O(2)、O(2A)构成平行四边形框架,O(2)-Cu(1)-O(2A)的键角为86.33°,Cu(1)-O(2)-Cu(1A)的键角为93.67°.此外,Cu(1)-N(2)的键长为1.9508Å,Cu(1)-N(1)的键长为1.9591Å,Cu(1)-O(1)的键长为1.9085Å,对比数据发现:中心原子Cu(1)与Cu(1A)的相关键长和键角均对应相等,可见该双核铜配合物是完全对称的.
从图5可以看出,沿b轴方向,在水杨醛缩乙二胺合铜配合物的固态结构中,配合物结构单元通过分子之间的弱相互作用形成一维链状结构.

表3 水杨醛缩乙二胺合铜配合物的部分键角(°)

表4 水杨醛缩乙二胺合铜配合物的主要键长(Å)
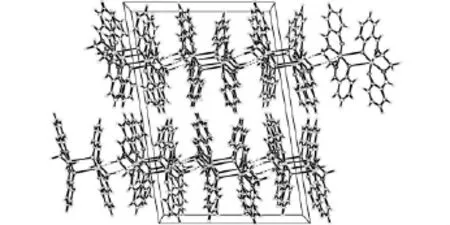
图5 水杨醛缩乙二胺合铜的晶体堆积图
3.2热重分析
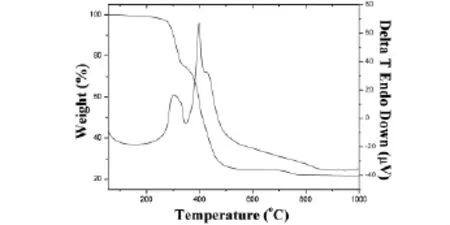
图6 水杨醛缩乙二胺合铜的差热热重图

图7 水杨醛缩乙二胺配体及配合物的荧光图
水杨醛缩乙二胺合铜配合物的TG曲线表现出失重过程(图6):第一步失重从278.9到322.6℃,实际失重9.54%,理论失重10.55%,这一过程归属为溶剂分子的失去,在从203.6到278.6℃出现一个平稳期,从322.6到760℃区间有一个多步失重过程,相对应于水杨醛缩乙二胺配体的分解,(实际失重66.78%,理论失重66.05%),而从760到1000℃则又出现了一个平台区.推测最终黑色残余物对应于分解产物CuO(测试值:23.65%,理论值:23.40%).从DSC曲线上可以看出,配合物在310?C有一个小的放热峰,在424.5℃有一个较强的放热峰.
3.3荧光光谱
如图7所示,在同样的激发波长(366nm)作用下,配体水杨醛缩乙二胺和配合物水杨醛缩乙二胺合铜的发射光谱有很大差别,配合物水杨醛缩乙二胺合铜具有很强的荧光,发射光谱范围在400~473nm之间,在418.1nm处出现最大峰;配体水杨醛缩乙二胺的发射光谱在472~536nm之间,在500.3nm处出现最大峰.在配合物中,由于金属离子对配体的作用,使配合物的最大发射峰发生了明显的蓝移.同时配合物的生成导致体系共轭程度增强,因此配合物的荧光强度比配体增强了许多.相比于配体,由于金属离子的存在,使配合物的荧光发射波长和强度都有变化.
4 总结
本论文以水杨醛和乙二胺为原料合成了水杨醛缩乙二胺,并以此为配体,用溶剂挥发法合成了双核水杨醛缩乙二胺合铜配合物.同时测定了该配合物的单晶结构,并对其热性能和荧光性能进行了表征.
〔1〕解庆范,卢慧强,游兴英,等.2-氨甲基吡啶缩5-溴水杨醛席夫碱配合物的合成、表征与抗氧化作用[J].化学研究,2015,26(1):35-38.
〔2〕徐刚,董文丽,任凌燕,刘火安.双水杨醛缩乙二胺合铜席夫碱金属配合物的合成及应用 [J].应用化学,2013,30(1):88-92.
〔3〕张逢源,刘翔宇.5-硝基水杨醛缩乙二胺双希夫碱铜(Ⅱ)配合物的合成、晶体结构及热稳定性研究[J].宁夏大学学报(自然科学版),2015,36(4):367-370.
〔4〕姚宏亮,李方实.水杨醛的应用及合成方法述评[J].江苏化工,2007,35(3):17-19.
〔5〕刘平,刘岩,马晓松,等.新型水溶性希夫碱化合物的合成.[J].石河子大学学报,2015,33(1):7-10.
〔6〕吴云龙,朱稳,夏昌坤,等.基于双希夫碱配体的两个过渡族配合物的合成、表征和晶体结构[J].江苏大学学报 (自然科学版),2016,37(3):337-340.
〔7〕王慧丽,胡英芝,阎娥,尹大学.希夫碱金属配合物应用进展[J].云南化工,2011,38(1):70-75.
〔8〕田晓雪,郑长征,唐小冬,严回.希夫碱配合物生物活性方面的应用研究进展[J].化工技术与开发,2011,40(9):28-29.
〔9〕贤景春.Cu(Ⅱ)、Zn(Ⅱ)Schiff碱配合物的光谱分析及其对超氧离子的抑制作用[J].光谱学与光谱分析,2010,30(3):725-728.
〔10〕张欣,杜聪,陈丹,等.氨基酸席夫碱镍、钴配合物的合成、晶体结构与抑菌活性.[J].无机化学学报.2010,26(3):489-494.
〔11〕Sheldrick,G.M.SHELX-97,Program for the Solution and Refinement of Crystal Structures,University of G?ttingen,Germany,1997.
TQ224.1
A
1673-260X(2016)10-0017-04
2016-06-04
内蒙古自治区教育厅项目(NJZY239)

