RAFT聚合法制备丙烯酰胺纳米凝胶的工艺优化
龚 霞,胡莹莹,尤祥宇,谢卫红
(湖北工业大学,湖北 武汉 430068)
RAFT聚合法制备丙烯酰胺纳米凝胶的工艺优化
龚霞,胡莹莹,尤祥宇,谢卫红
(湖北工业大学,湖北 武汉 430068)
对聚合物的粒径和分散性的精密控制是当前聚合物研究的重要课题。采用可逆加成-断裂链转移(RAFT)聚合法制备了丙烯酰胺纳米凝胶,考察了聚合时间、单体(AAm)+交联剂(EGDMA)用量、链转移剂(BDC)+引发剂(AIBN)用量、BDC用量、n(AAm)∶n(EGDMA)比值、聚合温度等对制备工艺的影响。结果表明,当延长聚合时间、增加AAm+EGDMA用量、升高聚合温度、减少BDC+AIBN用量、减少BDC用量、减小n(AAm)∶n(EGDMA)比值时,纳米凝胶的粒径和分散性增大;且粒径基本上与分散性呈正相关关系。通过控制反应条件,可以得到单分散、粒径在几十到几百纳米的丙烯酰胺纳米凝胶。
可逆加成-断裂链转移(RAFT)聚合;丙烯酰胺;纳米凝胶;优化
纳米凝胶是一种以纳米颗粒(粒径为1~1 000nm)形式存在的分子内交联聚合凝胶,其内部结构为典型的网络结构。与大颗粒聚合物不同,纳米凝胶粒径小[1]、比表面积大、传质能力强、结合位点易接近、表面热交换效率高、在外部条件下易收缩和膨胀[2],达到了弹性和刚性的平衡。纳米凝胶在生物医学(如药物载体[3-6]和基因传递[7])、酶固定化及酶活性调控、诊断[8-9]、治疗[10]等领域具有广阔的应用前景。
可逆加成-断裂链转移(RAFT)聚合反应是指在传统的自由基聚合体系中,引入一种具有高链转移常数的二硫代酯结构的链转移试剂,从而实现自由基聚合的活性/可控。RAFT属于活性/可控自由基聚合中的一种,其基本原理是通过衰减链转移从而提供可逆失活的聚合反应过程(图1)。
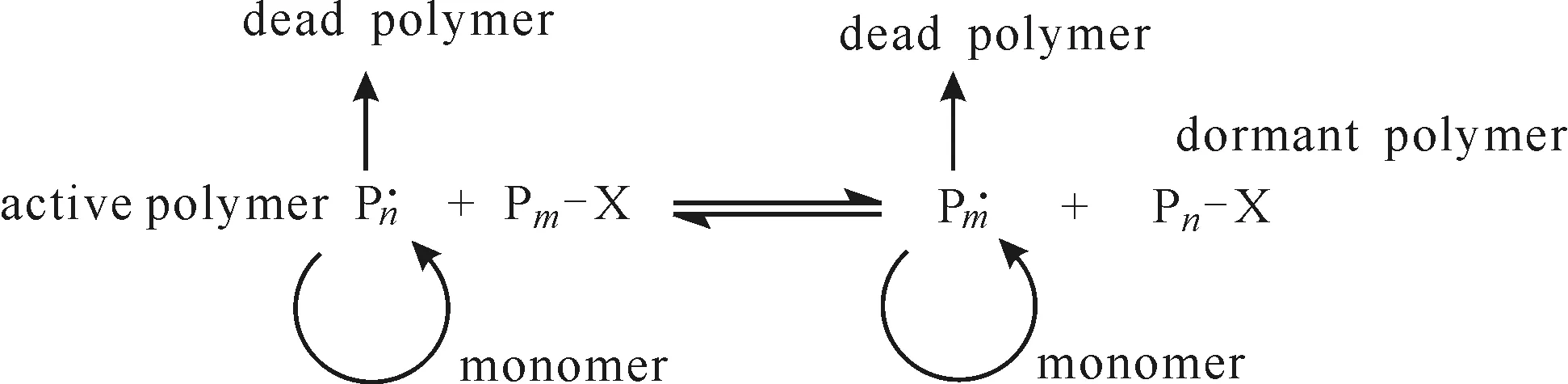
图1 RAFT聚合的反应机理Fig.1 Reaction mechanism of RAFT polymerization
由于RAFT聚合是活性自由基链(生长链)和“休眠物种”(RAFT基团链)之间的动态可逆平衡过程,从而能够有效地控制自由基聚合体系中活性增长自由基的浓度,避免不可逆偶合终止和歧化终止等副反应的发生,使得自由基聚合反应具有活性/可控特征[11-15]。RAFT涉及到低聚物的形成和增长。在聚合反应开始后,所有的链被引发,自由基与链转移剂结合,分枝型快速增长,在反应介质中形成大量的带有三维网络结构的低聚物。低聚物捕捉反应体系中的单体和低聚物,形成高交联度的粒子,使得单体转化率、聚合物粒径和分散性呈线性增长。RAFT聚合法具有适用单体范围广(几乎所有自由基聚合法的单体均适用)、反应条件温和等特点,能够在传统自由基聚合体系中或采用多种聚合方法[16](如本体聚合、溶液聚合、乳液聚合、悬浮聚合等)制备特殊结构聚合物,是制备新型聚合物的常用方法。作者采用RAFT聚合法制备丙烯酰胺纳米凝胶,并对聚合时间、单体(AAm)+交联剂(EGDMA)用量、链转移剂(BDC)+引发剂(AIBN)用量、BDC用量、n(AAm)∶n(EGDMA)比值、聚合温度等制备工艺进行了优化,拟为探索简单、高效、通用的纳米凝胶制备方法提供帮助。纳米凝胶的制备过程如图2所示。
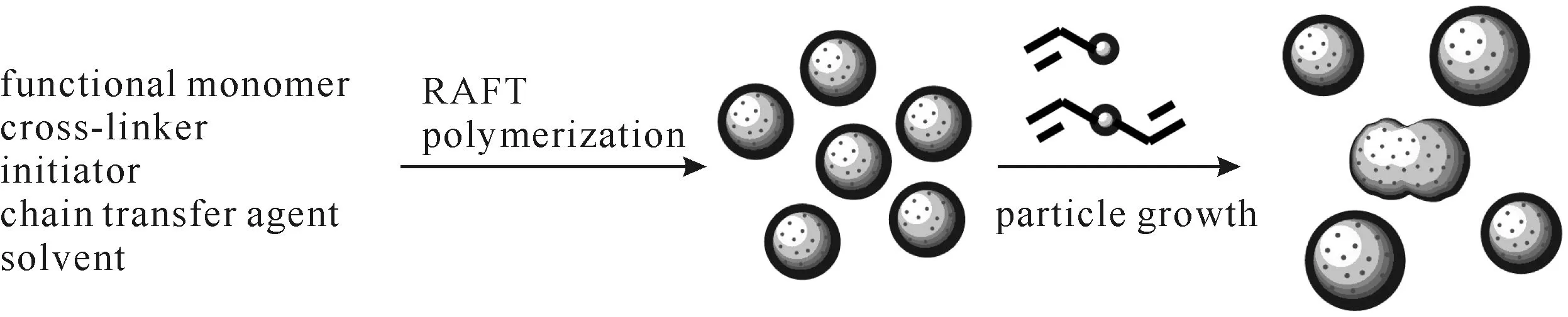
图2 丙烯酰胺纳米凝胶的制备过程Fig.2 Preparation of acrylamide nanogels
1 实验
1.1试剂与仪器
丙烯酰胺(AAm)、二甲基亚砜(DMSO),分析纯,国药集团化学试剂有限公司;乙二醇二甲基丙烯酸酯(EGDMA,98%),Sigma公司;二乙基二硫代氨基甲酸苄酯(BDC),分析纯,武汉大学;偶氮二异丁腈(AIBN,98%),上海源叶生物科技有限公司。
KQ5200G型超声波清洗器,昆山超声仪器有限公司;IKA-RET型控温电磁搅拌器,德国IKA公司;VP30型真空抽滤泵,北京莱伯泰科仪器股份有限公司;Zetasizer nano型粒度分析仪,马尔文仪器有限公司。
1.2制备方法
向反应瓶中加入10 mL的DMSO和一定量的功能单体AAm、交联剂EGDMA、链转移剂BDC、引发剂AIBN,超声5 min使之充分混合均匀。吸取混合液分装在12支试管中,每支试管10 mL,试管上部连接带有充满氮气的气球的三通管,每支试管用真空抽滤泵抽真空12 min,每3 min通氮气30 s。除氧完成后,将试管置于65 ℃油浴加热,不断搅拌反应一段时间后,浸入冰水浴冷却至室温,即得丙烯酰胺纳米凝胶,取2 mL进行粒径(D)和聚合物分散指数(PDI)分析。
1.3制备工艺优化
分别考察聚合时间、AAm+EGDMA用量(体积分数,下同)、BDC+AIBN用量、BDC用量、n(AAm)∶n(EGDMA)比值、聚合温度对纳米凝胶的粒径和分散指数的影响,以确定最优的制备工艺。
2 结果与讨论
2.1聚合时间对纳米凝胶的影响
在n(AAm)∶n(EGDMA)∶n(BDC)∶n(AIBN)=30∶90∶4∶1、AAm+EGDMA用量为0.8%、DMSO用量为10 mL、聚合温度为65 ℃的条件下,考察聚合时间对纳米凝胶的粒径和分散指数的影响,结果见图3。
由图3可看出,随着聚合时间的延长,纳米凝胶的粒径不断增大,当粒径超过200 nm后,分散性剧烈变化。这是因为,聚合时间越长,粒子表面残余的乙烯基基团捕获的低聚物自由基越多,导致颗粒越来越大,纳米凝胶的粒径相应增大。

图3 聚合时间对纳米凝胶的影响Fig.3 Effect of polymerization time on nanogels
2.2AAm+EGDMA用量对纳米凝胶的影响
在n(BDC)∶n(AIBN)=4∶1、DMSO用量为10 mL、聚合温度为65 ℃、聚合时间为100 min的条件下,考察AAm+EGDMA用量对纳米凝胶的粒径和分散指数的影响,结果见图4。

图4 AAm+EGDMA用量对纳米凝胶的影响Fig.4 Effect of AAm+EGDMA dosage on nanogels
由图4可看出,当AAm+EGDMA用量为0.6%~1.0%时,纳米凝胶的粒径从30 nm线性增大到180 nm,为单分散体系;当AAm+EGDMA用量为1.2%时,为多分散体系。这是因为,AAm+EGDMA用量增大,最初形成的分枝低聚物增加,导致粒子表面残余的乙烯基基团更容易捕获溶液中的低聚物自由基,使颗粒不断增长。
2.3BDC+AIBN用量对纳米凝胶的影响
在n(AAm)∶n(EGDMA)=30∶90、DMSO用量为10 mL、AAm+EGDMA用量为0.8%、聚合温度为65 ℃、聚合时间为100 min的条件下,考察BDC+AIBN用量[以原料配比中的比例表示,n(BDC)∶n(AIBN)=2.4∶0.6、3.2∶0.8、4∶1、4.8∶1.2]对纳米凝胶的粒径和分散指数的影响,结果见图5。

图5 BDC+AIBN用量对纳米凝胶的影响Fig.5 Effect of BDC+AIBN dosage on nanogels
由图5可看出,随着BDC+AIBN用量的增加,纳米凝胶的粒径先增大后减小,在用量为5.0[n(BDC)∶n(AIBN)=4∶1]时达到最大;分散指数变化不大。这是因为,引发剂AIBN浓度增大会促使正在增长的低聚物自由基浓度瞬间增大,同时加快低聚物聚积速度,促使体系中不稳定的聚合物核形成较大的粒子;随着链转移剂BDC浓度的增大,它与低聚物自由基形成暂时失活的休眠聚合物,降低和控制了自由基浓度。表明引发剂和链转移剂是相互制约的。
2.4BDC用量对纳米凝胶的影响
在n(AAm)∶n(EGDMA)∶n(AIBN)=30∶90∶1、DMSO用量为10 mL、AAm+EGDMA用量为0.8%、聚合温度为65 ℃、聚合时间为100 min的条件下,考察BDC用量(以原料配比中的比例表示)对纳米凝胶的粒径和分散指数的影响,结果见图6。
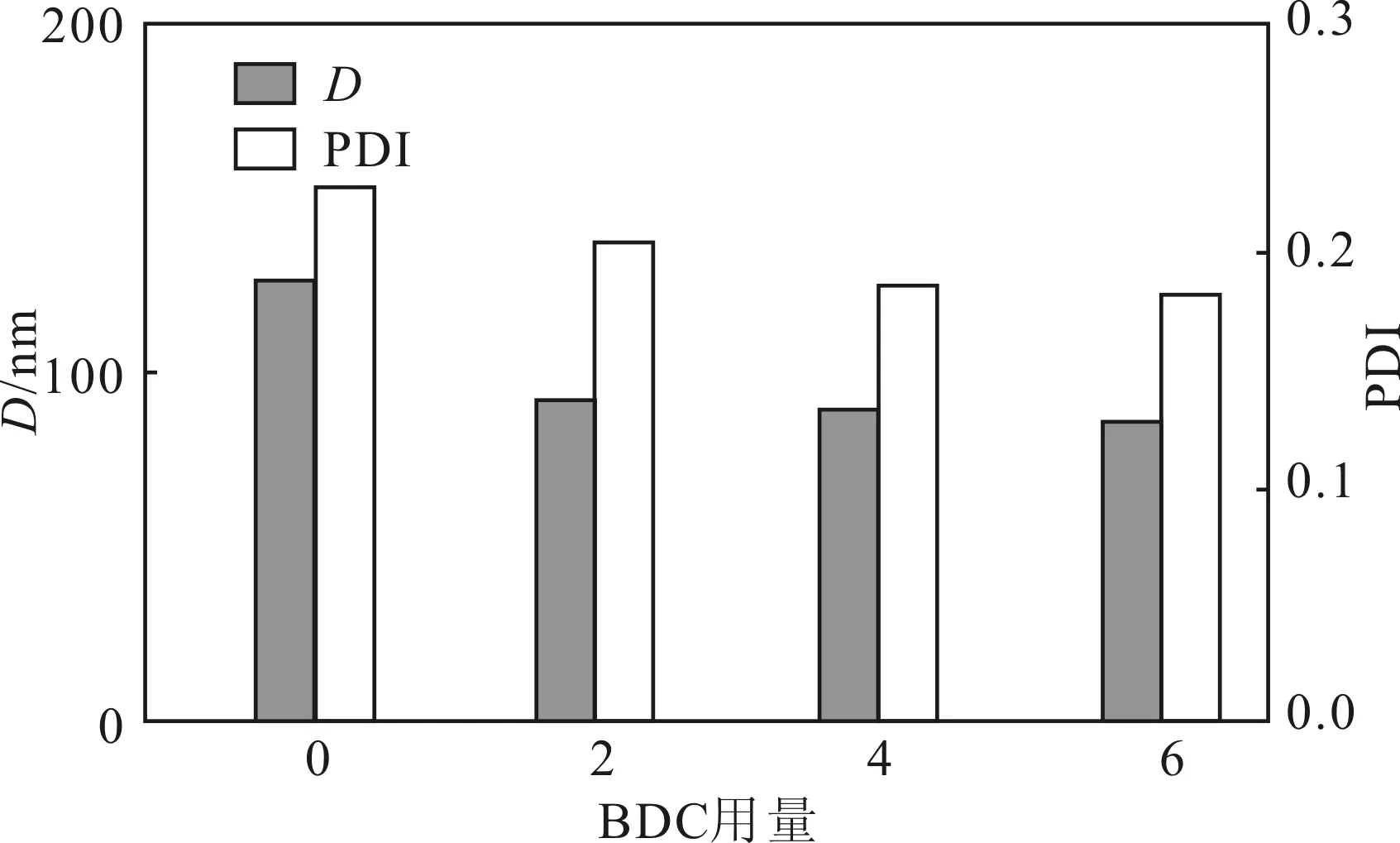
图6 BDC用量对纳米凝胶的影响Fig.6 Effect of BDC dosage on nanogels
由图6可以看出,BDC用量与纳米凝胶的粒径和分散指数成反比。这是因为,随着BDC用量的增加,它与低聚物自由基形成暂时失活的休眠聚合物的量增加,降低和控制了自由基浓度,体系中游离的自由基相应减少,聚合反应速率减慢,导致粒径和分散指数减小。表明,与常规聚合方法相比,加入链转移剂可使聚合物分散性更好。
2.5n(AAm)∶n(EGDMA)比值对纳米凝胶的影响
在聚合反应中,加入交联剂使纳米凝胶形成一定的刚性结构,维持其三维网络结构,但若交联剂过量会导致凝胶缺少柔韧性而影响传质。因此,适宜的单体与交联剂配比对纳米凝胶的性质影响较大。为此,在n(BDC)∶n(AIBN)=4∶1、DMSO用量为10 mL、AAm+EGDMA用量为0.8%、聚合温度为65 ℃、聚合时间为100 min的条件下,考察n(AAm)∶n(EGDMA)比值对纳米凝胶的粒径和分散指数的影响,结果见图7。
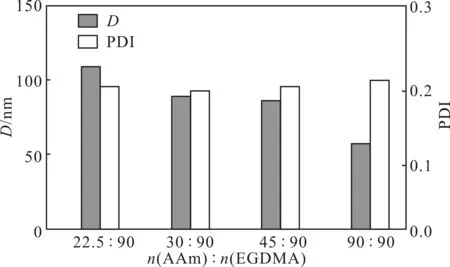
图7 n(AAm)∶n(EGDMA)比值对纳米凝胶的影响Fig.7 Effect of n(AAm)∶n(EGDMA) ratio on nanogels
由图7可以看出,随着n(AAm)∶n(EGDMA)比值的增大,即单体AAm用量的增加,纳米凝胶的粒径从110 nm减小到50 nm,而分散指数变化不大。这是因为,交联剂占比增大,颗粒的网状结构增大,乙烯基浓度也增大,粒径相应增大。
2.6聚合温度对纳米凝胶的影响
在n(AAm)∶n(EGDMA)∶n(BDC)∶n(AIBN)=30∶90∶4∶1、AAm+EGDMA用量为0.8%、DMSO用量为10 mL、聚合时间为100 min的条件下,考察聚合温度对纳米凝胶的粒径和分散指数的影响,结果见图8。
从图8可以看出,当聚合温度在60~75 ℃范围内时,纳米凝胶的粒径变化范围为50~160 nm,分散指数变化范围为0.16~0.25;聚合温度越高,粒径越大,分散性越差。这主要是因为,聚合温度升高时,引发剂分解产生的初级自由基增多,反应速率加快,导致纳米凝胶的粒径增大。
3 结论
对聚合物的粒径和分散性的精密控制是当前聚合物研究的重要课题。采用可逆加成-断裂链转移(RAFT)聚合法制备了丙烯酰胺纳米凝胶,考察了聚合时间、单体(AAm)+交联剂(EGDMA)用量、链转移剂(BDC)+引发剂(AIBN)用量、BDC用量、n(AAm)∶n(EGDMA)比值、聚合温度等对制备工艺的影响。结果表明,当延长聚合时间、增加AAm+ EGDMA用量、升高聚合温度、减少BDC+AIBN用量、减少BDC用量、减小n(AAm)∶n(EGDMA)比值时,纳米凝胶的粒径和分散性增大;且粒径基本上与分散性呈正相关关系。通过控制反应条件,可以得到单分散、粒径在几十到几百纳米的纳米凝胶。当纳米凝胶的粒径在200 nm以下时,基本上呈单分散体系。聚合时间、AAm+EGDMA用量和n(AAm)∶n(EGDMA)比值对纳米凝胶的粒径和分散指数影响最大。也可以对功能基团进行修饰(如嫁接亲水基团),提高生物相容性,进一步拓宽纳米凝胶的应用范围。
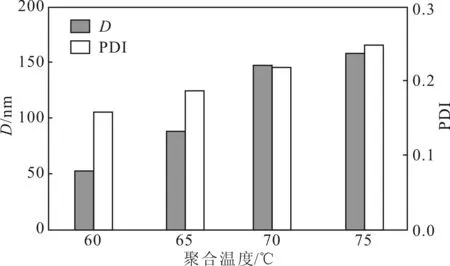
图8 聚合温度对纳米凝胶的影响Fig.8 Effect of polymerization temperature on nanogels
[1]DAOUD-MAHAMMED S,COUVREUR P,GREF R.Novel self-assembling nanogels:stability and lyophilisation studies[J].International Journal of Pharmaceutics,2007,332(1/2):185-191.
[2]CHOI S W,CHOI S Y,JEONG B,et al.Thermoreversible gelation of poly(ethylene oxide) biodegradable polyester block copolymers[J].Journal of Polymer Science Part A:Polymer Chemistry,1999,37(13):2207-2218.
[3]PAN G Q,GUO Q P,CAO C B,et al.Thermo-responsive molecularly imprinted nanogels for specific recognition and controlled release of proteins[J].Soft Matter,2013,9(14):3840-3850.
[4]HOARE T R,KOHANE D S.Hydrogels in drug delivery:progress and challenges[J].Polymer,2008,49(8):1993-2007.
[5]DURACHER D,ELAÏSSARI A,PICHOT C.Preparation of poly(N-isopropylmethacrylamide) latexes kinetic studies and characterization[J].Journal of Polymer Science Part A:Polymer Chemistry,1999,37(12):1823-1837.
[6]MURTHY N,XU M C,SCHUCK S,et al.A macromolecular delivery vehicle for protein-based vaccines:acid-degradable protein-loaded microgels[J].Proceedings of the National Academy of Sciences,2003,100(9):4995-5000.[7]FENILI F,MANFREDI A,RANUCCI E,et al.Poly(amidoamine) hydrogels as scaffolds for cell culturing and conduits for peripheral nerve regeneration[J].International Journal of Polymer Science,2011,2011:2341-2348.
[8]van der LINDEN H J,HERBER S,OLTHUIS W,et al.Stimulus-sensitive hydrogels and their applications in chemical(micro) analysis[J].Analyst,2003,128(4):325-331.
[9]DISHI M,SUMITANI S,NAGASAKI Y.On-off regulation of F-19 magnetic resonance signals based on pH-sensitive PEGylated nanogels for potential tumor-specific smart F-19 MRI probes[J].Bioconjugate Chemistry,2007,18(5):1379-82.
[10]YU Z,XU Z,LI H,et al.Recognition and neutralization of angiotensins Ⅰ and Ⅱ using an artificial nanogel receptor fabricated by ligand specificity determinant imprinting[J].Chemical Communications,2014,50(21):2728-2731.
[11]MA Y,PAN G Q,ZHANG Y,et al.Narrowly dispersed hydrophilic molecularly imprinted polymer nanoparticles for efficient molecular recognition in real aqueous samples including river water,milk,and bovine serum[J].Angewandte Chemie,2012,52(5):1511-1514.
[12]LIU J C,STANSBURY J W.RAFT-Mediated control of nanogel structure and reactivity:chemical,physical and mechanical properties of monomer-dispersed nanogel compositions[J].Dental Materials,2014,30(11):1252-1262.
[13]AN Z S,QIU Q,LIU G Y.Synthesis of architecturally well-defined nanogelsviaRAFT polymerization for potential bioapplications[J].Chemical Communications,2011,47(46):12424-12440.
[14]HENKEL R,VANA P.Increasing the tackiness of statistical poly-(butyl acrylate) and poly(ethyl acrylate) network materialsviaRAFT polymerization[J].Macromolecular Materials & Engineering,2015,300(5):551-561.
[15]JIN C,LIU C,JIANG B,et al.Synthesis and characterization of high molecular weight and low dispersity polystyrene homopolymers by RAFT polymerization[J].E-Polymers,2012,12(1):418-427.
[16]ATTA A M,EL-AZABAWY O E,ISMAIL H S,et al.Novel dispersed magnetite core-shell nanogel polymers as corrosion inhibitors for carbon steel in acidic medium[J].Corrosion Science,2011,53(5):1680-1689.
Process Optimization of Acrylamide Nanogels Prepared by RAFT Polymerization
GONG Xia,HU Ying-ying,YOU Xiang-yu,XIE Wei-hong
(HubeiUniversityofTechnology,Wuhan430068,China)
Precisioncontroloftheparticlesizeanddispersityofpolymersisanimportanttopicofcurrentpolymerresearch.Acrylamidenanogelswerepreparedbyreversibleaddition-fragmentationchaintransfer(RAFT)polymerization.Theeffectsofpolymerizationtime,dosageofmonomer(AAm)andcross-linker(EGDMA),dosageofchaintransferagent(BDC)andinitiator(AIBN),dosageofBDC,n(AAm)∶n(EGDMA)ratio,andpolymerizationtemperatureonpreparationprocesswereinvestigated.Resultsindicatedthat,whenincreasingthepolymerizationtime,thedosageofAAm+EGDMA,polymerizationtemperature,andreducingthedosageofBDC+AIBN,thedosageofBDC,n(AAm)∶n(EGDMA)ratio,theparticlesizeanddispersityofnanogelsincreased.Therewasapositivecorrelationbetweentheparticlesizeandthedispersity.Bycontrollingthereactionconditions,themonodispersedacrylamidenanogelwasprepared,anditsparticlesizewasintherangeoftenstohundredsofnanometers.
reversibleaddition-fragmentationchaintransfer(RAFT)polymerization;acrylamide;nanogel;optimization
中科院病毒所国家重点实验室开放研究基金资助项目(20875024)
10.3969/j.issn.1672-5425.2016.10.008
TQ 317
A
1672-5425(2016)10-0035-04
龚霞,胡莹莹,尤祥宇,等.RAFT聚合法制备丙烯酰胺纳米凝胶的工艺优化[J].化学与生物工程,2016,33(10):35-38,44.

