新生儿呼吸窘迫综合征发病危险因素的Logistic回归分析
麻伟博
·论著·
新生儿呼吸窘迫综合征发病危险因素的Logistic回归分析
麻伟博
目的探讨新生儿呼吸窘迫综合征(NRDS)发病的危险因素。方法采用病例对照研究,选择在北京市顺义区妇幼保健院新生儿科住院的RDS新生儿72例为病例组,同期住院未合并RDS的新生儿72例为对照组,采用χ2检验进行单因素分析,选择单因素分析中有统计意义的因素进行多因素Logistic回归分析。结果两组在羊水过少、胎膜早破、小于胎龄儿方面比较差异无统计学意义(P>0.05),在新生儿窒息、宫内窘迫、母亲糖尿病、多胎、早产、男性、剖宫产方面比较差异有统计学意义(P<0.05)。多因素Logistic回归分析显示新生儿窒息(OR=11.869,95%CI:1.323~106.515)、宫内窘迫(OR=21.400,95%CI:1.511~303.164)、母亲糖尿病(OR=8.517,95%CI:1.413~51.332)、早产(OR=76.748,95%CI:19.432~303.124)、男性(OR=5.264,95%CI:1.401~19.775)、剖宫产(OR=6.903,95%CI:1.803~26.428)与NRDS的发病存在相关性(P<0.05)。结论新生儿窒息、宫内窘迫、母亲糖尿病、早产、男性、剖宫产是NRDS发病的主要危险因素。
新生儿呼吸窘迫综合征;危险因素;肺表面活性物质;Logistic回归分析
新生儿呼吸窘迫综合征(neonatal respiratory distress syndrome, NRDS)是新生儿最常见的呼吸系统疾病之一,由新生儿肺发育不成熟、肺表面活性物质缺乏所致,以进行性呼吸困难、低氧血症为主要表现。NRDS对新生儿的生命健康造成严重的影响,因此通过对围产期NRDS发病危险因素的研究,对预防和减少NRDS的发生显得尤为重要。
资料与方法
一、 一般资料
选择2014年1月至2015年12月,在本院新生儿科住院的72例RDS新生儿为RDS组,随机选取同期住院未合并RDS的72例新生儿为对照组。RDS诊断标准[1]:①急性起病,出生后不久即出现呼吸窘迫,表现为呼吸急促、发绀、鼻扇、吸气三凹征等,吸氧无效,需要辅助通气;②呼吸窘迫呈进行性加重;③胸部X线片表现为两肺普遍性透亮度降低,网状、颗粒状阴影,支气管充气征,重症者为“白肺”;④除外引起呼吸窘迫的其他疾病。
二、研究方法
对两组新生儿的围产高危因素进行记录如:窒息、宫内窘迫、母亲糖尿病、羊水过少、胎膜早破、多胎、男性、早产及剖宫产等。
二、 统计学分析
采用SPSS18.0软件进行资料统计分析。采用χ2检验、校正χ2检验及Logistic回归分析评价各个危险因素与NRDS发病的相关性,以P<0.05为差异有统计学意义。
结 果
一、围产期情况单因素分析
两组患儿在窒息、宫内窘迫、母亲糖尿病、多胎、早产、男性、剖宫产方面比较差异均有统计学意义(P均<0.05);而在羊水过少、胎膜早破、小于胎龄儿方面比较差异无统计学意义(P均>0.05),见表1。

表1 两组患儿围产期情况单因素分析[n(%)]
二、NRDS危险因素的多因素Logistic回归分析
以是否发生RDS作为因变量,以单因素分析有统计意义的窒息、宫内窘迫、母亲糖尿病、多胎、早产、男性、剖宫产因素作为自变量,进行Logistic回归分析。经变量筛选后得到的危险因素有窒息(OR=11.869)、宫内窘迫(OR=21.400)、母亲糖尿病(OR=8.517)、早产(OR=76.748)、男性(OR=5.264)、剖宫产(OR=6.903),见表2。
讨 论
NRDS是由于肺表面活性物质(pulmonary surfactant, PS)缺乏及肺结构发育不成熟所致,多见于早产儿,自然病程为出生后当时或很快发病,并在出生后2 d内进行性恶化,如不及时治疗,因进行性缺氧和呼吸衰竭而死亡,存活者,在出生后2~4 d病情开始改善。胎龄越小,RDS发生率越高,病情越严重。近年来随着母胎医学和新生儿重症监护医学(neonatal intensive care unit, NICU)的飞速发展,新生儿呼吸窘迫综合征越来越受到人们的重视[2-5]。本研究通过对单因素和多因素两个方面对新生儿呼吸窘迫综合征发病的有关危险因素进行分析,筛选出:新生儿窒息、宫内窘迫、母亲糖尿病、早产、男性、剖宫产为主要危险因素,通过它们建立Logistic回归预测模型,对高危孕妇及新生儿进行早期干预。
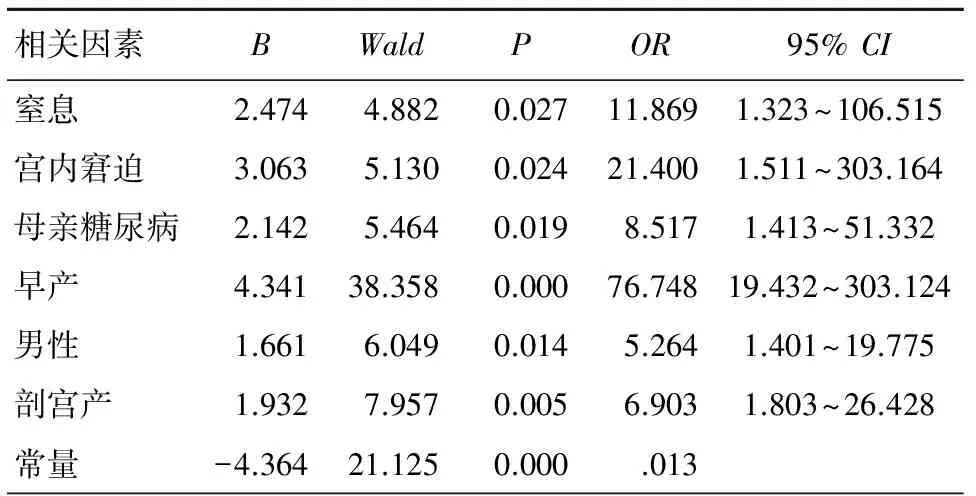
表2 多因素Logistic回归分析
新生儿出生时窒息导致的缺氧可直接损伤肺泡Ⅱ型上皮细胞,减少PS的生成。此外,缺氧可抑制肺表面活性物质的活性并加速其灭活,从而导致RDS发生[6]。有研究提示宫内窘迫是RDS的保护因子,本研究提示宫内窘迫是RDS的危险因素,其原因可能为宫内窘迫导致的急性缺氧更易导致肺泡表面活性物质合成及利用障碍。而慢性缺氧可能使胎儿出现生长延缓,胎肺发育相对成熟,从而降低RDS的发生率[7]。
母亲糖尿病是RDS的危险因素,其机制可能为孕妇高血糖持续经胎盘到达胎儿体内,刺激胎儿胰岛素分泌增加,形成高胰岛素血症。胰岛素可拮抗糖皮质激素促进肺泡Ⅱ型上皮细胞表面活性物质合成及释放的作用,使胎儿肺表面活性物质产生及分泌减少,致使胎儿肺成熟延迟[8]。
早产与RDS密切相关,胎龄愈小,肺泡表面活性物质分泌愈不足,RDS 的发病率就愈高。据欧洲新生儿协会关于2006 年 RDS发病指数的统计发现,胎龄 23~25周的发病率为 91%,26~27周为 58%,25~29周为 74%,30~31周为 52%[9]。本研究也提示早产是导致RDS的最主要危险因素之一(OR=76.748,95%CI:19.432~303.124)。
男性为新生儿 RDS 的独立危险因素,其机制可能与性激素有关。雄性激素可影响肺发育成熟并可抑制肺泡表面活性物质合成及分泌[10]。其机制为①雄性激素可延缓肺泡Ⅱ型细胞的发育成熟和减少肺泡表面活性物质的释放;②雄性激素可以通过调节生长因子信号传导来影响肺部的发育成熟;③雌激素可以促进肺泡表面活性物质的合成,同时可通过增加肺泡Ⅱ型细胞的数量和板层小体形成而促进胎儿肺的发育成熟,但雄激素没有这方面作用。
最近关于剖宫产对新生儿 RDS 的影响已有很多相关报道[11-12]。其机制可能为:①内源性糖皮质激素减少,不利于肺成熟。胎儿经阴道分娩时使孕妇和胎儿交感神经系统充分激活,胎儿体内的糖皮质激素如类固醇、儿茶酚胺等大量分泌,有助于胎儿肺成熟。而经剖宫产分娩的新生儿则缺少此过程,其内源性糖皮质激素水平处于低水平,从而影响新生儿肺泡表面活性物质的合成;②肺液清除减少。剖宫产新生儿胸部未经过宫缩和产道的有效挤压,肺液清除不充分,促使肺液吸收的Na+通道受损,肺泡表面活性物质消耗增加,导致肺内液体潴留,造成低通气[13];③肺泡表面活性物质释放减少。肺泡Ⅱ型上皮细胞的板层小体具有储存和释放肺表面活性物质作用,剖宫产儿缺乏宫缩应激,不利于板层小体释放肺表面活性物质,进一步影响肺成熟。
目前对胎膜早破是否为新生儿RDS的危险因素仍存在争议。Shimoya等[14]认为胎膜早破(premature rupture of membrane, PROM)后由于宫内感染可降低新生儿RDS发生率,而Piazze等[15]则明确指出PROM可显著增加新生儿RDS发生率。Piazza认为PROM后由于羊水量减少,可影响胎儿肺的发育导致肺的发育成熟障碍。PROM后易发生新生儿感染是导致足月儿RDS主要的原因。宫内感染、绒毛膜羊膜炎等均可导致肺发育成熟障碍及肺泡Ⅱ型细胞损伤,使肺表面活性物质合成及分泌减少。宫内感染及感染性肺炎致肺表面活性物质消耗增加及婴儿出生后对肺表面活性物质需要增加,进一步导致肺表面活性物质减少。PROM导致相对早产:PROM是早产的重要原因之一,而早产是NRDS最主要的原因。本研究显示PROM与NRDS的发生无明显相关性,可能与样本量少有关,尚有待于进一步大样本研究。另外在本研究中,Logistic回归分析显示:羊水过少、多胎、小于胎龄儿与NRDS的发生亦无明显相关性。
综上所述,围产期许多因素与RDS 的发生有关,本研究提示新生儿窒息、宫内窘迫、母亲糖尿病、早产、男性、剖宫产为RDS发生的独立危险因素,为降低RDS的发生率提供了一定参考价值。另外,RDS的防治应从出生前开始,需要一个包括儿科和产科医生在内的围产医学团队,应针对其围产危险因素,积极加强产前筛查、监护、及时处理和治疗高危因素如:加强糖尿病孕妇管理,对早产高危因素孕妇进行筛查并及早干预防治早产等;加强对孕产妇的宣教,减少社会因素剖宫产;提高医护人员助产技术和新生儿复苏技能;对 RDS患儿争取做到早期诊断、早期治疗以减少并发症,改善预后。
1沈晓明, 王卫平. 儿科学[M]. 第7版,北京:人民卫生出版社,2008: 110-114.
2易海英, 徐舒, 杨树杰, 等. 足月儿呼吸窘迫综合症发病相关因素分析[J]. 中国新生儿科杂志,2011, 26(5): 319-321.
3程秀永, 万玉, 郝志成, 等. 选择性剖宫产对(近)足月儿发生呼吸窘迫综合症的影响[J]. 实用儿科临床杂志, 2011, 26(2): 114-115.
4董慧芳, 吉玲, 白琼丹, 等. 足月新生儿呼吸窘迫综合症危险因素及肺表面活性物质疗效评估[J].中国循证儿科杂志,2012, 7(5): 393-396.
5代苗英, 李少兵, 胡金绘, 等. 不同胎龄新生儿呼吸窘迫综合征高危因素及临床分析[J]. 临床儿科杂志,2014, 32(7): 644-647.
6Nicole P, Sailesh K. Pathophysiology of respiratory distress syndrome[J]. Paediatr Child Health, 2008, 19(5): 153-157.
7蔡丽杰, 张军. 早产危险因素与早产儿肺透明膜病发病的相关性[J]. 中国妇幼保健, 2006, 21(12):1666-1667.
8Ma XL, Xu XF,Chen C, et al. Epidemiology of respiratory distress and the illness severity in late preterm or term infants: a prospective multi-center study[J]. Chin Med J(Engl), 2010, 123(20): 2776-2780.
9Trotter A, Kipp M, Sshrader RM, et al. Combined applieation of 17 beta-estradiol and Progesteron enhance vaseular endothelial growth faetor and surfaetant Protein expression in cultured Embryonic lung cells of mice[J]. Int J Pediatr, 2009:170491.
10Seaborn T, Simard M, Provost PR, et al. Sex hormone metabolism in lung development and maturation[J]. Trends Endocrinol Metab, 2010, 21(12): 729-730.
12黄为民. 剖宫产与新生儿疾病[J]. 实用妇产科杂志, 2011, 27(3): 169-171.
13李雷, 边旭明. 择期剖宫产与新生儿结局[J]. 中华围产医学杂志, 2011, 14(1):24-27.
14Shimoya K, Taniguchi T, Matsuzaki N, et al. Chorioamniomtis decreased incidence of respiratory distress syndrome by elevating fetal interleukin-6sorom concentration[J]. Hum Repord, 2000, 15(10):2234-2240.
15Piazze J, Anceschi MM, Cerekia A, et al. Validity of amniotic fuid index in preterm rupture of the amniotic fluid index in preterm rupture of mcmbranes[J]. J Perinat Med, 2007, 35(5): 394-398.
(本文编辑:黄红稷)
麻伟博. 新生儿呼吸窘迫综合征发病危险因素的Logistic回归分析[J/CD]. 中华肺部疾病杂志: 电子版, 2016, 9(2): 182-184.
Logistic regression analysis of risk factors for neonatal respiratory distress syndrome
MaWeibo.
DepartmentofObstetricsandGynecology,MaternalandChildHealthCareHospitalofShunyiDistrict,Beijing101300,China
ObjectiveTo explore the risk factors for neonatal respiratory distress syndrome(NRDS). MethodsCase-control study was conducted on 72 cases of NRDS which hospitalized in the newborn unit, and the infants without RDS in the same term were divided into control group. Chi-square test was used in single factor analysis, statistically significant factors of single factor analysis was used in in the multi-factor Logistic regression analysis. ResultsThere were no significant difference on oligohydramnios, premature rupture of membranes, small for gestational age between two groups(P>0.05). There were significant difference on suffocation asphyxia, fetal distress, mother with diabetes, multiple pregnancy, premature birth, male, cesarean section between two groups(P<0.05). By the multivariate Logistic regression analysis, it showed that suffocation asphyxia(OR=11.869, 95%CI:1.323-106.515), fetal distress(OR=21.400, 95%CI: 1.511-303.164), mother with diabetes (OR=8.517, 95%CI:1.413-51.332), premature birth (OR=76.748, 95%CI:19.432-303.124), male(OR=5.264, 95%CI: 1.401-19.775) , cesarean section (OR=6.903, 95%CI: 1.803-26.428) were related to NRDS(P<0.05). ConclusionSuffocation asphyxia, fetal distress, mother with diabetes, premature birth, male, cesarean section were the major risk factors for NRDS.
Neonatal respiratory distress syndrome;Risk factors;Pulmonary surfactant;Logistic regression analysis
10.3877/cma.j.issn.1674-6902.2016.02.015
101300 北京市顺义区妇幼保健院妇产科
R563
A
2016-02-23)

