基于离子液体的生物质组分分离研究进展
候其东,鞠美庭,李维尊,刘乐,杨茜,陈昱
(南开大学环境科学与工程学院,天津市生物质类固废资源化技术工程中心,天津 300071)
综述与专论
基于离子液体的生物质组分分离研究进展
候其东,鞠美庭,李维尊,刘乐,杨茜,陈昱
(南开大学环境科学与工程学院,天津市生物质类固废资源化技术工程中心,天津 300071)
生物质资源的开发利用是解决资源危机和能源危机的重要途径,但传统的生物质组分分离工艺效率较低且污染严重,极大地制约了生物质资源的高值化利用。作为一类新型溶剂,离子液体可以溶解纤维素、木质素和天然生物质材料,为生物质的组分分离及加工转化提供了有力的工具。本文简述了离子液体在生物质组分分离中的应用,包括离子液体作为溶剂直接从木质纤维素类生物质中提取分离纤维素和木质素,以及在离子液体介质中通过化学反应降解生物质来分离主要组分的方法。从离子液体优选、反应路径设计、生物质预处理、溶解条件和再生剂等方面分析了生物质组分分离工艺。成本高、效率低且容易引起二次污染是阻碍离子液体用于生物质组分分离的主要因素。为了提高生物质组分分离的经济性和绿色性,今后应着力设计低成本、低黏度、热稳定性强和低毒的离子液体,研发绿色高效的生物质组分分离工艺和离子液体再生方法。
离子液体;生物质;纤维素;木质素;组分分离
近年来随着我国城镇化和农业现代化的高速推进,以秸秆和园林绿化垃圾为代表的木质纤维素类生物质大量产生,造成了严重的环境问题[1]。木质纤维素类生物质作为固体废弃物不但会占用宝贵的耕地资源,污染水体,其燃烧也是形成灰霾的重要因素(4.8%~6.7%)[2]。木质纤维素类生物质材料主要由纤维素、半纤维素和木质素组成,这3种聚合物都有替代石油等化石燃料用作工业原料和能源的巨大潜力[1,3]。因此发展绿色高效的生物质资源化技术,不但是缓解环境污染、应对资源能源危机的关键举措,也是减少碳排放的重要途径。纤维素既可以用来造纸,又可以通过改性生产新型材料[3],还可以用来生产新型燃料和平台化合物,如纤维素乙醇、5-羟甲基糠醛和乙酰丙酸等[4]。半纤维素可以作为生产木糖醇、糠醛等高附加值产品的基础原料[5]。木质素是为数不多的适合生产芳香基化合物的可再生资源,具有取代石油等不可再生资源的潜力[6-7]。此外,木质素也可以用来生产黏结剂和分散剂等材料[8-9]。
将纤维素、半纤维素和木质素转化成高附加值的产品,首先要实现这些组分的有效分离[4]。然而,天然木质纤维素类生物质复杂致密的结构使其难以溶解在常规溶剂中,给生物质的组分分离带来巨大的障碍[10-11]。目前从生物质中分离纤维素最主要的工艺仍然是化学制浆法,该方法占据了全球纸浆生产量的70%左右[10]。化学制浆法产生的纤维素主要用来造纸,而木质素大部分被用于燃烧供热,用于高附加值产品生产的木质素不足2%[6]。传统的制浆工艺造成了严重的环境污染问题。一些基于有机溶剂的新型制浆方法可以生产出品质与传统制浆法接近的产品,但依然存在着成本过高,溶剂难以回收等问题[10]。近年来发现一些离子液体可以高效地溶解纤维素、半纤维素和木质素,甚至可以部分或完全溶解木质纤维素类生物质材料,为生物质材料的组分分离和加工转化提供了新的平台[11-13]。
1 离子液体对生物质的溶解
1.1 纤维素的溶解
2002年,ROGERS等[13]发现一种离子液体1-丁基-三甲基咪唑氯盐([Bmim]Cl)在加热条件下能够溶解20%的纤维素,开启了利用室温离子液体溶解和处理纤维素的研究热潮。到目前为止,已经发现数十种具有溶解纤维素能力的离子液体。在离子液体溶解纤维素方面,国内外已经有了大量的综述性文章归纳了近年来的主要进展[11-13],详细探讨了离子液体的组成结构、纤维素自身的性质和溶解条件等对纤维素溶解的影响。普遍认为具有强氢键形成能力的阴离子可以有效地打破纤维素分子内和分子间的氢键,从而将纤维素溶解[11]。ROGERS等[11]通过核磁研究认为,纤维素的溶解主要是阴离子在起作用,而阳离子与纤维素之间没有显著的作用力,只是起到分散溶质的作用[14]。因而在阳离子相同的条件下,离子液体对纤维素的溶解能力随着阴离子氢键形成能力的增强而提高。尽管纤维素聚合度和溶解条件可能存在一些差异,阳离子相同时离子液体对纤维素的溶解度一般具有以下顺序:[(CH3CH2)2PO4]-≈ [OAc]-> [SHCH2COO]->[HCOO]->Cl->Br-≈[SCN]-,这与上述阴离子的氢键形成能力是一致的。
离子液体是由阴阳离子共同组成的,阳离子对离子液体的黏度、熔点以及阴离子的扩散性能有着重要的影响,因此阳离子也会通过影响离子液体的理化性质对纤维素的溶解产生间接影响[11]。SUN等[10]研究发现,1-Cn-3-甲基咪唑氯盐型离子液体中,当n为奇数时,这类离子液体几乎不能溶解纤维素,而当n为偶数时,溶解纤维素能力很强,这说明阳离子对于纤维素的溶解也有非常重要的影响。综合起来,纤维素在离子液体中溶解和再生过程可以用图1来描述[15]。在纤维素分子中存在着大量的羟基,他们相互结合形成氢键,使得纤维素具有致密的结晶结构。离子液体1-烯丙基-3-甲基咪唑氯盐([Amim]Cl)中的 Cl-有较强的成键能力,可以破坏纤维素分子间的氢键打开纤维素分子链,从而使其溶解[15]。向纤维素的离子液体溶液中加入适量的再生剂,比如水,纤维素就会从溶液中再生出来。
除了改变离子液体的结构,加入助溶剂也可以显著提高离子液体对纤维素的溶解能力。XU等[16]研究发现向离子液体 1-丁基-3-甲基咪唑乙酸盐([Bmim]OAc)中加入一定比例的LiCl、LiOAc、LiNO3或LiBr可以显著提高离子液体对纤维素的溶解度,这可能是由于 Li+可以与一部分纤维素羟基中的氧发生作用,从而破坏纤维素分子间的氢键。RINALDI[17]发现,向离子液体[Bmim]Cl、1-乙基-3-甲基咪唑乙酸盐([Emim]OAc)中加入一定量的助溶剂二甲基亚砜(DMSO)、1,3-二甲基-2-咪唑啉酮(DMI)或二甲基甲酰胺(DMF),不但可以在缩短溶解时间的而且可以降低溶解所需温度。XU等[18]证明离子液体[Bmim]OAc和助溶剂DMSO按照一定比例组成的混合溶剂可以在室温条件下溶解高达9%的微晶纤维素,甚至可以在室温下溶解脱脂棉等高聚合度的纤维素,这可能是由于一定量的DMSO可以与阳离子作用释放出更多“自由”的乙酸根离子,从而更容易打破纤维素分子内的氢键。此外,超声辅助和微波加热都有助于提高纤维素的溶解度[11,13]。
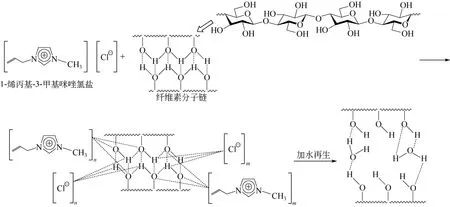
图1 纤维素在[Amim]Cl中溶解过程[1,15]
1.2 离子液体溶解木质素
木质素的组成结构比较复杂,生物质的种类不同,提取工艺不同,获得的木质素组成结构会存在较大的差异[19-22]。利用具有代表性的碱木质素作为模型木质素进行的溶解实验发现,一些常用于纤维素溶解的离子液体,包括[Amim]Cl、[Bmim]Cl和[Emim]OAc在较为温和的条件下就可以溶解 10%以上的碱木质素[23]。一些离子液体,例如[MMIM][MeSO4]和[BMIM][CF3SO3]虽然不能溶解纤维素,却可以溶解高达30%的碱木质素[24]。此外还有多种可以选择性溶解木质素而不溶解纤维素的离子液体,这将在第4部分进行详细探讨。
1.3 离子液体溶解木质纤维素类生物质
离子液体不仅能够溶解纤维素、木质素等生物大分子,也有可能直接溶解木质纤维素材料。FORT等[25]利用碳谱核磁对木材在[Bmim]Cl中溶解形成的溶液进行分析,发现可以同时检测到纤维素、半纤维素和木质素的核磁信号,且溶液中纤维素和木质素的比例与生物质自身的组成接近,表明[Bmim]Cl可以同时溶解纤维素、半纤维素和木质素。SUN等[26]的研究表明,[Emim]OAc在相同条件下对木粉的溶解效果优于[Bmim]Cl,在进行充分的球磨之后,无论是软木还是硬木都能够达到90%以上的溶解率。
离子液体对生物质具有很强的溶解能力,因而被广泛用于生物质的预处理[27-31]。在一定条件下,利用离子液体溶解生物质材料,经过一段时间后加入水等再生剂使生物质材料析出,过滤即可得到生物质材料,而滤液通过蒸馏、萃取等方法回收离子液体。经过离子液体预处理的生物质材料,能够显著破坏木质纤维素材料的结构,结构变得疏松,纤维素的聚合度和结晶度都有一定程度的下降,便于进行后续降解转化。利用离子液体处理木质纤维素类生物质材料与蒸汽爆破、酸碱预处理相比,条件更加温和,有毒有害物质的使用量显著减少,减少了对酶的毒害作用从而有利于后续的酶解处理。LI等[27]利用离子液体 1-乙基-3-甲基二乙基磷酸盐(1-ethyl-3-methylimidazolium diethyl phosphate)预处理稻草秸秆后再进行酶解,发现还原糖的产率显著提高。LEE等[28]利用离子液体[Emim]OAc对蔗渣进行预处理使得蔗渣的粒度变小,表面积增大了 100倍,再用纤维素酶进行水解,24h内还原糖产率达到了 90%以上。MONIRUZZAMAN等[29]利用[Emim]OAc在80℃条件下处理木粉1h,木材的组成基本不发生变化,但却使其结构更加疏松,再利用漆酶降解木质素时效率大幅提高。综上所述,利用离子液体对木质纤维素类生物质进行溶解和再生处理之后,无论是对纤维素酶降解纤维素还是漆酶降解木质素,都有非常显著的促进作用。
2 生物质组分分离的基本方式
在木质纤维素类生物质中,纤维素、半纤维素和木质素在复杂的物理缠绕和氢键、范德华力等化学作用下形成了十分复杂的结构。图2显示了木质纤维素的简化结构,纤维素镶嵌在半纤维素和木质素构成的复杂基质中[32]。需要特别指出的是,从木质纤维素的性质和结构出发,生物质的组分分离主要有3种基本方式[32]。第一种方式是“深度解聚”,利用酸性催化剂将生物质水解成低聚糖,木质素转化成溶解态的低聚物,通过加水稀释或化学反应使木质素沉淀析出,即可分别获得易于后续转化的糖类物质和木质素。例如,LUTERBACHER等[33]2014年在Sicence上报道,利用γ-戊内酯(GVL)与稀硫酸可以将玉米秸秆、硬木和软木中的纤维素和半纤维素转化成水溶性的低聚糖,同时木质素也被转化成了分子量较低的片段,反应结束后加入适量的氯化钠或者液态二氧化碳即可以通过相分离回收GVL,再向水溶液中过量加水可以把木质素和糖溶液分开。第二种方式是“去壳”,利用酸或碱的催化反应,使木质素和半纤维素形成可溶解的片段,同时避免纤维素发生剧烈的解聚,最后纤维素保留在生物质的基质中[31],制浆过程就是这种方式的应用。第三种方式是“溶芯”,将纤维素和半纤维素以单糖或低聚物的形式溶解,而将木质素保留在生物质基质中。纤维素和半纤维素都是糖类物质,通过酶或酸催化反应将他们完全水解成小分子糖类物质,便可以实现这种方式的组分分离。当然这只是一种大致的分类,实际应用中由于预处理方式和反应介质有很多,不同方式和介质组合起来构成了多种多样的组分分离方法。
离子液体的组成和功能具有多样性。作为溶剂,一些离子液体能够同时溶解纤维素、半纤维素和木质素,而一些离子液体对这3种物质的溶解是有选择性的。离子液体也可以作为纤维素和半纤维素水解成糖的反应介质。因此,以上3种生物质组分分离的方式都可以应用离子液体。下文主要从纤维素提取、木质素提取以及离子液体介质中生物质的降解3个角度来讨论生物质的组分分离。

图2 生物质组分分离的基本方式[32]
3 离子液体提取生物质中的纤维素
离子液体对纤维素、半纤维素和木质素的溶解特性是不同的。在生物质处理领域应用最多的是由二烷基咪唑阳离子和具有较强氢键形成能力的阴离子组成的离子液体,这类离子液体既可以溶解纤维素,又可以溶解半纤维素和木质素。虽然这类离子液体在溶解木质纤维素类生物质的过程中对纤维素和木质素没有显著的选择性,但是加入助溶剂或者再生剂可以显著改变体系的溶解特性。基于纤维素比木质素更容易被沉淀出来的性质,可以利用这类离子液体来提取木质素。这种纤维素提取方式可以用图3(a)来表示,即在加热和搅拌条件利用离子液体将生物质中的纤维素和木质素同时溶解,过滤去除不溶解的物质,然后加入能够选择性沉淀纤维素而使木质素保持溶解状态的沉淀剂,这样就获得了纤维素。另外,向滤液中加入合适的沉淀剂还可以获得一部分木质素。
早期的研究采用纤维素和碱木质素的混合物来模拟生物质材料,利用离子液体进行纤维素的选择性分离。LATEEF等[34]离子液体1-(2-氰乙基)-3-甲基咪唑嗅盐([Cymim]Br)、1-丙基-3-甲基咪唑溴盐([Pmim]Br)和[Bmim]Cl对木质素和纤维素的混合物进行了溶解,首先以水为沉淀剂使纤维素再生出来,然后再向离子液体-水混合体系中加入乙醇使木质素再生出来,从而使纤维素和木质素得以分离。但实际上,生物质材料中存在着复杂的结构,并不是纤维素、半纤维素和木质素的简单物理混合。FORT等[25]利用[Bmim]Cl溶解木屑,并采用丙酮/水、二氯甲烷或乙腈作为沉淀剂来再生溶解的生物质,他们发现再生产物是纯度较高的纤维素,纤维素的提取率高达60%。JIANG等[35]采用蒸汽爆破法去除了稻草秸秆中的半纤维素,再使用离子液体[Amim]Cl在40~60℃提取出了生物质材料的纤维素。WANG等[36]采用[Amim]Cl/DMSO(质量比84∶16)溶解木材,以DMSO和水的混合物为沉淀剂,提取出的纤维素纯度达到 85%。王雁南等[37]利用NaOH对结缕草进行活化,再利用离子液体[Amim]Cl可以提取出60%左右的纤维素。LI等[15]研究了用高温水对草进行预处理,再利用[Amim]Cl/DMSO提取出了71%的纤维素。CASAS等[38]采用离子液体[Amim]Cl溶解桉木和松木,溶解后加入3倍质量的DMSO降低溶液黏度,过滤去除未溶解的生物质,再向滤液中加水获得纤维素,纤维素的提取率为16%和11%。经过离子液体提取的纤维素,聚合度和结晶度都有显著下降,而表面积增大,从而有利于酶解和其他方式的降解转化。
上述使用离子液体直接提取生物质中纤维素的过程都使用了助溶剂DMSO,可以推断DMSO、离子液体和再生剂组成的混合体系可能会对木质素和半纤维素都有一定的溶解能力,因而从混合体系中析出的是纯度较高的纤维素。本文作者采用离子液体BMIMOAc 和助溶剂DMI组成溶剂系统来提取谷壳中的多糖,也发现了类似的现象[39]。通过对比未被溶解的剩余材料和原始的生物质,发现二者的组成没有显著差别,说明该溶剂体系本身对于木质素和多糖的溶解是没有选择性的。再生产物中主要是由纤维素等多糖组成的,其中纤维素含量显著高于原始的生物质,表明再生过程中纤维素更容易被沉淀出来,而木质素倾向于溶解在含有离子液体、助溶剂和再生剂的混合体系中。
ABE等[40]合成了一系列由 1-烷基-3-甲基咪唑阳离子和烷基磷酸阴离子构成的低黏度、强极性的离子液体。他们利用这类离子液体在较为温和的条件下溶解糠,过滤除去未溶解的固体,向溶液中加入过量乙醇,就可以将离子液体提取出的多糖沉淀出来。利用该方法在25℃和50℃条件下分别可以提取出糠中14%和42%的多糖。与木质纤维素类生物质相比,糠的结构相对简单且含有较多易溶解的淀粉,因此提取其中多糖比较容易实现。随后,ABE等[41]还利用四正丁基氢氧化膦的水溶液(含有40%的水)在25℃条件下溶解白杨木,利用甲醇做再生剂,可以提取出杨木中37%的多糖。水的含量对于提取效果有很大的影响,含有40%的离子液体溶液可以提取出最大量的多糖,而水升高或降低都会导致提取量降低。由于该方法所用溶剂本身就含有水,生物质就可以采用自然干燥而不需要使用高能耗的加热干燥,甚至可以直接使用湿的生物质。在使用湿生物质时,在25℃处理1h就提取出32%的多糖。离子液体溶液处理湿生物质后含水量会增加,但是自然放置就可以使其含水量逐渐复原。离子液体溶液的含水量还会影响纤维素和半纤维素的溶解度,实验发现含水量为30%时,木聚糖几乎不溶解,提高含水量到40%,木聚糖的溶解度仍然很低,只有含水量为50%或者更高时才能大量溶解木聚糖,因此通过控制离子液体溶液中的含水量就可以调控提取物的组成。当含水量为40%,提取物主要是由纤维素组成。当含水量为70%,提取物的主要成分是木聚糖。将再生剂由甲醇替换为水,可以选择性地获得纤维素。YAMADA等[42]研究发现,四正丁基氢氧化膦的水溶液也具有溶解木质素的能力,而且无论是在室温还是 121℃条件下四正丁基氢氧化膦的水溶液对柳杉中木质素的溶解速率都高于碳水化合物。这表明,室温条件下利用四正丁基氢氧化膦水溶液提取生物质中纤维素,仍然是基于沉淀剂易于把纤维素沉淀出来,而不是离子液体对纤维素的选择性溶解。
尽管在适当的条件下纤维素和碱木质素在离子液体溶解度分别可以达到25%和50%以上,但即使生物质添加量只有 5%,离子液体也不能将他们完全溶解分离。利用离子液体提取木质纤维素类生物质中纤维素和木质素时离子液体也不能将它们完全分离,这可能是由木质纤维素的复杂结构决定的。WANG等[43]采用小角中子散射研究了柳枝稷在离子液体[Bmim]Cl中形成的溶液,并采用纤维素、半纤维素和木质素组成混合物模拟了柳枝稷的组成进行对比研究。他们发现溶解过程中柳枝稷溶液中仍然存在着网状结构,表明离子液体的溶解不能完全破坏天然生物质中纤维素、半纤维素和木质素的之间的物理缠绕和化学键。因此可以推测,在不发生化学反应的条件下,单纯离子液体的溶解作用不能将糖水化合物和木质素完全分离。此外,向离子液体中加入DMSO之后,离子液体和DMSO的回收也比较困难。因此,未来应该尽量开发低成本、低黏度、安全无毒、热稳定性好、适用范围广、能够在室温或较为温和条件下溶解提取纤维素的离子液体,从而减少助溶剂的使用并降低离子液体的使用成本。
4 离子液体提取生物质中的木质素
如前文所述,能够溶解纤维素的离子液体大部分都可以在溶解纤维素的同时溶解木质素,因此将它们简称为非选择性离子液体。利用非选择性离子液体提取生物质中木质素的过程与图3(a)描述的纤维素提取过程是类似的,区别在于木质素的提取不需要将未溶解的生物质过滤出去。在利用离子液体溶解生物质之后,直接加入沉淀剂使木质素保持溶解状态,将析出的纤维素和未溶解的生物质过滤出去,再通过蒸馏、酸碱中和以及加入沉淀剂等方法就可以获得木质素。对于具有选择性溶解木质素能力的离子液体,纤维素在其中的溶解度很低,可以称他们为选择性离子液体。如图3(b)所示,利用这些离子液体可以直接将生物质中的木质素溶出,过滤后加入沉淀剂就可以获得木质素。另外,非选择性离子液体与水等组成的混合物一般情况下仍然具有溶解木质素而不溶解纤维素的能力,因此也可以起到类似选择性离子液体的提取效果。
4.1 非选择性离子液体
离子液体的组成结构、生物质的种类和溶解条件对于生物质溶解有着较大的影响,但对于非选择性离子液体来说决定提取物组成的关键因素是沉淀剂。表1列出了部分利用离子液体提取生物质中木质素的效果。SUN等[26]发现体积比1∶1的丙酮和水混合物可以溶解与碳水化合物之间没有化学键连接的木质素。因此他们采用体积比1∶1的丙酮和水混合物作为沉淀剂,使木质素溶解在丙酮和水组成的混合溶剂中而纤维素析出,过滤纤维素后通过蒸馏丙酮可以析出部分木质素,再用稀盐酸调节 pH到2~3,一共可以得到松木中31%的木质素。SUN等[10]还尝试使用多金属氧化物作为催化剂来打破糖类和木质素之间的共价键,使木质素的提取率有所提高。随后,WANG等[21]采用微波加热的方式进行木质素提取,他们发现微波加热可以有效缩短溶解时间,木质素提取率也有所增加。LEE等[44]使用离子液体溶解生物质材料后,加入0.1mol/L的氢氧化钠溶液使木质素保持溶解状态,固液分离后再通过加盐酸调节pH使木质素析出。尽管[Mmim][MeSO4]和[Bmim][CF3SO3]可以在温和条件下溶解高达30%的碱木质素,但在用来溶解生物质时却只能提取出不到 10%的木质素,而相同条件下[Amim]Cl和[Emim]OAc分别可以提取出60%和51%的木质素。
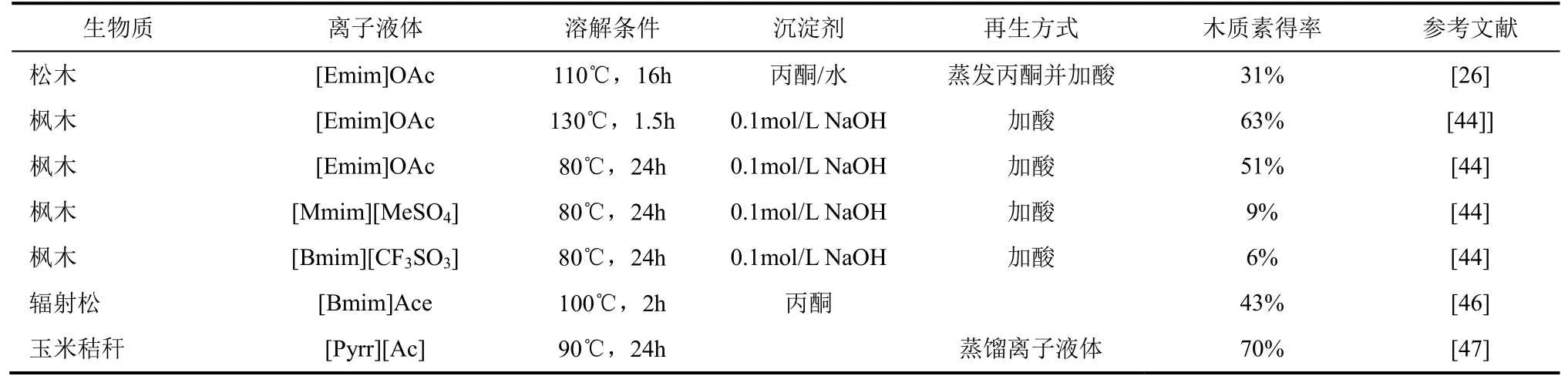
表1 生物质中木质素的提取
HOU 等[45]以胆碱和氨基酸为原料制备了一类离子液体,这类离子液体可以提取出生物质中40%~60%的离子液体。与咪唑类离子液体相比,这类离子液体可以使用可再生的原料制备,成本较低,而且易于生物降解,因此是一类更加环境友好的离子液体,具有大规模应用的潜能。利用非选择性离子液体提取木质素是有很多不足的,在碳水化合物再生阶段需要使用有机溶剂或碱溶液使木质素保持溶解状态,木质素再生阶段需要加入过量的酸以便使木质素完全析出,这就无法避免有机溶剂和含盐废水的污染。此外,从含有盐和离子液体的水溶液中回收离子液体也是很困难的。
4.2 选择性的离子液体
使用专一溶解木质素的离子液体,可以实现生物质中木质素的选择性提取。PINKERT等[46]利用安赛蜜(Kace)与离子液体[Bmim]Cl进行离子交换反应,制备了离子液体[Bmim]Ace,该离子液体可以溶解木质素而不能溶解纤维素。他们利用[Bmim]Ace选择性地溶解生物质中的木质素,溶解后过滤得到的滤液就是木质素的离子液体溶液,向溶液中加入过量的丙酮就可以使木质素析出。该过程可以提取出43%的木质素,加入助溶剂可以将提取率提高到60%。该方法的优势是不需要使用酸进行木质素的沉淀,同时对纤维素的结晶度破坏很小,得到富含纤维素的剩余物有应用到材料领域的潜能。
ACHINIVU等[47]以 N-甲基咪唑、吡啶、吡咯与乙酸通过一步反应制得 3种质子型离子液体[Py]OAc、[Mim]OAc和[Pyrr]OAc。这3种离子液体可以溶解50%以上的碱木质素,而纤维素的溶解度在 1%以下。利用[Pyrr]OAc在 90℃条件下溶解24h可以提取出玉米秸秆中70%以上的木质素,通过简单的过滤即可得到富含纤维素的材料。滤液通过减压蒸馏可以使离子液体分解,蒸馏气体冷却后重新反应得到离子液体,剩余固体即为木质素。同时他们还发现,离子液体对木质素的提取效率与木聚糖在离子液体中的溶解度有正相关关系。导致这一现象的可能原因是离子液体对半纤维素的溶解可以促使它接触到木质纤维素结构内部的木质素,因而可以促进木质素的提取。
4.3 混合溶剂
除了单纯的离子液体,利用酸性离子液体和水等组成的混合溶剂也可以从生物质中提取出木质素。适量的水有助于酸性离子液体催化生物质中糖类和木质素之间连接键的断裂,从而达到分离木质素的目的。BRANDT 等[48-49]利用离子液体[C4mim][HSO4]和水的混合物在 120℃条件下处理芒草 13h,提取出了 50%左右的木质素。LONG等[50]采用体积比80/20的乙醇和水混合物为溶剂,以酸性离子液体[C2H4COOHmim]Cl、[Bmim]HSO4,[mim]HSO4和[C4H8SO3Hmim]HSO4为催化剂在高温(200~240℃)下对蔗渣进行处理,可以提取出55.4%~100%的木质素。采用离子液体作为催化剂时需要特别注意的是离子液体的热稳定性,尽管热重分析得出的常见离子液体的热分解温度一般都在200℃以上,但这只是短期的热分解温度,长期使用条件下这些离子液体很容易降解而造成损失[51]。
4.4 离子液体和再生剂的回收利用
PRADO 等[52]研究了在提取木质素过程离子液体 1-丁基-3-甲基咪唑甲基硫酸盐的重复利用效果。实验结果表明该离子液体在前三次重复使用过程中保持结构不变同时也具有恒定的木质素提取能力,而在第四次重复使用时该离子液体对木质素的提取能力明显下降,这可能是由于离子液体被木质素污染所导致的。他们利用氢谱核磁分析证实了这个推断。
理论上来说,通过蒸馏和萃取回收离子液体和再生剂,但在实际生产中这可能会产生较高的成本。SATHITSUKSANOH等[53]在利用离子液体[Bmim]Cl对柳枝稷进行溶解时,使用1-辛醇作为再生剂,发现1-辛醇可以有效地将离子液体溶解的木质素沉淀出来,而且它与离子液体可以发生两相分离,因而很容易回收离子液体和再生剂。他们的实验结果表明,使用该方法离子液体在经过三次重复使用后仍然保持较好的提取效果。这种离子液体再生方法简单方便,很有应用前景。
5 离子液体介质中生物质的降解分离
利用离子液体对生物质的溶解能力,可以更容易地将生物质中的组分降解成可溶解的单体或低聚物,也是分离生物质组分的重要方法。纤维素和半纤维素的降解主要是酸催化的水解反应,产物主要是水溶性的糖类物质。
在利用溶解生物质后,加入酸作为催化剂,直接将生物质中纤维素和半纤维素水解为小分子糖类也是将碳水化合物与木质素分离的有效途径。BINDER等[54]首先利用离子液体[Emim]Cl充分溶解玉米秸秆,然后逐步加入盐酸和水使纤维素和半纤维素水解,可以获得玉米秸秆70%~80%的糖。在进行水解反应之前,首先在加热和搅拌下将生物质在离子液体中溶解一段时间,溶解过程可以有效打破纤维素的结晶结构,有助于后续的水解反应。在水解阶段,水的添加对于产物选择性十分重要。加水量过高会导致生物质沉淀析出,含水量过低则生成的糖类物容易发生脱水和聚合反应形成糠醛、5-羟甲基糠醛和胡敏素等副产物。他们还采用带电的离子交换树脂来将糖和离子液体分离,获得可回收的离子液体和易于后续处理的糖溶液。SUN等[55]采用[Bmim]Cl和类似的方法水解生物质,葡萄糖和木糖的产率分别为53%和88%。在水解完成后,通过向溶液中加入适量的NaOH溶液,含有糖和盐的水溶液会与离子液体形成两相分离,从而可以将离子液体和糖类分离开来。该方法需要使用大量的酸和碱,可能会产生较多的含盐废水。
纤维素的水解还可以在固体酸的催化下进行,但目前还没见到在离子液体介质中使用固体酸直接催化生物质水解的报道[56-57]。此外,还可以通过氧化使生物质中产生羧基,氧化态的生物质具有一定的催化性能,可以催化自身的水解。ZHOU等[58]在210℃条件下利用空气来氧化纤维素,氧化48h后,在150℃和无外加催化剂的条件下进行水解,经过8h获得了23.3%的葡萄糖产率。KOBAYASHI等[59]将桉木在空气和一定温度下碳化,获得碳基催化剂与桉木混合球磨后在水中进行水解,可以获得78%~82%的葡萄糖和89%~94%的木糖。这些反应都是在水中进行的,如果这些反应能够在离子液体中进行,有可能缩短反应时间并获得更高的产率。
需要特别指出的是,无论是木质素的提取,还是纤维素的提取,半纤维素都可能发生降解并进入到各个过程的液相中,同时部分半纤维素可能与木质素一起析出,部分半纤维素可能与纤维素一起析出,还有一部分存在于剩余材料中。但是半纤维素比较容易发生水解,高温水、稀酸和酶都可以很方便地将它们从木质素或纤维素上分离下来。基于上述原因,大部分文献报道中对于半纤维素的归类并没有做深入的分析,因此对于半纤维素的提取也没有做过多的区分。
6 结 论
离子液体可以溶解大量纤维素和木质素,而且可以选择性地从天然的木质纤维素类生物质中提取出纤维素和木质素。离子液体提取出的纤维素结构疏松,易于进行降解转化,离子液体提取出的木质素也有生产高附加值产品的潜能。利用离子液体作为溶剂或催化剂先进行生物质降解转化再进行组分分离也是一条有效途径。然而,无论是利用离子液体作为反应介质直接进行木质素和纤维素的提取,还是在离子液体中进行生物质的降解,都面临着离子液体成本高、难以回收等问题。因此,构建低成本、低黏度、选择性强的新型离子液体以及具有溶解和催化双重作用的功能化离子液体仍是未来研究的重点[60-61]。离子液体的应用,要和生物质预处理技术、超临界二氧化碳等绿色溶剂和新型催化剂充分结合,发展出高效率、低能耗和低污染的生物质组分分离和降解转化工艺。
[1] 李维尊. 咪唑类离子液体对生物质中木质纤维素选择性提取及分离[D]. 天津:南开大学,2013.
[2] HUANG R-J,ZHANG Y,BOZZETTI C,et al. High secondary aerosol contribution to particulate pollution during haze events in China[J]. Nature,2014,514(7521):218-22.
[3] 张智峰. 纤维素改性研究进展[J]. 化工进展,2010,29(08):1493-1501.
[4] TUCK C O. Valorization of biomass:deriving more value from waste[J]. Science,2012,338(6107):604-604.
[5] 高美香,刘宗章,张敏华. 生物质转化制糠醛工艺的研究进展[J].化工进展,2013,32(4):878-884.
[6] RAGAUSKAS A J,BECKHAM G T,BIDDY M J,et al. Lignin valorization:improving lignin processing in the biorefinery[J]. Science,2014,344(6185):709-719.
[7] 邱学青,楼宏铭,杨东杰,等. 工业木质素的改性及其作为精细化工产品的研究进展[J]. 精细化工,2005,22(3):161-167.
[8] 刘纲勇,邱学青,邢德松. 工业木质素在木材胶粘剂中应用的研究进展[J]. 精细化工,2007,24(2):190-193.
[9] 石起增,杨光瑞,刘巧茹. 木质素在人造板胶黏剂中的应用[J]. 化工进展,2005,24(5):502-505.
[10] SUN N,RODRIGUEZ H,RAHMAN M,et al. Where are ionic liquid strategies most suited in the pursuit of chemicals and energy from lignocellulosic biomass?[J]. Chemical Communications,2011,47(5):1405-1421.
[11] WANG H,GURAU G,ROGERS R D. Ionic liquid processing of cellulose[J]. Chemical Society Reviews,2012,41(4):1519-1537.
[12] 李昌志,王爱琴,张涛. 离子液体介质中纤维素资源转化研究进展[J]. 化工学报,2013,64(1):182-197.
[13] SWATLOSKI R P,SPEAR S K,HOLBREY J D,et al. Dissolution of cellulose with ionic liquids[J]. Journal of the American Chemical Society,2002,124(18):4974-4975.
[14] MOULTHROP J S,SWATLOSKI R P,MOYNA G,et al. High-resolution13C NMR studies of cellulose and cellulose oligomers in ionic liquid solutions[J]. Chemical Communications,2005(12):1557-1559.
[15] LI W Z,JU M T,WANG Y N,et al. Separation and recovery of cellulose from Zoysia japonica by 1-allyl-3-methylimidazolium chloride[J]. Carbohydrate Polymers,2013,92(1):228-235.
[16] XU A,WANG J,WANG H. Effects of anionic structure and lithium salts addition on the dissolution of cellulose in 1-butyl-3-methylimidazolium-based ionic liquid solvent systems[J]. Green Chemistry,2010,12(2):268-275.
[17] RINALDI R. Instantaneous dissolution of cellulose in organic electrolyte solutions[J]. Chemical Communications,2011,47(1):511-513.
[18] XU A,ZHANG Y,ZHAO Y,et al. Cellulose dissolution at ambient temperature:role of preferential solvation of cations of ionic liquids by a cosolvent[J]. Carbohydrate Polymers,2013,92(1):540-544.
[19] SATHITSUKSANOH N,HOLTMAN K M,YELLE D J,et al. Lignin fate and characterization during ionic liquid biomass pretreatment for renewable chemicals and fuels production[J]. Green Chemistry,2014,16(3):1236-1247.
[20] 王垫. 木质生物质预处理,组分分离及酶解糖化研究[D]. 北京:北京林业大学,2011.
[21] WANG H,MAXIM M L,GURAU G,et al. Microwave-assisted dissolution and delignification of wood in 1-ethyl-3-methylimidazolium acetate[J]. Bioresource Technology,2013,136:739-742.
[22] 郑大锋,邱学青,楼宏铭. 木质素的结构及其化学改性进展[J]. 精细化工,2005,22(4):249-252.
[23] ZAKZESKI J,JONGERIUS A L,BRUIJNINCX P C A,et al. Catalytic lignin valorization process for the production of aromatic chemicals and hydrogen[J]. ChemSusChem,2012,5(8):1602-1609.
[24] PU Y,JIANG N,RAGAUSKAS A J. Ionic liquid as a green solvent for lignin[J]. Journal of Wood Chemistry and Technology,2007,27(1):23-33.
[25] FORT D A,REMSING R C,SWATLOSKI R P,et al. Can ionic liquids dissolve wood? Processing and analysis of lignocellulosic materials with 1-n-butyl-3-methylimidazolium chloride[J]. Green Chemistry,2007,9(1):63-69.
[26] SUN N,RAHMAN M,QIN Y,et al. Complete dissolution and partial delignification of wood in the ionic liquid 1-ethyl-3-methylimidazolium acetate[J]. Green Chemistry,2009,11(5):646-655.
[27] LI Q,HE Y C,XIAN M,et al. Improving enzymatic hydrolysis of wheat straw using ionic liquid 1-ethyl-3-methyl imidazolium diethyl phosphate pretreatment[J]. Bioresource Technology,2009,100(14):3570-3575.
[28] SANT'ANA DA SILVA A,LEE S H,ENDO T,et al. Major improvement in the rate and yield of enzymatic saccharification of sugarcane bagasse via pretreatment with the ionic liquid 1-ethyl-3-methylimidazolium acetate ([Emim] [Ac])[J]. Bioresource Technology,2011,102(22):10505-10509.
[29] MONIRUZZAMAN M,ONO T. Separation and characterization of cellulose fibers from cypress wood treated with ionic liquid prior to laccase treatment[J]. Bioresource Technology,2013,127:132-137.
[30] 侯雪丹. 用[胆碱][氨基酸]离子液体预处理木质纤维素生物质的研究[D]. 广州:华南理工大学,2013.
[31] 陈龙. 基于离子液体的木质纤维素预处理和转化过程的基础研究[D]. 广州:华东理工大学,2014.
[32] RINALDI R. Plant biomass fractionation meets catalysis[J]. Angewandte Chemie:International Edition,2014,53(33):8559-8560.
[33] LUTERBACHER J S,RAND J M,ALONSO D M,et al. Nonenzymatic sugar production from biomass using biomass-derived gamma-valerolactone[J]. Science,2014,343(6168):277-280.
[34] LATEEF H,GRIMES S,KEWCHAROENWONG P,et al. Separation and recovery of cellulose and lignin using ionic liquids:a process for recovery from paper-based waste[J]. Journal of Chemical Technology and Biotechnology,2009,84(12):1818-1827.
[35] JIANG M,ZHAO M,ZHOU Z,et al. Isolation of cellulose with ionic liquid from steam exploded rice straw[J]. Industrial Crops and Products,2011,33(3):734-738.
[36] WANG X,LI H,CAO Y,et al. Cellulose extraction from wood chip in an ionic liquid 1-allyl-3-methylimidazolium chloride (AmimCl)[J]. Bioresource Technology,2011,102(17):7959-7965.
[37] 王雁南,鞠美庭,李维尊,等. 离子液体 AMIMCl 对碱液活化的结缕草纤维素的提取与再生[J]. 化工进展,2013,32(2):470-474.
[38] CASAS A,ALONSO M V,OLIET M,et al. Characterization of cellulose regenerated from solutions of pine and eucalyptus woods in 1-allyl-3-methilimidazolium chloride[J]. Carbohydrate Polymers,2013,92(2):1946-1952.
[39] HOU Q,LI W,JU M,et al. Separation of polysaccharides from rice husk and wheat bran using solvent system consisting of BMIMOAc and DMI[J]. Carbohydrate Polymers,2015,133:517-523.
[40] ABE M,FUKAYA Y,OHNO H. Extraction of polysaccharides from bran with phosphonate or phosphinate-derived ionic liquids under short mixing time and low temperature[J]. Green Chemistry,2010,12(7):1274-1280.
[41] ABE M,YAMADA T,OHNO H. Dissolution of wet wood biomass without heating[J]. RSC Advances,2014,4(33):17136-17140.
[42] YAMADA H,MIYAFUJI H,OHNO H,et al. A simple method for separating lignin and carbohydrates from softwood biomass in a glass tube using tetra-n-butylphosphonium hydroxide[J]. BioResources, 2015,11(1):839-849.
[43] WANG H,GURAU G,PINGALI S V,et al. Physical insight into switchgrass dissolution in ionic liquid 1-ethyl-3-methylimidazolium acetate[J]. ACS Sustainable Chemistry and Engineering,2014,2(5):1264-1269.
[44] LEE S H,DOHERTY T V,LINHARDT R J,et al. Ionic liquid-mediated selective extraction of lignin from wood leading to enhanced enzymatic cellulose hydrolysis[J]. Biotechnology and Bioengineering,2009,102(5):1368-1376.
[45] HOU X D,SMITH T J,LI N,et al. Novel renewable ionic liquids as highly effective solvents for pretreatment of rice straw biomass by selective removal of lignin[J]. Biotechnology and Bioengineering,2012,109(10):2484-2493.
[46] PINKERT A,GOEKE D F,MARSH K N,et al. Extracting wood lignin without dissolving or degrading cellulose:investigations on the use of food additive-derived ionic liquids[J]. Green Chemistry,2011,13(11):3124-3136.
[47] ACHINIVU E C,HOWARD R M,LI G,et al. Lignin extraction from biomass with protic ionic liquids[J]. Green Chemistry,2014,16(3):1114-1119.
[48] BRANDT A,RAY M J,TO T Q,et al. Ionic liquid pretreatment of lignocellulosic biomass with ionic liquid-water mixtures[J]. Green Chemistry,2011,13(9):2489-2499.
[49] HOU X D,LI N,ZONG M H. Renewable bio ionic liquids-water mixtures-mediated selective removal of lignin from rice straw:visualization of changes in composition and cell wall structure[J]. Biotechnology and Bioengineering,2013,110(7):1895-1902.
[50] LONG J,LI X,GUO B,et al. Catalytic delignification of sugarcane bagasse in the presence of acidic ionic liquids[J]. Catalysis Today,2013,200(1):99-105.
[51] MATON C,DE VOS N,STEVENS C V. Ionic liquid thermal stabilities:decomposition mechanisms and analysis tools[J]. Chemical Society Reviews,2013,42(13):5963-5977.
[52] PRADO R,ERDOCIA X,LABIDI J. Study of the influence of reutilization ionic liquid on lignin extraction[J]. Journal of Cleaner Production A,2016,111:125-132.
[53] SATHITSUKSANOH N,SAWANT M,TRUONG Q,et al. How alkyl chain length of alcohols affects lignin fractionation and ionic liquid recycle during lignocellulose pretreatment[J]. BioEnergy Research,2015,8(3):973-981.
[54] BINDER J B,RAINES R T. Fermentable sugars by chemical hydrolysis of biomass[J]. Proceedings of the National Academy of Sciences of the United States of America,2010,107(10):4516-4521.
[55] SUN N,LIU H,SATHITSUKSANOH N,et al. Production and extraction of sugars from switchgrass hydrolyzed in ionic liquids[J]. Biotechnology for Biofuels,2013,6(1):39.
[56] HU L,LIN L,WU Z,et al. Chemocatalytic hydrolysis of cellulose into glucose over solid acid catalysts[J]. Applied Catalysis B:Environmental,2015,174:225-243.
[57] HUANG Y B,FU Y. Hydrolysis of cellulose to glucose by solid acid catalysts[J]. Green Chemistry,2013,15(5):1095-1111.
[58] ZHOU L,YANG X,XU J,et al. Depolymerization of cellulose to glucose by oxidation-hydrolysis[J]. Green Chemistry,2015,17(3):1519-1524.
[59] KOBAYASHI H,KAIKI H,SHROTRI A,et al. Hydrolysis of woody biomass by a biomass-derived reusable heterogeneous catalyst[J]. Chemical Science,2016,7(1):692-696.
[60] 李汝雄,王建基. 绿色溶剂——离子液体的制备与应用[J]. 化工进展,2002,21(1):43-48.
[61] 黎汉生,张亚平,吴芹. 负载型离子液体催化剂中离子液体的溶剂效应研究进展[J]. 化工进展,2008,27(11):1736-1742.
Research progress on biomass fractionation using ionic liquids
HOU Qidong,JU Meiting,LI Weizun,LIU Le,YANG Qian,CHEN Yu
(Tianjin Engineering Research Center of Biomass Solid Waste Resources Technology,College of Environmental Science & Engineering,Nankai University,Tianjin 300071,China)
As one of the most abundant renewable resources on the earth,the utilization of lignocellulosic biomass is a promising solution to the resource and energy crisis. However,traditional methods for fractionating biomass have many disadvantages,including low efficiency and high pollution,seriously hindering the conversion of biomass into value-added products. This article gives an overview of the applications of ionic liquids in the fractionation of lignocellulosic biomass,including the separation of cellulose and lignin from biomass using ionic liquids as solvents and the fractionation of biomass through chemical reaction in the media of ionic liquids. The extraction of cellulose and lignin are analyzed from the point of ionic liquid selection,reaction route optimization,biomass pretreatment,dissolution conditions and anti-solvents. The commercial application of fractionation of biomass using ionic liquids is still constrained by the high cost,low efficiency,and secondary pollution. In order to improve the economy and greenness of biomass fractionation,it's very important to design novel ionic liquids with low cost,reduced viscosity,high thermal stability,low toxicity,and commercially viable regeneration methods and to develop environmentally friendly and more efficient biomass fractionation processes.
ionic liquids;biomass;cellulose;lignin;fractionation
TQ 352
A
1000-6613(2016)10-3022-10
10.16085/j.issn.1000-6613.2016.10.003
2016-02-29;修改稿日期:2016-03-18。
天津市科技支撑国际合作项目(13RCGFSF14300),天津市科技支撑科技创新体系及平台建设项目(14TXGCCX00012)及天津市津南区科技计划项目(2015JNKW0005)。
候其东(1991—),男,博士研究生,主要从事生物质固废资源化方向研究工作。联系人:鞠美庭,教授,博士生导师,研究领域为生物质类固体废弃物资源化、环境/生态规划,环境评价与管理,产业生态学,生态城市建设等。E-mail jumeit@nankai.edu.cn。

