干扰素抗病毒治疗小儿乙肝的临床效果分析
申远方
干扰素抗病毒治疗小儿乙肝的临床效果分析
申远方
目的 分析干扰素抗病毒治疗小儿乙肝的临床效果。方法 选择2014年1月~2015年1月本院收治小儿乙肝104例为研究对象,两组均在服用多磷脂酰胆碱的基础上,对照组采用苦参素,给予观察组干扰素a-2b,分析两组HBV-DNA阴转率及肝功能变化情况。结果 在治疗结束1年后HBV-DNA的阴转数7例,阴转率为13.5%;即观察组的阴转率高于对照组,差异有统计学意义(P<0.05);观察组的ALT和TBIL低于对照组,差异有统计学意义(P<0.05)。结论 干扰素抗病毒治疗小儿乙肝具显著效果,并且安全性好。
干扰素;抗病毒;小儿乙肝;临床效果
乙型病毒性肝炎(乙肝),它是通过乙肝性病毒(HBV)所引起的,主要通过肝脏类性质的病变为主体,可导致其它器官受损的疾病[1-2]。乙肝是一种流行病,遍布世界各国各地,主要的侵犯对象是青壮年或者儿童类,严重者可发展为肝癌或者是肝硬化。因此,乙肝疾病已经威胁及影响到人类的健康生活,须行及时的救治。本文对干扰素抗病毒治疗小儿乙肝效果分析,报告如下所述。
1 资料与方法
1.1一般资料
选择2014年1月~2015年1月本院收治小儿乙肝104例为研究对象,男44例,女60例,分为2组,每组均52例。其中观察组年龄3~13岁,平均年龄(7.6±4.3)岁,病程0.7~6年,平均病程(3.6±2.1)年;对照组年龄2~16岁,平均年龄(8.8±5.2)岁,病程0.6~7年,平均病程(4.1±2.8)年。两组患者在临床资料比较,差异无统计学意义(P>0.05)。
1.2方法
两组均在服用多磷脂酰胆碱(0.3~0.5 mg/次,1次/天)用以保肝的基础上,对照组采用苦参素(吉林津升制药有限公司,国药准字:H20031324),250 mg/次,1次/天;给予观察组干扰素a-2b(长春海伯尔生物技术有限责任公司,国药准字:S20070003),通过肌注进行治疗,300万U/次,1次/天。两组均持续6个月的治疗。
1.3观察指标与评定标准
观察两组在6个月的治疗中与在治疗结束1年后乙肝病毒含量(HBV-DNA)阴转率指标;并观察两组患者在治疗前、后的肝功能(转氨酶ALT和总胆红素TBIL)的变化情况。视HBV-DNA阴转为有效指标[3]。
1.4统计学方法
数据采用SPSS20.0统计学软件分析处理,计量资料用(均数±标准差)表示,采用t检验,计数资料用百分比(%)表示,采用χ2检验,P<0.05,差异有统计学意义。
2 结果
2.1比较两组HBV-DNA的阴转率
观察组在6个月的治疗中HBV-DNA的阴转数21例,阴转率为40.4%,在治疗结束1年后HBV-DNA的阴转有16例,阴转率为30.8%;对照组在6个月的治疗中HBV-DNA的阴转数11例,阴转率为21.2%,在治疗结束1年后HBV-DNA的阴转数7例,阴转率为13.5%;即观察组的阴转率高于对照组(P<0.05)。
2.2比较两组在治疗前后的肝功能变化情况
观察组的ALT和TBIL低于对照组,差异比较具有统计学意义(P<0.05),见表1。
表1 比较两组患者在治疗前后的肝功能变化情况
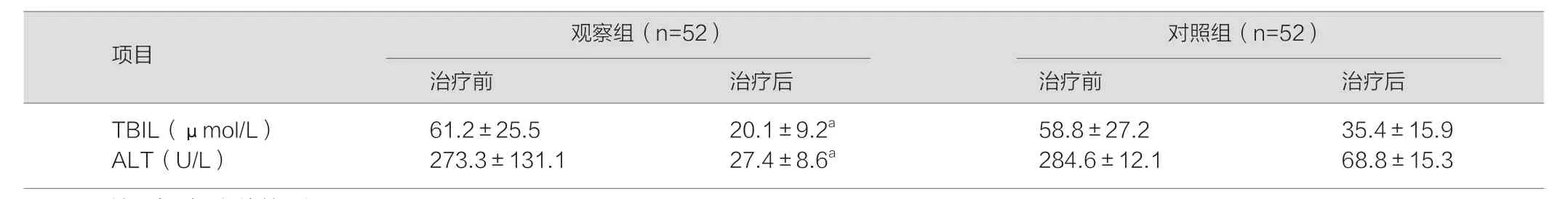
表1 比较两组患者在治疗前后的肝功能变化情况
注:与对照组比较,aP<0.05。
项目观察组(n=52) 对照组(n=52)治疗前 治疗后 治疗前 治疗后TBIL(μm o l/L) 61.2±25.5 20.1±9.2a 58.8±27.2 35.4±15.9 ALT(U/L) 273.3±131.1 27.4±8.6a 284.6±12.1 68.8±15.3
3 讨论
乙型病毒性肝炎属于难治性疾病,由于小儿的免疫系统在发育上尚未完善,较易受乙肝病毒的感染。研究表明,小儿乙肝病患因受到病毒的复制与免疫的不断攻击,致使肝细胞受损,已严重影响了患者的正常发育[4-5]。
研究结果显示,观察组的阴转率高于对照组,及其ALT和TBIL低于对照组,表明干扰素在治疗小儿乙肝的临床效果中具显著效果,并且安全性高。可能的因素是:苦参素为一种生物碱,在发挥抗病毒上具有一定的功效,具有保护肝细胞的作用,同时对机体免疫具有调节作用,但见效缓慢,药效短暂,故治疗效果欠佳。而干扰素为广谱抗病毒的药剂,不是直接性的抑制或杀伤其病毒,主要是经过细胞的表面因受体作用,促使细胞能产生大量的抗病毒蛋白,从而对乙肝病毒具有抑制其复制功能的作用[6-7]。同时,可自然的杀伤细胞、T淋巴细胞及巨噬细胞的活力,因此增强了免疫的调节及抗毒能力的作用,且该药物的半衰期在一般作用下较长,可持续的作用于患者的肝脏部位,在治疗的发挥作用上具有显著效果[8]。本文针对干扰素抗病毒治疗小儿乙肝的临床效果进行分析,因受时间及样本限制,具体结果有待临床进一步的研究。
综上所述,干扰素抗病毒治疗小儿乙肝具显著效果,并且安全性好。
[1]杨莹,谢科峰.儿童乙肝抗体定期检测的必要性分析[J].中国社区医师,2016,18(14):124-125.
[2]林如妹,陈文锋,邹辉祥.阳江市江城区学龄前儿童乙型肝炎病毒感染和免疫预防现状调查[J].中国当代医药,2016,23(2):154-156.
[3]邓智标,黎子辉,麦贤昌.佛山市成人乙型肝炎感染现状分析及对策[J].中国实用医药,2016,11(9):18-19.
[4]黄歆,周莉,牟李红,等.乙型肝炎高危儿免疫预防效果及乙肝病毒母婴传播影响因素分析[J].中国当代儿科杂志,2016,18(5):410-414.
[5]丛占杰,于亚波,王伟,等.1 248例学龄前儿童乙肝病毒感染状况分析[J].中国实验诊断学,2015,19(3):475-477.
[6]易爱芬.干扰素抗病毒治疗小儿乙肝44例临床分析[J].中国社区医师:医学专业,2013,15(9):168.
[7]林秀滨.乙肝患者行干扰素抗病毒治疗后出现不良反应的护理分析[J].中外医学研究,2014,12(21):83-85.
[8]薛闯.39例慢性乙型肝炎抗病毒治疗的临床效果探讨[J].中外医疗,2013,32(18):42.
Clinical Effect Analysis of interferon Antiviral Therapy in Children With Hepatitis B
SHEN Yuanfang Department of Pediatrics, Zhengzhou Children's Hospital,Zhengzhou He'nan 450000, China
Ob jective To analyze the clinical effect of interferon antiviral therapy in children With hepatitis B. Methods From January 2014 to January 2015, 104 cases of children hepatitis B in our hospital were selected as the research subjects. The two groups were all based on the use of multi phosphatidylcholine, the control group was treated With matrine,and the observation group was treated With interferon a-2b, the changes of HBV-DNA negative conversion rate and liver function in two groups were analyzed. Results 7 cases of Yin speed HBV-DNA after 1 years at the end of treatment, the negative rate was 13.5%. The negative rate of observationgroup was higher than that of control group, the difference was statistically significant (P<0.05). The ALT and TBIL of the observation group were lower than the control group, the difference was statistically significant (P<0.05). Conclusion Interferon antiviral treatment of children With hepatitis B has a significant effect, and the security is good.
Interferon, Antiviral, Hepatitis B, Clinical effect
R 725.1
A
1674-9308(2016)27-0146-03
10.3969/j.issn.1674-9308.2016.27.097
郑州市儿童医院儿科,河南 郑州 450000

