核黄素在电化学还原石墨烯/Nafion修饰电极上的电化学行为及分析检测
马 琦,李 坤,张素芳,宋金萍,,郭 永,董 川
(1.山西大同大学化学与环境工程学院,应用化学研究所,山西大同 037009;2.山西大学环境科学研究所,山西太原 030006)
核黄素又称维生素B2,它是异咯嗪的一种衍生物,在生物体内通过与三磷酸腺苷(ATP)反应生成腺嘌呤二核苷酸(FAD),从而参与生物体内的重要代谢活动[1]。当体内核黄素缺乏时,将造成机体代谢障碍,产生口角炎、唇炎、舌炎、结膜炎及阴囊炎等炎症,因而高效灵敏的检测体内的核黄素对于疾病的预防和监测具有重要的意义。目前,常用于检测核黄素的手段主要包括:紫外-可见分光光度法[2]、荧光法[3]、高效液相色谱法[4]及电化学法[5]。其中,电化学方法因高灵敏性、操作方便、价廉等优点已受到研究人员的广泛关注。例如,唐平等[6]研究了核黄素在裸金电极及分子自组装膜电极上的电化学行为,检出限可达10-7mol数量级。同时一些研究结果已经显示:纳米材料的引入会极好地提高核黄素检测的灵敏度。例如Fe2O3/MWCNTs/AuNPs复合材料可以检测nmol数量级的核黄素[7]。
作为继富勒烯和碳纳米管之后的另一个新型碳材料,石墨烯因其优良的电子传输性能、超大比表面积、高机械强度等特性已吸引了广大研究者的关注,并在电催化领域中显示了其独特的魅力。孙红力等[8]采用水合肼还原氧化石墨烯的方法制得石墨烯材料,随后用石墨烯/Nafion膜修饰电极测定了核黄素,但检出限只能达到1.0×10-6mol·L-1。倪永年等[9]利用聚脱氧腺苷酸将石墨烯固定在金电极表面,其对核黄素检测的检出限可达1.5×10-8mol·L-1。本文主要研究电化学还原石墨烯和Nafion复合材料修饰的玻碳电极上核黄素的电化学性质。与水合肼还原石墨烯相比[8],电化学还原石墨烯能够极大增强核黄素的电化学响应信号,使分析检出能力提高。
1 实验部分
1.1 仪器与试剂
电化学测量在CHI660 E电化学工作站(上海辰华仪器有限公司)上进行,以玻碳电极(直径为3 mm)为工作电极,饱和甘汞电极为参比电极,铂柱电极为对电极组成三电极系统。
石墨粉购自Alfa Aesar,采用Hummers方法[10]制备氧化石墨烯(GO),用水分散成1 mg/mL悬浮液备用。5%Nafion乙醇溶液购自Fluka。核黄素、维生素B1、维生素B6、烟酸、烟酰胺、尿酸、维生素C、色氨酸、多巴胺等均购自阿拉丁试剂公司,使用时配成1.0×10-3mol·L-1的储备液并保存于暗处。其它试剂均购自北京化工厂。所用试剂均为分析纯,使用前未被纯化。实验用水皆为二次蒸馏水。
1.2 修饰电极的制备
玻碳电极在使用前依次用粒径为1.0、0.3、0.05 μm 的Al2O3水糊打磨成镜面,经超声波清洗,再经乙醇洗涤后,备用。准确移取2 mL 500 μg/mL GO水溶液,加入200 μL 5%Nafion乙醇溶液,超声分散5 min,得GO/Nafion修饰液。用微量进样器均匀滴加6 μL上述GO/Nafion修饰液于预处理过的玻碳电极表面,用红外灯烤干得GO/Nafion修饰电极。把修饰好的电极放到pH=5.0的HAc-NaAc缓冲溶液中,在-1.0~1.0 V之间循环扫描5圈,即得电化学还原石墨烯(ECGO)/Nafion修饰电极,备用。
1.3 电化学测量
将核黄素用pH=5.0的HAc-NaAc 缓冲溶液稀释至所需浓度,以裸玻碳电极或修饰电极为工作电极,饱和甘汞电极及铂柱对电极组成三电极系统,在-1.0~1.0 V电位范围内,50 mV·s-1扫描速度下记录循环伏安曲线。差示脉冲伏安曲线扫描范围为-1.0~0 V,静置时间180 s。
2 结果与讨论
2.1 核黄素在不同电极上的循环伏安行为
图1显示了1.0×10-4mol·L-1核黄素在裸玻碳电极、GO/Nafion和ECGO/Nafion修饰电极上的循环伏安行为。结果表明,核黄素在裸玻碳电极上的电化学信号较弱,但在GO/Nafion修饰电极上电信号明显改善,其中还原峰电流增大更加明显。将GO/Nafion修饰电极在HAc-NaAc(pH=5.0) 缓冲溶液中扫描5圈后,GO被部分还原成ECGO,核黄素在ECGO/Nafion修饰电极上分别在Epa=-301 mV(Epc=-394 mV) 处出现一对氧化还原峰,且氧化还原峰电流明显强于GO/Nafion修饰电极,这说明GO经电化学作用后,所得ECGO对核黄素的电催化能力更强。
2.2 实验条件的优化
2.2.1缓冲溶液的选择图2显示了核黄素在Na2HPO4-NaH2PO4(pH=7.0) 缓冲溶液和HAc-NaAc(pH=5.0) 缓冲溶液中的循环伏安行为。结果显示:核黄素在以上两种底液中均显示出相应的氧化还原峰,其中在HAc-NaAc缓冲溶液中峰形较好,峰电流较强,而在Na2HPO4-NaH2PO4缓冲溶液中,峰电流明显较低,且峰形不对称,故随后的实验均选择HAc-NaAc缓冲溶液作为底液。
2.2.2修饰剂用量的选择进一步考察了GO/Nafion修饰液用量对电化学信号的影响。结果显示,随着GO/Nafion修饰液用量的不断增加,阳极峰电流明显增大,当修饰液体积为6 μL时,阳极峰电流达最大,随后随着修饰液用量的不断增加,阳极峰电流有所降低。故随后所有实验都选用6 μL修饰液进行修饰。
2.2.3还原圈数的影响众所周知,在较负的起始电位下,氧化石墨烯或石墨烯上未被还原的含氧官能团易被活化甚至还原,且随着扫描圈数的增加,还原程度越彻底。为此我们考察了电化学还原圈数的影响,结果显示:在HAc-NaAc缓冲溶液(pH=5.0)中,当扫描圈数为5圈时,氧化还原峰电流均达到最大,继续增加扫描圈数,峰电流反而有所减小。根据文献,氧化石墨烯上的羰基很容易被还原,然而羟基及环氧基则相对较为稳定,只有在更负的电位下(-1.5 V)才能被彻底还原[11]。因此在-1.0~1.0 V扫描范围内,氧化石墨烯的还原并不是很彻底,残留的羟基及环氧基很容易与核黄素分子中的多个羟基形成氢键,使核黄素更容易到达电极表面,显示增强的电化学信号。
2.2.4pH的影响图3显示了核黄素在不同pH值的HAc-NaAc缓冲溶液中,阳极峰电流值与pH的关系曲线。由图可知,随着pH值的增大,阳极峰电流逐渐增强,在pH=5.0时达最大,随后pH值继续增大,峰电流反而减小,故随后的实验均以pH=5.0的0.2 mol·L-1HAc-NaAc缓冲溶液作为底液。
2.2.5初始电位的影响图4显示了在不同电位范围内扫描的循环伏安曲线。结果显示:随着初始电位的不断降低,峰电流逐渐增加,同时氧化峰电位发生一定程度的正移,还原峰电位发生一定程度的负移,当扫描范围是-1.0~0.8 V时,峰电流达最大,随后峰电流有所降低。因此,在随后进行的实验中,都选-1.0~0.8 V。
2.2.6静态时间的影响以HAc-NaAc缓冲溶液作为支持电解质,用差分脉冲伏安法(DPV)对最佳静态时间进行了考察。结果表明,当静态时间为180 s时,峰电流值达最大,随后趋于稳定,故本实验选择静态时间为180 s。
2.3 线性范围及电极性能
图5显示了不同浓度的核黄素在最佳条件下的DPV曲线,可以看出核黄素的阳极峰电流与其浓度在一定范围成正比关系,实验结果表明:线性范围为:7.5×10-8~1.0×10-5mol·L-1,其线性方程为:ip=7.2126c+1.7037×10-5(r=0.9947)。检出限(S/N=3)可达2.5×10-8mol·L-1。
平行制作5支修饰电极,对1.0×10-5mol·L-1的核黄素溶液进行平行测定,峰电流相对标准偏差(RSD,n=5)为4.7%。此外,ECGO/Nafion修饰电极在干燥环境中放置3 d,修饰电极的催化性能仍为原来的96.3%。这些结果表明:ECGO/Nafion修饰电极具有良好的重现性和稳定性。
2.4 干扰研究
实验考察了常见的几种干扰物质对核黄素测定的干扰,结果显示:50倍的维生素B1、维生素B6、烟酸、烟酰胺、尿酸、维生素C、色氨酸、多巴胺对核黄素的检测几乎不干扰。而人体常见的金属离子如Na+、K+、Mg2+、Ca2+、Fe3+对核黄素的检测基本没有影响。
2.5 实际样品分析
取市售维生素B2片(海南制药厂有限公司)进行实际样品含量测定。样品预处理过程如下:取20片药片,称重,研磨成粉末,备用。准确称取一片剂量的粉末,用二次蒸馏水超声溶解,定容至50 mL,静置1 d后备用。取400 μL黄色上层液,用11.6 mL HAc-NaAc(0.2 mol/L,pH=5.0) 缓冲溶液稀释,在最佳实验条件下进行测定,计算核黄素含量,同时与药典所描述的紫外-可见方法进行对比,具体结果见表1。结果显示,该测定方法所得结果与药典法检测结果很接近,表明该方法是精确可行的,可以用于实际样品中核黄素含量的测定。
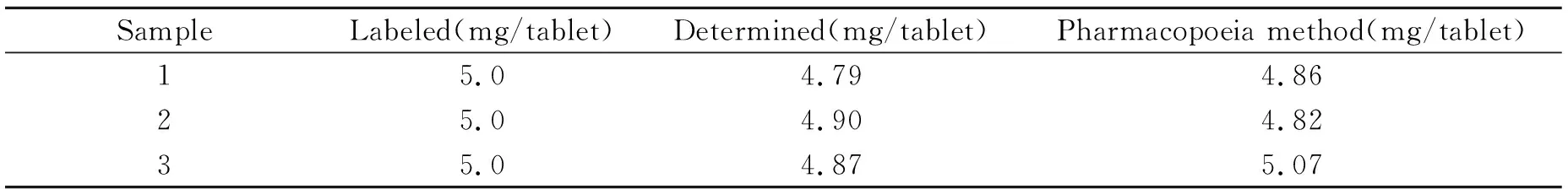
表1 实际药片中核黄素含量的测定(n=3)
3 结论
本文利用电化学还原石墨烯/Nafion修饰电极研究了核黄素的电化学行为,发展了一种检测核黄素的电化学传感器。该传感器具有较高的灵敏度,检测限可达2.5×10-8mol·L-1,在实际样品分析中,与药典法所得检测结果很接近,可用于实际样品中核黄素含量的测定。

