磁性纳米复合物对水中亚甲基蓝的吸附及其机理
姜德彬,余 静,叶芝祥,魏 贝,杨梓睿,杨 凌
磁性纳米复合物对水中亚甲基蓝的吸附及其机理
姜德彬,余 静*,叶芝祥,魏 贝,杨梓睿,杨 凌
(成都信息工程大学资源环境学院,四川 成都 610225)
利用正硅酸乙酯水解在磁性纳米锰锌铁氧体表面包裹SiO2,制备了一种新型“核/壳”结构磁性纳米复合物材料Si-Fe-MNCs.采用N2-吸附脱附法、透射电子显微镜(TEM)、振动样品磁强计(VSM)和傅利叶变换红外技术(FT-IR)分别对Si-Fe-MNCs的织构性能、形貌和磁性能进行了表征.结果表明,该磁性材料对亚甲基蓝表现出良好的吸附性能,318K时平衡吸附量在40.31~184.1mg/g之间,120min可达吸附平衡,符合准二级动力学方程.吸附过程符合Langmuir等温吸附模型,热力学计算结果表明Si-Fe-MNCs对亚甲基蓝的吸附是以表面物理吸附为主的自发吸热过程,红外结果表明氢键是Si-Fe-MNCs表面官能团与亚甲基蓝之间的主要作用力.Si-Fe-MNCs采用H2O2进行再生,5次循环使用后,对MB的平衡吸附量仍可维持在93.64mg/g.
磁性纳米复合物;亚甲基蓝;吸附;机理;磁分离
印染废水排放量大、水质复杂、毒性大,已成为重点环境污染源之一[1].亚甲基蓝(MB)是水溶性偶氮染料的代表性化合物,在水溶液中会形成一价阳离子型的季胺盐离子基团,且其色度很高,难以生物降解,进入水体后影响水生植物的光合作用从而破坏生态平衡,对环境污染严重[2-3].吸附技术是去除污染物最为简单和高效的方法之一,活性炭、硅藻土、膨润土等对染料具有一定的吸附脱色能力,但是大多为微孔材料,微孔吸附后难脱附, 使其再次利用较困难;同时将负载了染料的吸附剂从水体中分离出来也较困难.吸附剂如果不重复利用,既浪费资源又污染环境,最终导致吸附只是污染物的相转移过程,因此开发新型高效的吸附剂,制备高吸附容量、易于固液分离及再生的新型吸附剂,有望突破吸附法处理印染废水中的瓶颈问题,实现对印染废水的深度处理以及吸附剂的重复利用.
近年来,将磁性纳米复合物(MNCs)作为吸附剂用于废水的净化日益得到国内外学者的关注[4-10].MNCs吸附剂是在纳米磁性颗粒(MNPs)的表面包裹修饰聚合物[11]、表面活性剂[12]、贵金属[13]和无机氧化物[14]等,得到磁性强、耐侯性强、比表面积大、分散性好、易于固液分离的功能吸附材料.而用于废水处理的MNCs吸附剂的磁核多采用Fe3O4MNPs,虽然其价廉易得,但由于Fe3O4中的Fe2+处于亚稳态,很容易再失去一个电子成为Fe3+达到最稳定的氧化态,从而导致磁性能降低.若采用锰、锌替代Fe2+可改善Fe3O4MNPs的抗氧化性能,即采用锰锌铁氧体(Mn1-xZnFe2O4)MNPs为磁核制备锰锌铁氧体磁性纳米复合物(Fe-MNCs)可极大提高Fe3O4MNPs的磁性能及化学稳定性.
本课题前期研究中利用废弃碱性电池的极性材料,采用蔗糖-硝酸盐法制备出磁性纳米锰锌铁氧体[15](Fe-MNPs);然后以正硅酸乙酯(TEOS)作为包覆材料,采用简单、易操作控制的方法对Fe-MNPs进行SiO2包覆,制备得到硅包覆的Fe-MNCs吸附剂[16](Si-Fe-MNCs).本研究对Si-Fe-MNCs吸附剂的比表面积、形貌、磁性能进行了表征,考察了Si-Fe-MNCs对水中MB的吸附动力学及热力学,并推测了吸附机理,为进一步的实际应用提供基础理论数据.
1 材料与方法
1.1 试剂与仪器
试剂:正硅酸乙酯(TEOS,SiO2质量分数28%);亚甲基蓝(MB)(分子量为373.9,CAS号: 7220-79-3)、聚乙烯醇(PVA)、可溶性淀粉等,所用药品均为分析纯(成都市科龙化工试剂厂).
仪器:UV-2250型紫外-可见分光光度计(日本岛津公司);ALC-210.4型电子天平(北京赛多利斯仪器有限公司);THZ-82型回转式气浴恒温振荡器(江苏正基仪器有限公司);SSA-4220型孔隙比表面分析仪(北京彼奥德电子技术有限公司);-2100F场发射透射电子显微镜(JEOL, Japan);BHV-525型振动样品磁强计(Riken Denshi,Japan);Nicolet IS50型傅立叶红外光谱仪(美国Thermo Scientific公司).
1.2 Si-Fe-MNCs的制备及表征
取0.05mol/L的柠檬酸溶液150mL于250mL三口烧瓶中,加入已制备好的锰锌铁氧体0.5g[15],先将锰锌铁氧体在柠檬酸溶液中搅拌分散3h后,用氨水调节溶液pH值至5.5左右,再继续搅拌分散3h后,逐滴加入一定量的TEOS,继续水浴加热搅拌反应6h.待溶液冷却后,移去上层清液,用蒸馏水和无水乙醇对下层沉淀物进行抽滤洗涤3次.然后放入真空干燥333K干燥5h,从而制得Si-Fe-MNCs.
对所得Si-Fe-MNCs样品进行如下表征:氮气等温吸脱-脱附(测定比表面积、孔容和孔径分布)、透射电子显微镜分析以及磁性能分析.
1.3 吸附实验
将一定量的Si-Fe-MNCs加入一定体积,在一定温度、200r/min的条件下恒温振荡;一定时间后取出锥形瓶,置于铷铁硼磁铁(0.2T)上静置分离,4min后取上层清液分析亚甲基蓝的浓度. MB浓度采用紫外-可见光分光光度法进行测定[17];根据式(1)和(2)分别计算MB的脱色率及吸附量:
式中:为MB脱色率,%;1为处理后MB浓度, mg/L;0为初始MB浓度,mg/L;为吸附量,mg/g;为MB溶液的体积,L;:Si-Fe-MNCs的质量,g.
2 结果与讨论
2.1 Si-Fe-MNCs的表征
TEOS的水解反应属于亲核取代反应,TEOS的水解单体中含有Si-OH基团,可形成较多的Si(OH)4,在包覆过程中,经过柠檬酸分散的锰锌铁氧体表面有大量羧羟基,此为表面包覆的结合点.前期研究中,红外表征结果表明Si(OH)4依靠氢键与溶液中悬浮的锰锌铁氧体纳米粒子表面大量的羟基结合;随着Si(OH)4的不断生成, Si(OH)4与锰锌铁氧体粒子表面己包覆的Si(OH)4依靠分子间氢键结合,使Fe-MNPs表面包覆厚度不断增加,最终得到SiO2完全包覆的Si-Fe-MNCs;同时,XRD表征结果表明,包覆前后Fe-MNPs的晶型未改变,仍为为尖晶石型结构,在Si-Fe-MNCs中SiO2以无定型的形态存在[16].
从Si-Fe-MNCs的N2吸附-脱附曲线(图1)可知,此等温线是属于IUPAC分类中的Ⅳ型.在相对压力为0.4~0.7区域出现了滞后环(H4型),这是由于毛细管凝聚所造成的,是介孔材料的典型吸附行为,这说明Si-Fe-MNCs具有孔道结构,该磁性吸附材料中的孔道是由于多孔吸附质或均匀粒子堆积孔造成的.根据Si-Fe-MNCs的BJH孔径分布可知,材料中孔分布最广的孔主要集中在1.9nm左右.
由Si-Fe-MNCs的N2吸脱-附等温线得到的比表面积、孔容以及平均孔径(BET)如表1所示,Fe-MNPs包覆SiO2后,比表面积和孔容均有所增加,而平均孔径有较大幅度降低,这是由于包覆层具有狭缝孔道结构造成的.由此可见,所制备的磁性吸附剂Si-Fe-MNCs较大的比表面积,这可以为污染物提供更多的吸附位点.
由图2(a)可观察到,Fe-MNPs由于其具有较高的表面能,容易聚集,平均粒径为16.0nm;从图2(b)中可以观察到明显的核-壳结构(深色的为磁性核,浅色的为无定型的包覆层SiO2),包覆层厚度约为2.7nm;而经包覆所得的Si-Fe-MNCs颗粒呈球形,无明显团聚,分散性明显提高,平均粒径为18.7nm,且Fe-MNps被完全包覆;从图2(c)中可以观察到由无定型的包覆层SiO2所形成的狭缝状的孔道结构,这一结果也与上述Si-Fe-MNCs的N2吸附-脱附曲线的结果相吻合.
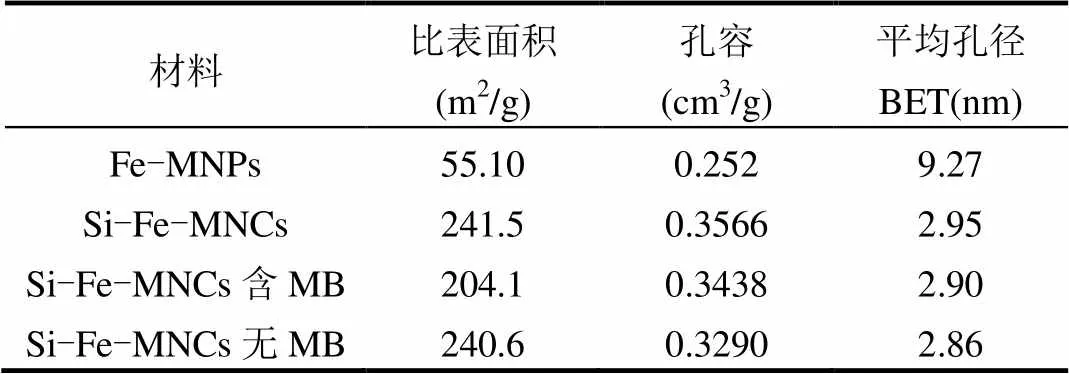
表1 Si-Fe-MNCs吸附MB前后及再生后物理性质Table 1 Textural parameters of Si-Fe-MNCs, Si-Fe- MNCs (with MB), Si-Fe-MNCs (without MB)
从磁滞回线可以看出(图3),Si-Fe-MNCs磁性粒子的饱和磁化强度(s)为18.6emu/g,比包覆前的Fe-MNPs粒子的s(26emu/g)有所降低,这是由于包覆颗粒的表面呈现磁惰性;而Si-Fe- MNCs磁性粒子的剩磁(r)和矫玩力(c)均比包覆前有所降低,说明包覆后使Fe-MNPs磁学特性发生改变,较低的矫玩力与剩磁可使得所制备的Si-Fe-MNCs在外加磁场反复作用后,仍具有较好的分散和磁分离效果.实验中,在外加磁场(0.2T)的作用下,吸附了MB的Si-Fe-MNCs磁性粒子能在3min之内实现固液分离;经再生后的Si-Fe-MNCs磁性粒子再次使用时,只需轻微振荡即可再次均匀分散.
上述表征结果说明,所制备的Si-Fe-MNCs磁性吸附剂具有无定形的SiO2包覆层和磁性内核的结构,易于实现固液分离;具有较大的比表面积,分散性能好,能充分发挥其对水中MB的吸附效果.
2.2 吸附动力学
为了分析Si-Fe-MNCs吸附MB的吸附速率并探讨吸附机理,采用如下2种动力学模型对数据进行模拟:
准一级动力学模型表达式[18]:
准二级动力学模型表达式[19]:
式中:e、q分别为平衡吸附量、时刻的吸附量,mg/g;1为准一级吸附速率常数,min-1;2为准二级吸附速率常数,mg/(g·min).动力学模型拟合相关参数如表2所示.
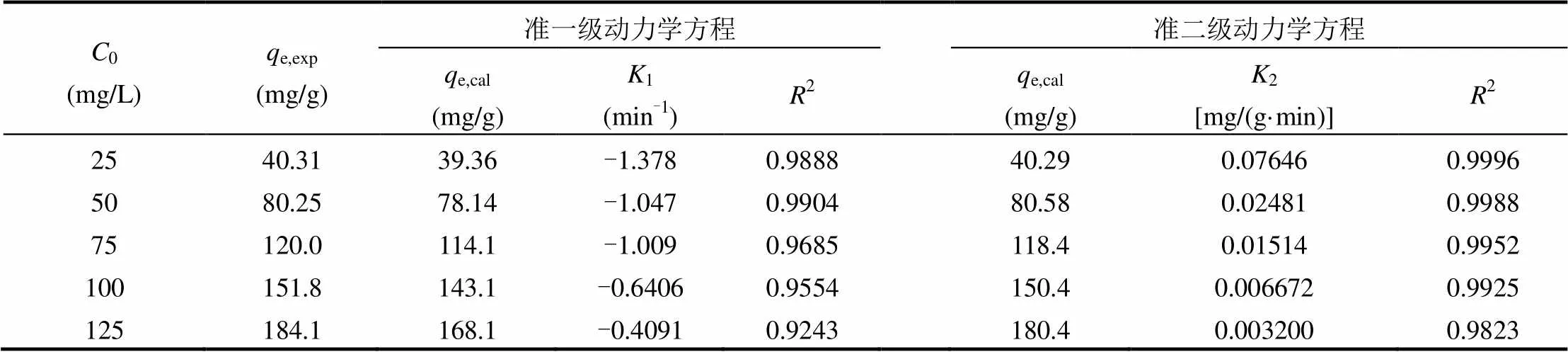
表2 动力学模型拟合参数(318K)Table 2 Fitting parameters of kinetic models (318K)
由表2可见,准二级动力学模型的相关系数2>0.99,模型计算得出的平衡吸附量e,cal与试验值e,exp非常接近,相对误差非常小.而准一级动力学模型在各浓度下的相关系数2>0.9,但模型计算得出的平衡吸附量e,cal与试验值e,exp相差相对较远.故准二级动力学模型最适合描述Si-Fe-MNCs磁性吸附剂对MB的吸附动力学过程[20].
2.3 吸附等温线和热力学
Langmuir和Freundlich吸附等温方程分别描述了均匀表面单层吸附和非均匀表面非均匀吸附[21-23],其表达式分别如下式(5)和(6):
式中:e为吸附平衡时MB的浓度,mg/L;e为平衡吸附量,mg/g;m为最大吸附量,mg/g;为吸附平衡常数,L/mg;K、均为Freundlich常数.

表3 不同温度下MB在Si-Fe-MNCs上的吸附等温方程常数Table 3 Adsorption isotherm equation parameters of MB adsorption on Si-Fe-MNCs at different temperature
图5和表3所示,在不同温度下,Langmuir吸附等温方程的相关系数最高(2>0.98),因此Si-Fe-MNCs对MB的吸附行为符合Langmuir等温吸附规律.在Langmuir吸附等温方程中,m越大,表明吸附能力越大,随着温度升高,m增加,说明升温有利于磁性吸附剂对MB的吸附,m在303K时为181.9mg/g.Langmuir吸附等温方程的一个重要特点是定义了无量纲的分离因子(L):
式中:L表示吸附过程的性质,0 根据Langmuir吸附等温方程、热力学公式以及van’t Hoff方程(式(8)和式(9))计算得到该吸附过程的热力学参数(表5): 式中:D为吸附过程吉布斯自由能变量,kJ/mol;c为等温吸附常数,L/g,c=e/e;为通用气体常数,8.314J/(mol·K);为热力学温度,K;D为吸附过程焓变,kJ/mol;D为吸附过程熵变,J/(mol·K). 表4 不同初始MB浓度在Si-Fe-MNCs上的Langmuir分离因子常数Table 4 Langmuir Separation factor for the adsorption of MB on Si-Fe-MNCs at different initial MB concentrations 由表5可知,D<0,表明Si-Fe-MNCs吸附MB是自发进行的过程,通常0 为了更深入理解吸附机理,通常利用Dubinin-Radushkevich(D-R)模型来确定吸附类型,其表达式如下: 式中:m为最大吸附量,mg/g;为吸附能常数, mol2/kJ2;为吸附吸附势;为吸附自由能, kJ/mol.将式(10)线性化后得,而 式中:为通用气体常数,J/(mol·K),为温度,K.则吸附自由能为: 由表3可知,不同温度下的吸附自由能均小于8kJ/mol,表明该吸附过程以物理吸附为主[24],这也与表5的热力学分析结果相吻合,吸附过程的作用力可能是氢键、范德华力以及电子共轭作用等. 吸附了MB的Si-Fe-MNCs的再生用3%的H2O2进行再生.在303K,再生4h后,通过磁性分离,将再生后的Si-Fe-MNCs用蒸馏水洗涤3次烘干后,进行第2次吸附MB的实验,如此反复5次,实验结果表明(图6),再生后的Si-Fe-MNCs重复使用5次,对MB仍具有较高的平衡吸附量,可循环使用. 吸附动力学和吸附热力学的研究结果表明,吸附过程受温度影响不大,同时平均吸附能()、吉布斯自由能的变化以及焓变均表明过程以物理吸附为主,而红外光谱可以通过分析吸附前后吸附剂以及吸附质的特征峰的变化,来定性描述参与吸附的官能团,为揭示吸附机理提供依据. 由图7a Si-Fe-MNCs的FTIR谱图可见,3424cm−1处和1628cm−1处的吸收峰分别归属于表面羟基伸缩振动和弯曲振动;553cm−1处的吸收峰归属于锰锌铁氧体的Fe-O特征吸收;1077cm-1处的吸收峰归属于O—Si—O的对称伸缩振动;456cm−1处和791cm−1处的吸收峰分别归属于O—Si—O和Si—OH的弯曲振动[16]. 由图7b亚甲基蓝的FTIR谱图可见, 3423cm−1处的吸收峰归属于表面羟基伸缩振动;1593cm−1处和1385cm−1处的吸收峰分别归属于亚甲基蓝杂环的C=N和C—N的伸缩振动;1487cm-1处的吸收峰归属于CH2的弯曲振动;1327cm-1处的吸收峰归属于N—CH3的伸缩振动;1245cm−1处和1216cm−1处的吸收峰归属于苯环Ar—N的弯曲振动;1165cm−1处和1136cm−1处的吸收峰分别归属于亚甲基蓝杂环的C=S和C—S的伸缩振动[26]. 由图7c Si-Fe-MNCs吸附亚甲基蓝后的FTIR谱图可见,3424cm−1处和1628cm−1处的吸收峰分别归属于表面羟基伸缩振动和弯曲振动;556cm−1处的吸收峰归属于锰锌铁氧体的Fe-O特征吸收;1608cm−1处和1397cm−1处的吸收峰分别归属于亚甲基蓝杂环上面C=N和C—N的伸缩振动;1491cm-1处的吸收峰归属于CH2的弯曲振动;1340cm-1处的吸收峰归属于N—CH3的伸缩振动;1077cm-1处的吸收峰归属于O—Si—O的对称伸缩振动;441cm−1处和788cm−1处的吸收峰分别归属于O—Si—O和Si—OH的弯曲振动.而苯环Ar—N的弯曲振动、C=S和C—S的特征峰被宽而强的O—Si—O的对称伸缩振动特征峰所掩盖. 亚甲基蓝为阳离子型染料,能以静电力吸附在带负电荷的Si-Fe-MNCs磁性粒子的表面[27],MB被吸附后,C=N和N—CH3的特征峰波数增加(蓝移),这是由于亚甲基蓝杂环上的N和N—CH3中的N与Si-Fe-MNCs表面的Si—OH形成了分子间氢键,而Si—OH的中O原子的电子云密度较N原子大,使得氢键中的电子云偏向N一侧,从而使得C=N和N—CH3的特征峰波数增加,与此同时,Si—OH被削弱,使得Si—OH的特征峰波数降低.但是氢键是介于分子间力(范德华力)和化学键之间的一种作用,此时吸附过程无旧键断裂也无新键形成,吸附过程以物理吸附为主,这也与前述热力学实验结果相吻合. 前述表征结果表明,所制备的Si-Fe-MNCs磁性吸附剂具有无定形的SiO2包覆层和磁性内核的结构,而无定型的包覆层SiO2形成了狭缝状的孔道结构,吸附的活性位点是在材料表面还是孔道中,对于吸附剂的再生非常重要. 由图8a Si-Fe-MNCs吸附MB前后的N2吸附-脱附等温曲线可见,吸附MB前后的Si-Fe-MNCs的N2吸附-脱附曲线形状相似,吸附前后仍然在相对压力为0.4~0.7区域出现了吸附滞后环;由图8b孔径分布可见,吸附MB前后的Si-Fe-MNCs的孔径分布几乎没有改变.吸附MB前后的Si-Fe-MNCs的孔容以及孔径都变化不大,而比表面积下降(表1),这表明Si-Fe- MNCs对亚甲基蓝的吸附没有改变材料的孔道结构和孔径分布,吸附应发生在Si-Fe-MNCs磁性粒子的外表面[26]. 根据Si-Fe-MNCs材料的比表面积,通过公式(13)和公式(14)可求得材料对MB的单分子层最大吸附量Q[28]. 式中:SSA为BET测得的比表面积,m2/g;MB为MB的分子横截面积,m2;为阿伏伽德罗常数, 6.02×1023;MB为MB的摩尔质量,373.9g/mol;为MB的密度,g/cm3.计算可得m为216.9mg/g,而由表3可知,298K时,由Langmiur模型拟合得到的单分子层最大吸附量m为168mg/g,这可能是由于阳离子染料在水溶液中有自聚集形成二聚体的倾向,因此低温时被吸附在磁性吸附剂表面的所有分子未必均与吸附剂表面形成氢键,故此时m大于m;随着温度升高,MB形成二聚体的倾向逐渐减弱,故此时m与m也逐渐接近,应为单分子层吸附[28],同时也进一步印证了Langmiur模型能较好的描述该吸附过程. 综上所述,Si-Fe-MNCs磁性吸附剂对MB的吸附机理如图9所示. 3.1 利用正硅酸乙酯水解制备得到一种新型的磁性吸附剂Si-Fe-MNCs,SiO2完全包裹在磁性铁氧体的表面,磁性颗粒经包裹后,比表面积和空容均有所增加,而平均孔径降至介孔尺度,与磁核相比,Si-Fe-MNCs的饱和磁化强度和矫玩力均有所下降,具有优良的磁分离性能. 3.2 Si-Fe-MNCs能有效去除水中的亚甲基蓝染料,318K时,平衡吸附量在40.31~184.1mg/g之间,吸附过程2h达到平衡,符合准二级动力学方程.吸附过程符合Langmuir等温吸附模型,0 <R<1,吸附过程为优惠吸附.Si-Fe-MNCs采用H2O2进行再生和多次循环使用后,对MB保持较高的平衡吸附量,具有良好的应用前景. 3.3 Si-Fe-MNCs对MB的吸附过程中,吉布斯自由能D为<0,吸附焓变D>0,吸附熵变D>0,该吸附过程为吸热和熵增的自发过程;通过D–R模型得到吸附自由能<8kJ/mol,该吸附过程为物理吸附,氢键为吸附主要作用力,为表面物理吸附. 任南琪,周显娇,郭婉茜,等.染料废水处理技术研究进展 [J]. 化工学报, 2013,64(1):84-94. Mondal P K, Chauhan B. Microbial degradation of dye-containg wastewater [J]. Environment Science and Engineering, 2012,12:317-338. Rafatullaha M, Sulaimana O, Hashima, et al. Adsorption of methylene blue on low-cost adsorbents: A review [J]. Journal of Hazardous Materials, 2010,177:70-80. Ge Fei, Ye Hui, Li Mengmeng, et al. Efficient removal of cationic dyes from aqueous solution by polymer-modified magnetic nanoparticles [J]. Chemical Engineering Journal, 2012,198- 199:11-17. 郭延辉,樊 静,王建玲,等.树脂固载纳米铁对偶氮染料直接湖蓝5B的脱色性能研究 [J]. 环境工程学报, 2010,4(2):337-341. 陈君良,姚屠鹏,朱宏亮,等.巯基功能化纳米Fe3O4-高分子磁性复合材料的合成及其对水中亚甲基蓝的吸附作用 [J]. 复合材料学报, 2014,31(2):323-330. 鲍晓磊,强志民,贲伟伟,等.磁性纳米复合材料CoFeM48对水中磺胺类抗生素的吸附去除研究 [J]. 环境科学学报, 2013,33(2): 401-407. Qiang Zhimin, Bao Xiaolei, Ben Weiwei. MCM-48modified magnetic mesoporous nanocomposite as an attractive adsorbent for the removal of sulfamethazine from water [J]. Water Research, 2013,47:4107-4114. Ai Lunhong, Zhang Chunying, Liao Fang, et al. Removal of methylene blue from aqueous solution with magnetite loaded multi-wall carbon nanotube: Kinetic, isotherm and mechanism analysis [J]. Journal of Hazardous Materials, 2011,198:282–290. Abbas Afkhami, Mohammad Saber-Tehrani, Hasan Bagheri. Modified maghemite nanoparticles as an efficient adsorbent for removing some cationic dyes from aqueous solution [J]. Desalination, 2010,263:240–248. Chang Yang-Chuang, Chen Dong-Hwang. Adsorption Kinetics and Thermodynamics of Acid Dyes on a Carboxymethylated Chitosan-Conjugated Magnetic Nano-Adsorbent [J]. Macromolecular Bioscience, 2005,5:254-261. 赵 静,刘勇健.磁流体在印染废水处理中的应用研究 [J]. 环境科学与管理, 2008,33(5):118-120. 张晓蕾,陈 静,韩京龙,等.壳-核结构Fe3O4/MnO2磁性吸附剂的制备、表征及铅吸附去除研究 [J]. 环境科学学报, 2013, 33(10):2730-2736. Zhang Yuanyuan, Xu Qiang, Zhang Shengxiao, et al. Preparation of thiol-modified Fe3O4@SiO2nanoparticles and their application for gold recovery from dilute solution [J]. Separation and Purification Technology, 2013,116:391-397. 邱海浪.废碱锰电池制备锰锌铁氧体及其应用 [D]. 成都:成都信息工程大学, 2015. 姜德彬,余 静,程庆峰,等.锰锌铁氧体/SiO2复合磁性材料的制备和表征 [J]. 化工环保, 2015,35(5):536-541. 肖 敏,李 丽,钟龙飞,等.活性炭吸附法处理印染废水的研究 [J]. 辽宁化工, 2009,38,(8):537-539. Ni Zheming, Xia Shengjie, Wang Ligeng, et al. Treatment of methyl orange by calcined layered double hydroxides in aqueous solution: Adsorption property and kinetic studies [J]. Journal of Colloid and Interface Science, 2007,316:284–291. Ho Y S, McKay G. Pseudo-second-order model for sorption processes [J]. Process Biochem., 1999,34:451-465. 刘 斌,顾 洁,邱 盼,等.稻壳活性炭对水中染料的吸附特性及其回收利用 [J]. 环境科学学报, 2014,34(9):2256-2264. 邓述波,余 刚.环境吸附材料及应用原理 [M]. 北京:科学出版社, 2012:211. 姚 超,刘 敏,李为民,等.凹凸棒石/氧化锌纳米复合材料对亚甲基蓝的吸附性能 [J]. 环境科学学报, 2010,30(6):1211-1219. 高淑玲,杨翠玲,罗鑫圣,等.坡缕石黏土污泥对水相中亚甲基蓝吸附研究 [J]. 中国环境科学, 2014,34(1):78-84. 刘 健,李耀威,王 刚,等.改性废报纸纤维对水中Cr(VI)的吸附研究 [J]. 中国环境科学, 2015,35(5):1368-1374. 刘 新,冷言冰,谷仕艳,等.油菜秸杆外壳对水溶液中六价铬的吸附作用 [J]. 中国环境科学, 2015,35(6):1740-1748. Gong Jiang, Liu Jie, Jiang Zhiwei, et al. A facile approach to prepare porous cup-stacked carbon nanotube with high performance in adsorption of methylene blue [J]. Journal of Colloid and Interface Science, 2015,445:195-204. Ma Jie, Yu Fei, Zhou Lu, et al. Enhanced Adsorptive Removal of Methyl Orange and Methylene Blue from Aqueous Solution by Alkali-Activated Multiwalled Carbon Nanotubes [J]. ACS Applied Materials & Interfaces, 2012,4:5749−5760. Lin Daohui, Xing Baoshan. Adsorption of Phenolic Compounds by Carbon Nanotubes: Role of Aromaticity and Substitution of Hydroxyl Groups [J] Environmental Science & Technology, 2008,42(19):7254-7259. * 责任作者, 副教授, yujing@cuit.edu.cn Adsorption and mechanism of methylene blue from water by magnetic nanocomposites JIANG De-bin, YU Jing*, YE Zhi-xiang, WEI Bei, YANG Zi-rui, YANG Ling (College of Resources and Environment, Chengdu University of Information Technology, Chengdu 610225, China)., 2016,36(6):1763~1772 A novel “core/shell” structured magnetic nanocomposite Si-Fe-MNCs was prepared by coating SiO2on the surface of Mn-Zn ferrite magnetic nanoparticles (Fe-MNPs) through in-situ hydrolysis of tetraethylorthosilicate (TEOS). The specific surface area, morphology, magnetic properties and surface species of Si-Fe-MNCs were characterized by N2-adsorption/desorption, transmission electron microscopy (TEM), vibrating sample magnetometer (VSM) and Fourier transform infrared spectroscopy, respectively. The synthesized magnetic adsorbents exhibited a good performance in the removal of methylene blue (MB) from water, and gave a maximum adsorption capacity of 184.1mg/g at 318K. The adsorption of MB on Si-Fe-MNCs reached equilibrium at 120min, and exhibited the kinetics of pseudo-second-order model according to the Langmuir adsorption isotherms. Additionally, it was found that the adsorption of MB on Si-Fe-MNCs was a spontaneous endothermic physical process according to thermodynamic calculations. FT-IR revealed that MB mainly interacted with the surface functional groups of Si-Fe-MNCs and MB through hydrogen bond. The regeneration of Si-Fe-MNCs after MB adsorption was found to be realized by conducting H2O2, and its adsorption capacity could preserve an excellent level of 93.64mg/g after five runs. magnetic nanocomposite;methylene blue;adsorption;mechanism;magnetic separation X703 A 1000-6923(2016)06-1763-10 姜德彬(1984-),男,重庆人,成都信息工程大学硕士研究生,主要研究方向水污染控制理论与技术. 2015-11-17 国家自然科学基金(51408076);四川省教育厅资助科研项目(15ZA0189)
2.4 吸附机理
3 结论

