基因A型和C型鸭甲型肝炎病毒卵黄抗体的研制及应用
王继练,张焕容,王 栋
(西南民族大学生命科学与技术学院,四川成都 610041)
基因A型和C型鸭甲型肝炎病毒卵黄抗体的研制及应用
王继练,张焕容*,王栋
(西南民族大学生命科学与技术学院,四川成都 610041)
旨在研制基因A型和C型鸭甲型肝炎病毒(DHAV)单价及二价高免卵黄抗体,以满足实际生产中基因A型和C型DHAV单独或混合感染防控的需要。采用基因A型和C型DHAV强毒株作为抗原制备单价和二价油乳剂灭活疫苗免疫接种高产蛋鸡,制备了高效价的基因A型和C型DHAV单价及二价高免卵黄抗体,卵黄抗体鸭胚中和效价在1∶204与1∶281之间,单价及二价卵黄抗体防治试验证明,所制备的卵黄抗体防治效果良好。
鸭甲型肝炎病毒;基因型;卵黄抗体;防治
鸭病毒性肝炎(Duck viral hepatitis,DVH)是由鸭肝炎病毒(Duck hepatitis virus,DHV)引起的雏鸭的一种致死率高且传播迅速的急性、败血性传染病,是危害养鸭业最主要的疫病之一。临床上引起DVH的病原统称为DHV。DHV分为Ⅰ、Ⅱ、Ⅲ型3种血清型,其中血清Ⅰ型DHV又称为鸭甲型肝炎病毒(Duck hepatitis A virus,DHAV),DHAV又分为A、B和C 3种基因型[1],3种基因型之间无交叉免疫保护。我国目前流行的DVH主要由基因A型和C型DHAV引起,预防和控制该病毒的方法主要有弱毒疫苗免疫、高免血清或卵黄抗体防治[2]。由于弱毒疫苗免疫接种后产生保护性抗体需要一定的时间[3],而DVH主要发生在3周龄以内的雏鸭,1周龄以内雏鸭感染病死率极高,雏鸭最好通过母源抗体获得保护,母源抗体低的雏鸭可通过注射高免血清或卵黄抗体进行预防或紧急治疗。因此,弱毒疫苗或灭活疫苗主要用于免疫种鸭以便后代雏鸭获得高水平的母源抗体。高免血清分离自免疫动物的血液,而卵黄抗体仅需收集免疫蛋鸡所产的鸡蛋,在鸡蛋的卵黄中即含有高水平的特异性抗体,因高免血清产量有限,生产成本高,相比较而言,卵黄抗体的生产成本远远低于高免血清[4]。卵黄抗体已广泛应用于动物疫病的防治[5],已证实鸭肝炎病毒高免卵黄抗体用于鸭病毒性肝炎的防治效果良好。本研究旨在制备基因A型和C型DHAV单价和二价高免卵黄抗体用于鸭病毒性肝炎的防治。
1 材料与方法
1.1材料
鸭胚半数致死量(ELD50)10-5.356/0.1 mL的基因A型DHAV(DHAV-A)A4强毒株、ELD5010-5.568/0.1 mL的基因C型DHAV(DHAV-C)C2强毒株,均由西南民族大学生命科学与技术学院动物医学实验室分离、鉴定并保存;SPF鸭胚,购自中国农业科学院哈尔滨兽医研究所;17周龄伊莎蛋鸡,购自成都正大有限公司温江蛋鸡养殖场。
1.2方法
1.2.1DHAV-A和DHAV-C单价和二价佐剂疫苗的制备将1 000×ELD50的DHAV病毒液加入终浓度1 mL/L的福尔马林溶液混匀,于37 ℃灭活16 h后,加入终浓度40 mL/L的吐温-80,充分混匀后得到灭活病毒液,灭活病毒液与弗氏佐剂按1∶1体积比混合乳化制备单价灭活苗;等量的1 000×ELD50的DHAV-A和DHAV-C混合物2体积与1体积弗氏佐剂混合乳化制备二价灭活苗。
1.2.2蛋鸡免疫开产前3周(17周龄)的健康伊莎蛋鸡12只随机分成4组,每组3只,分别为DHAV-A单价苗免疫组、DHAV-C单价苗免疫组、二价苗免疫组及不免疫对照组。疫苗免疫剂量及间隔时间如下:第1次免疫采用弗氏完全佐剂疫苗胸部肌肉注射,每只1 mL。第1次免疫后10 d进行第2次免疫,第2次和第3次免疫采用弗氏不完全佐剂疫苗颈部皮下注射,每只2 mL,第2次和第3次免疫间隔为10 d。三免后10 d进行第4次免疫,单价免疫苗组分别采用1 000×ELD50DHAV-A和DHAV-C强毒1 mL翅静脉注射加强免疫,二价苗免疫组同时静脉注射上述2种强毒各1 mL。
1.2.3卵黄抗体的制备及效价检测第4次加强免疫后7 d开始收集鸡蛋取其卵黄液,于卵黄液中加入等体积的生理盐水充分混合均匀后,12 000 r/min离心10 min取上清,每亳升上清液加入100单位的青霉素、链霉素(双抗)即为卵黄抗体。将1 000×ELD50/mL病毒液与2倍系列稀释的不同稀释度的卵黄抗体按1∶1均匀混合后置37 ℃恒温箱中感作1 h后,每枚鸭胚接种0.2 mL,接种后放入37 ℃孵化箱孵育观察,除去24 h内死亡的胚外,记录7 d内鸭胚存活数和死亡数。根据Reed-Muench法计算卵黄抗体的中和效价。
1.2.4基因A型和C型DHAV卵黄抗体预防和治疗试验基因A型和C型DHAV卵黄抗体预防和治疗试验分组及处理见表1和表2。预防试验为先注射卵黄抗体后24 h攻毒;治疗试验为攻毒24 h后注射卵黄抗体。
2 结果
2.1基因A型和C型DHAV单价和二价卵黄抗体效价
取第4次加强免疫后7 d~14 d内产的蛋制备得到的卵黄抗体效价检测结果见表3、表4、表5和表6。DHAV-A单价卵黄抗体中和效价为1∶281,DHAV-A和DHAV-C二价卵黄抗体中DHAV-A中和效价1∶204,DHAV-C单价卵黄抗体中和效价1∶240,DHAV-A和DHAV-C二价卵黄抗体中DHAV-C中和效价1∶213。

表1 卵黄抗体预防试验分组及处理

表2 卵黄抗体治疗试验分组及处理
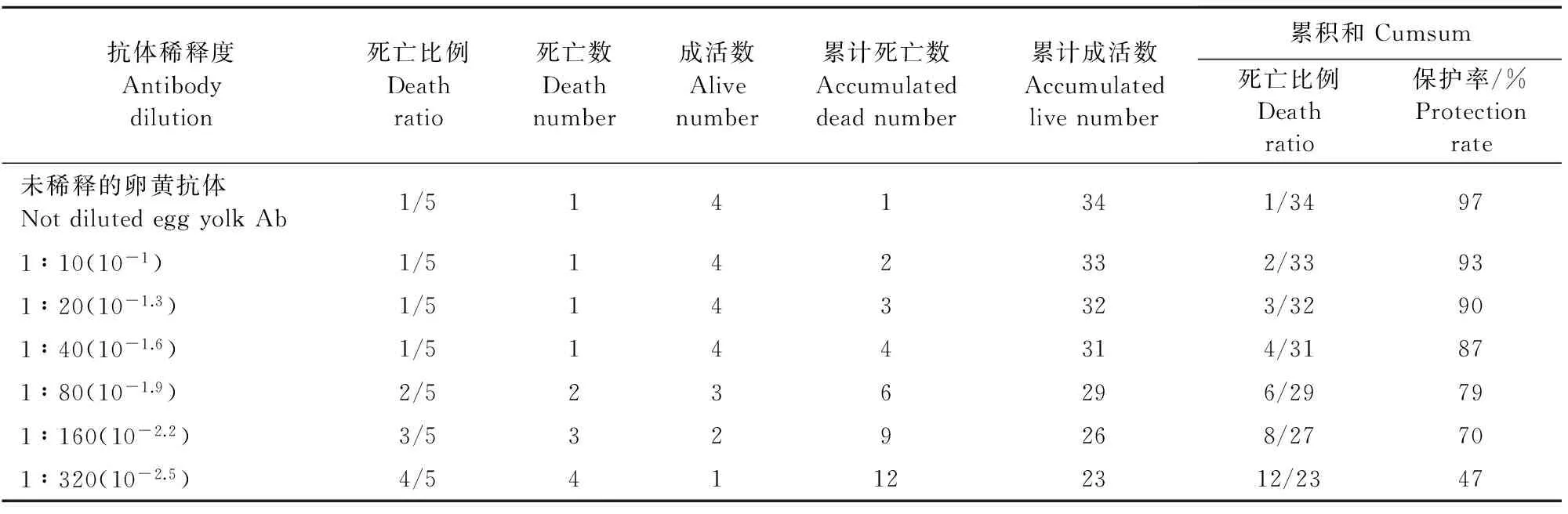
表3 DHAV-A单价卵黄抗体中和效价
按照Reed-Muench法计算,能保护50%的鸭胚免于死亡的抗体稀释度介于10-2.2和10-2.5之间。距离比例=(70-50)/(70-47)=0.86,高于50%保护率抗体稀释度的对数+距离比例×稀释系数的对数,即-2.2+0.86×(-0.3)=-2.45,-2.45的反对数=281,即1∶281稀释的抗体可保护50%的鸭胚免于死亡,即为该抗体50%的中和价。

表4 DHAV-A和DHAV-C二价卵黄抗体中DHAV-A中和效价
按照Reed-Muench法计算,能保护50%的鸭胚免于死亡的抗体稀释度介于10-2.2和10-2.5之间。距离比例=(60-50)/(60-33)=0.37,高于50%保护率抗体稀释度的对数+距离比例×稀释系数的对数。即-2.2+0.37×(-0.3)=-2.31,-2.31的反对数=204,即1∶204稀释的抗体可保护50%的鸭胚免于死亡,即为该抗体50%的中和价。病毒对照组全部死亡,空白对照组全部存活。

表5 DHAV-C单价卵黄抗体中和效价
按照Reed-Muench法计算,能保护50%的鸭胚免于死亡的抗体稀释度介于10-2.2和10-2.5之间。距离比例=(65-50)/(65-40)=0.60,高于50%保护率抗体稀释度的对数+距离比例×稀释系数的对数。即-2.2+0.60×(-0.3)=-2.38,-2.38的反对数=240,即1∶240稀释的抗体可保护50%的鸭胚免于死亡,即为该抗体50%的中和价。

表6 DHAV-A和DHAV-C二价卵黄抗体中DHAV-C中和效价
按照Reed-Muench法计算,能保护50%的鸭胚免于死亡的抗体稀释度介于10-2.2和10-2.5之间。距离比例=(65-50)/(65-33)=0.46,高于50%保护率抗体稀释度的对数+距离比例×稀释系数的对数,即-2.2+0.46×(-0.3)=-2.33,-2.33的反对数=213,即1∶213稀释的抗体可保护50%的鸭胚免于死亡,即为该抗体50%的中和价。病毒对照组全部死亡,空白对照组全部存活。
2.2卵黄抗体对雏鸭的预防效果
卵黄抗体对雏鸭的预防试验结果见表7。每组10只雏鸭中,DHAV-A单价卵黄抗体试验组死亡1只,DHAV-C单价卵黄抗体试验组无死亡,DHAV-A和DHAV-C双价卵黄抗体试验组死亡2只,3个对照组的30只雏鸭全部死亡,不处理对照组全部存活。3种卵黄抗体的保护率分别为:DHAV-A单价卵黄抗体保护率90%,DHAV-C单价卵黄抗体保护率100%,DHAV-A和DHAV-C双价卵黄抗体保护率80%。
2.3卵黄抗体治疗试验结果
卵黄抗体对雏鸭的治疗试验结果见表8。每组10只雏鸭中,DHAV-A单价卵黄抗体组死亡2只,DHAV-C单价卵黄抗体组死亡1只,DHAV-A和DHAV-C双价卵黄抗体组死亡2只,对照组的30只雏鸭全部死亡,不处理对照组全部存活。3种卵黄抗体的治愈率分别为:DHAV-A单价卵黄抗体治愈率80%,DHAV-C单价卵黄抗体90%,DHAV-A和DHAV-C双价卵黄抗体治愈率80%。

表7 雏鸭注射卵黄抗体后攻毒发病情况统计

表8 雏鸭攻毒后注射卵黄抗体发病情况统计
3 讨论
卵黄抗体是鸭病毒性肝炎预防和治疗最常用的生物制品[6-7],为获得高效价的卵黄抗体,应采用高品质免疫原、有效的佐剂及恰当的免疫间隔时间。许多因素会影响高品质免疫原的获得[8-9],最重要的因素是抗原量和所使用的佐剂,以及抗原是否与佐剂充分混合,免疫原的制备效果能直接影响免疫原刺激免疫应答的力度和最终的抗体效价。王岳[10]采用从淄博市分离到的Ⅰ型鸭肝炎病毒免疫接种鸡制备得到的卵黄抗体对发病鸭群进行治疗,总体保护率可达94.6%。张占龙等[11]采用自行分离的基因A型和C型鸭甲型肝炎病毒研制了双价卵黄抗体,取得了良好的防治效果。本研究采用基因A型和C型DHAV强毒株作为抗原制备的单价和二价油乳剂灭活疫苗免疫高产蛋鸡后,获得了高效价的基因A型和C型DHAV单价及二价高免卵黄抗体,单价及二价卵黄抗体防治试验证明所制备的卵黄抗体防治效果良好,这为基因A型和C型DHAV引起的鸭病毒性肝炎的综合防控提供了理论依据和实践参考。
[1]Wang L,Pan M,Fu Y,et al.Classification of duck hepatitis virus into three genotypes based on molecular evolutionary analysis [J].Virus Genes,2008,37(1): 52-59.
[2]张雪,龚文孝,胡勇,等.Ⅰ型鸭肝炎病毒基因C型株的分离与鉴定[J].动物医学进展,2015,36(1):23-26.
[3]张小飞,黄显明,尹秀凤,等.鸭肝炎病毒A66弱毒株的水平传播感染[J].江苏农业学报,2011,27(4):813-817.
[4]高岭,刘聚祥,杨娜娜.鸡卵黄抗体及其在养猪业中的应用研究进展[J].动物医学进展,2013,34(5):110-114.
[5]张辉,崔焕忠,杨欢,等.卵黄抗体及其在疾病防制与饲料中的应用研究进展[J].中国畜牧兽医,2014,41(5)124-127.
[6]陈贤德,汪洋.鸭病毒性肝炎病毒高免卵黄抗体的免疫攻毒保护试验[J].黑龙江畜牧兽医,2013(12):97-98.
[7]郭全海,赵香菊,王伟龙.鸭肝炎病毒的分离、鉴定及其卵黄抗体高效制备研究[J].黑龙江畜牧兽医,2013(17):112-115.
[8]Broderson J R.A retrospective review of lesions associated with the use of Freund's adjuvant [J].Lab Anim Sci,1989,39(5):400-405.
[9]Mallon F M,Graichen M E,Conway B R,et al.Comparison of antibody response by use of synthetic adjuvant system and Freund complete adjuvants in rabbits [J].Am J Vet Res,1991,52 (9):1503.
[10]王岳.淄博市鸭病毒性肝炎的综合防治研究[D].山东泰安:山东农业大学,2008.
[11]张占龙,李敏,宋永鸿,等.鸭甲肝病毒基因A型和C型双价卵黄抗体的研制与保护效果研究[J].黑龙江畜牧兽医,2015(17):222-224.
Development and Application of Egg Yolk Antibodies Against Hepatitis A Virus Genotypes A and C
WANG Ji-lian,ZHANG Huan-rong,WANG Dong
(College of Life Science and Technology,Southwest University for Nationalities,Chengdu, Sichuan,610041,China)
The objective of this study was to develop monovalent and bivalent egg yolk antibodies against duck hepatitis A virus genotypes A and C to meet the requirement of prevention and treatment of duck viral hepatitis caused by duck hepatitis A virus genotypes A and C.Firstly,virulent duck hepatitis A virus genotype A and C strains were used as antigens to prepare monovalent and bivalent duck hepatitis A virus genotype A and C inactivated vaccine in oil-emulsion with Freud's adjuvant.Then the vaccines were used to immunize layer hens to produce immunized eggs for preparing highly immunized egg yolk antibodies.The good experimental prevention and treatment effects were acquired with both monovalent and bivalent egg yolk antibodies.
Duck hepatitis A virus; genotype; egg yolk antibody; prevention and treatment
2016-01-17
中央高校基本科研业务费专项资金项目(2014NZYQN58);兽医专业学位研究生教育实践基地建设项目
王继练(1989-),男,贵州盘县人,硕士研究生,主要从事动物疫病防治研究。*通讯作者
S852.659.6;S858.32
A
1007-5038(2016)09-0043-06

