不同评价标准在经动脉化疗栓塞联合索拉非尼治疗肝细胞癌中的应用价值*
陕西省肿瘤医院肿瘤消化科(西安710061)
黄山平 郑 鑫 ▲
不同评价标准在经动脉化疗栓塞联合索拉非尼治疗肝细胞癌中的应用价值*
陕西省肿瘤医院肿瘤消化科(西安710061)
黄山平郑鑫▲
目的:探讨mRECIST与RECIST疗效评价标准在经动脉化疗栓塞(TACE)联合索拉非尼治疗肝细胞癌疗效评价应用中的价值。方法:纳入我院采用TACE联合索拉非尼治疗肝细胞癌患者41例,通过对患者联合治疗前基线以及治疗后3个月复查的影像学检查结果,分别采用mRECIST与RECIST疗效标准对疗效进行评价,并对两种评估标准评价的结果进行对比,比较两组肿瘤反应结果与生存期的关系。结果:RECIST标准评价客观有效率(CR+PR)为2.44%,疾病控制率(CR+PR+SD)为87.80%,疾病进展率(PD)为12.20%;mRECIST标准评价客观有效率(CR+PR)为60.98%,疾病控制率(CR+PR+SD)为95.12%,疾病进展率(PD)为4.88%。两种不同标准下治疗效果对比客观有效率有显著性差异(P<0.05);而疾病控制率无显著性差异(P>0.05);通过Kaplan-Meier生存分存的Log-rank检验得出:RECIST标准中的PR与SD所对应的生存曲线之间无显著性差异(P>0.05),而与mRECIST标准中CR、PR、SD、PD所对应的生存曲线之间有显著性差异(P<0.05)。结论: mRECIS疗效评价标准以“存活肿瘤”对靶病灶进行疗效评价,结果更为客观、可靠,更适应目前TACE与靶向药物等具有新作用机制的治疗效果的评估。
主题词癌,肝细胞/诊断癌,肝细胞/药物疗法@经动脉化疗栓塞@mRECIST@RECIST
肝细胞癌是临床上较为常见的一种消化系统恶性肿瘤,手术是目前临床上治疗本病较为有效的一种方式[1]。但是,对一些丧失手术机会的患者而言,经动脉化疗栓塞(TACE)联合索拉非尼则成为主要的治疗手段[2]。随着临床研究的不断深入,RECIST评价标准受到不断的质疑[3]。2008年,美国肝脏病研究协会制定了mRECIST评价标准[4]。为进一步探讨mRECIST与RECIST疗效评价标准在TACE联合索拉非尼治疗肝细胞癌疗效中的价值,我院于2012年6月至2014年6月收治不可手术治疗的肝细胞癌患者41例,现分析报告如下。
资料与方法
1 一般资料选择我院收治且符合mRECIST以及RECIST疗效评价标准要求的不可手术切除的肝细胞癌患者41例,均符合纳入标准:①经影像学、血清甲胎蛋白(AFP)检查证实或病理检查证实为肝细胞癌的患者;②自愿参加本次研究并签字同意的患者;③患者至少有一个可以评估的病灶;④不适合手术治疗的患者等。也符合排除标准:①对本研究用药过敏的患者;②治疗时间小于3个月的患者;③服药期间存在因不良反应严重或其他原因停药的患者。其中男36例,女5例;年龄33~65岁,平均46.6±8.2岁;目标病灶中肿瘤直径2.4~14.4cm,平均4.7±3.5cm。肝功能Child-Pugh分级:A级患者36例,B级患者5例。
2治疗方法Seldinger法进行股动脉穿刺插管,置入导管行动脉造影,确定肿瘤位置和大小,根据肿瘤供血情况、患者肝功能情况等设定化疗药物及用量,将化疗药物(表柔比星、吡柔比星等)与碘油混合注入,明胶海绵栓塞。患者同时口服索拉非尼(规格:0.2g/片)治疗,2片/次,2次/d。
3影像学复查方法患者在接受TACE联合索拉非尼治疗后的4~6周,进行增强CT和(或)增强MRI的影像学复查。
4疗效评价标准观察两组患者治疗效果,比较两组肿瘤反应结果与生存期的关系。根据实体瘤疗效标准以及改良实体瘤疗效标准,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)以及进展(PD)。①RECIST标准:目标病灶选择标准为能够进行可重复测量的病灶。包括所有被累及器官。存在多个能够被测量的病灶时,按照病灶的大小以及可重复测量的原则,进行目标病灶的选择。病灶数量限定为每个器官最多选择2个,全身则不超过5个,其它均为非目标病灶。影像学复查方法进行CT、MRI检查;②mRECIST标准:目标病灶选择RECIST标准下能够被准确、重复测量的病灶。进行CT或MRI增强扫描可以见到病灶内的存活肿瘤区域强化。动脉期强化的病灶可选择作为mRECIST标准的目标病灶。影像学复查方法进行增强CT、增强MRI检查。两种疗效评价标准均采用单径测量,均采用完全缓解(CR)、部分缓解(PR)、病变稳定(SD)、病变进展(PD)作为疗效评价的结果,详见表1。

表1 RECIST与mRECIST标准比较
5疗效评价方法由两名具有丰富工作经验的高年资副主任以上影像科医师共同评阅患者联合治疗前基线以及治疗后3个月复查的影像学资料。每例患者均进行mRECIST与RECIST两种标准进行疗效评价。
6统计学方法采用SPSS18.0统计学软件包进行统计数据的处理分析,采用Marginal Homogeneity方法检测mRECIST标准与RECIST疗效评价标准间的差异,计数资料采用百分比表示,进行卡方检验,计量资料以均数±标准差表示,进行t检验,以P<0.05为有显著性差异,P<0.01为有极显著性差异。
结 果
1两种标准疗效评价结果分析见表2。41例患者中,经RECIST标准评估CR 0例,PR 1例,SD 35例,PD 5例;经mRECIST标准评估CR 4例,PR 21例,SD 14例,PD 2例;RECIST标准评价客观有效率(CR+PR)为2.44%,疾病控制率(CR+PR+SD)为87.80%,疾病进展率(PD)为12.20%;mRECIST标准评价客观有效率(CR+PR)为60.98%,疾病控制率(CR+PR+SD)为95.12%,疾病进展率(PD)为4.88%。两种不同标准下治疗效果对比客观有效率有显著性差异(P<0.05);而疾病控制率无显著性差异(P>0.05)。
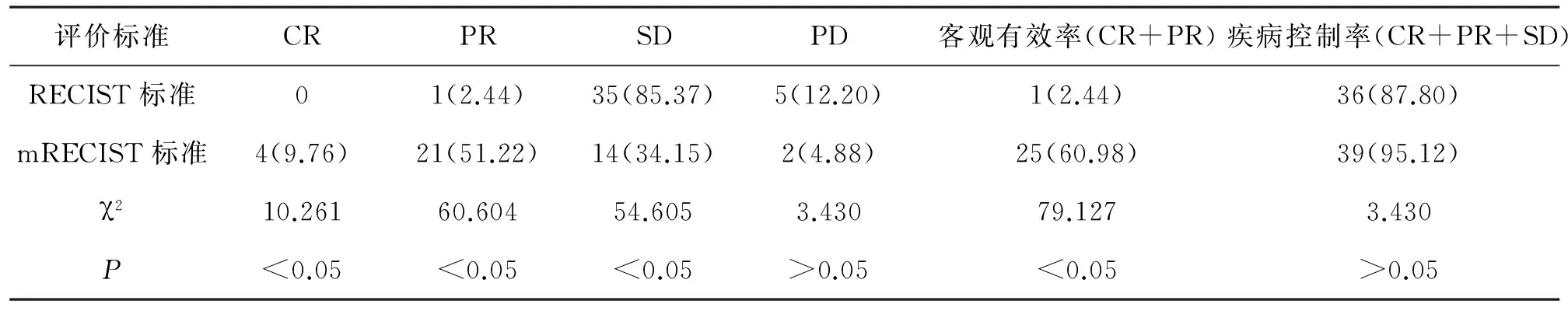
表2 两种标准疗效评价结果分析[n(%)]
2RECIST标准与mRECIST标准肿瘤反应结果与生存期的关系见表3。通过Kaplan-Meier生存分存的Log-rank检验得出:RECIST标准中的PR与SD所对应的生存曲线之间无显著性差异(P>0.05),而与mRECIST标准中CR、PR、SD、PD所对应的生存曲线之间有显著性差异(P<0.05)。

表3 RECIST标准与mRECIST标准肿瘤反应
讨 论
肝癌是临床上常见的恶性肿瘤之一,其病死率之高,位居男性恶性肿瘤病死率第二位,仅次于肺癌,严重威胁我国人民的生命安全[5]。临床上以外科手术切除为主要治疗手段。但由于肝癌生长缓慢,隐匿性强,早期临床症状不明显,多数患者就诊时已达到中晚期,错过最佳手术时机,甚至部分患者已经无法手术治疗。对于晚期肝癌患者临床上仍然以经皮肝动脉化疗栓塞术为主[6]。TACE是临床上较长采用的化疗方式,也是目前临床上最主要治疗晚期肝癌的手段,虽然理论上TACE对肿瘤细胞具有较强杀伤力,可有效治疗肝癌。但在实际应用中人们发现,TACE治疗容易发生肿瘤转移、复发情况,长期疗效并不理想。主要是由于TACE治疗导致肿瘤血管内皮细胞生长因子(VEGF)明显高于正常组织,而VEGF可促进新生血管的生成,导致肿瘤细胞重新建立血供循环,引起肿瘤的复发、转移,故如何有效治疗肝癌,防止肝癌细胞的复发成为人们关注的重点问题[7]。
随着分子领域的不断发展,分子靶向治疗恶性肿瘤成为人们研究的重点。索拉非尼是近年来研制出的分子靶向治疗新药物,其是一种多靶点和多激酶抑制药物,可明显抑制恶性肿瘤的增殖,对肿瘤新生血管同样有强大的抑制作用。研究显示:在TACE治疗后,肿瘤细胞处于缺氧环境,会导致VEGF的过度表达,导致新生血管生成,降低治疗效果。但在联合索拉非尼治疗后,可避免肿瘤的复发、转移,抑制VEGF的表达,抑制新生血管生成,促进治疗效果。随着肿瘤治疗药物作用机制以及治疗方法的不断变化,以往的一些疗效标准,包括WHO标准以及RECIST标准等,均不能全面、客观、准确的对治疗效果进行评价[8]。因此,为了突破传统疗效评价标准的局限性,制定新的评价标准就成为临床研究的热点。2000年,欧洲肝脏研究协会建议进行肿瘤治疗的疗效评价时,以增强扫描动态CT或MRI动脉期中显示的“存活肿瘤”的变化对疗效进行评估[9]。2008年,美国肝脏病研究协会则将“存活肿瘤”的概念应用到肝癌治疗的疗效评价标准中,并制定了mRECIST标准。但在临床研究中发现:不同标准下采用TACE联合索拉非尼治疗的报道并不一致,临床上无法统一,导致治疗结果存在较多争议,故采用统一治疗标准来评价TACE联合索拉非尼治疗肝细胞癌的治疗效果有着重要意义[10]。
为进一步探讨mRECIST与RECIST疗效评价标准在TACE联合索拉非尼治疗肝细胞癌疗效中的价值,我们对41例肝细胞癌不可手术患者进行了分析,发现两种标准在评价疗效时存在较大的差异。经RECIST标准评估CR 0例,PR 1例,SD 35例,PD 5例; 经mRECIST标准评估CR 4例,PR 21例,SD 14例,PD 2例; RECIST标准评价客观有效率(CR+PR)为2.44%,疾病控制率(CR+PR+SD)为87.80%,疾病进展率(PD)为12.20%;mRECIST标准评价客观有效率(CR+PR)为60.98%,疾病控制率(CR+PR+SD)为95.12%,疾病进展率(PD)为4.88%。 两种评价标准的评价结果存在显著性差异。结果表明:mRECIS评价更为严格,能有效地体现出临床疗效,更适合成为临床疗效标准的判断指标。
需要注意的是,mRECIST疗效评价标准在临床应用中也有一定的局限性。有研究表明:当肝细胞癌患者病灶为弥漫、多发性时,目标病灶的选择较为困难,导致无法准确的测量目标病灶的变化情况。另外,由于“存活肿瘤”主要以增强CT或MRI检查下的动脉期强化作为标准,但强化程度尚缺乏量化指标以及病理对照研究依据等。我们通过对RECIST标准与mRECIST标准肿瘤反应结果与生存期的关系进行分析发现RECIST标准中的PR和SD所对应的生存曲线之间无显著性差异,而mRECIST标准中CR、PR、SD、PD所对应的生存曲线之间有显著性差异,结果表明:mRECIS评价更为严格,能有效地体现出临床疗效,更适合成为临床疗效标准的判断指标。
[1]戴志军,马军,吴小红,等.mRECIST和RECIST对肝癌RFA术后疗效评价的比较[J].宁夏医学杂志,2015,37(6):547-549.
[2]魏照光,陆骊工,邵培坚,等.肝动脉化疗栓塞联合索拉非尼治疗中晚期肝细胞癌的临床疗效观察[J].中华放射学杂志,2012,46(3):252-256.
[3]冯晓波,刘玉林,陈 宪,等.CT对原发性肝癌TACE疗效评价的mRECIST和RECIST对比研究[J].临床放射学杂志,2012,31(9):1334-1337.
[4]丁婕,戴旭,苏红英,等.RECIST1.0和mRECIST在原发性肝癌TACE术后疗效评价中的对比研究[J].中国临床医学影像杂志,2014,25(9):623-626.
[5]吴昶皓,张红卫,许林峰,等.AFP和mRECIST评价索拉非尼治疗晚期肝癌疗效及预后价值的分析[J].中华肿瘤防治杂志,2013,20(13):1016-1020.
[6]华余强,雷蕾.结直肠癌肝转移TACE后疗效评价的RECIST和mRECIST对比研究[J].临床和实验医学杂志,2013,12(12):936-939.
[7]Kawaoka T,Aikata H,MurakamiE,etal.Evaluation of the mRECIST and α-fetoprotein ratio for stratification of the prognosis of advanced-hepatocellular-carcinoma patients treated with sorafenib[J].Oncology: International Journal of Cancer Research and Treatment,2012,83(4):192-200.
[8]姚雪松,闫 东,刘德忠,等.mRECIST标准与RECIST标准评价经动脉化疗栓塞联合索拉非尼治疗不可切除肝细胞癌疗效的比较[J].中华肝胆外科杂志,2013,19(5):332-336.
[9]Li H,Guo Z,Si T,etal.EASL and mRECIST responses are independent predictors of survival in hepatocellular carcinoma patients treated with cryoablation[J].European Journal of Gastroenterology and Hepatology,2013,25(5):620-627.
[10]王琳,王馨.靶向时代肿瘤疗效评价标准的探索[J].中国肿瘤临床,2015,42(6):366-370.
(收稿:2016-03-20)
西安交通大学医学院第一附属医院
R735.7
A
10.3969/j.issn.1000-7377.2016.09.038
*国家自然科学基金资助项目(81301743)
陕西省科技攻关项目(2014K11-01-01-21)

