不同防污涂层下5083铝合金的海水腐蚀性能研究
曹京宜,张寒露,张锋,全乐,唐聿明
(1.海军涂料分析检测中心,北京 102442;2.西三环中路19号,北京 100036;3.北京化工大学,北京 100029)
不同防污涂层下5083铝合金的海水腐蚀性能研究
曹京宜1,张寒露1,张锋2,全乐3,唐聿明3
(1.海军涂料分析检测中心,北京 102442;2.西三环中路19号,北京 100036;3.北京化工大学,北京 100029)
目的 研究舰船用不同类型防污漆下5083铝合金的海水腐蚀性能。方法 采用电化学交流阻抗方法研究加入不同防污剂的三种舰船常用防污体系在完好状态下和人工破损状态下的耐蚀性能。结果 获得了3种不同防污体系对5083铝合金在海水浸泡条件下的耐蚀性能结果。结论 在涂层体系完好时,加入不同种类防污剂的防污漆体系对基体5083铝合金都有很好的保护作用。其中低表面能类型的防污涂料不易发生水解,所以涂层阻抗随时间变化的幅度很小,涂层的屏蔽性更好、涂层孔隙率更低、颜料与溶液反应阻力更大,保护作用最优异,性能最稳定。在涂层破损状态下,三种防污体系的腐蚀速率为低表面能<硫氰酸亚铜<Cu2O防污涂层,防污涂层中存在的防污剂Cu2O可加速铝合金基体的腐蚀。
防污涂层;电化学交流阻抗;铜离子释放;铝合金;腐蚀
舰船在海洋中航行、停泊时,会有部分生物、微生物附着。船底附着海洋生物后,粗糙度增加,机械磨损增大,造成航行时阻力增大,航速降低,燃油消耗量增加。涂覆防污涂层是最有效的方法,且应用广泛、比较经济[1—3]。目前所使用的具有化学活性的防污涂料中很多都添加氧化亚铜作为填料[4]。铜在生物体内沉积的可能性很小[5],不像有机锡对海洋生物及海洋环境的破坏巨大[6],严重影响生态环境。前人针对自抛光防污涂层中Cu2+的渗出以及对海洋环境的影响做了大量的研究[7—10],关于自抛光防污涂层中渗出的Cu2+对船体腐蚀尤其是铝合金船体的腐蚀情况的研究相对较少。文中主要研究了含氧化亚铜、硫氰酸亚铜和低表面能等三种防污剂的防腐防污涂层在3.5%NaCl溶液浸泡过程中对5083铝合金基体腐蚀行为影响,对比了三种舰船常用防污体系在完好状态下和人工破损状态下的耐蚀性能。
1 实验
1.1材料
实验材料是5083铝合金板,规格为12 cm×5 cm×0.5 cm,其化学成分(以质量分数计)为:Mg 4.0%~4.9%,Si≤0.4%,Cu≤0.1%,Zn≤0.25%, Mn 0.4%~1.0%, Ti≤ 0.15%, Cr 0.05%~0.25%,Fe 0~0.4%,Al余量。应用的涂料体系见表1。

表1 5083铝合金防污涂层配套体系W1,W2和W3Table 1 W1,W2 and W3 antifouling coating systems of 5083 aluminum alloy
1.2材料准备
先用120#干砂纸将5083铝合金打磨至露出基材表面,然后用酒精擦拭干净。涂刷时,先涂刷厚度为120~150 μm的防腐底漆,再涂刷厚度为100 μm的中间漆,最后涂刷防污面漆,厚度为250 μm。
1.3电化学测试
采用CS300电化学工作站(武汉Corrtest公司生产)对浸泡于3.5%NaCl溶液中的涂层/铝合金试样及铝合金试样进行动电位极化曲线测试。扫描速率为1 mV/s。工作电极为试样,暴露面积为1 cm2,辅助电极为铂电极,参比电极为饱和甘汞电极(SCE)。
采用普林斯顿公司的PARSTAT 2273电化学工作站对涂层/铝合金试样进行交流阻抗测试。频率范围为10 mHz~100 kHz,振幅为10 mV。试样的暴露面积为10 cm2,介质为3.5%NaCl溶液。在开路电位下进行。
2 结果和讨论
在三种舰船常用防污漆配套涂层体系中,W1配套的防污漆中含有Cu2O,W2配套的防污漆中含有CuSCN,W3配套的防污漆是低表面能类型的防污漆,不含任何的含铜离子的防污剂。下面通过实验,对比研究W1,W2和W3三种涂层体系对5083铝合金基材防护性能的影响。
2.1完好涂层的电化学交流阻抗测试
W1完好涂层/铝合金试样在3.5%NaCl溶液中浸泡637 d过程中的EIS图谱如图1所示。可以看出,W1在浸泡初期(2 h)Bode图是近似于斜率为-1的一条直线,低频阻抗模值(|Z|0.01Hz)在1010~1011Ω·cm2,而Nyquist图谱表现为一个不完整的半圆。表明浸泡初期W1作为一个屏蔽层,较好地隔绝了腐蚀介质与基体的直接接触,从而使铝合金基体得到较好的保护。浸泡8 h后,W1试样的Nyquist图谱中容抗弧半径减小,Bode图中涂层的低频阻抗模值(|Z|0.01 Hz)也有所下降,表明溶液通过涂层中的微孔不断向涂层渗入。随着浸泡时间的延长,2 d后W1低频阻抗模值有所回升,可能是涂层中颜料反应后生成的腐蚀产物堵塞了一些涂层上的微孔,从而使涂层阻抗值逐渐上升。45 d 后W1低频阻抗模值下降,这是由于随着溶液渗入,涂层中的颜料继续反应,使得涂层的孔隙率变大,涂层的屏蔽性能下降。浸泡至466 d,Bode图低频阻抗模值下降了一个数量级。至637 d,变化不大,低频阻抗值在109~1010Ω·cm2,说明涂层的保护性能依然很好。
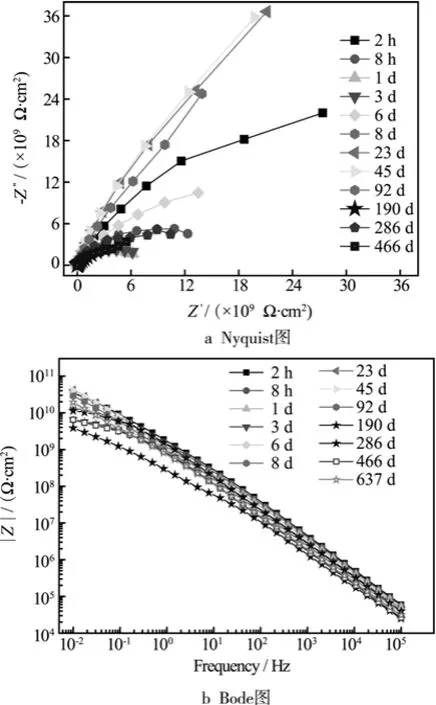
图1 W1完好涂层/铝合金试样在3.5%NaCl溶液中浸泡637 d的EIS图谱Fig.1 EIS plots of W1 antifouling coating/Al alloy after immersion in 3.5%NaCl solution for 637 d
采用等效电路对W1的阻抗数据进行拟合,如图2所示。浸泡2~8 h,用ModelA进行等效电路拟合,浸泡1~637d,用ModelC进行等效电路拟合。
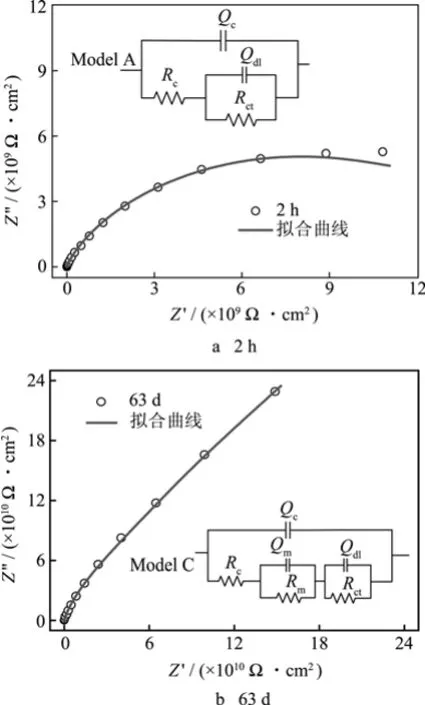
图2 W1完好涂层体系的阻抗数据的等效电路拟合结果Fig.2 The fitted EIS plots of W1 antifouling coating samples
W2完好涂层体系在3.5%NaCl溶液中浸泡不同时间的EIS图谱如图3所示。可以看出,涂层体系在浸泡初期(2 h)Bode图是近似于斜率为-1的一条直线,低频阻抗模值在 1010~1011Ω·cm2;Nyquist图谱表现为一个不完整的半圆,表明浸泡初期复合涂层作为一个屏蔽层,较好地隔绝了腐蚀介质与基体的直接接触,从而使铝合金基体得到较好的保护。浸泡8 h后,W2试样的Nyquist图谱中容抗弧半径减小,Bode图中涂层的低频阻抗模值也有所下降,表明溶液通过涂层中的微孔不断向涂层渗入。随着浸泡时间的延长,190 d后W4的低频阻抗模值有所回升,可能是涂层中颜料反应后生成的腐蚀产物堵塞了一些涂层上的微孔,从而使涂层阻抗值逐渐上升并维持不变。时间延长,变化不大,至634 d,低频阻抗值仍在109Ω·cm2以上,说明涂层的保护性能依然很好。
采用图4的电路图对涂层进行等效电路拟合。浸泡2~8 h,用Model B进行等效电路拟合,浸泡1~634 d,用Model C进行等效电路拟合。

图3 W2完好涂层/铝合金试样在3.5%NaCl溶液中浸泡634天的EIS图谱Fig.3 EIS plots of W2 antifouling coating/Al alloy after immersion in 3.5%NaCl solution for 634 d

图4 W2完好涂层试样的阻抗数据的等效电路拟合结果Fig.4 The fitted EIS plots of W2 antifouling coating samples
W3完好涂层/铝合金试样在3.5%NaCl溶液中浸泡604 d过程中的EIS图谱如图5所示。可以看出,涂层体系在浸泡初期(2 h)Bode图是近似于斜率为-1的一条直线,低频阻抗模值接近超过1011Ω·cm2;而Nyquist图谱表现为一个不完整的半圆。这表明浸泡初期复合涂层作为一个屏蔽层,较好地隔绝了腐蚀介质与基体的直接接触,从而使铝合金基体得到较好的保护。随着浸泡时间的延长,直至604 d阻抗图谱基本没有明显变化,低频阻抗值仍在1011Ω·cm2以上,说明涂层的防护性能优异,性能非常稳定状态。
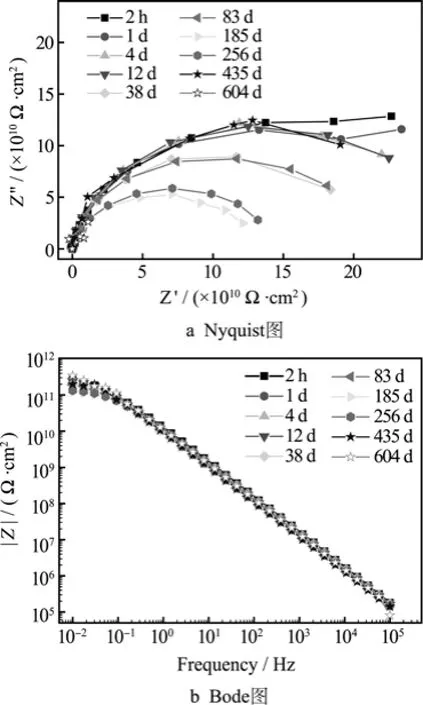
图5 W3完好涂层/铝合金试样在3.5%NaCl溶液中浸泡不同时间的EIS图谱Fig.5 EIS plots of W3 antifouling coating/Al alloy after immersion in 3.5%NaCl solution for different times
采用图6的电路图对涂层进行等效电路拟合。浸泡2 h~604 d,用Model B进行等效电路拟合。
W1,W2和W3的涂层电阻Rc随浸泡时间(总计466天)的变化曲线如图7所示。可以看出,在浸泡初期,W1和W2的涂层电阻都是先下降,这是因为电解质溶液渗入涂层,涂层吸水造成的涂层电阻下降;随着浸泡时间的延长,W1和W2涂层电阻趋于稳定,这是因为涂层的吸水达到饱和,涂层电阻维持在一个较为稳定的值;当浸泡了100 d左右以后,W1和W2的涂层电阻增大,可能是由于腐蚀产物堵塞了涂层的孔隙,阻碍了电解质溶液的渗入,造成涂层电阻增大。在整个浸泡过程中,W3的涂层电阻虽然整体随着浸泡时间的变化有缓慢的下降,但始终处于一个较稳定的范围,变化不超过一个数量级。W2比W1的涂层屏蔽作用稍好些。
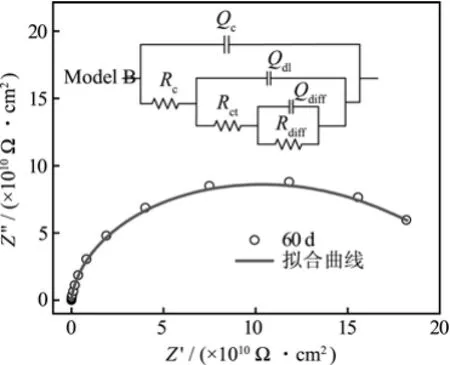
图6 W3完全好涂层试样的阻抗数据的等效电路拟合结果Fig.6 The fitted EIS plots of W3 antifouling coating samples
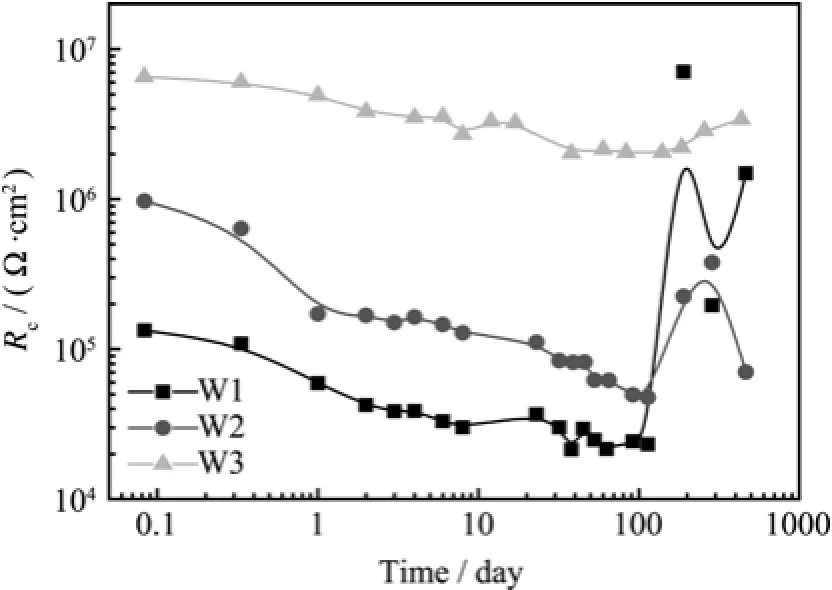
图7 W1,W2和W3涂层电阻Rc随浸泡时间的变化曲线Fig.7 The variations of Rcof W1,W2 and W3 antifouling coatings with the immersion time in seawater
W1,W2和W3防腐蚀底漆中颜料表面的反应电阻(Rct)随时间(总计466 d)变化曲线如图8所示。可以看出,在浸泡初期Rct先下降,这是由于电解质溶液渗入,电解质溶液与涂层中的颜料接触,迅速反应;随着浸泡时间的延长,Rct逐渐上升,于这可能是由于腐蚀产物包覆在颜料表面或是堵塞了涂层的空隙,增加了涂层颜料与电解质的反应阻力。
根据对W1,W2和W3三种涂层体系的Rc和Rct的分析可知,浸泡初期,W3比较稳定,Rc随时间变化的幅度很小,并且Rc,Rct的值都较W1以及W2高,说明与W1,W2相比较,W3的涂层屏蔽性好、涂层孔隙率低、颜料与溶液反应阻力大。可能是由于W3为低表面能类型的防污涂料,该涂料不发生水解,所以Rc随时间变化的幅度很小,并且涂层屏蔽性好、涂层孔隙率低。总体来说,W3对基体5083铝合金具有非常优异的保护作用。W1和W2在超过600 d的时间内对基体也具有很好的保护作用。
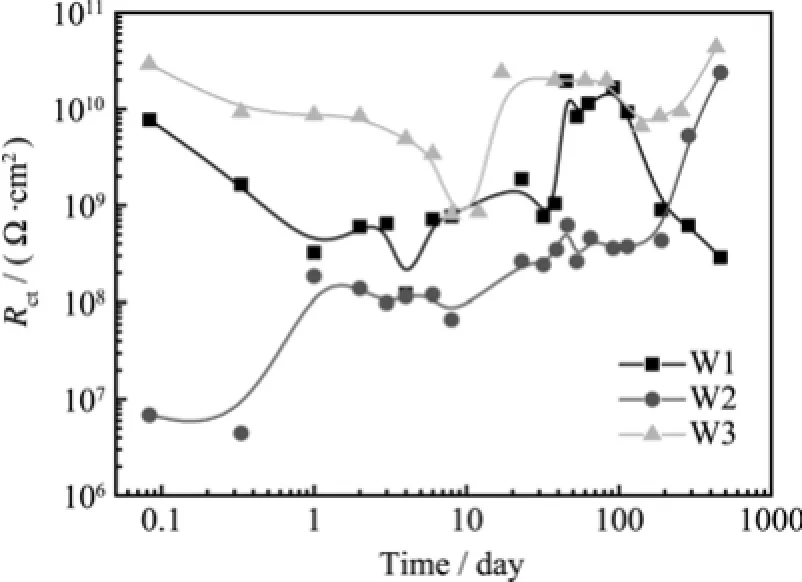
图8 W1,W2和W3的表面反应电阻Rct随时间变化曲线Fig.8 The variations of Rctof W1,W2 and W3 antifouling coatings with the immersion time in seawater
2.2W1,W2和W3人工十字破损的涂层电化学交流阻抗测试
W1人工十字破损涂层在3.5%NaCl溶液中浸泡93天的EIS图谱如图9所示。可以看出,人工十字破损的W1在浸泡2 h后,Nyquist图是一个不完整的半圆弧,阻抗值|Z|0.01 Hz略低于107Ω·cm2;在浸泡了2 h之后,低频阻抗值下降,Nyquist图弧半径减小,涂层的保护作用下降;浸泡不到一周,Bode图低频区出现一个较宽的平台,阻抗值|Z|0.01 Hz也降至106Ω·cm2,涂层失去保护作用。但随着时间的延长,涂层的阻抗又有所增大,可能与腐蚀产物的堆积有关。
W2人工十字破损涂层在3.5%NaCl溶液中浸泡120 d的EIS图谱如图10所示。可以看出,人工十字破损的W2在浸泡2 h后,Nyquist图是一个不完整的半圆弧,阻抗值|Z|0.01 Hz于107~108Ω·cm2;浸泡22 d之后,Nyquist图低频区出现第二个圆弧,此时溶液已经进入涂层与基体的界面,溶液与基体发生反应;在浸泡了43 d之后,低频阻抗值下降,Nyquist图弧半径先增大后减小,bode图出现一个较宽的台阶,涂层屏蔽性能下降,失去保护作用。随着时间的继续延长,变化不大,120 d,低频阻抗值在106Ω·cm2左右。
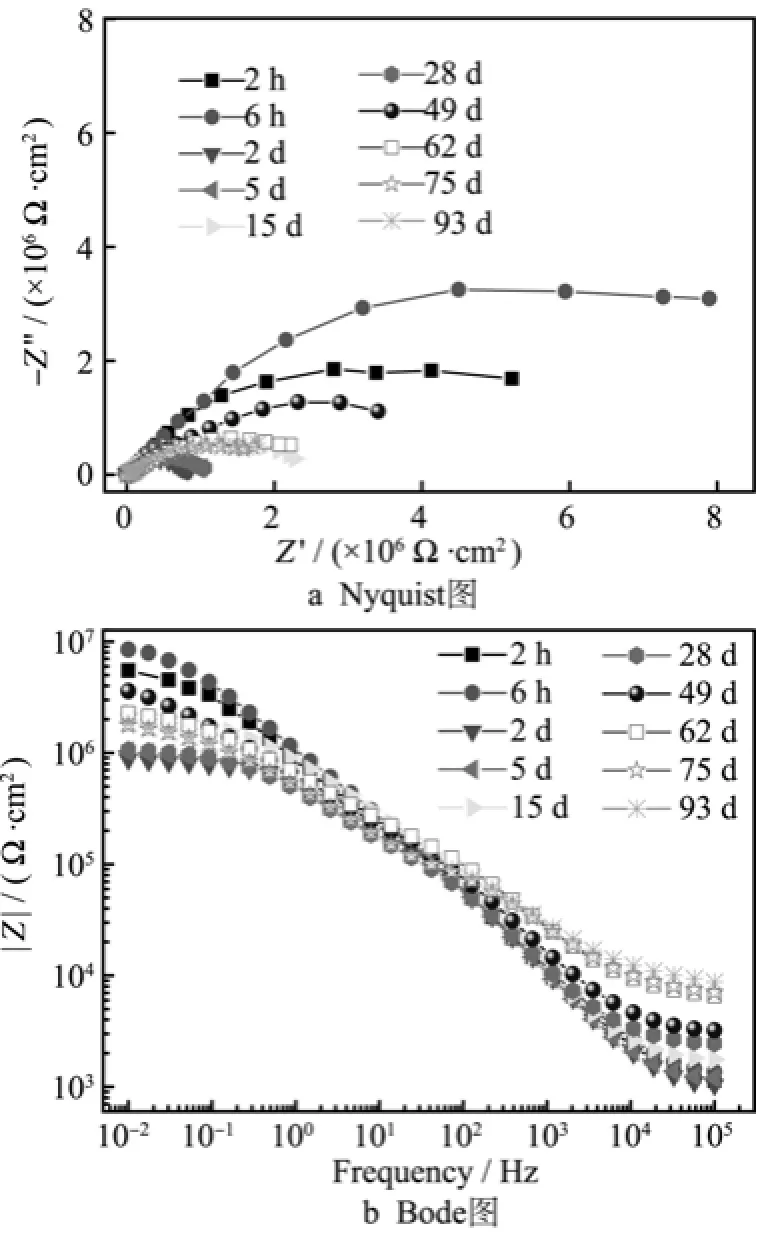
图9 W1人工十字破损涂层/铝合金试样在3.5%NaCl溶液中浸泡93天的EIS图谱Fig.9 EIS plots of W1 broken cross antifouling coating/Al alloy after immersion in 3.5%NaCl solution for 93 d

图10 W2人工十字破损涂层/铝合金试样在3.5%NaCl溶液中浸泡120天的EIS图谱Fig.10 EIS plots of W2 broken cross antifouling coating/Al alloy after immersion in 3.5%NaCl solution for 120 d
W3人工十字破损涂层在3.5%NaCl溶液中浸泡不同时间的EIS图谱如图11所示。可以看出,人工十字破损的W3在浸泡2 h后,Nyquist图是一个不完整的半圆弧,并且低频阻抗值上升,Nyquist图弧半径增大,涂层起到阴极保护作用,在浸泡过程中,W7的一直处于稳定状态,对基体有较好的保护作用。时间延长至94 d,低频阻抗值|Z|0.01 HZ维持在107Ω·cm2。至145 d,Bode图低频区出现一个较宽的台阶,涂层屏蔽性能下降,失去保护作用,|Z|0.01 HZ降为106Ω·cm2。
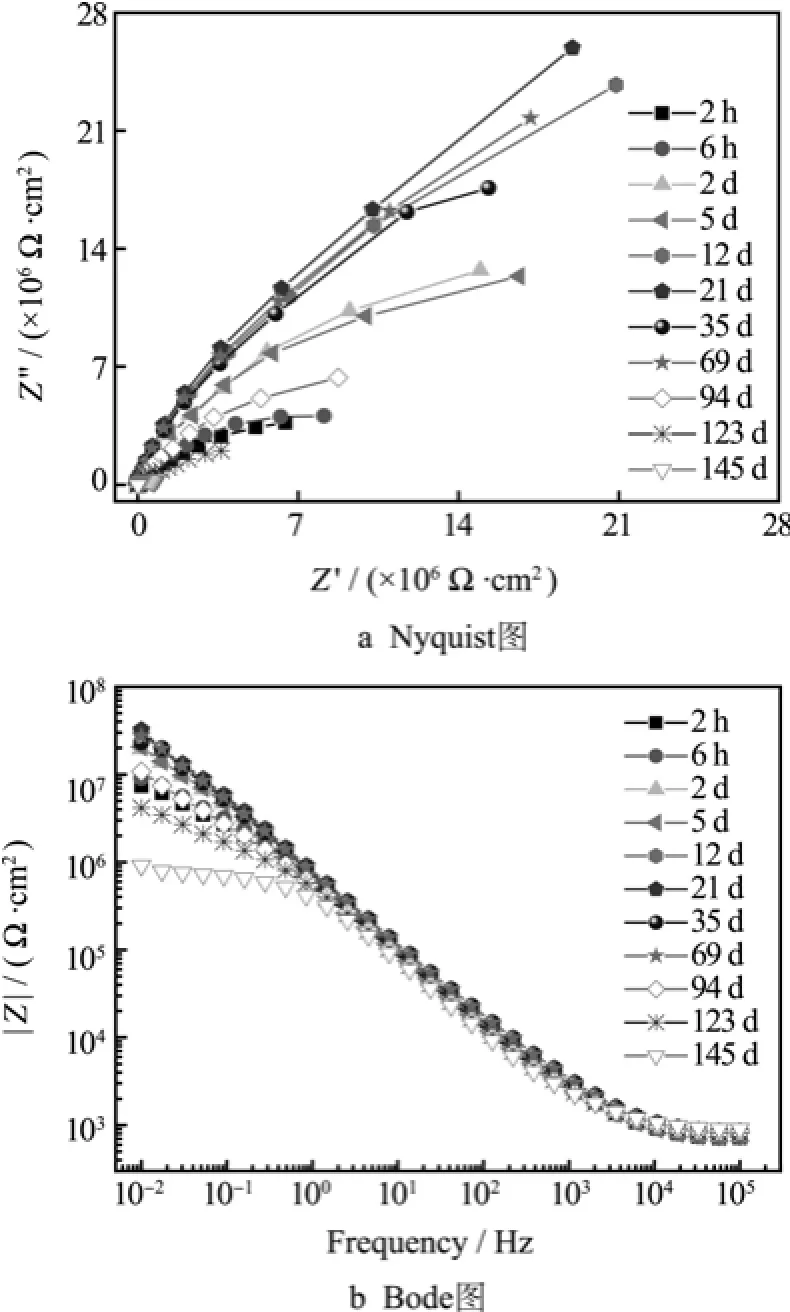
图11 W3人工十字破损涂层/铝合金试样在3.5%NaCl溶液中浸泡145天EIS图谱Fig.11 EIS plots of W3 broken cross antifouling coating/Al alloy after immersion in 3.5%NaCl solution for 145 d
通过比较W1,W2和W3三种人工十字破损涂层/铝合金试样的电化学交流阻抗测试结果,可以发现,W3在浸泡145 d之后失去对基体的保护作用,在此之前一直对基体起到很好的保护作用,这可能是由于W3为低表面能类型的防污涂层,不含任何的防污剂。而W1和W2由于分别含有氧化亚铜和硫氰酸亚铜,Cu2+释放到溶液中,通过破损处和铝合金基体反应,涂层很快就失去了对基体的保护作用。当涂层破损后,W1对基体的保护时间不到一周,W2在3周内对基体还有保护作用。相比较而言,含硫氰酸亚铜的W2比含有氧化亚铜的W1对基体的保护作用更长。
3 结论
1)在涂层体系完好时,加入不同种类防污剂的防污漆体系对基体5083铝合金都有很好的保护作用。其中,W3为低表面能类型的防污涂料,该涂料不易发生水解,所以涂层阻抗(Rc)随时间变化的幅度很小,涂层的屏蔽性更好、涂层孔隙率更低、颜料与溶液反应阻力更大。总体来说,W3的保护作用最优异,性能最稳定。与W1(含氧化亚铜防污漆)相比,W2(含硫氰酸亚铜)的涂层对5083铝合金的屏蔽作用更好一些。
2)在涂层破损的情况下,W3低表面能防污漆在两个月的时间内仍然可以较好地保护铝合金基体;含氧化亚铜的W1对基体的保护作用不到一周,含硫氰酸亚铜的W2在三周内对基体还有一定的保护作用。试验证明,涂层发生破损后,防污剂中的铜释放出来的Cu2+在破损处周围集聚,会大大促进破损处基体铝合金的腐蚀。含铜量越高对基体腐蚀的促进作用越明显,含有Cu2O的防污剂腐蚀速率最高。
3)可以利用 0.01 Hz频率下的阻抗模值(|Z|0.01 Hz)评价防腐防污涂层体系对基体的保护性能。在涂层破损状态下,三种防污体系的腐蚀速率为低表面能<硫氰酸亚铜<Cu2O防污涂层,防污涂层中存在的防污剂Cu2O可加速铝合金基体的腐蚀。
[1]SHAW B A,DAVIS G D,FRITZ T L,et al.The Influence of Tungsten Alloying Additions on the Passivity of Aluminum[J].Journal of The Electrochemical Society,1991,138(11):3288—3295.
[2]DAVIS G D,MOSHIER W C,LONG G G,et al.Passive Film Structure of supersaturated Al-Mo Alloys[J].Journal of The Electrochemical Society,1991,138(11):3194—3199.
[3]SZKLARSKA-SMIALOWSKA Z.Pitting Corrosion of Aluminum[J].Corrosion Science,1999,41(9):1743—1767.
[4]CARROL W,BRESLIN C.Stability of Passive Films Formed on Aluminum in Aqueous Halide Solutions[J]. British Corrosion Journal,1991,26(4):255—259.
[5]HORST R.Corrosion Evaluation of Aluminum Easy-open Ends on Tinplate Cans[J].Mater Perform,1977,16(3):23—28.
[6]LIAO C M,OLIVE J M,GAO M,et al.In-situ Monitoring of Pitting Corrosion in Aluminum Alloy 2024[J].Corrosion,1998,54(6):451—458.
[7]LIAO C M,WEI R P.Galvanic Coupling of Model Alloys toAluminum—AFoundationforUnderstanding Particle-inducedPittinginAluminumAlloys[J]. Electrochimica Acta,1999,45(6):881—888.
[8]ALAVI A,COTTIS R A.The determination of pH,PotentialandChlorideConcentrationinCorroding Crevices on 304 Stainless Steel and 7475 Aluminium Alloy[J].Corrosion Seience,1987,27(5):443—451.
[9]NISANCIOGLUK.ElectrochemicalBehaviorof Aluminum-BaseIntermetallicsContainingIron[J]. Journal of the Electrochemical Society,1990,137(1):69—77.
[10]BUCHHEIT R G,MARTINEZ M A,MONTES L P. Evidence for Cu Ion Formation by Dissolution and Dealloying the Al2CuMg Intermetallic Compound in Rotating Ring-Disk Collection Experiments[J].Joumal of the Electrochemical Society,2000,147(1):119—124.
Seawater Corrosion Performances of 5083 Aluminum Alloy under
Antifouling Coating Systems
CAO Jing-yi1,ZHANG Han-lu1,ZHANG Feng2,QUAN Le3,TANG Yu-ming3
(1.Naval CoatingsAnalysis and Test Center,Beijing 102442,China;2.Middle Road No 19 of XISANHUAN,Beijing 100036,China;3.Beijing University of Chemical Technology,Beijing 100029,China)
Objective To investigate the seawater corrosion performances of 5083 Aluminum Alloy under different kinds of ship antifouling coating systems.Methods Corrosion resistances of three kinds of ship antifouling coating systems containing different antifouling agents with and without artificial damages were studied by electrochemical impedance spectroscopy. Results The corrosion resistances results of three kinds of ship antifouling coating systems on 5083 aluminum alloy immersed in seawater were obtained.Conclusion For coatings without artificial damages,all the antifouling coating systems had very good protective property on 5083 aluminum alloy.Among them,the antifouling coating with low surface free energy showed the best barrier property and stable performance,this is probably because it was difficult for the coating system with low surface free energy to be hydrolyzed so as to have slight variation of the impedance with immersion time and much lower porosity and bigger reaction resistance of pigment with electrolyte.Under condition of artificial damages of the antifouling coatings,the corrosion rate for three coating systems followed the order of v(low surface free energy coating)<v(CuSCN)<v(Cu2O). Therefore,Cu2O in the antifouling coating might accelerate the corrosion of the aluminum alloy.
antifouling coating;EIS;release of cupric ion;aluminum alloy;corrosion
2016-03-28;Revised:2016-04-06
10.7643/issn.1672-9242.2016.04.005
TJ04;TG172.5
A
1672-9242(2016)04-0028-07
2016-03-28;
2016-04-06
曹京宜(1972—),女,安徽人,博士,高级工程师,主要研究方向为材料加工工程。
Biography:CAO J ing-yi(1972—),Female,from Anhui,Ph.D.,Senior engineer,Research focus:material processing engineering.

