乙基环己烷催化裂解制低碳烯烃反应动力学
张睿,郭少鹏,刘贵丽,刘海燕,刘植昌,孟祥海
(中国石油大学(北京)重质油国家重点实验室,北京 102249)
乙基环己烷催化裂解制低碳烯烃反应动力学
张睿,郭少鹏,刘贵丽,刘海燕,刘植昌,孟祥海
(中国石油大学(北京)重质油国家重点实验室,北京 102249)
利用小型固定床实验装置研究了乙基环己烷在基于ZSM-5分子筛介孔催化剂上的裂解性能,发现乙基环己烷具有较好的裂解性能,原料转化率在80%以上,乙丙烯收率(质量分数)可达41%,低碳烯烃收率(质量分数)接近50%,液体产物主要是苯、甲苯、二甲苯等芳香烃。同时考虑乙基环己烷催化裂解过程中的热反应与催化反应,建立了包含14个反应的动力学模型。基于4个反应温度下的裂解实验数据,求取了反应动力学模型的参数。求得的表观活化能均在90 kJ·mol-1以下,主要组分收率的模型预测值与实验值的平均相对误差不高于10%。
反应动力学;催化;固定床;乙基环己烷;乙烯;丙烯
引 言
乙烯和丙烯等低碳烯烃是重要的有机化工原料,其生产一直受到工业界的重视。蒸汽裂解是乙丙烯生产最重要的工艺过程,其原料一般为乙烷、丙烷、丁烷、石脑油等轻烃以及加氢裂化尾油,尽管乙丙烯收率很高,但是裂解所需反应温度高,过程能耗大,且产物中乙丙烯的比例不易调控,丙烯/乙烯比值较低。催化裂化工艺通过调整催化剂、工艺条件以及反应器型式能够增产丙烯,且丙烯收率远高于乙烯收率,但是催化裂化的主要产物为汽柴油,丙烯增产幅度有限[1]。近些年来出现的催化裂解工艺兼具蒸汽裂解与催化裂化的优势,不仅乙丙烯收率高,乙丙烯比例易调控,且反应温度较低[2-3]。催化裂解的原料范围广泛,不仅包括传统的蒸汽裂解原料[4-5],还包括减压瓦斯油[6]、渣油[7-8]等催化裂化原料,以及碳四烯烃[9-10]、催化裂化汽油[11-12]、焦化汽油[12-13]等原料。
轻烃是催化裂解的重要原料,有关轻烃催化裂解的反应规律已有众多研究报道。在石脑油原料中,大分子正构烷烃有着优异的裂解性能,小分子正构烷烃、异构烷烃与环烷烃的裂解性能居中,芳香烃的裂解性能较差。催化裂解过程中,环烷烃既能开环分解生成低碳烯烃,也能通过氢转移、脱氢等反应生成芳香烃。因此对于裂解催化剂,强化环烷烃的开环分解反应是催化剂设计的重点之一。
反应动力学研究对于催化裂解过程的优化操作以及新型裂解工艺的开发有着重要的作用,轻烃催化裂解反应动力学研究也有相关报道。Meng等[14]研究了碳四烃的催化裂解性能并建立了六集总动力学模型,其中原料丁烷、丁烯分别集总,目的产物乙烯、丙烯分别集总,氢气与小分子烷烃作为1个集总,液体产物与焦炭作为1个集总,研究发现丁烯具有良好的裂解性能,而丁烷只有在高温下才具有裂解性能。Sedighi等[15]研究了石蜡基石脑油的催化裂解性能并建立了六集总动力学模型,其中石脑油原料作为1个集总,目的产物乙烯、丙烯分别集总,其他气体产物作为1个集总,液体产物、焦炭分别集总。研究发现需要在高温短停留时间的条件下操作才能获得高的低碳烯烃收率。孙忠超等[16]利用结构导向集总模型和Monte Carlo模拟方法研究了催化裂化汽油的催化裂解反应动力学,建立了分子尺度的动力学模型。Lee等[17]研究了石蜡基石脑油的催化裂解与热裂解性能,发现在高反应温度下热裂解作用不能忽视,当反应温度高于 675℃时热裂解作用将超过一半;基于反应机理分析建立了一个包含121个物质与143个反应的复杂热反应与催化反应动力学模型。
环烷烃作为石脑油中的重要组分,研究其催化裂解反应动力学将有助于加深对轻烃催化裂解的认识,并可为裂解催化剂的设计开发与裂解工艺条件的优化提供指导。考虑到直馏石脑油中环烷烃的平均碳数一般在8左右,本文对乙基环己烷的催化裂解反应动力学进行研究。
1 实验材料和方法
1.1裂解原料与催化剂
裂解所用原料为分析纯的乙基环己烷。所用催化剂为中国石油大学(北京)针对轻烃催化裂解专门开发的基于ZSM-5分子筛介孔催化剂,其制备方法见文献[18],其主要物性见表1;其中ZSM-5分子筛的比表面积为 371 m2·g-1,总孔体积为 0.38 cm3·g-1,介孔体积为0.24 cm3·g-1。轻烃催化裂解的焦炭收率远低于传统的瓦斯油或重油催化裂化的焦炭收率。对此,固定床或移动床反应器比流化床或提升管反应器更加合适。无论轻烃固定床或移动床催化裂解,催化剂的尺寸一般较大。因此,本研究采用大颗粒的催化剂,以便于研究数据与结果能更好地指导工业实践。

表1 催化剂的物化性质Table 1 Physicochem ical properties of catalyst
1.2裂解装置与实验
乙基环己烷催化裂解在固定床实验装置上进行。如图1所示,该装置包括5个部分:进油系统、进蒸汽系统、反应系统、温控系统以及产物分离收集系统。该固定床反应器高50 cm,内径1.4 cm。裂解实验间歇进行,反应器内催化剂装量为10 g。当反应器温度达到设定值后,蒸馏水泵入加热炉生成蒸汽,之后进入反应器。当反应器温度恒定后,烃类原料泵入反应器与催化剂接触并发生裂解反应。当反应器温度再次恒定后,开启产物收集系统,并同时开始计时。反应产物冷凝冷却得到气体与液体样品,并分别收集到相应的容器内。该实验装置的物料衡算高于97%,具有良好的重复性。

图1 实验装置Fig.1 Schematic diagram of experimental apparatus
1.3产物分析方法
气体样品用Agilent-6890炼厂气体分析仪进行分析,得到气体样品中各产物的体积分数,然后由气体样品体积结合理想气态方程、各气体产物的相对分子质量求得各产物的质量,进而计算出各产物的质量收率。Agilent-6890炼厂气体分析仪是多维色谱,有FID和TCD两个检测器、4个切换阀、5根色谱柱。
液体样品用北京分析仪器厂生产的SP-3420气相色谱仪进行分析,之后采用PONA分析软件对色谱图进行产物族组成分析,结合液体样品的质量计算出相应产物的质量收率。该气相色谱仪配有FID检测器和PONA毛细管柱(50 m×250 μm×0.25 μm)。
反应后沉积在催化剂表面上的焦炭含量采用无锡高速分析仪器有限公司的 HWF-900高频红外碳硫分析仪进行测定。
2 裂解反应规律
在重时空速为4.27 h-1和水油稀释比0.35的条件下,考察了反应温度对原料转化率与裂解产物分布的影响,结果如图2所示。乙基环己烷具有较好的裂解性能,原料转化率都在80%以上,且随温度的升高逐渐增大,乙丙烯收率可达41.00%,三烯收率可达 48.91%。随反应温度的升高,乙烯收率在680℃时达到最大值 18.94%,丙烯收率在 660℃时达到最大值22.59%,丁烯收率在640℃时达到最大值7.97%,液体收率逐渐下降。
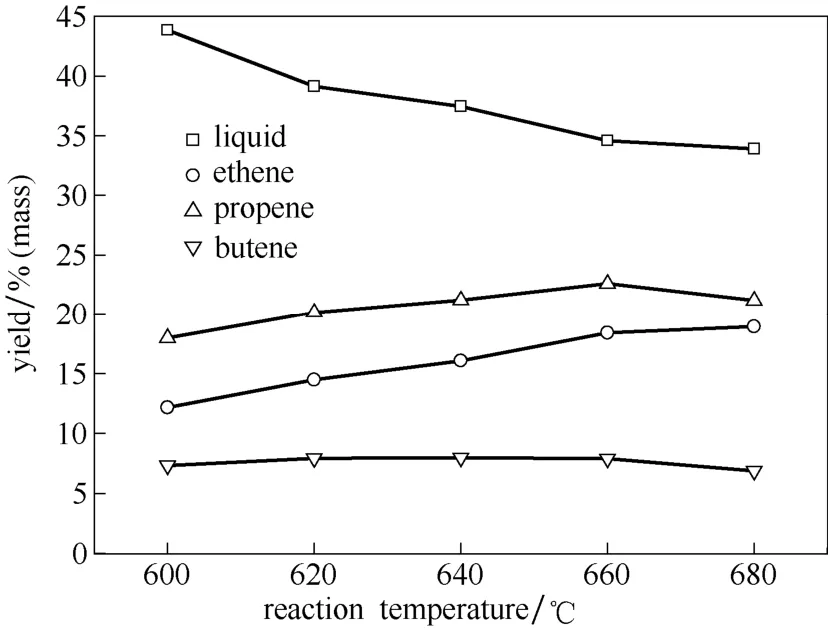
图2 不同反应温度下的主要组分收率Fig.2 Yields of main components at different reaction temperatures
液体样品的组成分布见表 2,主要组成是环烷烃与芳香烃,烯烃与烷烃的含量相对较低。环烷烃主要是未反应的乙基环己烷,且其含量随温度的升高逐渐减少。芳香烃主要是苯、甲苯和二甲苯,随反应温度的升高,苯、甲苯以及总芳香烃的含量逐渐增大,二甲苯的含量变化不大。大量芳香烃组分的存在说明裂解过程中发生了较多的芳构化反应。结合图2与表2,可以发现随反应温度的升高,原料的裂解性能增大,同时裂解产物的分解、芳构化等二次反应也在加剧,正碳离子的相对作用在下降,自由基热裂化反应的相对作用在加剧。从多产乙丙烯的角度考虑,最佳的反应温度是680℃。

表2 不同反应温度下的液体样品组成分布Table 2 Liquid com ponent distribution at different reaction temperatures/% (mass)
3 反应动力学模型
3.1反应模型建立
石脑油催化裂解的反应温度较高(一般 600℃以上),烃类在发生催化反应的同时也会发生热裂化反应,且热裂化反应的程度较深,不能忽略[17],这与热裂化在重油催化裂解过程中作用机理相似[19]。因此,在反应动力学研究中需要同时考虑催化裂化反应以及热裂化反应。乙基环己烷的热裂化过程遵循自由基机理,首先通过碳碳键的断裂或者氢转移生成烷基自由基,其会发生β位断裂生成小分子的烯烃和更小的烷基自由基,因此热裂化主要包括碳碳键的断裂、夺氢反应、氢转移、β位断裂反应等。乙基环己烷的催化裂化过程遵循正碳离子机理,包括单分子机理和双分子机理。单分子机理过程,乙基环己烷得到一个H+生成五配位的正碳离子,要么断裂生成三配位正碳离子和一个小分子烷烃,要么开环生成三配位正碳离子;生成的三配位正碳离子会在β位发生断裂,生成更小的正碳离子和小分子烯烃。双分子机理过程,乙基环己烷被夺去一个H-生成三配位正碳离子,进而发生β位的断裂,生成更小的烯烃和三配位正碳离子。乙基环己烷通过裂化反应生成的小分子几乎都是乙烯、丙烯等不饱和烃。分析乙基环己烷催化裂解反应历程,将每一个反应步骤用1个反应方程式来表示,之后再将相同的反应方程式进行合并,进而归纳出以下的反应式

热裂化过程中会产生大量的甲基自由基和乙基自由基,这些自由基除了以夺氢的方式生成烷烃外,还会相互结合生成丙烷、丁烷等。可以用式(8)、式(9)来表示自由基之间的相互结合及裂化生成自由基的过程。乙基环己烷在反应过程中还会发生脱氢、氢转移等反应,进一步生成芳烃、焦炭等。可以用式(10)、式(11)两个反应来表示。反应产物之间也会发生相互转化反应,其中乙烯转化生成丙烯是重要的产物间的反应,用式(12)表示。综合以上反应过程的分析,可以将乙基环己烷的催化裂解反应表示为所述的14个反应过程。
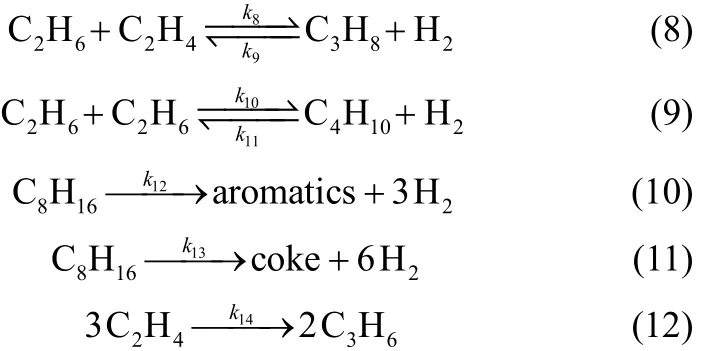
3.2反应模型的数学表达
动力学建模的基本假设如下:(1)认为固定床反应器是一个等温活塞流反应器;(2)裂解原料简单,反应速率遵循一级幂次定律;(3)外扩散实验考察结果表明在实验考察范围内的外扩散影响可以忽略;(4)催化剂的活性稳定性研究表明,当进料量达到催化剂质量的12.5倍时,原料转化率与产物收率几乎保持不变,表明催化剂具有稳定的活性和较长的使用寿命。在后续研究过程中,乙基环己烷的处理量远低于验证实验中的处理量,因此不考虑催化剂的失活。
基于上述模型假设,乙基环己烷催化裂解动力学模型方程可以由连续性方程式(13)得到。在一级反应中,i组分的消失速度应正比于i组分的浓度(ρɑi)和催化剂相对于气体体积的密度(ρc/ε)。所以反应速度ri如式(14)所示。由式(13)、式(14)可得式(15)。

对固定床反应器,当体系达到稳态之后,催化剂床层各处的浓度不随时间变化,仅与催化剂床层位置有关,故式(15)左端对时间的偏导数项为零。设催化剂床层总高为L,在某截面处距离以x表示,则用 X=x/L表示床层中 x截面处的量纲 1相对距离。
物料表面质量流量 GV可由式(16)表示。因此式(15)重新整理得到式(17)。根据理想气体状态方程可得式(18),其中混合气体的平均分子质量随着床层距离的变化而变化并可用式(19)表示。根据式(17)~式(19),最终得到动力学表达式(20)。


3.3模型参数的求取
为获得动力学参数求取的实验数据,分别在600、620、640、660℃下进行乙基环己烷催化裂解实验。在每个反应温度下,保持水油质量比为0.35不变,在重时空速3~9 h-1的范围内进行实验,获得了十多组数据。采用全局优化算法-遗传算法,先用微分方程组对反应器进口到出口进行积分,然后以各个组分的计算值与实验结果的差值平方和作为目标函数,使用Matlab编程并对目标函数进行优化求解,计算出各个反应的表观反应速率常数,结果见表3。然后依据Arrhenius方程,对不同温度下的表观速率常数进行拟合,得到各个反应的表观活化能与指前因子,结果见表4。

表3 乙基环己烷催化裂解反应速率常数Table 3 Rate constants of ethylcyclohexane catalytic pyrolysis/cm3·g-1·h-1
通过对表3中反应速率常数分析可以发现,乙基环己烷生成主产物小分子烃的裂解反应过程速率常数比较大,如 k2、k3、k4等,而生成非主要产物戊烯的反应过程(k5、k6)和生成焦炭反应过程(k13)的反应速率常数比较小,这与产物的分布相一致。乙基环己烷生成芳烃的反应过程(k12)的反应速率常数较大,这是因为乙基环己烷比较容易脱氢生成芳烃,因而产物中芳烃的含量比较大,生成芳烃反应的速率常数也比较大。丁烯进一步分解生成乙烯的反应速率常数k7非常大,说明烯烃的分解比烷烃容易,这与实验结果是一致的[20-21]。乙烯转化为丙烯的反应速率常数 k14也较大,说明低碳烯烃产物之间易通过聚合-分解等反应途径进行相互转化[22]。甲基自由基与乙基自由基之间相互结合的反应速率常数(k8、k10)很大,同时小分子烷烃热分解生成甲基自由基与乙基自由基的反应速率常数(k9、k11)随温度的升高快速增大。

表4 乙基环己烷催化裂解反应表观活化能与指前因子Table 4 Apparent activation energies and pre-exponential factors
由表4可知,对于乙基环己烷裂解生成低碳烯烃的反应(k2),低碳烯烃之间的相互反应(k7与k14),甲基自由基与乙基自由基相互结合的反应(k8与k10),这些反应的表观活化能很低(约10 kJ·mol-1),表明这些反应容易发生。而小分子烷烃热分解生成甲基自由基与乙基自由基的反应(k9、k11),其表观活化能相对较大(>70 kJ·mol-1),说明这类反应相对难以发生。其他反应的表观活化能在 20~65 kJ·mol-1之间。总体来说,求得的表观活化能远低于烃类热裂解的活化能,说明催化剂的使用降低了反应活化能,使得反应更容易进行。
Rahimi等[23]研究了丁烷在La/HZSM-5催化剂上的裂解性能,并建立了丁烷催化裂解动力学模型,求取的活化能约360 kJ·mol-1。Konno等[24]研究了正己烷在ZSM-5分子筛上的裂解反应动力学,求得的活化能为123~128 kJ·mol-1。本研究求得的乙基环己烷裂解的活化能小于65 kJ·mol-1。尽管烃类裂解活化能的大小与催化剂相关,但一般原料分子较小,CC键能较大,裂解所需要的能量较大,表现为反应活化能较高,相关动力学研究结果也说明了这一点。此外,催化剂的理化性质也影响着相应的动力学参数及催化剂裂解性能[25]。本研究所使用的基于 ZSM-5分子筛介孔催化剂具有较小的晶粒(平均约为150 nm)、适宜的酸性与晶体内介孔性质[18],这些特性使该催化剂在轻烃催化裂解过程中发挥了重要作用。
3.4模型验证
表5列出了不同反应温度下乙基环己烷催化裂解主要组分收率的模型计算值与实验值的平均相对误差。大部分组分收率的平均相对误差在10%以下。主要产物乙烯、丙烯、丁烯的平均相对误差在10%以下,平均绝对误差不大于1.5%。总体来说,模型计算值与实验值比较接近,计算误差较小。
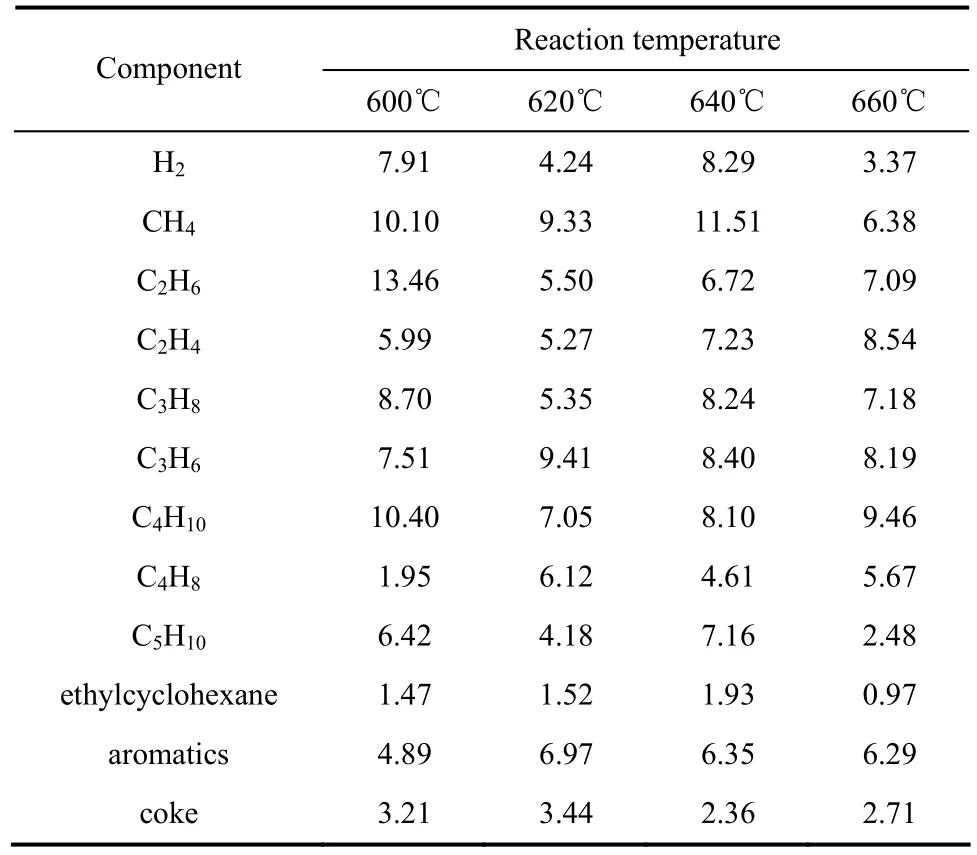
表5 不同反应温度下主要组分收率的平均相对误差Table 5 Average relative errors of main components/%
4 结 论
乙基环己烷具有较好的裂解性能,原料转化率在80%以上,乙丙烯收率可达41%,低碳烯烃收率接近50%。发现随着反应温度的升高,乙烯收率单调增大,丙烯收率、丁烯收率均存在最大值。液体产物主要是苯、甲苯、二甲苯等芳香烃。
同时考虑乙基环己烷催化裂解过程中的热反应与催化反应,建立了包含 14个反应的动力学模型。基于4个反应温度下的裂解实验数据,求取了反应动力学模型的参数。求得的表观活化能均在90 kJ·mol-1以下,主要组分收率的模型预测值与实验值的平均相对误差不高于10%。
符号说明
A——指前因子,cm3·g-1·h-1
ɑi——i集总浓度,mol·(g气体)-1
Ea——表观活化能,kJ·mol-1
GV——蒸气表观(横截面)质量流速,g·cm-2·h-1
ki——i集总速率常数,cm3·(g催化剂)-1·h-1
Mi——i集总的相对分子质量
p——反应压力,MPa
R——气体常数,8.3143 J·mol-1·K-1
ri——i集总反应速率,mol·cm-3·h-1
SWH——真实重时空速,(g原料)·(g催化剂)-1·h-1
T——反应温度,K
t——从运转开始算起的时间,h
x——从入口算起的进入反应器的距离,cm
ε——床层空隙率
ρ——气体密度,g·cm-3
ρc——催化剂密度,(g催化剂)·(cm3床层)-1
References
[1]王梦瑶, 周嘉文, 任天华, 等. 催化裂化多产丙烯 [J]. 化工进展,2015, 34 (6): 1619-1624. DOI: 10.16085/j.issn.1000-6613.2015.06.019. WANG M Y, ZHOU J W, REN T H, et al. Catalytic cracking
processes for maxim izing propylene production [J]. Chem ical Industry and Engineering Progress, 2015, 34 (6): 1619-1624. DOI: 10.16085/j.issn.1000-6613.2015.06.019.
[2]RAHIM I N, KARIMZADEH R. Catalytic cracking of hydrocarbons over modified ZSM-5 zeolites to produce light olefins: a review [J]. Appl. Catal. A-Gen., 2011, 398 (1/2): 1-17. DOI: 10.1016/j.apcata.2011.03.009.
[3]王志喜, 王亚东, 张睿, 等. 催化裂解制低碳烯烃技术研究进展[J]. 化工进展, 2013, 32 (8): 1818-1824. DOI: 10.3969/ j.issn.1000-6613.2013.08.017.
WANG Z X, WANG Y D, ZHANG R, et al. Advances of catalytic pyrolysis for producing light olefins [J]. Chem ical Industry and Engineering Progress, 2013, 32 (8): 1818-1824. DOI: 10.3969/ j.issn.1000-6613.2013.08.017.
[4]ALEKSANDROV Y A, SHEKUNOVA V M, DIDENKULOVA, I I,et al. Catalytic pyrolysis of propane and butane over silica surface [J]. Russ. J. Gen. Chem., 2008, 78 (10): 1900-1901. DOI: 10.1134/ s1070363208100137.
[5]JEONG S M, CHAE J H, KANG J H, et al. Catalytic pyrolysis of naphtha on the KVO3-based catalyst [J]. Catal. Today, 2002, 74 (3/4): 257-264. DOI: 10.1016/S0920-5861(02)00035-4.
[6]李丽, 孟祥海, 王刚, 等. 环烷基瓦斯油催化裂解反应规律及产品性质 [J]. 化工学报, 2010, 61 (9): 2365-2372.
LI L, MENG X H, WANG G, et al. Reaction performance and product properties of catalytic pyrolysis of naphthenic-base gas oils [J]. CIESC Journal, 2010, 61 (9): 2365-2372.
[7]李成霞, 高永地, 李春义, 等. 重油催化裂解多产乙烯丙烯催化剂的研究 [J]. 燃料化学学报, 2006, 34 (1): 47-50.
LI C X, GAO Y D, LI C Y. et al. Study on the catalysts for catalytic pyrolysis of heavy oil to ethylene and propylene [J]. Journal of Fuel Chem istry and Technology, 2006, 34 (1): 47-50.
[8]MENG X H, XU C M, GAO J S, et al. Catalytic and thermal pyrolysis of atmospheric residue [J]. Energy Fuels, 2009, 23 (1): 65-69. DOI: 10.1021/ef8006867.
[9]刘俊涛, 孙凤侠, 滕加伟. 碳四烯烃催化裂解制乙烯和丙烯热力学分析及反应性能考察 [J]. 工业催化, 2015, 23 (6): 486-490. DOI: 10.3969/j.issn.1008-1143.2015.06.014.
LIU J T, SUN F X, TENG J W. Thermodynam ics analysis and reaction performance for catalytic cracking of C4olefins to propylene and ethylene [J]. Industrial Catalysis, 2015, 23 (6): 486-490. DOI: 10.3969/j.issn.1008-1143.2015.06.014.
[10]李兆飞, 郭成玉, 王骞, 等. 不同硅铝比ZSM-5分子筛的合成及其在丁烯催化裂解中的应用 [J]. 石油化工, 2016, 45 (2): 163-168. DOI: 10.3969/j.issn.1000-8144.2016.02.007.
LI Z F, GUO C Y, WANG Q, et al. Synthesis of ZSM-5 zeolites w ith different silica-alum ina ratio and their application in catalytic cracking of 1-butene [J]. Petrochem ical Technology, 2016, 45 (2): 163-168. DOI: 10.3969/j.issn.1000-8144.2016.02.007.
[11]SIDDIQUI M A B, AITANI A M, SAEED M R, et al. Enhancing the production of light olefins by catalytic cracking of FCC naphtha over mesoporous ZSM-5 catalyst [J]. Top. Catal., 2010, 53 (19/20): 1387-1393. DOI: 10.1007/s11244-010-9598-1.
[12]LIU W K, MENG X H, ZHAO X, et al. Pyrolysis performances of catalytic cracking naphtha and coker naphtha on inert carriers and an active catalyst [J]. Energy Fuels, 2009, 23 (12): 5760-5764. DOI: 10.1021/ef900645s.
[13]杨连国, 徐春明, 孟祥海, 等. 焦化汽油催化裂解生产低碳烯烃研究 [J]. 炼油技术与工程, 2008, 38 (3): 4-8.
YANG L G, XU C M, MENG X H, et al. Catalytic pyrolysis of coker naphtha for production of light olefins [J]. Petroleum Refinery Engineering, 2008, 38 (3): 4-8.
[14]MENG X H, XU C M, LI L, et al. Kinetic study of catalytic pyrolysis of C4hydrocarbons on a modified ZSM-5 zeolite catalyst [J]. Energy Fuels, 2010, 24: 6233-6238. DOI: 10.1021/ef100943u.
[15]SEDIGHI M, KEYVANLOO K, TOWFIGHI J. Kinetic study of steam catalytic cracking of naphtha on a Fe/ZSM-5 catalyst [J]. Fuel, 2013, 109: 432-438. DOI: 10.1016/j.fuel.2013.02.020.
[16]孙忠超, 山红红, 刘熠斌, 等. 基于结构导向集总的FCC汽油催化裂解分子尺度动力学模型 [J]. 化工学报, 2012, 63 (2): 486-492. DOI: 10.3969/J.ISSN.0438-1157.2012.02.021.
SUN Z C, SHAN H H, LIU Y B, et al. Molecular kinetic model for catalytic pyrolysis of FCC gasoline by structure-oriented lumping [J]. CIESC Journal, 2012, 63 (2): 486-492. DOI: 10.3969/J.ISSN.0438-1157.2012.02.021.
[17]LEE J H, KANG S, KIM Y, et al. New approach for kinetic modeling of catalytic cracking of paraffinic naphtha [J]. Ind. Eng. Chem. Res.,2011, 50 (8): 4264-4279. DOI: 10.1021/ie1014074.
[18]ZHANG Q, HU S, ZHANG L, et al. Facile fabrication of mesopore-containing ZSM-5 zeolite from spent zeolite catalyst for methanol to propylene reaction [J]. Green Chem., 2014, 16 (1): 77-81. DOI: 10.1039/c3gc41327f.
[19]MENG X H, XU C M, GAO J S, et al. Studies on catalytic pyrolysis of heavy oils: reaction behaviors and mechanistic pathways [J]. Appl. Catal. A-Gen., 2005, 294 (2): 168-176. DOI: 10.1016/j.apcata.2005.07.033.
[20]MENG X H, XU C M, GAO J S. Secondary cracking of C4hydrocarbons from heavy oil catalytic pyrolysis [J]. Can. J. Chem. Eng., 2006, 84 (3): 322-327.
[21]JIANG G Y, ZHANG L, ZHAO Z, et al. Highly effective P-modified HZSM-5 catalyst for the cracking of C4alkanes to produce light olefins [J]. Appl. Catal. A-Gen., 2008, 340 (2): 176-182. DOI: 10.1016/j.apcata.2008.02.011.
[22]LI L, GAO J S, XU C M, et al. Reaction behaviors and mechanisms of catalytic pyrolysis of C4hydrocarbons [J]. Chem. Eng. J., 2006,116 (3): 155-161. DOI: 10.1016/j.cej.2005.11.002.
[23]RAHIM I N, KARIMZADEH R. Kinetic modeling of catalytic cracking of C4alkanes over La/HZSM-5 catalysts in light olefin production [J]. J. Anal. Appl. Pyrolysis, 2015, 115: 242-254. DOI: 10.1016/j.jaap.2015.08.004.
[24]KONNO H, OKAMURA T, KAWAHARA T, et al. Kinetics of n-hexane cracking over ZSM-5 zeolites—effect of crystal size on effectiveness factor and catalyst lifetime [J]. Chem. Eng. J., 2012, 207: 490-496. DOI: 10.1016/j.cej.2012.06.157.
[25]XIONG K, LU C, WANG Z, et al. Quantitative correlations of cracking performance w ith physiochem ical properties of FCC catalysts by a novel lump kinetic modelling method [J]. Fuel, 2015,161: 113-119. DOI: 10.1016/j.fuel.2015.07.081.
Reaction kinetics of ethylcyclohexane catalytic pyrolysis for production of light olefins
ZHANG Rui, GUO Shaopeng, LIU Guili, LIU Haiyan, LIU Zhichang, MENG Xianghai
(State Key Laboratory of Heavy Oil Processing, China University of Petroleum, Beijing 102249, China)
The cracking performance of ethylcyclohexane on a mesoporous catalyst based on ZSM-5 molecular sieve was investigated in an apparatus w ith a fixed-bed reactor. The results showed that ethylcyclohexane had good cracking performance, the conversion was above 80%, the yield of ethylene and propylene reached 41% (mass), the yield of total light olefins was near 50% (mass), and the main components of liquid products were benzene, toluene and xylene. As reaction temperature increased, the yield of ethylene increased monotonously, and those of propylene and butene showed maxima. With the consideration of both thermal and catalytic reactions, a kinetic model involving 14 reactions was established for the catalytic pyrolysis of ethylcyclohexane. The experimental data were obtained at reaction temperatures of 600, 620, 640 and 660℃, and the reaction rate constants were estimated by genetic algorithm regression analysis. Apparent activation energies and pre-exponential factors were subsequently calculated according to the Arrhenius equation. All of the apparent activation energies obtained were below 90 kJ·mol-1, indicating that the mesoporous ZSM-5 catalyst provides high catalytic activity for ethylcyclohexane catalytic pyrolysis. The model predicted values were in good agreement w ith the experimental data, and the average relative errors of the main products were below 10%.
reaction kinetics; catalysis; fixed-bed; ethylcyclohexane; ethylene; propylene
date: 2016-03-30.
MENG Xianghai, mengxh@cup.edu.cn
supported by the National Basic Research Program of China (2012CB215001) and the Program for New Century Excellent Talents in the University of China (NCET-12-0970).
TE 624.4
A
0438—1157(2016)08—3422—07
10.11949/j.issn.0438-1157.20160380
2016-03-30收到初稿,2016-05-25收到修改稿。
联系人:孟祥海。第一作者:张睿(1979—),男,博士,助理研究员。
国家重点基础研究发展计划项目(2012CB215001);教育部新世纪优秀人才项目(NCET-12-0970)。