聚L-精氨酸/石墨烯修饰电极测定诱惑红
胡晴晴,陶姣姣,刘 旭,孙登明
(淮北师范大学化学与材料科学学院,安徽淮北235000)
聚L-精氨酸/石墨烯修饰电极测定诱惑红
胡晴晴,陶姣姣,刘旭,孙登明*
(淮北师范大学化学与材料科学学院,安徽淮北235000)
利用电化学聚合法制备了聚L-精氨酸/石墨烯复合修饰电极,探究了诱惑红在此修饰电极上的电化学行为,建立了测定诱惑红的新方法。结果表明,修饰电极对诱惑红有较好的催化活性,在pH3.5的磷酸盐介质中,诱惑红在修饰电极上产生一对灵敏的氧化还原峰,峰电位分别为Epa=0.296 V和Epc=0.083 V。采用循环伏安法,对诱惑红进行测定的线性范围为7.50×10-7~1.00×10-4mol/L,检出限为1.0×10-8mol/L。该修饰电极具有良好的稳定性和选择性,用于样品中诱惑红的测定,结果满意。
石墨烯;诱惑红;L-精氨酸;修饰电极
0 引言
诱惑红(Allura red,AR),又名艳红,是一种人工合成色素,溶于水,不溶于油脂。因其具有鲜艳的深红色,广泛应用于汽水、硬糖、糕点、冰淇淋等食品的着色,以改善它们在加工生产中的色泽,使其更加诱人。有研究表明,合成色素大多对人体存在一定的不安全性,过量添加对人体有害[1-2]。诱惑红属于偶氮类色素,被人体吸收后会在体内分解出致癌物,不恰当的食用此类色素会对人体的健康造成不同程度的危害。近年来,文献报道诱惑红的检测方法有高效液相色谱法[3],紫外可见分光光度法[4],磁性富集分光光度法[5]等,这些方法有些操作复杂,有些灵敏度不高。电化学检测方法具有成本较低,操作简单,检测速度快等优点,但对诱惑红的测定报道不多[6]。因此建立测定诱惑红的灵敏快速的电化学检测方法具有重要意义。石墨烯(GO)是一种新型碳材料,具有较大的比表面积[7],能够提高电子的传输速率,实现良好的重现性和再生性[8]。目前,石墨烯已在电子、储能和转换以及生物科学和生物技术方面获得有效的开发和运用[9-10],同时,在电化学领域也得到了一些重要应用[11-12]。该实验将两种具有催化活性的L-精氨酸(LA)和石墨烯通过聚合的方法制备了PLA-ERGO/GCE修饰电极。用该电极研究了诱惑红的电化学行为,并且对实际样品中诱惑红进行了检测,取得了令人满意的结果。
1 实验部分
1.1仪器与试剂
BAS100/W电化学分析系统 (美国BAS公司);pHS-3C型酸度计(上海康仪仪器有限公司);三电极系统:铂丝电极为对电极,PLA-ERGO/ GCE玻碳电极为工作电极,Ag/AgCl电极为参比电极。
GO分散液:2 mg/mL(南京先锋纳米材料科技有限公司);AR贮备液:1.00×10-3mol/L,LA贮备液:5.0×10-3mol/L,两者均避光保存,使用时逐级稀释至所需浓度;磷酸盐缓冲溶液(PBS):pH2.0~pH9.0,用0.1 mol/L磷酸盐按常规方法配制,并在pH计校准。
1.2修饰电极的制备
玻碳电极(Ф=3 mm)的预处理按文献[13]进行。放入10 mL含有1.00 mg/mL GO,1.00×10-3mol/L的LA,pH=5.5的聚合底液中,以玻碳电极为工作电极,铂丝电极为对电极,Ag/AgCl电极为参比电极,静置12 s,在-2.5~2.4 V电位范围内,以100 mV/s扫描速率循环扫描9周,即制得PLA-ERGO/GCE修饰电极,用亚沸水冲洗,晾干备用。
1.3实验方法
向10 mL电解池中,加入一定量的诱惑红标准溶液和5.0 mL pH为3.5的PBS溶液,用亚沸水定容后充分摇匀。以铂电极为对电极,Ag/AgCl电极为参比电极,修饰的玻碳电极为工作电极。在-0.4~0.6 V的电位范围内,静置180 s,进行循环伏安扫描,并记录峰电流和峰电位。扫描结束后,将修饰电极放入空白液中,扫至无峰,即可进行下一次实验测定。
2 结果与讨论
2.1修饰电极的最佳聚合条件
氧化石墨烯的表面具有含氧官能团,会阻碍电子的传递速率,需用电化学方法进行还原,因此GO和LA的用量和酸度,扫描次数,循环电位区间等条件都会对诱惑红的灵敏度,检出限有较大的影响。实验表明,修饰电极的最佳聚合条件为:GO的用量为5.0 mL,精氨酸的用量为2.0 mL,扫描电位为-2.5~2.4 V,扫描速率为 100 mV/s,扫描周次为9周,静置时间为12 s时,制得的修饰电极对诱惑红的响应电流最大。
2.2电化学阻抗谱分析
图1为电化学阻抗图谱。由图可知,PLAERGO/GCE修饰电极的容抗弧较裸玻碳电极明显减小,这可能是因为石墨烯修饰在电极后,增大了电子传递速率,同时也说明在该实验条件下成功制备了聚L-精氨酸/石墨烯复合修饰电极。
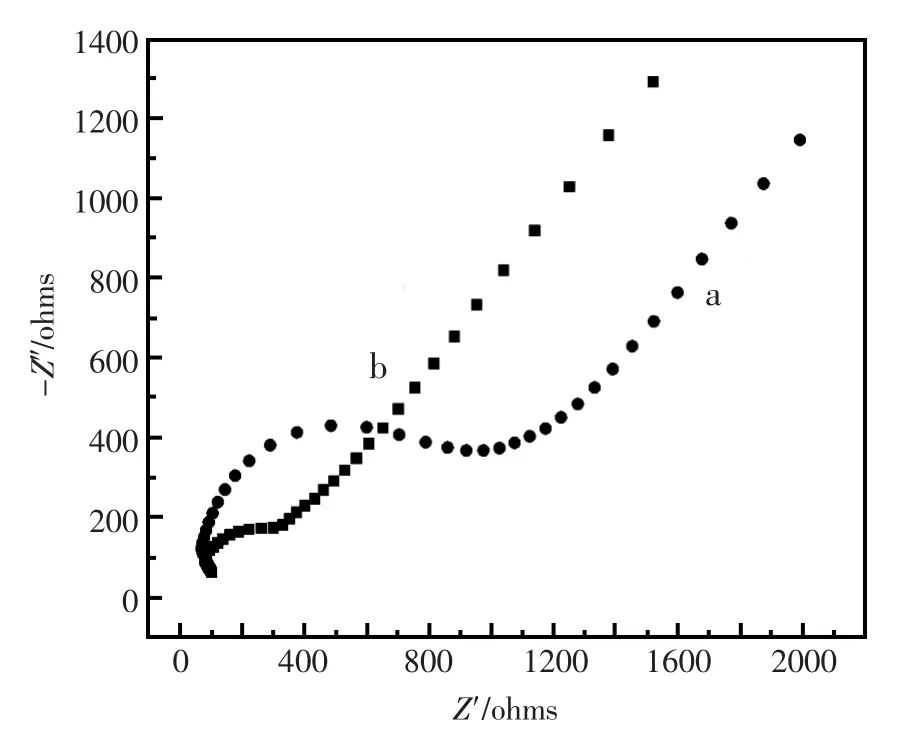
图1 GCE(a)和PLA-ERGO/GCE(b)在含5.0×10-3mol/L K3[Fe(CN)6],1.0 mol/L KCl溶液的交流阻抗谱图Fig.1 EIS graph of GCE(a)and PLA-ERGO/GCE(b)in 5.0×10-3mol/L K3[Fe(CN)6],1.0 mol/L KCl solution
2.3诱惑红在修饰电极上的电化学行为
2.3.1诱惑红循环伏安特性
用循环伏安法研究了诱惑红的电化学行为,图2是在-0.4~0.6 V的扫描电位范围内,pH=3.5 的PBS中静置180 s后,1.00×10-4mol/L的诱惑红在裸电极和修饰电极上的循环伏安曲线。在GCE上,诱惑红只出现氧化峰而无还原峰,氧化峰电位为 Epa=0.242 V,在 PLA/GCE和 PLAERGO/GCE修饰电极上均出现氧化还原峰,峰电位分别为Epa=0.276 V、Epc=0.102 V和Epa=0.296 V、Epc=0.083 V,峰电流也明显变大,其中PLAERGO/GCE修饰电极上的氧化峰电流比GCE提高近11倍,比PLA/GCE提高了20%,说明PLAERGO/GCE修饰电极对诱惑红的催化效果最强,这可能是因为石墨烯沉积在电极表面,增大了表面积,并与PLA共同作用的结果。
2.3.2底液酸度的影响
图3表示不同pH对1.00×10-4mol/L的诱惑红测定结果的影响。结果表明,在pH3.5的磷酸盐介质内,用PLA-ERGO/GCE修饰电极测定诱惑红,得到的氧化峰电流最大。故该实验选择的最佳酸度为pH=3.5。在pH2.5~pH8.0范围内,随着pH的增大氧化峰电位负移,峰电位(Epa)与pH呈线性关系,线性方程为:Epa=0.4981-0.06024pH,r=0.9952,斜率为60 mV/pH,接近59 mV/pH,可以说明,诱惑红在修饰电极上发生的是等电子等质子反应。
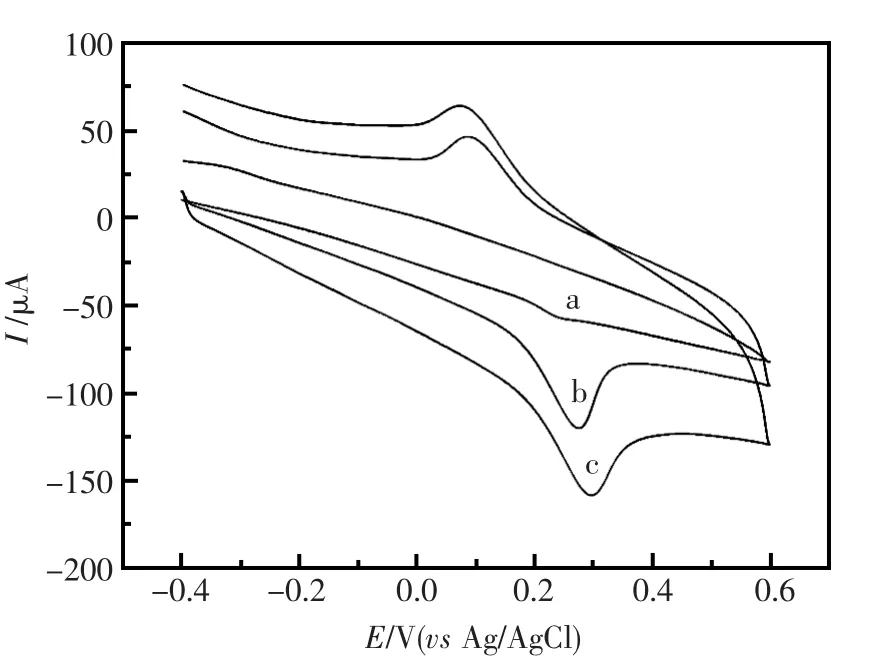
图2 AR在GCE(a),PLA/GCE(b)和PLA-ERGO/GCE (c)上的循环伏安曲线Fig.2 CVs of AR on GCE(a),PLA/GCE(b)and PLAERGO/GCE(c)at a scan rate of 0.10 V/s in PBS(pH3.5)
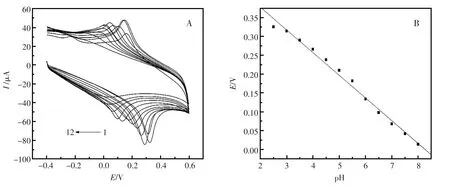
图3 AR在不同pH下的CV曲线(A)和E与pH的关系曲线(B)Fig.3 CVs of AR with different pH(A)and the corresponding relationship curve between the peak potential and pH(B)pH 1~12:2.5,3.0,3.5,4.0,4.5,5.0,5.5,6.0,6.5,7.0,7.5,8.0;Scan rate of 0.10 V/s
2.3.3扫描速率对诱惑红电化学行为的影响
图4是1.00×10-4mol/L的诱惑红在pH=3.5 PBS中,改变扫描速率测定的CV曲线。结果表明,随着扫描速率逐渐增大,诱惑红在PLAERGO/GCE修饰电极上的电化学信号也在增大,但可逆性随着扫速的增大变差,故该实验选择最佳扫描速率为100 mV/s。在20~400 mV/s范围内,扫描速率与氧化峰电流呈线性关系,其回归方程为I=9.921+0.2298 v,r=0.9938,说明诱惑红在PLA-ERGO/GCE修饰电极上的电化学行为受吸附控制。由吸附量公式[14]计算,在扫速为100 mV/s,pH=3.5底液中,对诱惑红进行测定,得出诱惑红在电极表面的吸附量为4.17×10-9mol/cm2。
在诱惑红的电化学反应过程中,扫速在40~400 mV/s范围内,Epa与lnυ呈线性关系,线性方程为:Epa=0.06148+0.04907lnυ,r=0.9903。根据文献[15],E~lnv方程中的斜率等于RT/anF,其中,电子传递系数a一般取理论值0.5,n为得失电子数,F为法拉第常数,R为气体常数,T为绝对温度,求得诱惑红参与电极反应的实际得失电子数为0.96,接近理论得失电子数1。
2.3.4最佳静置时间的选择
采用CV法对1.00×10-4mol/L的诱惑红进行测定,结果表明,静置时间对诱惑红的吸附过程有较大的影响。由图5可知,改变静置时间,随着时间的增加,峰电流逐渐增大,当静置时间为180 s时,峰电流达到最大,之后无明显变化。这说明诱惑红在修饰电极上的吸附已经达到饱和。故静置时间为180 s。
2.3.5工作曲线与检出限
在最佳实验条件下,用循环伏安法对诱惑红进行测定。实验结果见图6。定量分析的线性范围、回归方程、相关系数和检出限见表1。
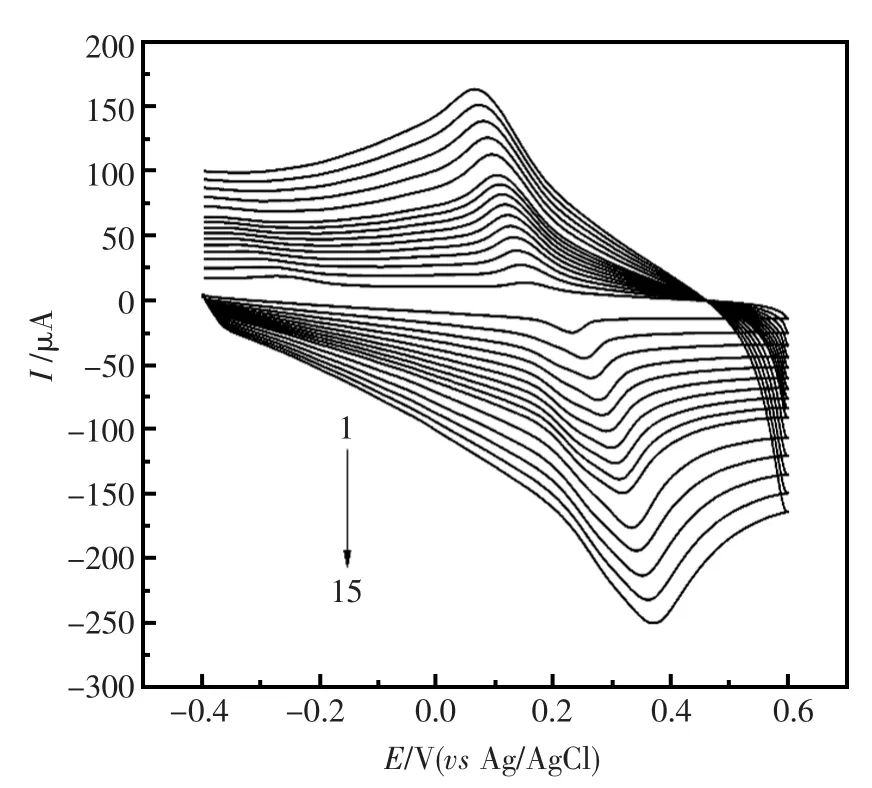
图4 AR在不同扫速下的CV图Fig.4 CVs of AR at PLA-ERGO/GCE with various scan rates from 1 to 15:0.02,0.04,0.06,0.08,0.10,0.12,0.14,0.16,0.18,0.20,0.24,0.28,0.32,0.36,0.40
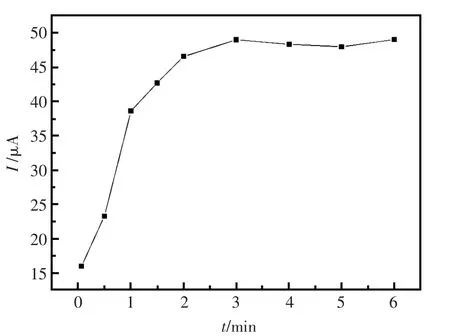
图5 静置时间的影响Fig.5 Effect of standing time
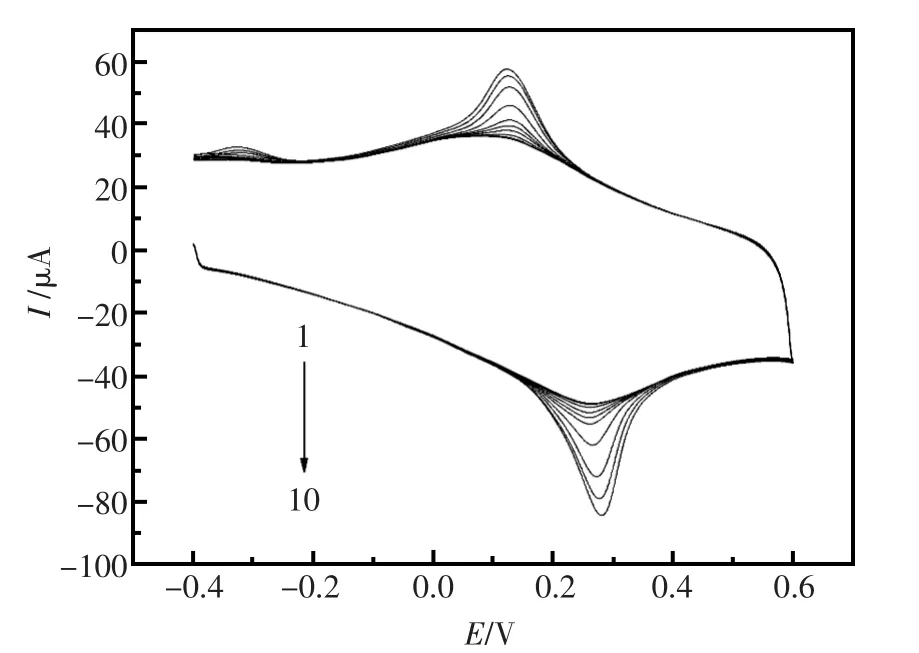
图6 测定AR的CV曲线Fig.6 CVs of different concentrations of AR(from 1 to 10:7.50×10-7,1.00×10-6,2.50×10-6,5.00×10-6,7.50×10-6,1.00×10-5,2.50×10-5,5.00×10-5,7.50×10-5,1.00×10-4mol/L)
2.4精密度和稳定性
对1.00×10-4mol/L AR进行20次平行实验,RSD为3.1%,表明PLA-ERGO/GCE修饰电极对测定物具有良好的重现性。将该电极在室温下放置10 d,相同实验条件下再次测定时,峰电位和峰电流的数值均较为稳定,这表明PLA-ERGO/ GCE修饰电极有良好的稳定性。
2.5干扰实验
对1.00×10-4mol/L的诱惑红进行测定,测定允许误差控制在±5%之间,测定结果表明,L-酪氨酸、L-半胱氨酸、L-精氨酸、L-苏氨酸、L-色氨酸草酸、葡萄糖、叶酸(≥1 mg,未做最高限);抗坏血酸、胭脂红(0.1 mg)、尿酸(0.3 mg)、柠檬酸(0.5 mg)均不干扰测定。
2.6样品分析
将此方法用于两种不同饮料中诱惑红的测定,取一定量的样品加pH=3.5的磷酸盐溶液,按实验方法测定诱惑红的含量,平行测定5次。用标准加入法计算其回收率。实验结果见表2。

表1 测定AR的线性范围、线性回归方程、相关系数和检出限Tab.1 Linear ranges,regression equations,correlation coefficients and detection limits for determination of AR on PLA-ERGO/GCE
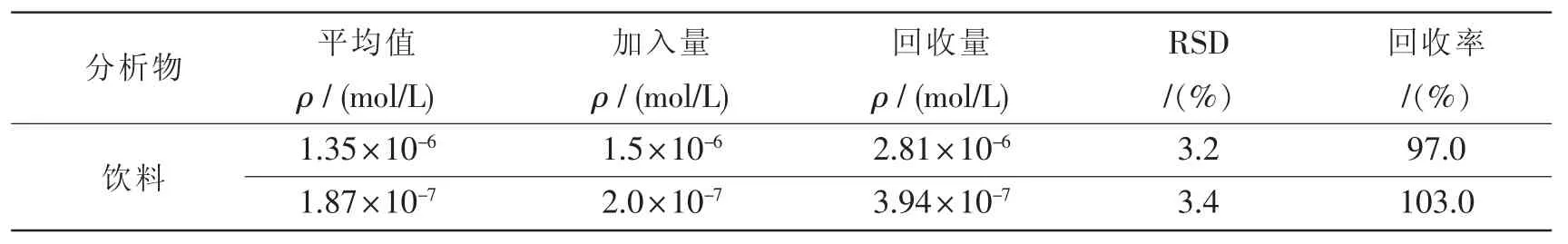
表2 样品中诱惑红的分析结果Tab.2 Analytical results of AR in samples(n=5)
3 结论
该实验制备了PLA-ERGO/GCE修饰电极,并应用于诱惑红电化学行为的研究。实验表明,该电极对诱惑红有较强的催化作用,且电极的稳定性好。用于实际样品的测定,结果满意。
[1]沈坚,傅晓,潘旭,等.高效液相色谱法测定动物性食品中合成色素[J].理化检验-化学分册,2011,47(2): 139-143.
[2]蒋晓彤,陈国松,姜玲玲,等.高效液相色谱法同时检测6种甜味剂[J].食品科学,2011,32(6):165-168.
[3]Yoshioka N,Ichihashi K.Determination of 40 Synthetic Food Clours in Drinks and Candies by High-Performance Liquid Chromatography Using a Short Column with Photodiode Array Detection[J].Talanta,2008,74 (15):1408-1413.
[4]邢海燕,郝媛媛,孙有娥,等.UV法和HPLC法测定合成色素诱惑红的比较[J].广州化工,2013,41(2):91-92.
[5]饶通德,陈书鸿,张六一,等.磁性分离富集-分光光度法测定食品中的诱惑红[J].光谱实验室,2012,29(4): 2164-2168.
[6]孙章华,陈美凤,尹明静,等.聚甘氨酸修饰电极测定食品中的诱惑红[J].食品与发酵工业,2014,40(12): 185-189.
[7]杨常玲,刘云芸,孙彦平.石墨烯的制备及其电化学性能[J].电源技术,2010,34(2):177-180.
[8]Shan C S,Yang H F,Song J F,et al.Direct Electrochemistry of Glucose Oxidase and Biosens-ing for Glucose Based on Graphene[J].Anal.Chem.,2009,81(6): 2378-2382.
[9]黄毅,陈永胜.石墨烯的功能化及其相关应用[J].中国科学B辑:化学,2009,39(2):887-896.
[10]Shao Y Y,Wang J,Wu H,et al.Graphene Based Electrochemical sensors and Biosensors[J].Electroanalysis,2010,22(10):1027-1036.
[11]黄克靖,余晟,王兰,等.石墨烯/铁氰化钴复合膜修饰玻碳电极同时测定对苯二酚、邻苯二酚和间苯二酚[J].化学学报,2012,70(6):735-740.
[12]方艳红,连慧婷,陈国华.石墨烯/壳聚糖修饰玻碳电极测定水样中痕量铜离子[J].华侨大学学报:自然科学版,2011,32(5):529-531.
[13]Tian X Q,Cheng C M,Yuan H Y.Simultaneous determination of l-ascorbic acid,dopamine and uric acid with gold nanoparticles-β-cyclodextrin-graphene-modified electrode by square wave voltammetry[J].Talanta,2012,93:79-85.
[14]陆宝仪,赖艳艳,李红.功能化碳纳米管的电化学性质及在 6-巯基嘌呤分析检测中的应用[J].电化学,2009,15(1):67-72.
[15]Laviron E.Adsorption,autoinhibition and autocatalysis in polarography and in linear potential sweep voltammetry [J].Electroanalytical Chemistry and Interfacial Electrochemistry,1974,52(3):355-393.
Determination of allura red by poly(L-arginine)-graphene modified electrode
Hu Qing-qing,Tao Jiao-jiao,Liu Xu,Sun Deng-ming*
(College of Chemistry and Materials Science,Huaibei Normal University,Huaibei 235000,China)
The poly(L-arginine)-graphene modified electrode was fabricated and the electrochemical behaviors of allura red was studied by cyclic voltammetric method.A new method was developed for determination of allura red. The study results showed that the modified electrode has better catalytic ability to the allura red.In phosphate buffer solution at pH=3.5,the redox peaks of allura red were Epa=0.296 V and Epc=0.083 V.The linear range for the determination of allura red was 7.50×10-7~1.00×10-4mol/L by cyclic voltammetric method.The detection limit was 1.0×10-8mol/L.The modified electrode demonstrated excellent stability and selectivity.This method had been successfully applied to the determination of allura red in the sample with satisfactory results.
graphene;allura red;L-arginine;modified electrode
国家级大学生创新创业训练计划项目 (201610373033);安徽省大学生创新创业训练计划项目(201510373093)
*通信联系人,E-mail:sundengming@126.com

