蒿甲醚结肠定位微丸的制备及体外释放度评价
马 寅,张 伟,张国丽,张锐武,杨兆祥*
(1.大理大学,云南大理 671000;2.昆药集团股份有限公司,昆明 650106)
蒿甲醚结肠定位微丸的制备及体外释放度评价
马寅1,张伟2,张国丽2,张锐武2,杨兆祥2*
(1.大理大学,云南大理671000;2.昆药集团股份有限公司,昆明650106)
目的:拟制备蒿甲醚pH依赖型结肠定位微丸,并对其体外释放度进行考察。方法:采用挤出滚圆法制备丸芯,采用Eudragit S100作为包衣材料,柠檬酸三乙酯作为增塑剂,使用流化床包衣设备进行包衣。结果:在pH 1.2溶液2 h中未检测到蒿甲醚;在pH 6.8磷酸盐缓冲液中4 h累积释放度均小于5%;而在pH 7.6磷酸盐缓冲液中,3 h累积释放度均达90%以上。结论:本方法制备的蒿甲醚结肠定位微丸能达到结肠定位释药的目的。
蒿甲醚;pH依赖型;结肠定位;体外释放度
[DOI]10.3969/j.issn.2096-2266.2016.08.003
蒿甲醚是青蒿素的脂溶性衍生物,它有抗疟疾、抗血吸虫、抗弓形虫、抗心律失常和肿瘤细胞毒性等作用〔1〕。除此之外,蒿甲醚还具有抗肿瘤血管生成的作用〔2〕。蒿甲醚可以通过影响细胞周期来抑制人慢性髓性白血病细胞株K562细胞的增殖〔3〕。牛红妹等〔4〕研究发现,青蒿酿液在体外对人结肠癌SW620细胞、LOVO细胞、胃癌AGS细胞以及肝癌Hep-2细胞均有明显的作用。因此将蒿甲醚制成结肠定位微丸,不仅可以提高其靶向性,还可以提高其生物利用度,是一种性价比很高的抗癌药物。
口服结肠定位给药系统(OCDDS)是一种新型的给药系统,它是指采用一种适当的方法,避免药物在胃、十二指肠、空肠及回肠释放,运送至结肠部位才可释放而发挥局部或全身治疗作用的一种释药系统〔5〕。该给药系统,可以将治疗药物直接运送至结肠,既能降低毒副作用,又能将药物靶向输送至病灶处。同时这种给药方式可以避免药物被胃肠道酶所降解,有助于提高疫苗、蛋白、多肽类药物口服给药的生物利用度〔6〕。本实验制备了蒿甲醚结肠定位微丸,并对其体外释放度进行考察。
1 仪器与试药
1.1仪器挤出滚圆机(重庆英格造粒包衣技术有限公司;多功能流化床(重庆英格造粒包衣技术有限公司);智能溶出仪(德国PHARMATEST公司);高效液相色谱仪1260(美国Agilent公司);电子天平(德国赛多利斯公司);pH酸度计(姆特勒-托利多公司)。
1.2试药蒿甲醚(昆药集团股份有限公司);微晶纤维素(FMC BioPolymer美国);乳糖(DFE Pharma荷兰);羧甲基淀粉钠(安徽山河药用辅料股份有限公司);聚乙烯吡咯烷酮(安徽山河药用辅料股份有限公司);Eudragit S100(尤特奇S100德国罗姆公司);柠檬酸三乙酯(蚌埠丰原医药科技公司);滑石粉(德国罗姆公司)。
2 方法与结果
2.1蒿甲醚载药微丸的制备采用挤出滚圆的方法制备载药微丸,操作如下:称取处方量的蒿甲醚、微晶纤维素、乳糖、羧甲基淀粉钠,混合均匀,加一定量的聚维酮水溶液制软材,然后将制好的软材放进挤出机进行挤出,将得到的长条物放进滚圆机内进行滚圆。取出,采用多功能流化床进行40.0℃流化烘干,取20~40目微丸作为载药微丸进行包衣。按照上述处方和工艺,制备3批载药微丸,考察3批载药微丸的外观、崩解特性和制剂工艺的稳定性。结果显示,所制3批载药微丸,圆整度好,表面光洁,崩解时间、堆密度、硬度、脆碎度均符合要求,由此可证明该载药微丸的处方和工艺稳定性都良好。
2.2结肠定位微丸的制备
2.2.1包衣工艺及条件将制备好的载药微丸80g加到WBF-2G型流化床中,底喷法,喷嘴直径0.2mm,进风温度45℃,物料温度37~40℃,流化压力30kPa,喷雾压力120 kPa,喷液速率0.2 g/min。包衣结束后,微丸在流化床内继续流化干燥3 h,以使包衣膜融合完整〔7〕。
2.2.2包衣液的配制按包衣处方称取Eudragit S100,滑石粉,增塑剂。A相:先量取一定量的95%乙醇溶剂,将称取的Eudragit S100慢慢加入溶剂中,并使其分散溶解成均匀透明胶体溶液;B相:将滑石粉,增塑剂慢慢加入到剩余95%乙醇溶剂中,持续搅拌15 min,使混合均匀;然后将B相缓慢倒入A相中,并继续搅拌30 min,过100目筛,即得。
2.3蒿甲醚含量测定
2.3.1色谱条件Kromasil C18色谱柱(4.6 mm×150 mm,5μm);流动相乙腈-水(62:38),流速1mL/min;检测波长216 nm,柱温30℃,进样量20 μL。
2.3.2标准曲线的制备精密称取蒿甲醚对照品适量,置量瓶中,选用pH 6.8磷酸盐缓冲液,pH 7.6磷酸盐缓冲液作为溶出介质。两种介质中蒿甲醚的质量浓度为50~120 μg/mL,在216 nm处测定峰面积,并对质量浓度进行线性回归。在pH 6.8磷酸盐缓冲液中,线性方程为Y=589 432.1X+0.780 41,r= 0.999 9;在pH 7.6磷酸盐缓冲液中,线性方程为Y= 57 642.3X+0.648 50,r=0.999 9,由此可知,蒿甲醚在两种介质中线性良好。
2.3.3体外释放度的测定体外释放度测定方法:①载药微丸溶出度测定:按照《中国药典》2010年版第二部附录溶出度测定法第二法,取适量(相当于含主药100 mg)载药微丸,以1 000 mL pH 6.8磷酸盐缓冲液(人工小肠液),pH 7.6磷酸盐缓冲液(人工结肠液)的溶液为溶出介质,在37.5℃,75 r/min条件下,分别在5、10、20、30、45、60 min取样5 mL,过0.45 μm微滤膜,同时补液5 mL。在Kromasil C18色谱柱(4.6 mm×150 mm,5 μm),乙腈-水(62:38),1 mL/min,柱温30℃,检测波长216 nm条件下,进样测定溶出液中蒿甲醚含量,计算累积释放度。②包衣微丸释放度测定:取包衣微丸适量(相当于主药100 mg),放入900 mL pH 1.2盐酸溶液(人工胃液)中2 h,再将微丸放入1 000 mL pH 6.8磷酸盐缓冲液(人工小肠液),4 h后,再放入1 000 mL pH 7.6磷酸盐缓冲液(人工结肠液)3 h。每次变换溶出介质需在5 min内完成,测定方法同载药微丸的测定方法。
2.4包衣处方的筛选
2.4.1包衣材料的选择pH依赖型的结肠包衣材料主要为丙烯酸树脂类,目前多采用Eudragit这类包衣材料。其中Eudragit S100和Eudragit L100常被作为结肠定位包衣材料的首选。但是由于Eudragit L100包衣材料本身的化学性质,其在pH>5.5的溶出介质中,就会溶解,因此药物释放大多发生在小肠中远段。Eudragit S100包衣材料只在pH>7.0的溶出介质中时开始溶解并释放药物,其释药部位在结肠。因此本实验选择Eudragit S100作为包衣材料。
2.4.2增塑剂用量的筛选现对柠檬酸三乙酯用量进行考察。将Eudragit S100用量固定为6.35%,滑石粉的用量固定为1.31%,变化柠檬酸三乙酯的用量。变化的量分别为0.34%,0.63%,1.42%。按照上述的变化数据分别配制包衣液进行包衣,使丸芯都增重28%后,测定不同包衣微丸的体外释放度,柠檬酸三乙酯的用量对该制剂的体外释放影响较大。当柠檬酸三乙酯用量为0.34%时,药物在pH 6.8的溶出介质中释放较多,达到32.3%,不符合结肠定位释放的要求。而柠檬酸三乙酯用量为0.63%时,药物在pH 6.8的溶出介质中释放的量较少,且在pH 7.6的溶出介质中3 h后,蒿甲醚累积释放度达到98.47%,结肠定位效果较好,所以选择柠檬酸三乙酯用量为0.63%。见表1。
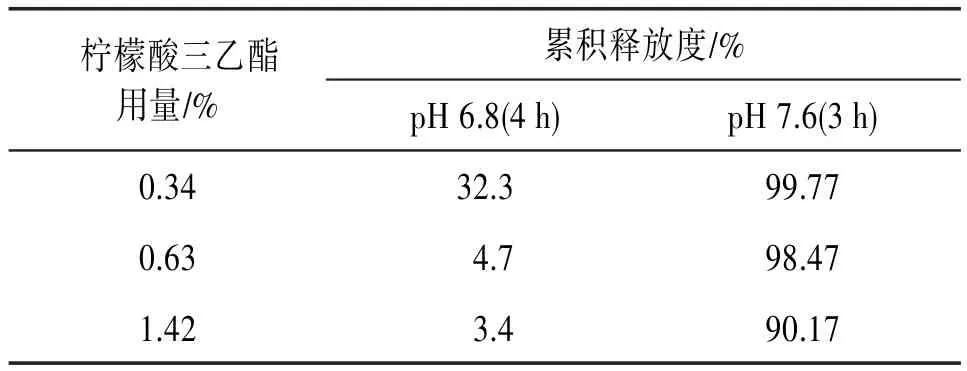
表1 不同柠檬酸三乙酯用量对释放度的影响
2.4.3包衣厚度的筛选包衣增重的厚度直接影响到该制剂的体外释放度,因此,本实验对包衣厚度进行了筛选。按上述包衣液配比,分别考察Eudragit S100增重为18%、28%、40%微丸的释放情况。结果表明,当包衣增重达到18%时,该制剂在pH 6.8的溶出介质中释放达到26.5%。不符合结肠定位释放的要求。当包衣增重达到40%时,pH 6.8的溶出介质中释放较少,但是在pH 7.8的溶出介质中未能达到要求。只有包衣增重在28%时,才符合结肠定位释放的要求。见表2。因此,确定包衣增重为28%。其累计溶出度曲线如下图1所示。
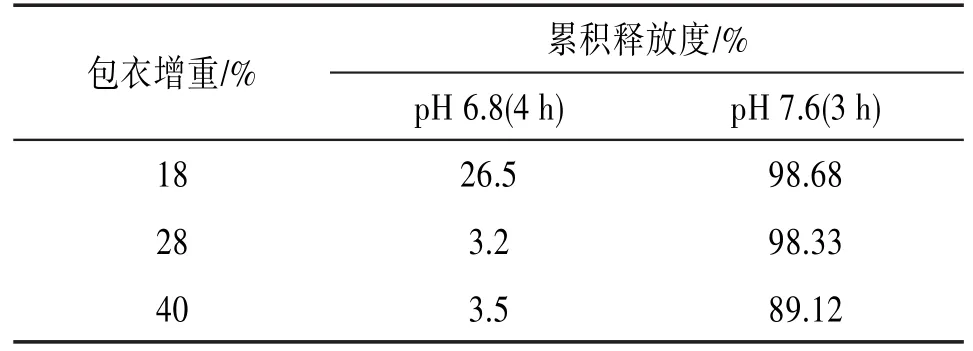
表2 不同包衣增重对释放度的影响
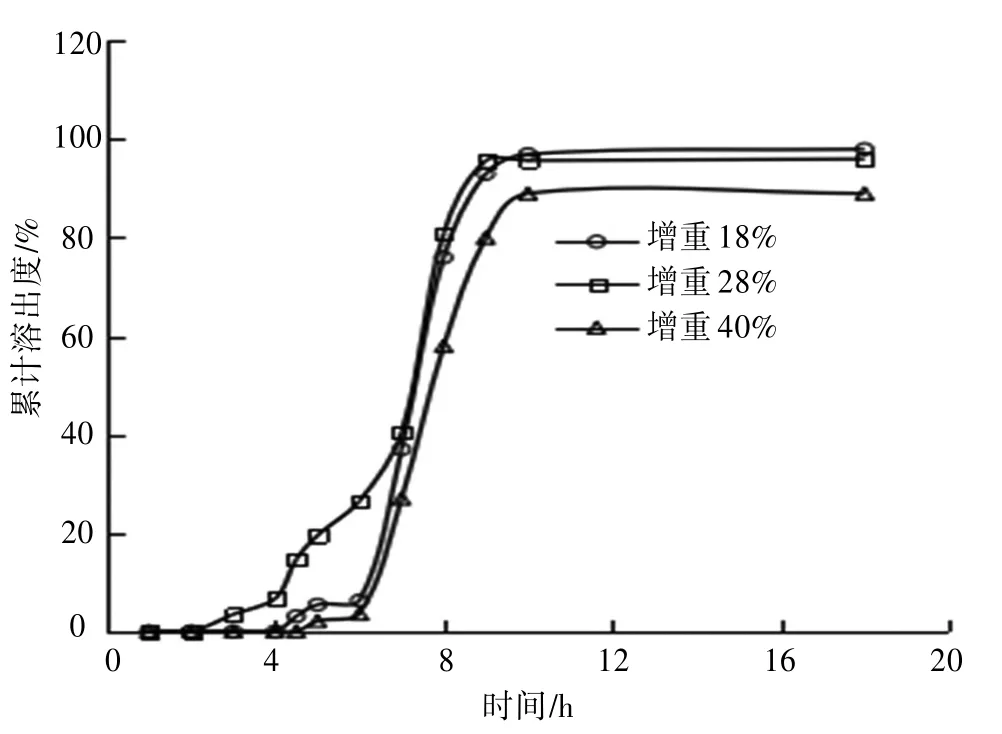
图1 不同包衣增重比例的蒿甲醚结肠定位微丸的累计释放度曲线
3 结论
实验结果表明,该剂型在pH 1.2的溶出介质中未检测到蒿甲醚,在pH 6.8的溶出介质中释放度小于10%,在pH 7.6的溶出介质中释放度达到90%,说明该剂型的处方及工艺是稳定可行的。但是由于此研究的剂型为新剂型,新工艺,并且现在蒿甲醚结肠定位缓放微丸还处于实验室研究阶段,因此,该剂型还需要进行进一步的完善和提高,同时其体内研究和临床研究还需要进一步考察。
〔1〕谭涛,秦宗会,谭蓉.青蒿素类药物的药理作用研究进展〔J〕.中国药业,2009,18(3):63-64.
〔2〕陈欢欢,周慧君.青蒿琥酯的抗血管生成作用〔J〕.药学学报,2004,39(1):29-33.
〔3〕左曙光,刘淳,刘馨,等.蒿甲醚对K562细胞作用的体外实验研究〔J〕.实用医学杂志,2010,26(20):3680-3682.
〔4〕牛红妹,庞来祥,郭振军.青蒿酿液体外抗肿瘤活性研究〔J〕.现代中药研究与实践,2013,27(5):33-35.
〔5〕崔福德.药剂学〔M〕.7版.北京:人民卫生出版社,2011.
〔6〕任国莲,张淑秋.口服结肠定位给药系统的研究进展〔J〕.中国药物与临床,2006,6(1):8-10.
〔7〕CHEN T,CHEN Q H.Aqueous ethylcellubose coating technologyⅡ:influence of curing process on film properties〔J〕. Chin J Pharm,2000,31(7):298-301.
〔Abstract〕Objective:To prepare Artemether colon-specific pellets controlled by pH and study the release in vitro.Methods:The cores of pellets were made by extrusion-spheronization.Pellets were prepared using a fluid bed coater,with Eudragit S100 as the out layer,triethyl citrate added to the dispersion as the plasticizer.Results:Artemether was not detected in solution of pH 1.2 for 2 h.The accumulative release in pH 6.8 phosphate buffer for 4 h was smaller than 5%.While the accumulative release in the pH 7.6 phosphate buffer for 3 h was more than 90%.Conclusion:Colon-specificpellets prepared in this way can well perform colon-specific delivery.
〔Key words〕Artemether;pH controlled;colon-specific;release in vitro
(责任编辑李杨)
Study on the Preparation of Artemether Colon-specific Pellets and the Release in Vitro
Ma Yin1,Zhang Wei2,Zhang Guoli2,Zhang Ruiwu2,Yang Zhaoxiang2*
(1.Dali University,Dali,Yunnan 671000,China;2.KPC Pharmaceutical Inc.,Kunming 650106,China)
R944
A
2096-2266(2016)08-0008-03
2016-03-08
2016-03-28
马寅,硕士研究生,主要从事药物制剂研究.
杨兆祥,高级工程师.

