平菇子实体化学成分的分析研究
朱明洪 陈 屏 王 琦 李 玉(吉林农业大学食药用菌教育部工程研究中心,吉林 长春 130118)
平菇子实体化学成分的分析研究
朱明洪陈屏王琦李玉*
(吉林农业大学食药用菌教育部工程研究中心,吉林 长春 130118)
摘要利用正相硅胶、凝胶等分离材料结合高效液相色谱等分离技术对平菇子实体的化学成分进行分离纯化,并根据光谱数据分析鉴定化合物的结构。从平菇子实体中分离得到8个化合物,分别为(1)麦角甾醇、(2)麦角甾醇过氧化物、(3)22E,24R-5α,6α-环氧麦角甾-8(14),22-二烯-3β,7α-二醇、(4)烟酸、(5)腺苷、(6)D-甘露醇、(7)尿苷、(8)烟酰胺。其中化合物3和5为首次从该菌中分离得到。
关键词平菇;环氧麦角甾;腺苷;烟酰胺
平菇[Pleurotus ostreatus (Jacq.) Quél.],隶属于 担子 菌门 ( Basidomycota)、伞 菌纲(Agaricomycetes)、伞菌亚纲(Agaricomycetide)、侧耳科(Pleurotaceae)、侧耳属(Pleurotus),英文名:Oyster Mushroom、Common Oyster Mushroom,中文别名:冬菇、北风菌、糙皮侧耳、贝形平菇、蛤蛎菇、蚝菌等[1]。在我国大陆大部分地区及台湾、香港都有分布;在国外主要分布于欧洲、北美洲、亚洲、非洲、澳大利亚、南美洲等地[2]。
平菇子实体不仅含有蛋白质、氨基酸、矿物质等多种营养成分[3],而且有抗肿瘤[4]、抗氧化活性[5]、降血糖降血脂[6]等多种功效;它还是“舒筋散”的成分之一[7,8],可用来治疗经络不疏、腰腿疼痛、手脚麻木等疾病[9]。合理开发这种价廉味美质优的食药兼用真菌的重要意义不言而喻。国内外对平菇的化学研究主要集中在多糖[10,11]、多酚[12]及甾类[13~15]等成分上,为深入开展平菇的化学成分研究,在前人研究的基础上我们对人工栽培的平菇子实体化学成分进行了分离及鉴定,结果如下。
1 实验材料与仪器
1.1材料与试剂
平菇子实体购自吉林农业大学食用菌高新技术园区,经吉林农业大学食药用菌教育部工程研究中心李玉教授鉴定确证为平菇[Pleurotus ostreatus (Jacq.) Quél.]。所用试剂:石油醚、二氯甲烷、三氯甲烷、乙酸乙酯、丙酮、乙醇、正丁醇、甲醇(以上试剂均为分析纯,北京化工);甲醇(色谱纯,天津四友);乙腈(色谱纯,山东禹王)。
1.2仪器
KDM 调温电热套(山东鄄城华鲁电热仪器有限公司),RE52-AA旋转蒸发器(上海亚荣生化仪器厂),SHB-B95循环水式多用真空泵(郑州长城科工贸有限公司),AL104电子天平(上海梅特勒-托利多仪器有限公司),WFH-203B三用紫外分析仪(上海精科实业有限公司),TH-Ⅱ型薄层加热器(上海科哲生化科技有限公司),shimadazuLC-6AD高效液相色谱分析仪(日本岛津),shim-pack prep-ODS C18制备柱(20 mm×25 cm,15 µm),Bruker 600M AVANCEⅢ型核磁共振波普仪(瑞士Bruker公司)。
2 实验方法
取平菇干燥子实体5.2 kg,粉碎,95%乙醇提取3次,每次3 h,得提取液,过滤后减压浓缩得流浸膏 496 g。将浸膏分散至水中,分别用石油醚、乙酸乙酯、正丁醇萃取,各得萃取浸膏103.5 g、11.9 g和25.2 g。
石油醚层浸膏采用硅胶柱层析,用石油醚:乙酸乙酯(25︰1、9︰1、9︰1.5、9︰2、7︰3、6︰4、1︰1、0︰1)溶剂系统梯度洗脱,分离得到5个部分Fr.1~5。Fr.2经甲醇反复重结晶得化合物1(45 mg)。Fr.4经石油醚︰二氯甲烷︰乙酸乙酯5︰4︰1硅胶柱洗脱后,再经凝胶柱甲醇反复纯化得化合物2(23 mg)。Fr.5经石油醚︰乙酸乙酯6︰4→4︰6洗脱后再通过HPLC纯化得化合物3(7.6 mg)。
乙酸乙酯层萃取浸膏采用三氯甲烷︰甲醇(200︰1、100︰1、50︰1、20︰1、10︰1、5︰1、2︰1、1︰1、0︰1)溶剂系统梯度洗脱,分离得到8个部分Fr.1~8。Fr.6凝胶柱甲醇洗脱,HPLC纯化得化合物4(12 mg)。
正丁醇层浸膏用乙酸乙酯、甲醇(1︰0→2 ︰1→1︰1→0︰1)溶剂系统梯度洗脱得到 6个部分Fr.1~6。Fr.3经凝胶柱甲醇洗脱后,甲醇反复重结晶得化合物5(13.3 mg)。Fr.4经凝胶柱甲醇洗脱,得化合物6(8.6 mg)。Fr.2经凝胶柱甲醇洗脱,HPLC纯化得化合物7(15.5 mg)和化合物8(8.6 mg)。
3 结构鉴定
化合物 1:无色针状结晶(三氯甲烷)。1H-NMR (600 MHz,CDCl3) δ: 5.58 (1H,dd,J=5.27,1.88Hz,H-6),5.37-5.46(1H,m,H-7),5.21-5.26(1H,m,H-23),5.16-5.27(1H,m,H-22),3.65(1H,tt,J=11.25,4.19Hz,H-3),1.05 (3H,d,J=6.40Hz,H-21),0.96 (3H,s,H-19),0.93 (3H,d,J=6.78Hz,H-28),0.85(3H,d,J=6.78Hz,H-26),0.83(3H,d,J=6.78Hz,H-27),0.63(3H,s,H-18);13C-NMR (150 MHz,CDCl3)δ: 39.34(C-1),32.23(C-2),70.68 (C-3),37.25 (C-4),140.10(C-5),119.81(C-6),116.52 (C-7),141.65 (C-8),46.51 (C-9),38.61(C-10),21.35 (C-11),40.53 (C-12),41.03(C-13),54.80(C-14),23.21 (C-15),28.46(C-16),56.01(C-17),12.26(C-18),16.50(C-19),40.57(C-20),21.30(C-21),135.78(C-22),132.23(C-23),43.05(C-24),33.31(C-25),19.84(C-26),20.13(C-27),17.80(C-28)。以上数据与文献报道基本一致[16],故鉴定此化合物为麦角甾醇[(22E,24R)-ergosta-5,7,22-trien-3β-ol]。

化合物1 麦角甾醇化学结构式
化合物 2:无色针状结晶(三氯甲烷)。1H-NMR (600 MHz,CDCl3) δ: 6.51 (1H,d,J=8.66Hz,H-7),6.24 (1H,d,J=8.66Hz,H-6),5.20-5.25 (1H,m,H-22),5.13-5.18(1H,m,H-23),3.97(1H,dt,J=11.11,5.65Hz,H-3),1.20-1.26(3H,m,H-19),1.00(3H,d,J=6.78Hz,H-21),0.91(3H,d,J=7.15Hz,H-28),0.89 (3H,s,H-18),0.83(3H,d,J=3.01Hz,H-26),0.82(3H,s,H-27);13C-NMR (150 MHz,CDCl3) δ: 37.19(C-1),30.35(C-2),66.65(C-3),34.92(C-4),82.34(C-5),135.40(C-6),130.94(C-7),79.61(C-8),51.36(C-9),37.17(C-10),20.83(C-11),39.58(C-12),44.77(C-13),51.91(C-14),23.61(C-15),28.80(C-16),56.45(C-17),13,07(C-18),18.36(C-19),39.87(C-20),21.07(C-21),135.62(C-22),132.54(C-23),43.00(C-24),33.27(C-25),19.82(C-26),20.12(C-27),17.74(C-28)。以上数据与文献报道基本一致[17],故鉴定此化合物为麦角甾醇过氧化物[24R-5α,8α-epidioxyergosta-6,22-dien-3β-ol]。
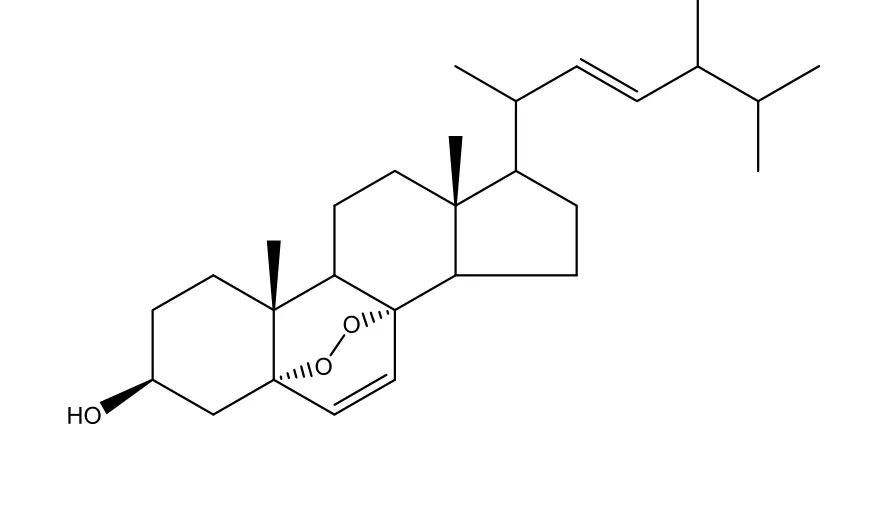
化合物2 麦角甾醇过氧化物化学结构式
化合物3:白色针状结晶(丙酮)。1H-NMR(600 MHz,CD3OD) δ: 5.23-5.25 (2H,m,H-22,23),4.41 (1H,d,J=1.83Hz,H-7),3.74-3.77(1H,m,H-3),3.05(1H,d,J=2.93Hz,H-6),0.90-0.91(3H,m,H-28),0.84-0.88(12H,m,H-18,26,27);13C-NMR (150 MHz,CD3OD) δ: 32.13(C-1),28.66(C-2),69.46(C-3),40.61(C-4),68.19(C-5),62.84(C-6),66.06(C-7),126.78(C-8),40.91(C-9),38.09(C-10),20.55(C-11),37.30(C-12),44.36(C-13),153.07(C-14),25.89(C-15),33.61(C-16),58.39(C-17),18.77(C-18),17.09(C-19),40.76(C-20),21.99(C-21),137.07(C-22),133.57(C-23),44.61(C-24),34.59(C-25),20.31(C-26),20.70(C-27),18.43(C-28)。以上数据与文献报道基本一致[18],故鉴定此化合物为22 E,24 R-5α,6α-环氧麦角甾-8(14),22-二烯-3 β,7α-二醇[22E,24R-5α,6α-epoxyergosta-8(14),22-diene-3β,7α-diol]。

化合物 3 22E,24R-5α,6α-环氧麦角甾-8(14),22-二烯-3β,7α-二醇化学结构式

化合物4 烟酸化学结构式
化合物4:无色针状结晶(甲醇)。1H-NMR (600 MHz,CD3OD) δ: 9.01 (1H,s,H-2),8.67 (1H,d,J=4.77Hz,H-6),8.28 (1H,d,J=7.70Hz,H-5),7.53(1H,dd,J=7.70,5.14Hz,H-4);13C-NMR (150 MHz,CD3OD) δ: 167.95(-COOH),153.84 (C-2),128.89(C-3),139.43(C-4),125.43(C-5),151.45(C-6)。以上数据与文献报道基本一致[19],故鉴定此化合物为烟酸(nicotinic acid)。化合物5:白色粉末(二甲基亚砜)。1H-NMR (600 MHz,DMSO) δ: 8.36(1H,s,H-8),8.15(1H,s,H-2),7.36(2H,br.s.,NH2-6),5.88(1H,d,J=6.24Hz,H-1'),5.46(2H,d,J=6.24Hz,-OH),5.21(1H,d,J=4.77Hz,-OH),4.62(1H,q,J=5.87Hz,H-2'),4.15(1H,d,J=3.30Hz,H-3'),3.97(1H,d,J=2.93Hz,H-4'),3.68(1H,dt,J=12.01,3.53Hz,H-5'),3.57(1H,td,J=7.79,3.48Hz,H-5');13C-NMR (150 MHz,DMSO) δ: 152.43(C-2),149.09(C-4),119.39(C-5),156.20(C-6),139.98(C-8),87.94(C-1'),73.46(C -2'),70.71(C -3'),85.94(C -4'),61.72(C -5')。以上数据与文献报道基本一致[20],故鉴定此化合物为腺苷(adenosine)。

化合物5 腺苷化学结构式

化合物6 D-甘露醇化学结构式
化合物6:无色簇状结晶(水)。13C-NMR (150 MHz,D2O) δ: 63.2(C-1,6),70.7(C-2,5),69.2 (C-3,4)。以上数据与文献报道基本一致[21,22],故鉴定此化合物为D-甘露醇(Mannitol)。化合物7:白色粉末(水)。1H-NMR (600 MHz,D2O) δ: 7.77(1H,d,J=7.91,H-6),5.84(1H,d,J=3.76Hz,H-1'),5.80(1H,d,J=7.91Hz,H-5),4.24-4.29(1H,m,H-2'),4.15(1H,t,J=5.08Hz,H-3'),4.05(1H,br.s.,H-4'),3.83(1H,d,J=12.42Hz,H-5'a),3.72(1H,dd,J=12.80,3.76Hz,H-5'b);13C-NMR (150 MHz,D2O) δ: 153.00(C-2),168.04(C-4),102.33(C-5),141.58(C-6),89.43(C-1'),73.59(C-2'),69.41(C-3'),84.08(C-4'),60.75(C-5')。以上数据与文献报道基本一致[23],故鉴定此化合物为尿苷(uridine)。

化合物7 尿苷化学结构式
化合物 8:白色粉末(水)。1H-NMR (600 MHz,D2O) δ: 8.82(1H,br.s.,H-2),8.61(1H,d,J=4.14Hz,H-6),8.13(1H,d,J=7.91,H-4),7.45-7.52(1H,m,H-5);13C-NMR (150 MHz,D2O)δ: 170.72(-C=O),147.61 (C-2),129.25(C-3),136.41(C-4),124.17(C-5),151.80(C-6)。以上数据与文献报道基本一致[24],故鉴定此化合物为烟酰胺(nicotinamide)。
4 结 论

化合物8 烟酰胺化学结构式
本实验利用正相硅胶、凝胶等分离材料结合高效液相色谱等分离技术从平菇子实体中分离得到8个化合物,其中麦角甾类化合物3个:麦角甾醇,麦角甾醇过氧化物和 22E,24R-5α,6α-环氧麦角甾-8(14),22-二烯-3β,7α-二醇。吡啶类衍生物2个:烟酸和烟酰胺。生物碱类化合物2个:腺苷和尿苷。22E,24R-5α,6α-环氧麦角甾-8(14),22-二烯-3β,7α-二醇和腺苷为首次从平菇中分离得到,国内外文献尚未见报道。甾醇是菌物细胞膜的重要组成部分,大部分菌物中含有该类物质,甾醇在菌物抗菌抗肿瘤等方面起到了重要作用,同时也是生产“可的松” “黄体酮”等药物的前体物质[25]。有研究发现22E,24R-5ɑ,6ɑ-环氧麦角甾-8(14),22-二烯-3β,7α-二醇能体外有效抑制 HCT15等癌细胞株的生长[26],而烟酰胺是人体合成辅酶 I和辅酶 II的前体物质,具有抗氧化、抗炎和DNA修复等多种功效,是细胞正常生命活动必不可少的重要成分之一[27]。这些化合物的药理活性表明,研究平菇对合理开发和利用该菌具有重要意义,有望从中获得新的药用资源。
参考文献
[1]李传华,曲明清,曹晖,等. 中国食用菌普通名名录[J].食用菌学报,2013,20(3): 50-72.
[2]王呈玉. 中国侧耳属[Pleurotus(Fr.)Kumm.]真菌系统分类学研究[D]. 长春: 吉林农业大学,2004.
[3]刘晓峰,孙晓波. 侧耳属真菌化学成分及药用活性研究进展[J]. 吉林农业大学学报1998,20(3): 92-98.
[4]Kong Fanli,Li Feng-e,He Zhongmei et al.. Anti-tumor and macrophage activation induced by alkali-extracted polysaccharide from Pleurotus ostreatus[J]. International Journal of Biological Macromolecules,2014,69: 561-566.
[5]Singh Vinita,Vyas Deepak,Pandey Rajshree et al.. Pleurotusostreatus produces antioxidantand antiarthritic activity in wistar albino rats[J]. World Journal of Pharmacy and Pharmaceutical Sciences,2015,4(5): 1230-1246.
[6]Dos Santos Leandro Freire,Zanatta Ana Lucia,Soccol Vanete Thomaz et al.. Hypolipidemic and antiatherosclerotic potential of Pleurotus ostreatus,cultived by submerged fermentation inthe high-fat diet fed rats[J]. Biotechnology and Bioprocess Engineering,2013,18(1): 201-208.
[7]上海农业科学院食用菌研究所. 中国食用菌志[M]. 北京: 中国林业出版社,1991.
[8]中国科学院青藏高原综合科学考察队. 川西地区大型经济真菌[M]. 北京: 科学出版社,1994.
[9]戴玉成,杨祝良. 中国药用真菌名录及部分名称的修订[J]. 菌物学报,2008,27(6): 801-824.
[10]Sun Yongxu,Liu Jicheng. Purification,structure and immunobiological activity of a water-soluble polysaccharide from the fruiting body of Pleurotus ostreatus[J]. Bioresource Technology,2009,100(2): 983-986.
[11]Irene Palacios,Ana García-Lafuente,Eva Guillamón et al.. Novel isolation of water-soluble polysaccharides from the fruiting bodies of Pleurotus ostreatus mushrooms[J]. Carbohydrate Research,2012,358: 72-77.
[12]M. Bhattacharya,P.P. Srivastav,H.N. Mishra. Optimization of process variables for supercritical fluid extraction of ergothioneine and polyphenols from Pleurotus ostreatus and correlation to free-radical scavenging activity[J]. The Journal of Supercritical Fluids,2014,95: 51-59.
[13]Vladimir Chorot,Lubomír Opletal,Luděk ahodář et al.. ERGOSTA-4,6,8,22-TETRAEN-3-ONE FROM THE EDIBLE FUNGUS,PLEUROTUS OSTREATUS (OYSTERFUNGUS)[J]. Phytochemistry,1997,45(8): 1669-1671.
[14]Ana Plemenitaš,Tatjana Kastelic-Suhadolc,Dušan Žigon et al.. Steroido-genesis in the fungus Pleurotus ostreatus[J]. Comparative Biochemistry and Physiology. Part B: Biochemistry and Molecular Biology,1999,123(2): 175-179.
[15]Lefki-Maria Papaspyridi,Nektarios Aligiannis,Paul Christakopoulos et al.. Production of bioactive metabolites with pharmaceutical and nutraceutical interest by submerged fermentation of Pleurotus ostreatus in a batch stirred tank bioreactor[J]. Procedia Food Science 2011,1: 1746-1752.
[16]万辉,孙荣奇,吴达俊,等. 栗色圆孔牛肝菌中的三种甾醇成分[J]. 天然产物研究与开发,1999,11(6): 18-21.
[17]许明峰,沈莲清,王奎武. 雷丸化学成分的研究[J].中草药,2011,42(2): 251-254.
[18]李艳军,李小霞,陈国栋,等. 内生真菌 Sporormiella irregularis (No.71-11-4-1) 中一个新的二裂甾体[J]. 沈阳药科大学学报,2012,29(9): 678-701.
[19]孙忠华,肖建辉,潘卫东,等. 江西虫草菌丝体化学成分研究[J]. 中药材,2010,33(12): 1878-1881.
[20]韦柳斌. 青天葵及翻白叶树根化学成分研究 [D]. 广州:暨南大学,2012.
[21]王晓岩,图力古尔,包海鹰. 多脂鳞伞的化学成分研究[J]. 上海中医药杂志,2015,49(5): 106-110.
[22]郑宏亮,图力古尔,包海鹰,等. 荷叶离褶伞的化学成分研究[J]. 中国中药杂志,2013,38(24): 4335-4339.
[23]秦艳,吴亦晴,尹成乐,等. 天山堇菜的化学成分研究[J]. 中草药,2014,45(21): 3057-3061.
[24]朱小迪,李永慈,王建忠,等. 黄心卫矛化学成分的分离与鉴定[J]. 中成药,2011,33(1): 107-110.
[25]宋明杰,包海鹰. 菌物中麦角甾类化合物的研究进展[J]. 菌物研究,2013 (4): 266-274.
[26]宋珊珊,王乃利,高昊,等. 海洋真菌 96F197 抗癌活性成分研究[J]. 中国药物化学杂志,2006,16(2): 93-97.
[27]杨驰,郑咏秋,戴敏. 烟酰胺药理作用研究进展[J].临床肺科杂志,2011,16(12): 1914-1916.
*为通讯作者
中图分类号:S646
文献标识码:A
文章编号:2095-0934(2016)04-242-06
基金项目:公益行业(农业)科研专项“作物秸秆基质化利用”(201503137);吉林省秸秆综合利用技术创新平台
作者简介:朱明洪(1990—),女,硕士,主要从事药用真菌方面的研究,E-mail:996513924@qq.com
Research on chemical constituents of the fruiting bodies of Pleurotus ostreatus
Zhu MinghongChen PingWang QiLi Yu*
(Engineering Research Center of Chinese Ministry of Education for Edible and Medicinal Fungi,Jilin Agricultural University,Changchun,Jilin 130118,China)
AbstractTo investigate the chemical constituents of the fruiting bodies of Pleurotus ostreatus. The chemical constituents were separated and purified by chromatographic methods such as silica gel and Sephadex LH-20,HPLC etc.,and identified by spectroscopic analyses. Eight compounds were isolated and their structures were identified as (1) (22E,24R)-ergosta-5,7,22-trien-3β-ol,(2) 24R-5α,8α-epidioxyergosta-6,22-dien-3β-ol; (3) 22E,24R-5α,6α-epoxyergosta-8 (14),22-diene-3β,7α-diol; (4) nicotinic acid; (5) adenosine; (6) mannitol; (7) uridine; (8) nicotinamide. Compounds 3 and 5 were separated from the fruiting bodies of Pleurotus ostreatus for the first time.
KeywordsPleurotus ostreatus; epidioxyergosta; adenosine; nicotinamide

