铜与硝酸反应实验的一体化设计
伍强 方瑞光
摘要:介绍了全国第十二届化学实验教学创新研讨会上关于铜与硝酸反应的3例优秀作品。在此基础上,设计了一套新的实验装置。用该装置可连续演示铜与浓硝酸、二氧化氮与水、铜与稀硝酸及一氧化氮与氧气反应等实验,达到实验一体化的目的。实验具有对比性、直观性、自控性、调控性、操控性、低污染的优点,具有较好的实验教学功效。
关键词:铜与硝酸;反应实验;一体化设计;实验改进与创新
文章编号:1005–6629(2016)6–0060–04 中图分类号:G633.8 文献标识码:B
中国教育学会化学教学专业委员会主办的全国第十二届化学实验教学创新研讨会于2015年10月27日~10月30日,在福建省厦门第一中学举行。研讨会上展示了来自全国各地203件实验创新作品。在闭幕式上,华东师范大学王程杰教授作了精彩点评,强调“一看就懂,一学就会,重在思维引导”的实验创新设计理念。
1 Cu和HNO3反应实验创新作品分析
Cu与HNO3反应实验创新是一个永恒的课题,许多研究者已做了创新设计[1~4]。在本届研讨会上,展示的Cu与HNO3反应实验创新作品共有12件,Cu与HNO3反应的容器分别是注射器(4件)、U型管(3件)、试管(2件)、胶头滴管(1件)、移液管(1件)、小玻璃瓶(1件)。其中湖南省代表队贾超老师的作品“铜与稀硝酸反应制取一氧化氮实验装置的改进”、浙江省代表队顾建鸣老师的作品“铜与浓、稀硝酸反应实验的改进”、福建省代表队马东老师的作品“硝酸性质实验的一体化设计”受到评委组好评,获一等奖。笔者反复观看了现场展示实验的视频,按照作者的实验装置以及试剂的用量和浓度、操作的步骤和方法,对三件优秀作品做了实验再现。领悟了实验创新设计的理念,受益匪浅,同时也发现了作品存在的不足之处,提出了改进的方案。
(1)“铜与稀硝酸反应制取一氧化氮实验装置的改进”[5],实验装置如图1所示。向大试管中加入约2/3试管预先水浴加热的稀HNO3(1:3),再加适量植物油至接近试管口,然后塞紧挂有铜片的橡皮塞,铜片与稀HNO3反应生成NO气体慢慢地将注射器的活塞往上推,收集3mL NO气体后取下橡皮塞(包括铜片)。向注射器里再吸入适量空气,气体颜色由无色变为红棕色。
[实验的优点]实验装置简便,Cu与稀HNO3反应生成的NO气体没有直接与空气接触。清晰地观察到无色NO和O2反应生成红棕色NO2的实验过程和现象。
[实验的缺点]取下橡皮塞时,在试管口处观察到少量的红棕色气体生成,有氮氧化合物外逸。橡皮塞如果蘸上植物油,则易引起脱塞现象。稀HNO3要预先水浴加热,学生会误认为Cu与稀HNO3在加热条件下才能反应。
[试剂的改进]不用植物油,单用稀HNO3直接加至接近试管口,实验操作简单,效果却相同。将铜片换成细铜丝且适当增大稀HNO3浓度,这样Cu与稀HNO3反应较快,就可省去水浴加热稀HNO3的操作。
(2)“铜与浓、稀硝酸反应实验的改进”[6],实验装置如图2所示(注:移液管用滴定管夹固定,固定装置略)。往锥形瓶中加入30mL浓HNO3,用洗耳球对准上方橡皮管口吸气,至浓HNO3充满整个移液管,关闭弹簧夹A。铜丝与浓HNO3反应生成NO2,液面下降固液分离,关闭弹簧夹B。通过上方橡皮管口用注射器将5mL水注入移液管中,NO2与水反应生成NO。用注射器吸取移液管中的部分NO,再抽出注射器针(注:此操作必须使移液管内产生负压)。在锥形瓶中加入50mL水用于稀释浓HNO3,打开弹簧夹B,倒吸约5mL的稀HNO3。铜丝与稀HNO3反应产生微小气泡,液面下降非常缓慢,过了十几分钟固液分离。向移液管中注入空气,气体颜色由无色变为红棕色。
[实验的优点] Cu与浓、稀HNO3反应生成一定量的气体使固液自动分离,就像作者所说的:“类似于启普发生器原理,达到固液分离效果”。能清晰地观察到NO2与NO相互转化的实验现象。
[实验的缺点]用注射器吸取移液管中部分的NO,使移液管内产生负压,操作难度大。打开弹簧夹B使稀HNO3倒吸,难以控制移液管中稀HNO3的浓度。移液管中NO气体没有被完全清除,假如铜与稀HNO3反应生成H2,向NO和H2的混合气体中注入空气也能生成红棕色气体,因此向移液管中注入空气,气体颜色由无色变为红棕色,不能说明Cu与稀HNO3反应生成NO。
[操作的改进]改进铜丝与稀HNO3反应的操作,打开弹簧夹A、B,用洗耳球对准上方橡皮管口吸气,至稀HNO3充满整个移液管,这样移液管中生成的NO气体都是铜丝与稀HNO3反应生成的。
(3)“硝酸性质实验的一体化设计”[7],实验装置如图3所示。稍压扁塑料瓶,塞上橡皮塞。用注射器向小玻璃瓶中注入1mL浓HNO3,铜片与浓HNO3反应生成NO2。拉推注射器活塞2次,水经过三通管吸入小玻璃瓶中,吸入约20~30mL水。NO2与水反应生成NO,铜片与稀HNO3反应极微弱,近距离能观察到稀少微小的气泡。同时挤压加压球和外拉注射器活塞向小玻璃瓶中注入空气,气体颜色由无色变为红棕色。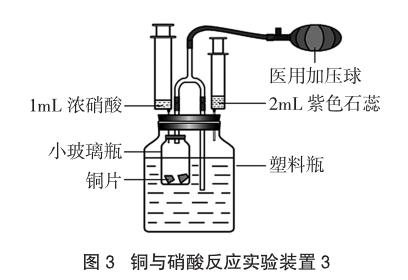
[实验的优点]拉推注射器活塞使水吸入小玻璃瓶中,能清晰地观察到NO2与NO相互转化的实验现象。
[实验的缺点]向小玻璃瓶中注入20~30mL水,铜片与稀HNO3反应极微弱,此时小玻璃瓶中的NO气体主要是NO2与H2O反应生成的,因此向小玻璃瓶中注入空气,气体颜色由无色变为红棕色,不能说明Cu与稀HNO3反应生成NO。另外实验装置复杂,不符合“一看就懂,一学就会,重在思维引导”的实验创新设计理念,难以找到合适的塑料瓶和小玻璃瓶。
[装置的改进]用矿泉水瓶和细口瓶分别替代合适的塑料瓶和小玻璃瓶,设计成如图4所示的实验装置,达到一看就懂的目的,而装置功能不变。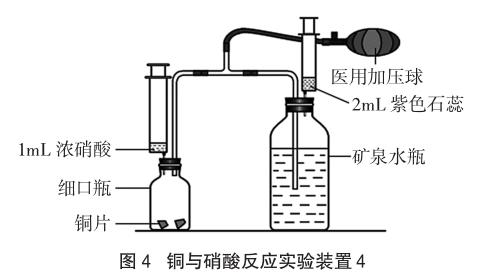
三件优秀作品其主要优点如下:贾超老师的作品,Cu与稀HNO3反应生成的NO气体没有与空气直接接触。顾建鸣老师的作品,Cu与浓、稀HNO3反应生成一定量的气体使固液自动分离。马东老师的作品,拉推注射器活塞能使水吸入小玻璃瓶中。借鉴三件优秀作品的优点,笔者设计了一套新的实验装置用于Cu与浓、稀HNO3反应实验演示。
2 Cu与HNO3反应实验再创新
2.1 实验仪器及试剂
实验仪器:250mL吸滤瓶、干燥管(25mL容积)、30mL塑料注射器的外壳、T型玻璃管、弹簧夹、250mL锥形瓶、100mL注射器(化学实验用注射器,出口口径较大,便于液体或气体的进出)
实验试剂:65%~68%浓硝酸、粗铜丝、细铜丝(从软导线中取出)、浓NaOH溶液
2.2 实验装置的设计
设计的实验装置如图5所示。吸滤瓶侧口连接30mL塑料注射器的外壳,内装蘸有浓NaOH溶液的棉花团。吸滤瓶上口插入带有橡皮塞的干燥管,再通过T型玻璃管连接100mL注射器。
2.3 实验操作、现象和结论
2.3.1 Cu与浓HNO3反应、NO2与H2O反应
(1)在吸滤瓶中加入30mL浓HNO3,在干燥管中加入粗铜丝,按如图5所示组装装置。
(2)打开K1关闭K2,外拉注射器活塞,吸滤瓶中的浓HNO3被吸入干燥管中至充满,关闭K1。干燥管中生成红棕色气体,溶液呈现绿色,液面下降固液分离。粗铜丝与浓HNO3反应生成NO2,NO2溶于含有Cu(NO3)2的浓HNO3溶液中呈现绿色。
(3)打开K2关闭K1,注射器吸入50~80mL水。关闭K2打开K1,注射器中的水被自动吸入干燥管中。干燥管中红棕色气体消失,约有1/3干燥管的无色气体生成,吸滤瓶中溶液呈现蓝色。NO2与水反应生成NO。
2.3.2 Cu与稀HNO3反应、NO与O2反应
(1)将橡皮管从锥形瓶中取出,控制K1、K2,向干燥管中注入一注射器的空气(清除干燥管中氮氧化合物),打开干燥管塞子,向干燥管中添加一团细铜丝,塞紧塞子。
(2)外拉注射器活塞,吸滤瓶中的稀HNO3被吸入干燥管中至充满,关闭K1。干燥管中生成无色气体,液面下降固液分离。铜丝与稀HNO3反应生成NO。
(3)打开K1关闭K2,外拉注射器活塞吸入NO,关闭K1,打开K2,再外拉注射器活塞吸入少量空气。注射器中气体颜色由无色变成红棕色。NO与空气中O2反应生成NO2。
(4)将橡皮管插入锥形瓶中,控制K1、K2,将锥形瓶中的水转移到吸滤瓶中,实验结束。
2.4 实验设计的思考
2.4.1 Cu与HNO3反应的速率
Cu与浓、稀HNO3反应速率不同,为控制反应速率,选用粗铜丝与浓HNO3反应,用细铜丝与稀HNO3反应。在常温下,对于Cu与稀HNO3的反应,浓HNO3与水体积比以1:1.7至1:2.7配制稀HNO3较好,稀HNO3浓度过大反应会生成少量NO2,稀HNO3浓度过小反应缓慢。Cu与HNO3反应速率受温度影响较大,在气温较低的冬天,可将铜丝绕成螺旋状或球状,提高铜丝周围溶液的温度,从而增大反应速率。铜丝的粗细、HNO3的浓度、反应物的温度均影响Cu与HNO3反应的速率,通过对比实验证实:生成的Cu(NO3)2也会明显提高Cu与稀HNO3的反应速率。
2.4.2 NO2与H2O反应生成NO
1体积的NO2与H2O反应应有1/3体积的NO生成,其实NO2与水反应较复杂。当温度为294K左右时,红棕色气体为NO2和N2O4的混合物,其中约含15%的NO2[8]。假设1体积NO2和N2O4的混合物与水完全反应生成NO,则至多生成0.62体积的NO,因此有较多的NO生成。NO2易溶于水,并歧化生成HNO3和HNO2:2NO2+H2O=HNO3+HNO2,HNO2不稳定,受热(或强酸性条件)立即分解:3HNO2=HNO3+2NO+H2O[9],因此实验条件下HNO2分解的量不确定。在实验时,若向干燥管中注水过快,HNO2未分解就进入吸滤瓶中,生成NO量不到1/3干燥管;若向干燥管中注水较慢,生成NO量超过1/3干燥管,甚至达到1/2干燥管,因此在教学中观察到有无色的NO气体生成即可,不必深究生成NO气体的多少。
2.5 实验创新的意义
用设计的实验装置可连续地演示Cu与浓HNO3、NO2与H2O、Cu与稀HNO3、NO与O2的反应实验,实验现象明显,达到一体化设计的目的。实验具有以下六个方面的优点,因此具有良好的实验教学功效。
(1)对比性。Cu与浓HNO3反应、Cu与稀HNO3反应都是在隔绝任何气体的相同情况下进行的。
(2)直观性。能看到干燥管中的NO2气体与H2O反应生成一定量的NO气体。
(3)自控性。Cu与浓、稀HNO3反应生成一定量的气体使固液自动分离。
(4)调控性。在实验过程中,可以添加细铜丝增大Cu与稀HNO3的反应速率。
(5)操控性。如控制好K1、K2,可将锥形瓶中的水转移到吸滤瓶中。
(6)低污染。用注射器的外壳,内装浸有浓 NaOH溶液的棉花团来吸收氮氧化物较为完全。
参考文献:
[1]张正飞,柏书梅.利用胶头滴管演示铜与硝酸的反应[J].化学教学,2010,(2):8.
[2]雷玉芳.铜与硝酸反应实验的质疑和探究[J].化学教学,2010,(5):15~16.
[3]谭文生.铜与浓、稀硝酸反应实验的绿色化设计[J].化学教学,2012,(11):45~46.
[4]王玉芬.在注射器中进行铜和硝酸反应实验[J].化学教学,2013,(7):41~42.
[5][6][7]中国教育学会化学教学专业委员会.全国第十二届化学实验教学创新研讨会资料汇编[M].福建,2015:267,329,394.
[8][9]北京师范大学等.无机化学(下册)(第4版)[M].北京:高等教育出版社,2003:527,527.

