盐酸阿霉素分子印迹传感器的制备及识别特性
张 燕, 郑 晶, 王 娟, 郭满栋
(山西师范大学化学与材料科学学院, 临汾 041004)
盐酸阿霉素分子印迹传感器的制备及识别特性
张燕, 郑晶, 王娟, 郭满栋
(山西师范大学化学与材料科学学院, 临汾 041004)
摘要采用自组装以及电聚合的方法, 在磷酸盐缓冲液(PBS)中以3,4-乙烯二氧噻吩(EDOT)为功能单体, 盐酸阿霉素(DOX)为模板, 在金电极表面电聚合制备DOX印迹敏感膜(MIPs), 构建了一种选择性检测DOX的分子印迹电化学传感器. 采用循环伏安法(CV)及交流阻抗法(EIS)对其性能进行了表征. 优化实验条件后, 在含0.005 mol/L K3 [Fe(CN)6]及0.1 mol/L KCl的PBS中, 应用差分脉冲伏安法(DPV)测试了该传感器的响应性能. 实验结果表明, 该传感器检测DOX的线性范围为4.0×10-7~1.0×10-6mol/L, 相关系数为0.9967, 检出限(S/N=3)达6.5×10-8mol/L; 采用电化学洗脱法可使传感器再生, 对DOX的测定具有良好重现性及稳定性; 该传感器对于干扰物长春碱、 放线菌素D及5-氟尿嘧啶有微弱的电流响应, 显示出良好的选择性. 将该传感器用于人体血样中盐酸阿霉素的分析, 回收率为96.0%~106.7%, 表明其具有潜在的实用价值.
关键词分子印迹聚合物; 电化学传感器; 3,4-乙烯二氧噻吩; 盐酸阿霉素

Fig.1 Structures of DOX and EDOT
盐酸阿霉素(DOX, 结构式见图1)属蒽环类抗生素, 是一种抗肿瘤药物, 抗瘤谱较广, 临床上用于治疗急性白血病、 恶性淋巴瘤、 乳腺癌、 肺癌、 卵巢癌、 骨及软组织肉瘤、 肾母细胞瘤、 神经母细胞瘤、 膀胱癌、 甲状腺癌、 前列腺癌、 头颈部鳞癌、 睾丸癌、 胃癌和肝癌等. 它在人体内的存在量直接影响人体健康状况, 因此构建一种能对血样中盐酸阿霉素进行快速、 灵敏、 准确的检测方法, 在与其相关疾病的快速有效诊断上具有重要的实际价值. 目前, 检测DOX的方法主要有高效液相色谱法[1], 毛细管电泳法[2], 荧光法[3]及流动注射化学发光法[4]等, 这些方法普遍存在仪器操作复杂、 耗时且高成本等不足, 因此研究高效、 快速且简单的DOX检测方法仍有必要.
分子印迹电化学传感器[5~10]因其灵敏度高、 选择性好及性能稳定等优点[11], 已逐渐成为电化学分析法中极有潜力的研究对象, 其中电流型传感器应用最广. 相比于传统聚合法[12~14], 电化学聚合法因对印迹膜厚度及多孔性的可控性[15~17]使其近年来得到迅速发展. 本文采用电聚合3,4-乙烯二氧噻吩(EDOT, 结构式见图1)制备了导电聚合膜聚3,4-乙烯二氧噻吩(PEDOT). 以PEDOT[18]为功能单体, 盐酸阿霉素为模板分子, 构建了盐酸阿霉素分子印迹传感器. 与文献[19]报道的浸蜡石墨电极伏安法相比, 本传感器响应快、 成本低、 选择性良好且具有更低的检出限, 可满足盐酸阿霉素痕量分析的要求. 将其初步应用于测定人体血清中盐酸阿霉素含量, 获得了较满意的结果.
1实验部分
1.1试剂与仪器
盐酸阿霉素(扬子江药业有限公司); 3,4-乙烯二氧噻吩(合肥博美生物科技有限责任公司); 壳聚糖(国药集团化学试剂有限公司); 氯金酸(武汉鑫思锐科技有限公司); 柠檬酸钠(天津市科密欧化学试剂有限公司); 磷酸二氢钾和磷酸氢二钠(天津市申泰化学试剂有限公司)配成不同pH值的PBS缓冲液. 所用试剂均为分析纯, 实验用水为去离子水. 实验过程均在室温下进行.
LK2005A型电化学工作站(天津市兰力科化学电子高技术有限公司);KQ-250B型超声波清洗器(昆山市超声仪器有限公司);JSM-7500F型扫描电子显微镜(日本电子公司);pHS-3C型酸度计(上海伟业仪器厂). 电化学实验采用三电极系统: 金电极为工作电极(d=2mm);Ag/AgCl为参比电极; 铂电极为对电极.
1.2实验过程
1.2.1分子印迹膜传感器的制备向50mL去离子水中加入0.35mLHAuCl4溶液, 加热沸腾后快速滴加3mL质量分数为1%的柠檬酸钠溶液, 搅拌30min, 待溶液变为紫红色后移去热源, 再搅拌10min, 得到纳米金溶胶[20]. 取200μL纳米金加入壳聚糖溶液中, 超声溶解, 制得CS-AuNPs混合液. 移取3μLCS-AuNPs混合液滴涂于基体电极表面, 于室温下晾干后, 将其置于含4×10-3mol/LEDOT和1×10-5mol/L盐酸阿霉素的PBS缓冲溶液(pH=7.23)中, 以50mV/s的速率在-0.2~1.5V电位窗口内电聚合7圈, 得到嵌有盐酸阿霉素分子的导电聚合膜电极. 经电化学方法洗脱, 除去镶嵌在导电聚合膜内的盐酸阿霉素模板, 制得分子印迹聚合膜传感器, 其示意图见Scheme1.

Scheme 1 Schematic diagram for the preparation of the MIP electrode
在相同条件下不加模板分子制备了非印迹膜传感器. 将制得的传感器保存于4 ℃冰箱中, 备用.
1.2.2电化学测试以铁氰化钾为电化学探针对盐酸阿霉素进行差分脉冲伏安法(DPV)检测, 检测电位窗口为1.2~1.8V, 电位增量为4mV, 脉冲振幅为50mV, 脉冲宽度为50mV. 测试底液为含0.1mol/LKCl和5mmol/LK3[Fe(CN)6]的磷酸缓冲溶液(pH=7.23).
2结果与讨论
2.1电化学制备分子印迹聚合膜
为模拟血液的pH环境[21], 将基底电极置于含4.0mmol/L3,4-乙烯二氧噻吩的PBS溶液(pH=7.23)中, 在-0.2~1.5V聚合电位内以50mV/s的速率扫描聚合10圈, 得到导电聚合膜电极PEDOT/AuNPs-CS/Au/CME. 图2(A)为EDOT在基底金电极上电聚合过程的循环伏安(CV)曲线,
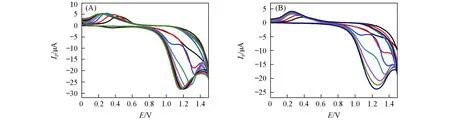
Fig.2 CV curves for the electrochemical polymerization of EDOT in the absence(A) and presence(B) of DOX in PBSScan rate: 50 mV/s; cycling number: (A) 10; (B) 7.
可见EDOT的电聚合为不可逆过程. 电流响应随扫描圈数的增多逐渐增大, 表明电极表面已逐渐形成一层致密导电聚合膜. 图2(B)为加入模板分子DOX后的EDOT电聚合曲线, 与图2(A)相比并无显著差异, 表明DOX的存在不干扰EDOT的电聚合.
2.2印迹膜的表征
2.2.1循环伏安法表征以5mmol/LK3[Fe(CN)6]溶液为电化学探针, 采用循环伏安法对制备的分子印迹膜传感器进行了表征, 结果如图3(A)所示. 在基底金电极上观察到1对明显的氧化还原峰. 在电极表面电聚合3,4-乙烯二氧噻吩后, 电流响应明显增大[图3(A)曲线b]. 当CS-AuNPs复合材料修饰到电极表面后, 电流响应进一步提高[图3(A)曲线c]. 而当电极表面形成MIPs薄膜后, 电流响应迅速下降[图3(A)曲线d]. 这可能是由于K3[Fe(CN)6]无法穿过聚合物层到达电极表面所致, 但由于功能单体PEDOT是一种导电聚合物, 故此时的电流响应仍比裸电极大. 洗脱模板后,K3[Fe(CN)6]的氧化还原峰电流又呈现增加趋势[图3(A)曲线e], 表明模板洗脱后形成的识别位点可促进电子传输, 使K3[Fe(CN)6]更容易通过孔穴到达电极表面.
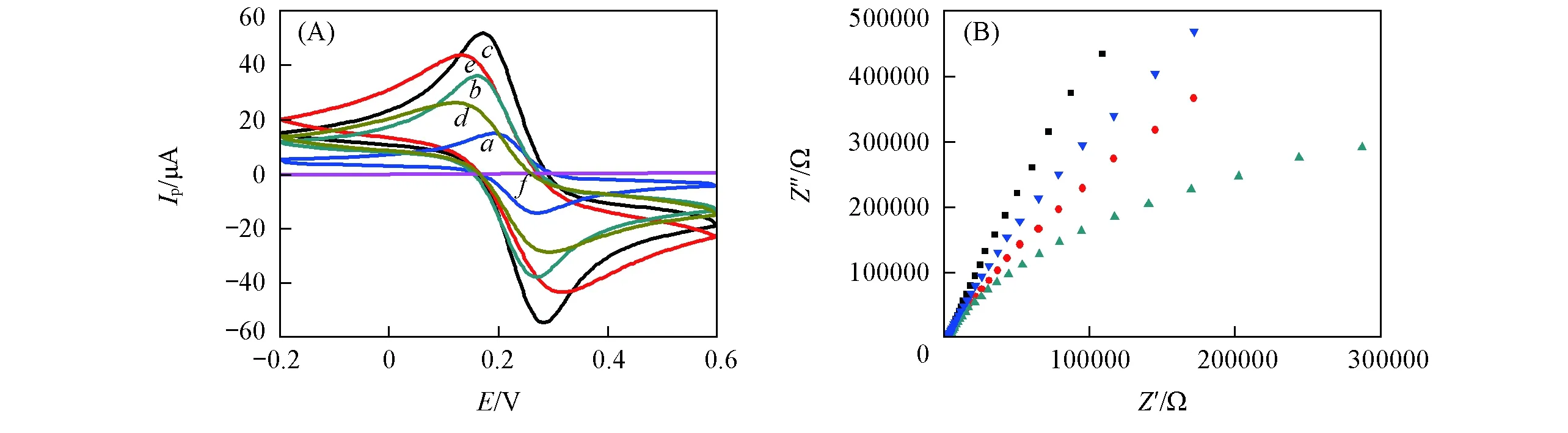
Fig.3 CV curves of the electrodes in 0.1 mol/L KCl containing 5 mmol/L K3[Fe(CN)6](A) and electrochemical impedance spectroscopy of the electrodes(B) (A) a. Au/CME; b. PEDOT/Au/CME; c. AuNPs-CS/PEDOT/Au/CME; d. DOX-MIPs/AuNPs-CS/PEDOT/Au/CME; e. MIPs/AuNPs-CS/PEDOT/Au/CME; f. NMIPs/AuNPs-CS/PEDOT/Au/CME. (B) ■ Au/CME; ▼ DOX-MIPs/AuNPs-CS/PEDOT/Au/CME; ● PEDOT/Au/CME; ▲ AuNPs-CS/PEDOT/Au/CME.
2.2.2交流阻抗法表征由电化学阻抗谱(EIS)[图3(B)]可见, 裸金电极的Nyquist图基本呈线性, 表明裸电极表面不存在阻挡电子传输的物质, 铁氰根离子迅速到达电极表面发生电子传递反应. 电聚合PEDOT后, 半圆的直径明显下降, 表明PEDOT层可促进[Fe(CN)6]3-/4-的电子转移. 当CS-AuNPs修饰到电极表面后, 半圆直径进一步下降, 表明CS-AuNPs纳米复合物能提高电导率. 然而, 当MIPs修饰到电极表面后, 电阻明显增大, 表明电极上形成了印迹膜, 并进一步抑制了氧化还原探针到达电极表面. 以上结果与循环伏安法所得结果一致.
综上所述, 循环伏安实验和阻抗谱实验均证实了盐酸阿霉素在聚合膜中的印迹效应.

Fig.4 SEM images of MIP-modified electrode(A), eluted electrode(B) and NIP-modified electrode(C)
2.2.3不同电极的SEM表征不同电极的扫描电子显微镜(SEM)照片如图4所示. 由图4(A)可见, 在CS-AuNPs复合膜中较为紧密地排列着由EDOT单体电聚合得到的PEDOT粒子. 洗脱模板分子前的印迹聚合膜呈现质地紧密, 较为均匀的形态. 而在洗脱模板分子后, 印迹聚合膜表面凹凸不平, 呈现出多孔结构, 这可能是模板分子洗脱后在膜中留下了孔穴所致, 使其表面粗糙度增加, 电极表面的吸附面积增大, 有利于提高传感器对模板分子的选择性结合能力. 而洗脱后的非印迹电极表面虽有一层致密薄膜[图4(C)], 却少有印迹孔穴存在, 且非印迹膜上有突出的“颗粒”状亮点出现, 这是由于CS-AuNPs在电极表面被非印迹膜包裹所致.
由Randles-Sevcik方程Ip=2.69×105Acn3/2D1/2v1/2(扩散系数D值取6.3×10-6cm2/s)可得Au/CME,PEDOT/Au/CME和AuNPs-CS/PEDOT/Au/CME的有效表面积A分别为0.1412, 0.3389和0.4857cm2. 这说明基底金电极经CS-AuNPs和PEDOT修饰后有效表面积明显增大, 电化学活性位点增多, 促进了电极表面的电子传递. 这进一步验证了阻抗谱实验和循环伏安实验分析结果.
2.3实验条件的优化
2.3.1聚合电位和扫描圈数的选择选择4.0mmol/L3,4-乙烯二氧噻吩的PBS(pH=7.23)溶液作为聚合底液, 考察了不同聚合电位对聚合过程的影响. 结果表明, 电位范围为-0.2~0.8, -0.2~1.0, -0.2~1.2和-0.2~1.5V时, 3,4-乙烯二氧噻吩均可在电极表面聚合形成导电膜. 但是聚合电位越高, 3,4-乙烯二氧噻吩越有可能在电极上发生氧化反应. 综合考虑, 选择-0.2~1.5V为聚合电位窗口. 聚合膜厚度对传感器的性能有很大影响. 膜过薄, 膜内的印迹点少, 导致检测时的线性范围窄、 灵敏度低; 膜过厚, 物质在膜内的传输速率变慢, 响应时间延长, 影响分析速度, 因此膜的厚度必须适宜. 膜的厚度由电聚合时间即扫描圈数决定[22]. 对于导电聚合, 聚合时间越长, 膜越厚. 由图1(A)可知, 电流响应随着CV扫描圈数的增多呈现增大趋势, 但7圈后,PEDOT的氧化峰电流不再增大, 反而有减小趋势, 这是因为PEDOT膜聚合圈数过多导致膜太厚阻碍了电子转移. 因此, 选择7圈为选择最佳电聚合圈数.
2.3.2模板去除条件的优化盐酸阿霉素分子中含有多个强极性官能团, 模板与单体间的作用位点多, 分子间作用力大, 导致模板深陷在聚合物膜中, 溶剂洗脱困难. 为提高洗脱效率, 采用电化学洗脱法去除模板. 将DOX-PEDOT/AuNPs-CS/Au/CME电极置于0.050mol/LPBS缓冲溶液(pH=7.23) 中, 以50mV/s的扫描速度, 分别在0~1.0, 0~1.2, 0~1.4, 0~1.6, 0~1.8和0~2.0V电位范围内循环扫描10圈, 比较不同电位范围扫描下模板的清除效果. 发现扫描去除效果最佳的电位范围为0~2.0V. 固定扫描电位, 考察了不同扫描圈数对模板去除的影响, 发现扫描4~8 圈后电极于铁氰化钾中的峰电流相同, 考虑到扫描圈数过多会对聚合膜造成破坏, 选择0~2.0V内扫描4圈作为去除模板的最佳条件.
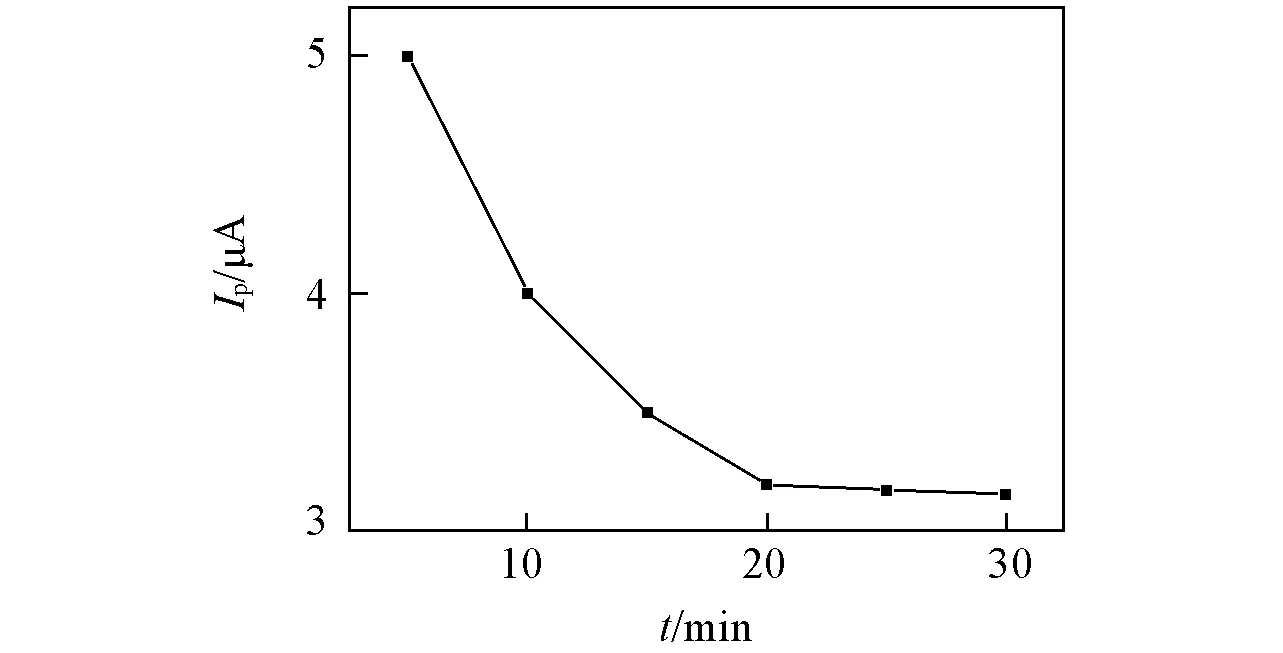
Fig.5 Influence of the adsorption time on the response of the sensor
2.3.3吸附时间对传感器电化学响应的影响考察了盐酸阿霉素在所构建传感器上的吸附时间对K3[Fe(CN)6]峰电流的影响. 将印迹膜电极浸入一定浓度的阿霉素溶液中进行吸附, 每隔5min取出, 在0.005mol/LK3[Fe(CN)6]PBS中用DPV法测定其响应电流的变化(图5). 结果表明, 随着吸附时间的延长,K3[Fe(CN)6]氧化峰电流逐渐下降, 表明印迹位点逐渐被阿霉素分子占据; 当吸附时间达到20min后, 峰电流出现平台, 电流不再下降, 说明盐酸阿霉素与印迹膜传感器的物质交换达到平衡状态, 膜中盐酸阿霉素已达到饱和. 因此, 最佳吸附时间为20min. 根据Laviron公式IP=
n2F2ΓAv/4RT=QnFv/4RT计算得到DOX印迹敏感膜对DOX的吸附容量Γ=1.1368×10-9mol/cm2[式中: Γ(mol/cm2)为DOX印迹敏感膜在电极表面的覆盖度; Ip(A)为背景电流; n为电子转移数; F(96500C/mol)为法拉第常数; A(cm2)为电极表面积; Q(C)为电荷量; v(V/s)为扫描速率; R(J·K-1·mol-1)为气体常数; T(K)为热力学温度].
2.4印迹膜传感器的响应特性
2.4.1线性范围与检出限在最优实验条件下, 将分子印迹膜传感器放入不同浓度的盐酸阿霉素溶液中吸附20min, 进行DPV测定, 结果如图6所示. 传感器的响应电流ΔIp(测试底液中含有DOX与不含DOX时的峰电流之差)与DOX浓度c在4.0×10-7~1.0×10-6mol/L范围内呈现良好的线性关系, 线性方程为ΔIp=-4.0424-1.0099c(R2=0.9967), 最低检出浓度为2.0×10-7mol/L, 检出限为6.5×10-8mol/L(3σ).
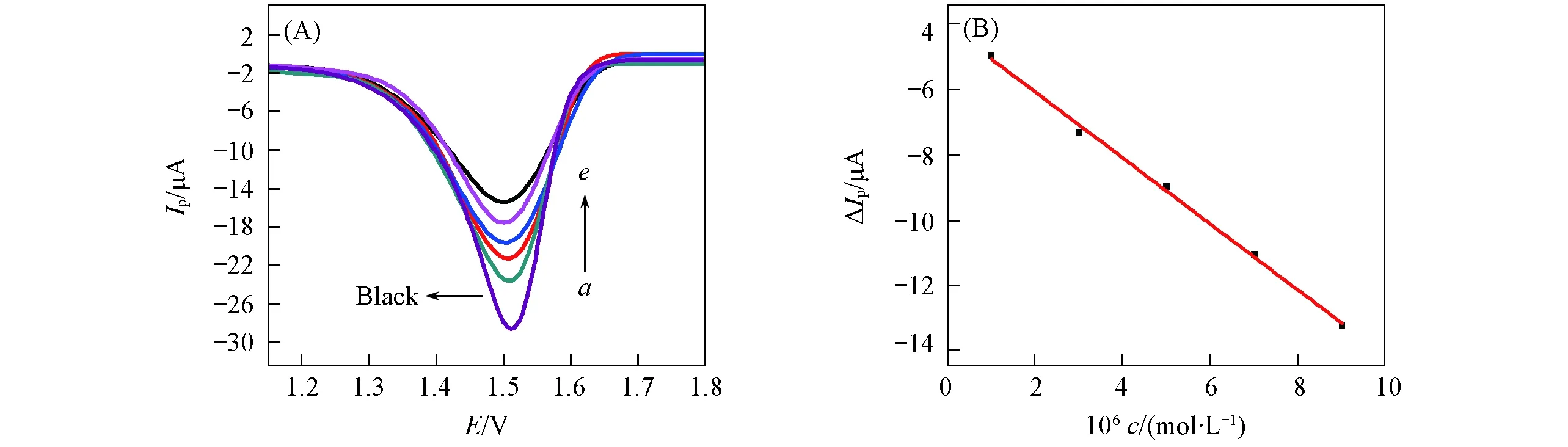
Fig.6 DPV curves of MIP/AuNPs-CS/PEDOT/Au/CME after adsorption in different concentrations of DOX(A) and linear relationship of current peak difference vs. DOX concentration on MIP/AuNPs-CS/PEDOT/Au/CME(B)
表1列出了不同方法检测DOX的结果. 与其它方法相比, 本传感器具有更低的线性范围和检出限, 适用于快速检测低浓度水平的盐酸阿霉素.
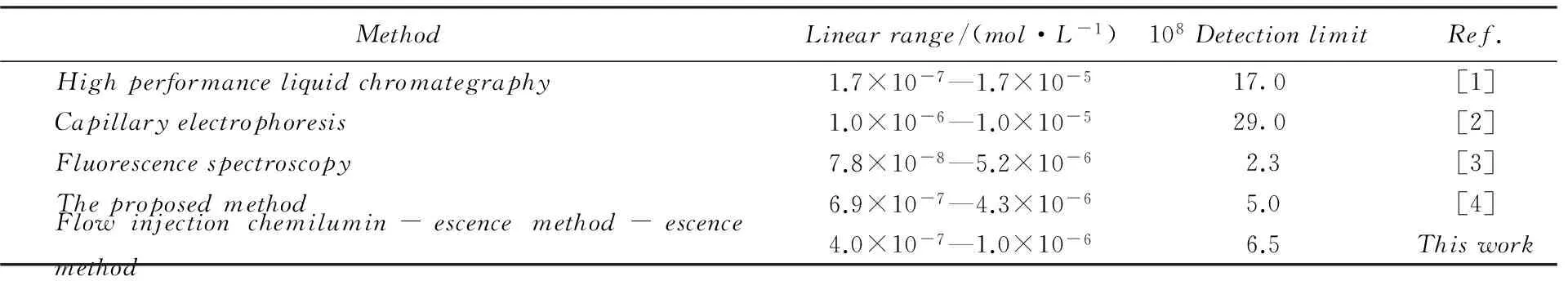
Table 1 Comparison of detection results of DOX by this method and literature methods
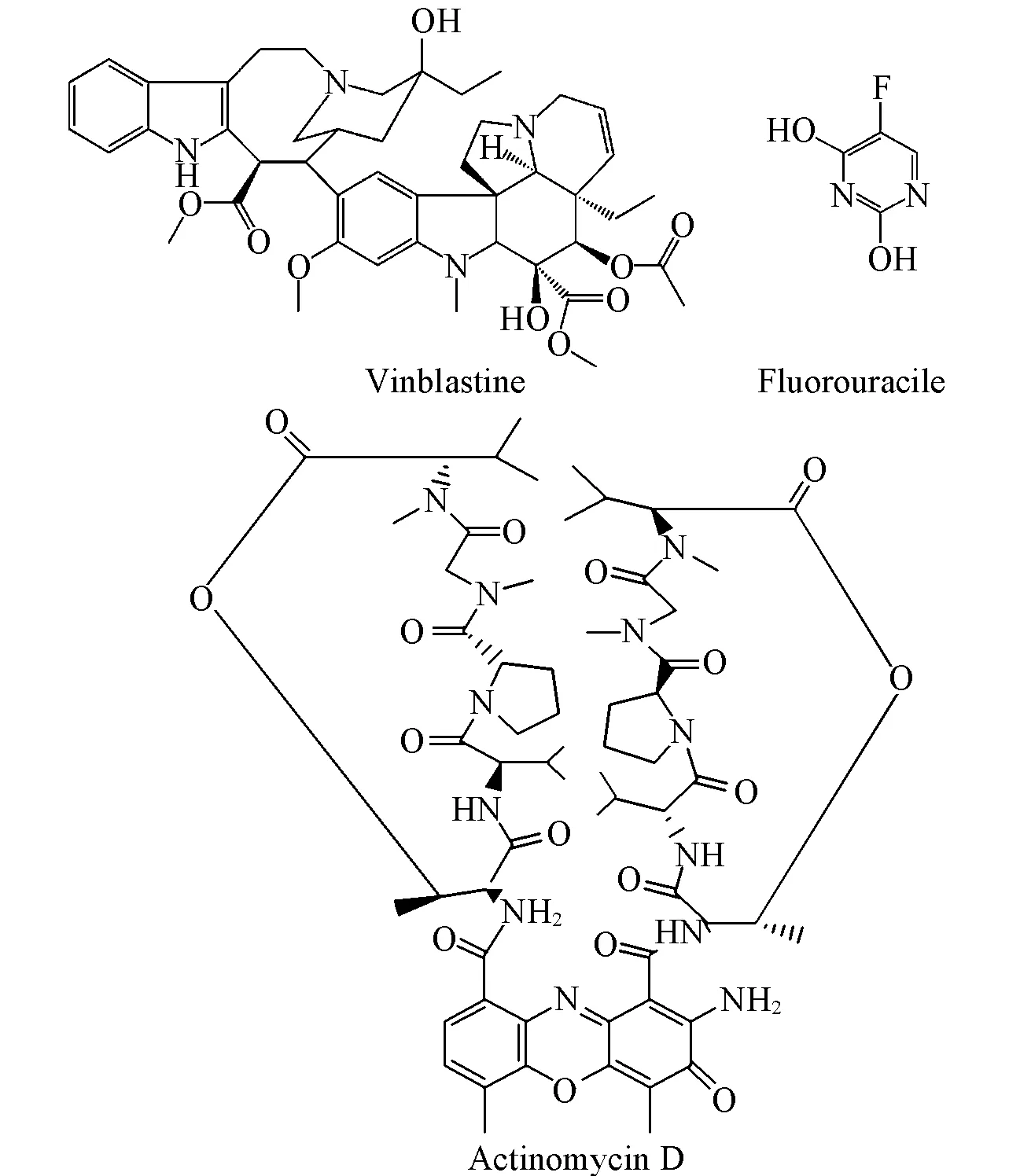
Fig.7 Structures of substance used in interference experiments
2.4.2印迹膜传感器的选择性为验证印迹传感器的选择性, 选用可能会对血样中DOX的测定产生影响的长春碱、 5-氟尿嘧啶及放线菌素D(结构式见图7)进行了干扰实验.
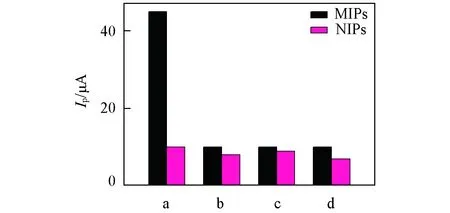
Fig.8 Current response of different substances on MIP sensor and NIP sensor a. DOX; b. VLB; c. 5FU; d. ACD.
将浓度均为2×10-6mol/L的各干扰物质分别加入到铁氰化钾溶液中, 在相同条件下测定印迹传感器和非印迹传感器对盐酸阿霉素和各干扰物质所产生的电流响应, 结果如图8所示. 可见, 传感器对以上干扰物质的电流响应很小, 表明干扰物质无法结合到分子印迹膜传感器上. 对于非印迹传感器, 无论是盐酸阿霉素还是干扰物质, 电流响应均很小, 这是由于在非印迹传感器中没有盐酸阿霉素的印迹结合位点所致. 此结果证实基于分子印迹聚合物的传感器对于盐酸阿霉素有良好的选择性.
由于实验测定选择的是血清样品, 因此对血清中存在的一些离子也进行了干扰实验. 在2×10-6mol/L盐酸阿霉素溶液中加入0.1mol/LNa+, 0.5mmol/LCa2+, 0.5mmol/LMg2+, 0.5mmol/LZn2+和0.5mmol/LK+作为竞争底物进行测定, 结果表明峰电流值在±0.19μA范围内变化, 说明这些常见离子对测定的干扰很小, 表明该分子印迹电化学传感器在实际的应用中有较好的选择识别性.
2.5印迹膜传感器的重现性和稳定性
在最优实验条件下, 用同一传感器对2×10-6mol/L盐酸阿霉素溶液平行测定5次, 其相对标准偏差为1.20%; 电极不使用时, 保存于4 ℃冰箱内放置过夜, 在相同条件下测定2×10-6mol/L盐酸阿霉素溶液, 电流响应几乎接近于初始值; 存放一个月后, 响应电流降为初始值的81.54%, 表明印迹传感器具有良好的重现性及稳定性.
2.6实际样品检测
将血浆在室温下放置1h, 待凝结出血饼后将其移除, 以3000r/min转速离心15min; 取上层清液振荡至均匀, 以15000r/min转速离心15min, 取上层清液, 重复操作2次. 将经过前处理的样品储存于冰箱中备用. 取5.0mL血清样品, 采用标准加入法加入一定量的盐酸阿霉素标准溶液制成储备液. 在最优实验条件下, 考察DOX在1, 3, 5和7μmol/L4个加标浓度下的回收率及相对标准偏差, 每个样品平行测定3次. 由表2可见, 该方法的回收率为96.0%~106.7%, 相对标准偏差为0.86%~1.66%.

Table 2 Determination result of DOX in blood serum samples
采用差分脉冲伏安法以血清样品为背景对该传感器的性能进行了测试. 在最优实验条件下, 将印迹膜传感器置于含0, 1, 3, 5, 7和9μmol/L盐酸阿霉素溶液中, 进行DPV测定. 结果表明, 在4.0×10-7~1.0×10-6mol/L范围内, 峰电流差值ΔI与血清样品中的DOX浓度c呈良好的线性关系. 线性方程为ΔIp=-2.8006-0.9905c(R2=0.9952). 传感器的检出限为8.6×10-8mol/L(S/N=3), 略高于在标准溶液中所得值, 这是由于实际应用中血清背景在某一程度上存在干扰.
3结论
通过电聚合方法在金电极上构建了盐酸阿霉素分子印迹电化学传感器, 用于盐酸阿霉素的检测.CS-AuNPs/PEDOT复合材料能显著增强电化学响应. 电化学表征结果证实,MIPs膜能选择性地重结合模板分子, 且构建的传感器对DOX的选择性明显优于其它结构类似的抗癌药物. 优化传感器参数后, 该传感器可初步用于人体血样中DOX的检测, 所构建的传感器制作简单, 分析性能良好.
参考文献
[1]ChenJ.H.,XiaP.Y.,WangZ.Y.,WuN.,DaiQ.,SunF.J.,YangB.,XiangR.F., Chinese Journal of Hospital Pharmacy, 2010, 30(5), 353—356(陈剑鸿, 夏培元, 王章阳, 吴南, 戴青, 孙凤军, 杨波, 向荣凤. 中国医院药学杂志, 2010, 30(5), 353—356)
[2]PengH.D.,SunY.,MoM.F.,YangD.H.,LiH.X., Journal of Guangdong PharmaCeutical University, 2011, 27(6), 587—590(彭怀东, 孙悦, 莫满芳, 杨端辉, 李海秀. 广东药学院学报, 2011, 27(6), 587—590)
[3]HuR.,YangQ.,ZhangS.R.,YangJ.D., Chinese Journal of Antibiotics, 2009, 34(7), 411—416(胡蓉, 杨琼, 张书然, 杨季冬. 中国抗生素杂志, 2009, 34(7), 411—416)
[4]GeC.,FuH.,HeY.,YiG., Chinese Journal of Analysis Laboratory, 2013, 32(6), 105—107(葛闯, 付虎, 何云, 易钢. 分析试验室, 2013, 32(6), 105—107)
[5]SuryanarayananV.,WuC.T.,HoK.C., Electroanalysis, 2010, 22(16), 1795—1811
[6]XuW.,LiX.,ZhangW.Y.,YingX.G., Chem. J. Chinese Universities, 2012, 33(10), 2199—2204(徐雯, 李晓, 张卫英, 英晓光. 高等学校化学学报, 2012, 33(10), 2199—2204)
[7]MalitestaC.,MazzottaE.,PiccaR.A.,PomaA.,ChianellaI.,PiletskyS.A., Anal. Bioanal. Chem., 2012, 402(5), 1827—1846
[8]ZhangJ.,WangC.Y.,LiX.P.,NiuY.H., Chem. J. Chinese Universities, 2013, 34(10), 2296—2302(张进, 王超英, 李小平, 牛延慧. 高等学校化学学报, 2013, 34(10), 2296—2302)
[9]SpivakD.A.,SheaK.J., J. Mol. Recognit., 2012, 25(6), 319
[10]VishnuvardhanV.,PrathishK.P.,NaiduG.R.K.,PrasadaR.T., Electrochim. Acta, 2007, 52(24), 6922—6928
[11]LuC.Y.,MaX.X.,HeX.W.,LiW.Y.,ChenL.X.,HeH.C., Chem. J. Chinese Universities, 2005, 26(7), 1356—1359(卢春阳, 马向霞, 何锡文, 李文友, 陈朗星, 何海成. 高等学校化学学报, 2005, 26(7), 1356—1359)
[12]TangK.J.,GuX.H.,ZhuS.,TangJ.,WangH.J., Acta Chim. Sinica, 2009, 67(7), 687—692(唐凯洁, 顾小红, 朱松, 汤坚, 王海军. 化学学报, 2009, 67(7), 687—692)
[13]NiuJ.,LiuZ.H.,FuL.,ShiF.,MaH.W.,OzakiY.,ZhangX., Langmuir, 2008, 24(20), 11988—11994
[14]ZhangN.W.,DingM.X.,LiuG.Y.,SongW.W.,ChaiC.Y., Acta Chim. Sinica, 2008, 66(7), 1961—1966(张挪威, 丁明星, 刘国艳, 宋巍巍, 柴春彦. 化学学报, 2008, 66(7), 1961—1966)
[15]ChengZ.L.,WangE.,YangX.R., Biosens. Bioelectron, 2001, 16(3), 179—185
[16]WeetallH.H.,RogersK.R., Talanta, 2004, 62(2), 329—4107
[17]LiaoH.P.,ZhangZ.H.,LiH., Electrochim. Acta, 2004, 49, 4101
[18]HoK.C.,YehW.M.,TungT.S.,LiaoJ.Y., Anal. Chim. Acta, 2005, 542, 90—96
[19]YangZ.J.,LiuS.H.,YeJ.N.,FangY.Z., Chin. J. Anal. Chem., 1996, 24(4), 471—474(杨志洁, 刘盛辉, 叶建农, 方禹之. 分析化学, 1996, 24(4), 471—474)
[20]MarkS.,Michael.J.,DebraE.W., Sens. Actuators B: Chemical, 2015, 221, 1003—1008
[21]SongJ.L., Bulletin of Biology, 2002, 37(11), 47—49
[22]XieC.G.,GaoS.,GuoQ.B., Microchim. Acta, 2010, 169(1/2), 145—152
(Ed.:D,K)
†SupportedbytheNaturalScienceFoundationofShanxiProvince,China(No.20001057).
doi:10.7503/cjcu20150938
收稿日期:2015-12-17. 网络出版日期: 2016-04-12.
基金项目:山西省自然科学基金(批准号: 20001057)资助.
中图分类号O657.1
文献标志码A
PreparationandPropertiesofDoxorubicinHydrochlorideSensorBasedonMolecularlyImprintedPolymer†
ZHANGYan,ZHENGJing,WANGJuan,GUOMandong*
(College of Chemistry and Material Science, Shanxi Normal University, Linfen 041004, China)
AbstractAn electrochemical sensor was developed for the determination of doxorubicin hydrochloride(DOX) using the molecularly imprinted technique. A molecular imprinted polymer(MIP) on the surface of a gold electrode was prepared by electropolymerization of 3,4-ethylenedioxythiop-hene(EDOT) in the presence of DOX in the phosphate buffer solution. Under the optimum conditions, the properties of the electrochemical sensor modified with DOX-imprinted membrane were characterized by cyclic voltammetry, differential pulse voltammetry and electrochemical impedance spectroscopy. A linear relationship between oxidation peak current and DOX concentration was obtained over the range of 4.0×10-7—1.0×10-6mol/L with a correlation coefficient of 0.9967 and a detection limit(S/N=3) of 6.5×10-8mol/L. After regeneration by washing with electrochemical method, the sensor showed excellent reproducibility and good stability. The MIP electrode exhibited very weak response to vinblastine, actinomycin D and fluorouracile, proving a good selectivity. The imprinted sensor was applied to the determination of doxorubicin hydrochloride in human blood serum samples with the relative standard deviation(RSD) below 4% and recovery ranging from 96.0% to 106.7%.
KeywordsMolecularly imprinted polymer; Electrochemical sensor; 3,4-Ethylene dioxythiophene; Doxorubicin hydrochloride
联系人简介: 郭满栋, 男, 教授, 主要从事生物传感器与电分析化学研究.E-mail:guomd@dns.sxnu.edu.cn

