离子液体1-烷基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐的合成及在油品中的脱硫应用
刘治庆, 薛 飞, 雷振凯, 刘晨江
(石油天然气精细化工教育部 & 自治区重点实验室, 乌鲁木齐绿色催化与合成技术重点实验室,新疆大学理化测试中心, 乌鲁木齐 830046)
离子液体1-烷基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐的合成及在油品中的脱硫应用
刘治庆, 薛飞, 雷振凯, 刘晨江
(石油天然气精细化工教育部 & 自治区重点实验室, 乌鲁木齐绿色催化与合成技术重点实验室,新疆大学理化测试中心, 乌鲁木齐 830046)
摘要合成并表征了一类新型离子液体1-烷基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐, 将其与双氧水组合用于脱除模型油中的硫化物. 结果表明, 当模型油与萃取/催化剂1-辛基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐([C2O2OBIM][Tf2N])的质量比为5∶1, H2O2/S摩尔比为5∶1, 于75 ℃反应1 h后, 模型油中二苯并噻吩(DBT)脱硫率为98.8%; 脱硫过程符合一级动力学方程, 5种硫化物的脱硫速率大小顺序为二苯并噻吩(DBT)> 4,6-二甲基二苯并噻吩(4,6-DMDBT)> 苯并噻吩(BT)> 2,5-二甲基噻吩(2,5-DMT)> 噻吩(T), 其中脱除DBT和BT的反应表观活化能分别为44.16和52.10 kJ/mol. 该离子液体循环再生使用14次, 脱硫率无明显下降. 该深度脱硫方法具有操作简便及条件温和的特点.
关键词苯并咪唑; 离子液体; 萃取-氧化脱硫; 动力学
E-mail:pxylcj@126.com
燃料油中含有的有机硫化物燃烧后生成的SOx和颗粒物可引起酸雨和空气污染[1,2]. 加氢脱硫是一种被广泛应用于燃油脱硫的技术[3,4], 可以有效脱除硫醇、 硫醚和二硫醚等硫化物, 然而其缺点是消耗大量的氢气、 需要昂贵的催化剂以及高温和高压等苛刻条件[5~7], 且难以脱除二苯并噻吩衍生物[8,9]. 近年来, 生物脱硫[10,11]、 萃取脱硫[12~14]、 吸附脱硫[6,15,16]及氧化脱硫[17,18]等脱硫方法得到了发展. 其中离子液体作为浓缩的绿色化学符号应用于油品的深度脱硫已成为近年来的研究热点之一[19,20].
本文在前期工作[21]的基础上, 合成了一类新型离子液体1-烷基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐(合成路线见Scheme1), 并与H2O2组成催化氧化体系, 探讨了该体系对模拟油品中含硫化合物的脱除效果.

1a, 2a: R=C2H5; 1b, 2b: R=C4H9; 1c, 2c: R=C5H11; 1d, 2d: R=C8H17Scheme 1 Synthetic routes of the carboxyl functionalized ionic liquids
1实验部分
1.1试剂与仪器
4,6-二甲基二苯并噻吩(4,6-DMDBT)、 二苯并噻吩(DBT)、 苯并噻吩(BT)和噻吩(T)均购自北京百灵威科技有限公司; 2,5-二甲基噻吩(2,5-DMT)购自天津阿法埃莎化学有限公司; 双三氟甲磺酰亚胺锂购自上海泰坦科技有限公司; 正辛烷和一氯乙酸购自天津市福晨化学试剂厂; 以上试剂均为分析纯.
VarianInova-400型超导核磁共振波谱仪(400MHz,TMS, 美国Varian有限公司);BrukerEquinox55型红外光谱仪(KBr压片, 德国Bruker公司);HP1100型液相色谱-质谱仪(美国Agilent公司);BüchiB-560型熔点仪(瑞士Büchi公司);TSN-2000A型硫氮分析仪(江苏江分电分析仪器有限公司).
1.21-烷基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐酸性离子液体(2a~2d)的合成
以离子液体2a的合成为例. 将1-乙基苯并咪唑(16.42g, 0.1mol)和一氯乙酸(9.45g, 0.12mol)置于100mL圆底烧瓶内, 缓慢升高温度至90 ℃并反应48h, 冷却至室温, 用混合溶剂[V(乙醚)∶V(乙腈)=2∶1]浸泡、 洗涤和抽滤, 滤饼于真空干燥至恒重, 即得1-乙基-3-羧甲基苯并咪唑氯盐[C2O2EBIM][Cl](1a, 白色固体,m.p. 210~212 ℃). 采用相同方法制得1-丁基苯并咪唑氯盐[C2O2BBIM][Cl](1b, 白色固体,m.p. 176~177 ℃)、 1-戊基苯并咪唑氯盐[C2O2PBIM][Cl](1c, 白色固体,m.p. 150~152 ℃)和1-辛基-3-羧甲基苯并咪唑氯盐[C2O2OBIM][Cl](1d, 白色固体,m.p. 136~137 ℃). 将化合物1a(2.05g, 0.01mol)溶于蒸馏水中, 加入双三氟甲磺酰亚胺锂(3.45g, 0.012mol), 搅拌下加热回流12h停止反应, 下层溶液用蒸馏水洗涤至加入硝酸银溶液无沉淀生成为止, 减压旋蒸除去反应体系中的水分, 真空干燥至恒重, 即得1-乙基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐离子液体[C2O2EBIM][Tf2N](2a). 同法制得1-丁基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐离子液体[C2O2BBIM][Tf2N](2b)、 1-戊基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐离子液体[C2O2PBIM][Tf2N](2c)和1-辛基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐离子液体[C2O2OBIM]5[Tf2N](2d). 离子液体2a~2d的物质状态、 熔点、 质谱和红外数据见表1. 核磁共振数据见表2.
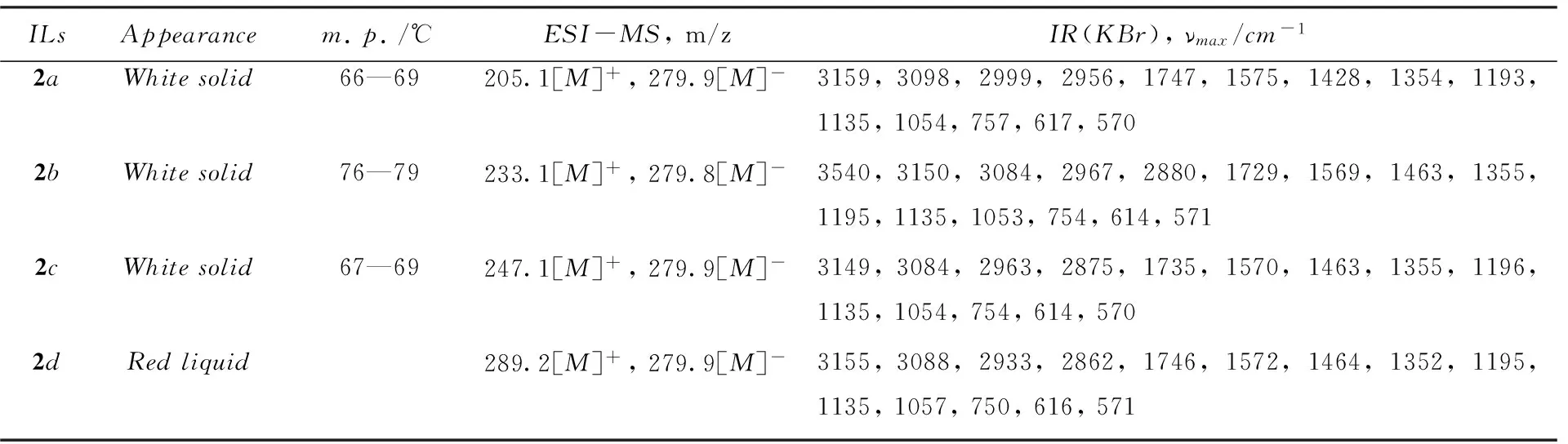
Table 1 Appearance, melting points ESI-MS and IR data of ionic liquids 2a—2d

Table 2 1H NMR and 13C NMR data of ionic liquids 2a—2d
1.3模型油的制备
将0.8705g4,6-DMDBT(质量分数97%), 1.0761gDBT(质量分数98%), 0.7368gBT(质量分数98%), 0.6284g2,5-DMT(质量分数98%)和0.3976gT(质量分数98%)分别定溶至500mL正辛烷中, 配成硫含量分别为255, 367, 345, 352和297mg/L的模型油.
分别称取上述5种不同浓度的模型油(各3.0g)混合成硫化物模型油, 其总硫含量为278mg/L.
1.4脱硫实验
向圆底烧瓶内依次加入一定质量的上述模型油、 离子液体和30%(质量分数)的H2O2, 在一定的温度下以500r/min的转速搅拌反应, 待反应完毕, 静置、 分层, 取少量油相中的油样, 用硫氮测定仪测定硫含量, 计算脱硫率. 分离后的离子液体相经旋转蒸发除去水分, 于真空下干燥至恒重后待下次循环使用.
2结果与讨论
2.1不同离子液体脱硫体系对模型油的萃取-氧化脱硫效果
不同离子液体脱硫体系对模型油中DBT的萃取-氧化脱硫效果如表3所示. 结果表明, 模型油中硫化物的脱除效果与离子液体阳离子的烷基链长度密切相关, 当阳离子烷基链增长时, 萃取脱硫率也增大, 其原因可能随着烷基链的增长, 离子液体的熔点逐渐降低(乙基除外), 导致离子液体的流动性增加, 更易于萃取硫化物. 在不加入任何氧化剂的情况下, 离子液体[C2O2OBIM][Tf2N]的萃取脱硫率仅为22.1%; 当离子液体[C2O2OBIM][Tf2N]与H2O2共同应用于模拟油脱硫时, 脱硫率可达98.8%, 这可能是由于该离子液体发挥了萃取剂和催化剂的双重作用所致. 此外, [C2O2OBIM][Tf2N]对混合模型油的单次脱硫率达到82.5%, 表明此类离子液体对含不同芳香硫化物的模型油也具有很好的选择性.
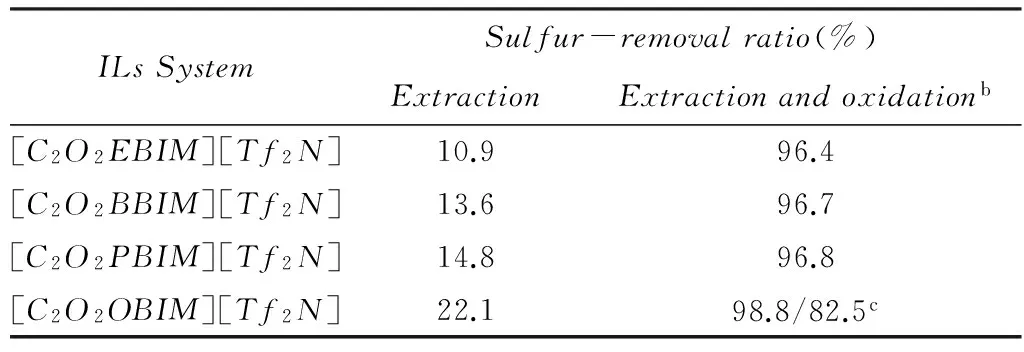
Table 3 Effect of different desulfurization systemson DBT removala
a.Experimentalconditions:temperature=75 ℃, t=1h, m(Modeloil)∶m(Ionicliquid)=5∶1, n(H2O2)∶n(DBT)=5∶1,DBT(S: 367mg/L)inn-octane; b.addingacertainamountofH2O2(massfraction30%); c.mixedsulfide[c(S) = 278mg/L].
2.2氧化剂用量对脱硫效果的影响
氧化剂用量对脱硫效果的影响如图1所示. 可见, 当H2O2用量增加时,DBT的脱除率增大. 随着H2O2/DBT摩尔比由1∶l增加到5∶1, 脱除率从58.6%升高到98.8%; 继续增加摩尔比至6∶1时, 脱硫率几乎不变. 因此, 最佳H2O2/DBT摩尔比为5∶1.

Fig.1 Effect of molar ratios of H2O2/DBT on DBT removal Experimental conditions: temperature=75 ℃, t=1 h, m(Model oil)∶m([C2O2OBIM][Tf2N])=5∶1, DBT(S: 367 mg/L) in n-octane.
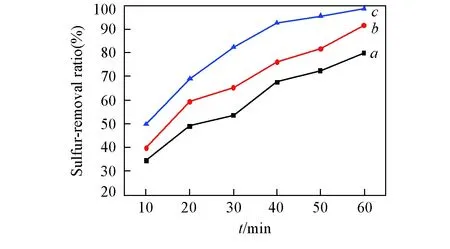
Fig.2 Effects of reaction temperatures and time on DBT removal Experimental conditions: m(Model oil)∶m([C2O2OBIM]5[Tf2N])=5∶1, n(H2O2)∶n(DBT)=5∶1, DBT(S: 367 mg/L) in n-octane. Temperature/℃: a. 55, b. 65, c. 75.
2.3反应温度和反应时间对脱硫效果的影响
在55, 65和75 ℃下, 反应时间对脱硫率的影响如图2所示. 可见, 随着反应温度的升高, 脱硫率明显增大. 这是因为温度升高时, 离子液体黏度下降, 流动性增强, 有利于增强离子液体对DBT的萃取效果; 当温度达到75 ℃时, 离子液体流动性改善已经不明显, 此时的脱硫率为98.8%, 因此将75 ℃定为最佳反应温度. 在75 ℃时, 延长反应时间后, 脱硫率增大, 反应60min的脱硫率达到98.8%. 因此, 确定60min为最佳反应时间.
2.4不同油剂质量比对脱硫效果的影响
由离子液体用量对脱硫效果的影响(图3)可见, 随着油剂(模型油/离子液体)质量比的减小, 脱硫率相应增大, 这是由于H2O2将离子液体中羧酸根氧化为过氧酸根的数量越多, 越有利于DBT的氧化. 当油剂质量比下降到3∶1时, 脱硫率几乎不变, 考虑到经济性因素, 选择最佳油剂质量比为5∶1.

Fig.3 Effect of mass ratio of model oil/ionic liquid on DBT removal Experimental conditions: temperature=75 ℃, t=1 h, n(H2O2)∶n(DBT)=5∶1, DBT(S: 367 mg/L) in n-octane, IL=[C2O2OBIM][Tf2N].
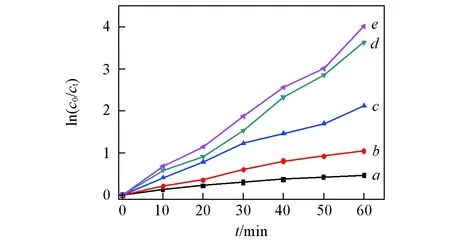
Fig.4 Oxidation of different sulfur-containing compounds Experimental conditions: temperature=75 ℃, m(Model oil)∶m([C2O2OBIM][Tf2N])=5∶1, n(H2O2)∶n(DBT)=5∶1. a. T; b. 2.5-DMT; c. BT; d. 4,6-DMDBT; e. DBT.
2.5不同硫化物对脱硫效果的影响
分别考察了离子液体[C2O2OBIM][Tf2N]对含有DBT, 4,6-DMDBT,BT, 2,5-DMT和T的模型油
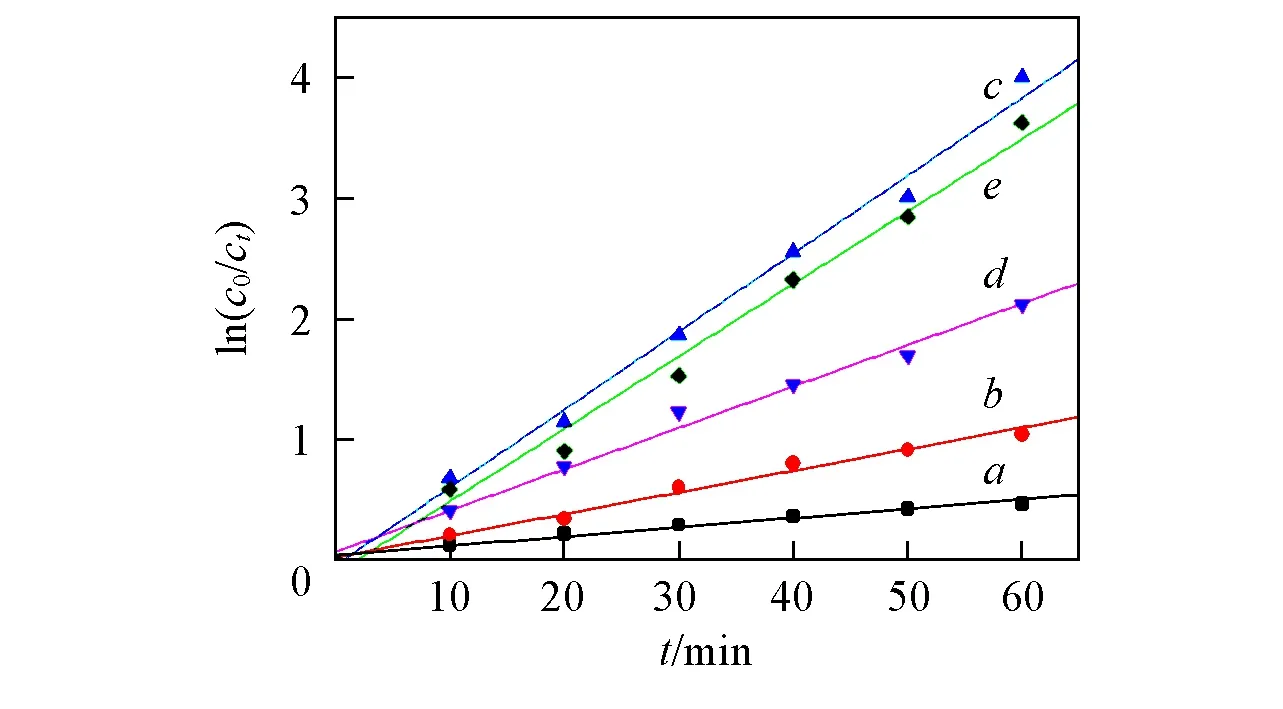
Fig.5 Pseudo-first-order kinetics for oxidation of different substratesa. T; b. 2,5-DMT; c. DBT; d. BT; e. 4,6-DMDBT.
的脱硫效果. 在最优实验条件下, 5种不同硫化物模型油的硫浓度随反应时间的变化关系曲线[ln(c0/ct)~t]如图4所示. 通过曲线拟合得到的各种硫化物的速率方程基本是一条直线[如图5(A)~(E)所示], 可以判定脱硫反应为一级动力学反应. 速率方程为ln(c0/ct)=k1t+B(其中: c0为反应物的初始浓度; ct为t时刻反应物浓度; B为常数), 斜率k1即为不同硫化物模型油的脱硫速率, 半衰期t1/2=ln2/k1, 得到的5种不同硫化物模型油脱硫反应的动力学参数k1和t1/2如表4所示.
实验结果表明, 5种模型油的脱硫速率不同, k1越大, 脱硫速率越大, 效率越高, 5种硫化物脱除速率大小顺序为DBT>4,6-DMDBT>BT>2,5-DMT>T. 这可能是由于不同硫化物中硫原子的电子云密度存在差异, 电子云密度越高, 氧化反应活性越高, 4,6-DMDBT,DBT,BT, 2,5-DMT和T的硫原子电子云密度分别为5.760, 5.758, 5.739, 5.716和5.696[22], 大小顺序为4,6-DMDBT>DBT>BT>2,5-DMT>T; 实际脱硫效果为DBT>4,6-DMDBT, 这可能是由于4,6-DMDBT中4位和6位上甲基的空间位阻效应致使DBT的脱硫率大于4,6-DMDBT. 因此, 噻吩类硫化物中硫原子的电子云密度和空间位阻效应会共同影响氧化脱硫反应的脱硫效果.
Table4First-orderdesulphurizationrateandhalf-livesofdifferentsubstrates

SubstrateDBT4,6-DMDBTBT2,5-DMTTk1/min-10.0650.0600.0340.0190.009t1/2/min10.6611.5520.3936.4877.02
2.6不同硫化物的阿伦尼乌斯(Arrhenius)活化能计算
阿伦尼乌斯公式为lnk =lnA-Ea/RT[其中: k为速率常数; R为摩尔气体常数; T为热力学温度; Ea为活化能; A为指前因子(也称频率因子)]. 由实验数据作lnk~1/T图为一直线, 由斜率可得表观活化能Ea, 由截距可得指前因子A. 如果温度变化不大, Ea可视为常数, 将微分式作定积分可得到不同温度下反应速率常数与其对应温度之间的关系.

Table 5 First-order rate constant(k) of DBT and BT*
* k:First-orderrateconstant.
实验得出含有DBT和BT的2种模型油分别在55, 65和75 ℃下的k值如表5所示. 对2种硫化物作-lnk~1/T关系图, 可得到活化能曲线, 如图6所示, 符合一级动力学方程, 得到Ea(DBT)=44.16kJ/mol, Ea(BT)=52.10kJ/mol. 表观活化能越小, 反应速率越大, 因此DBT的脱除速率大于BT, 这与图5结果一致.
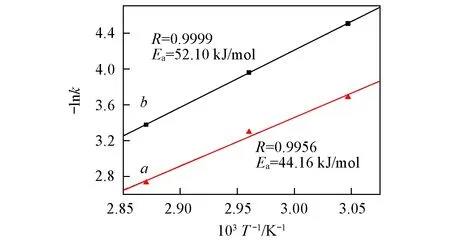
Fig.6 Apparent activation energy of removal of DBT(a) and BT(b)
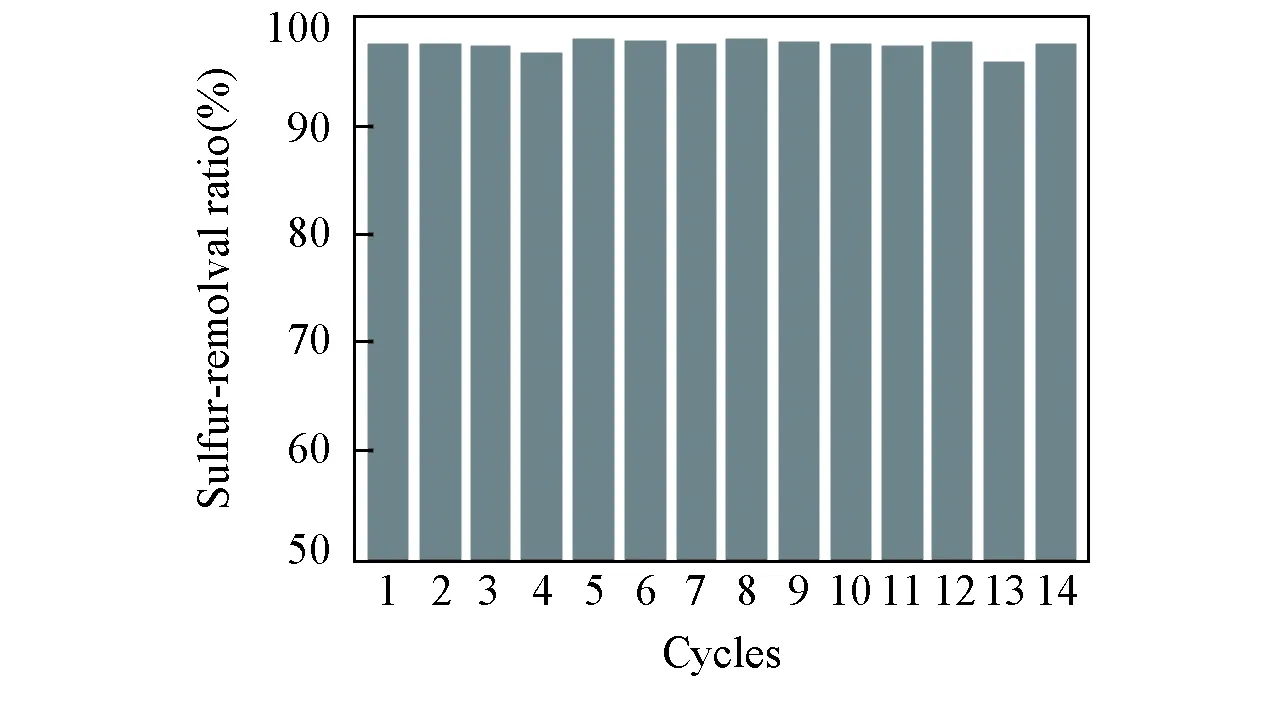
Fig.7 Recycling of IL on removal of DBT in model oilExperimental conditions: temperature=75 ℃, t=1 h, m(Model oil)∶m([C2O2OBIM][Tf2N])=5∶1, n(H2O2)∶n(DBT)=5∶1.
2.7离子液体的循环使用性
分离后的离子液体经减压蒸馏除水, 再经真空干燥至恒重后, 可用于新的模型油脱硫循环实验. 该离子液体循环使用次数对脱硫率的影响如图7所示. 结果表明, 离子液体[C2O2OBIM][Tf2N]循环14次后脱硫活性无明显变化, 脱硫率仍然为97.5%.
综上所述, 在模拟油的萃取催化氧化脱硫反应中, 离子液体1-辛基-3-羧甲基苯并咪唑双三氟甲磺酰亚胺盐[C2O2OBIM][Tf2N]既是很好的萃取剂又是优异的催化剂, 这种脱硫方法简便高效, 脱硫率高, 能达到深度脱硫的目的. 脱硫的最佳条件: 离子液体[C2O2OBIM][Tf2N]为萃取/催化剂, 氧硫摩尔比5∶1, 最佳油剂质量比5∶1, 在75 ℃下反应时间1h. 在此条件下, 起始浓度为367mg/L的二苯并噻吩(DBT)的正辛烷模型油的脱硫率为98.8%, 5种不同硫化物的脱除速率大小为二苯并噻吩>4,6-二苯并噻吩>苯并噻吩>2,5-二甲基噻吩>噻吩, 其中脱除DBT和BT的反应表观活化能分别为44.16和52.10kJ/mol. 离子液体循环再生使用14次后的脱硫率为97.5%, 保持了很好的脱硫活性.
参考文献
[1]ZhangC.,PanX.Y.,WangF.,LiuX.Q., Fuel, 2012, 102, 580—584
[2]ZhangH.X.,GaoJ.J.,MengH.,LiC.X., Ind. Eng. Chem. Res., 2012, 51, 6658—6665
[3]WanM.W.,YenT.F., Appl. Catal. A-Gen., 2007, 319, 237—245
[4]DharaskarS.A.,WasewarK.L.,VarmaM.N.,ShendeD.Z.,YooC.K., Ind. Eng. Chem. Res., 2014, 53, 19845—19854
[5]CarnaroglioD.,GaudinoE.C.,MantegnaS.,MoreiraE.M.,CastroA.V.,FloresE.M.M.,CravottoG., Energy Fuels, 2014, 28, 1854—1859
[6]SubhanF.,AslamS.,YanZ.F.,IkramM.,RehmanS., Microporous Mesoporous Mater., 2014, 199, 108—116
[7]JiangW.,ZhuW.S.,LiH.P.,WangX.,YinS.,ChangY.H.,LiH.M., Fuel, 2015, 140, 590—596
[8]WangA.J.,RuanL.F.,TengY.,LiX.,LuM.H.,RenJ.,WangY.,HuY.K., J. Catal., 2005, 229, 314—321
[9]YuF.L.,WangY.Y.,LiuC.Y.,XieC.X.,YuS.T., Chem. Eng. J., 2014, 255, 372—376
[10]BhatiaS.,SharmaD.K., Pet. Sci. Technol., 2006, 24, 1125—1159
[11]DinamarcaM.A.,RojasA.,BaezaP.,EspinozaG.,Ibacache-QuirogaC.,OjedaJ., Fuel, 2014, 116, 237—241
[12]KulkarniP.S.,AfonsoC.A.M., Green Chem., 2010, 12, 1139—1149
[13]Rodríguez-CaboB.,ArceA.,SotoA., Fluid Phase Equilib., 2013, 356, 126—135
[14]DharaskarS.A.,WasewarK.L.,VarmaM.N.,ShendeD.Z.,YooC.K., Ind. Eng. Chem. Res., 2014, 53, 19845—19854
[15]WangF.,ZhangZ.Q.,YangJ.,WangL.P.,LinY.,WeiY., Fuel, 2013, 107, 394—399
[16]KhanN.A.,HasanZ.,JhungS.H., Chem. Eur. J., 2014, 20, 376—380
[17]MaC.H.,DaiB.,LiuP.,ZhouN.,ShiA.J.,BanL.L.,ChenH.W., J. Ind. Eng. Chem., 2014, 20, 2769—2774
[18]XiaoJ.,WuL.M.,WuY.,LiuB.,DaiL.,LiZ.,XiaQ.B.,XiH.X., Appl. Energ., 2014, 113, 78—85
[19]XuP.P.,WangC.F.,SunD.,ChenY.J.,ZhunK.L., Chem. Res. Chinese Universities, 2015, 31, 730—735
[20]MaY.Q.,WangR., Chem. J. Chinese Universities, 2014, 35(7), 1515—1522(马云倩, 王睿. 高等学校化学学报, 2014, 35(7), 1515—1522)
[21]XueF.,MaR.,SunY.D.,AbdukaderaA.,ZhangY.H.,LiuC.J., Chem. J. Chinese Universities, 2015, 36(7), 1298—1303(薛飞, 麻荣, 孙亚栋, 阿布力米提·阿布都卡德, 张永红, 刘晨江. 高等学校化学学报, 2015, 36(7), 1298—1303)
[22]OtsukiS.,NonakaT.,TakashimaN.,QianW.H.,IshiharaA.,ImaiT.,KabeT., Energy Fuels, 2000, 14, 1232—1239
(Ed.:P,H,S,K)
doi:10.7503/cjcu20160124
收稿日期:2016-03-01. 网络出版日期: 2016-04-20.
基金项目:新疆维吾尔自治区重点实验室开放课题(批准号: 2015KL014)、 国家自然科学基金(批准号: 21572195, 21262035, 21162025)、 新疆维吾尔自治区青年科技创新人才培养工程(批准号: 2014721004)和新疆大学自然科学基金(批准号: BS110133)资助.
中图分类号O621.14; O643.1
文献标志码A
SynthesisofILs1-Alkyl-3-carboxymethylBenzimidazoleDoubleTrifluoromethanesulfonimideandApplicationinDesulfurizationofFuels†
LIUZhiqing,XUEFei,LEIZhenkai,LIUChenjiang*
(Key Laboratory of Oil and Gas Fine Chemicals, Ministry of Education & Xinjiang Uygur Autonomous Region,Urumqi Key Laboratory of Green Catalysis and Synthesis Technology, Physics and Chemistry Detecting Center,Xinjiang University, Urumqi 830046, China)
AbstractA new class of ionic liquids(ILs) 1-alkyl-3-carboxymethyl benzimidazole double trifluoromethanesulfonimide was synthesized and characterized. Ionic liquids and hydrogen peroxide were tested in extraction-oxidative desulfurization system, the sulphur removal efficiency of S-compounds in the model oil was investigated. The results showed that the 1-butyl-3-carboxymethyl double trifluoromethanesulfonimide salt([C2O2OBIM][Tf2N]) was both extractant and catalyst, n(H2O2)∶n(DBT)=5∶1, m(Model oil)∶m(Ionic liquid)=5∶1, at 75 ℃ for 1 h. The ratios of desulfurization to the model oil of dibenzothiophene(DBT) reached 98.8%. All oxidation desulfurization processes conformed to the pseudo first-order kinetics equation. The sulfide removal rate of the order of five sulfide is dibenzothiophene(DBT)>4,6-dimethyldibenzothiophene(4,6-DMDBT)>thianaphthene(BT)>2,5-dimethylthiophene(2,5-DMT)>thiophene(T). The apparent activation energy of removal of DBT and BT is 44.16 and 52.10 kJ/mol, respectively. Ionic liquid can be recycled for 14 times with an unnoticeable decrease in desulfurization activity. The method can realize deep desulfurization the depth and have the advantages of both simple operation and mild reaction condition.
†SupportedbytheOpenIssueoftheXinjiangUygurAutonomousRegionKeyLaboratory,China(No.2015KL014),theNationalNaturalScienceFoundationofChina(Nos. 21572195, 21262035, 21162025),theProgramforOutstandingYouthScienceandTechnologyInnovationTalentsTraininginXinjiangUygurAutonomousRegion,China(No.2014721004)andtheNaturalScienceFoundationofXinjiangUniversity,China(No.BS110133).
KeywordsBenzimidazole; Ionic liquid; Extraction-oxidative desulfurization; Kinetics
联系人简介: 刘晨江, 男, 博士, 教授, 主要从事有机合成方法学、 绿色化学和功能杂环化合物的合成研究.

