不同化学发光分析系统在皮质醇检测中的性能评价与比较*
陈 翊,李颖能,陈焕辉,林 涛,汤勇才
(1.广东省广州市妇女儿童医疗中心中心实验室 510120;2.广东省广州市第一人民医院检验科 510180)
不同化学发光分析系统在皮质醇检测中的性能评价与比较*
陈翊1,李颖能2,陈焕辉1,林涛1,汤勇才2
(1.广东省广州市妇女儿童医疗中心中心实验室510120;2.广东省广州市第一人民医院检验科510180)
摘要:目的比较贝克曼Access 2 Immunoassay System化学发光免疫分析系统及罗氏COBAS E 411电化学发光免疫分析系统对皮质醇的分析性能与检测结果相关性。方法按照ISO15189中方法评估贝克曼及罗氏分析系统对皮质醇检测的精密度、功能灵敏度、参考范围、方法学、阳性符合率、阴性符合率。结果贝克曼与罗氏分析系统在皮质醇检测中精密度良好,功能灵敏度符合各自厂商设定的临床检测的下限,实验室自建参考范围后,将两分析系统对皮质醇的测定值进行线性回归分析,二者间相关性良好,线性回归系数r2=0.977,阳性符合率、阴性符合率均为100%。结论两分析系统对于皮质醇的分析性能优异,均可满足临床检验需求。经过方法学比对,二者相关性良好,能够通过回归方程对二者间测定值进行引证。
关键词:皮质醇;化学发光免疫分析;电化学发光免疫分析;性能评价
近年来,化学发光免疫法越来越多地被应用于人体激素的测定,作为一种灵敏度非常高的化学发光测定技术和高特异性免疫反应技术相结合的新型标记免疫测定技术,该方法有着广阔的应用前景。但在实际临床检测的应用中,不同检测系统的测定结果存在差异。如何评估化学发光免疫法的测定结果,推动检测标准化,并达到实验室间的检验结果互认,尚需进一步研究。本课题组以皮质醇为对象,通过对现阶段化学发光免疫法应用最广泛的2种方法(化学发光免疫法和电化学发光免疫法)进行方法学评价,探讨化学发光免疫法不同检测仪器间结果的相关性。皮质醇是体内循环系统中的一种高丰度甾类化合物,其主要用于血压维持、抗过敏反应,以及糖类、蛋白质、脂肪的新陈代谢调节等[1]。皮质醇是一种主要由肾上腺皮质合成和分泌的糖皮质激素,在促肾上腺皮质激素(ACTH)的作用下,肾上腺增加对皮质醇的分泌,而高浓度的皮质醇会抑制ACTH的合成,从而使皮质醇浓度维持恒定[2]。因此,血液中皮质醇水平常用于诊断肾上腺相关疾病,如阿狄森症和库欣综合征等[3-4]。临床上皮质醇的检验主要通过免疫法进行。其中,化学发光免疫法和电化学发光免疫法同时具备化学发光法灵敏度及免疫法高特异性的优点,在皮质醇的定量测定中应用广泛。本文按照临床实验室标准化协会(CLSI)的EP12-A2文件及ISO15189医学检验实验室认可的要求[5-6],对本实验室贝克曼Access 2 Immunoassay System(化学发光免疫法)与罗氏COBAS E 411(电化学发光免疫法)检测系统的皮质醇检测结果进行比对,并对二者结果进行评估,现报道如下。
1资料与方法
1.1一般资料样本来自广州市第一人民医院2015年3~6月门诊、住院患者血清,年龄5~73岁。血清样本按照相应检测需求进行收集,样本无溶血与脂血,待测血清样本保存于-20 ℃。
1.2仪器与试剂贝克曼Access 2 Immunoassay System分析仪(化学发光免疫法),罗氏COBAS E 411分析仪(电化学发光免疫法),皮质醇检测试剂盒、校准品、质控品均为各自仪器配套试剂。
1.3方法
1.3.1样本检测所有测试均严格按照相应仪器和试剂操作规程进行,保证测试时仪器校准合格,质控在控。
1.3.2精密度试验收集临床皮质醇样本,配制成皮质醇高、低值两浓度样本。将两样本当日内各重复检测20次,计算测定值结果均值、标准偏差及变异系数(CV),得出批内重复性。将两样本每天测定1次,连续测定20 d,计算测定值结果均值、标准偏差及CV,得出批间重复性。
1.3.3功能灵敏度验证以空白样本对低值质控进行稀释,稀释最终浓度为各自宣称检出限附近(贝克曼0.4 μg/dL和罗氏0.018 μg/dL)。利用两分析系统分别对上述浓度皮质醇样本进行测定,每天测定1次,连续测定10 d,计算各分析系统对上述样本测定结果的均值、标准偏差及CV。
1.3.4参考范围建立选取120例健康人血清临床样本(早晨10:00前取血),分别以贝克曼和罗氏免疫分析仪进行检测,并根据检测结果进行参考范围建立。
1.3.5方法学比对选取40例能够均匀覆盖皮质醇检测范围的临床样本,利用贝克曼Access 2 Immunoassay System分析系统和罗氏COBAS E 411分析系统分别检测上述样本,并对两分析系统的测定值相关性进行比对分析。
1.3.6阴性符合率与阳性符合率结合实验室自建的参考范围及40例临床样本的检测结果,统计两分析系统对皮质醇检测的阴性符合率与阳性符合率。
2结果
2.1精密度评价贝克曼和罗氏分析系统对皮质醇测定的精密度通过批内精密度和批间精密度呈现,见表1。贝克曼和罗氏分析系统对皮质醇测定的批间、批内CV均小于10%,具备良好的精密度,符合临床检验要求。
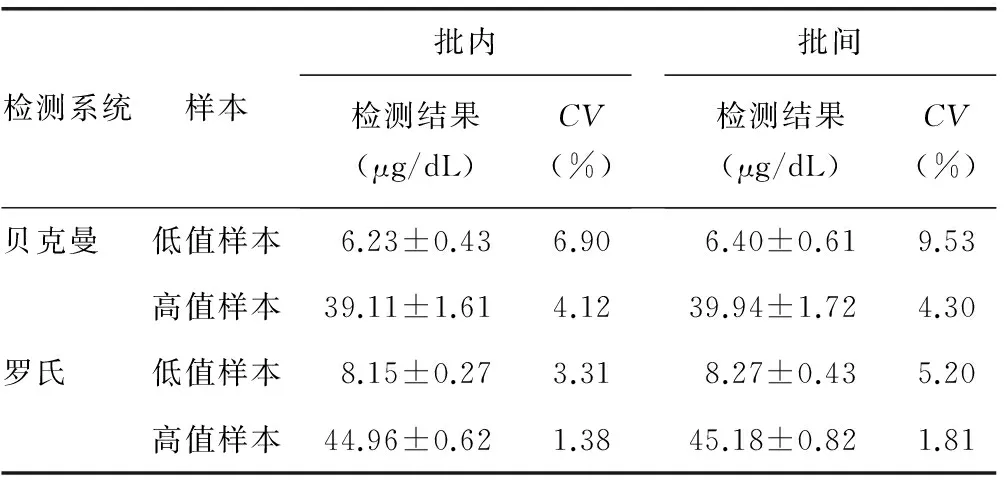
表1 贝克曼和罗氏分析系统检测皮质醇的精密度
2.2功能灵敏度评估本文测定贝克曼与罗氏分析系统在皮质醇测定中的功能灵敏度,用于评估二者功能灵敏度的差异。利用皮质醇低值质控品分别配制检出限(贝克曼0.4 μg/dL和罗氏0.018 μg/dL)附近的浓度样本0.50 μg/dL和0.05 μg/dL,以两分析系统每日分别测定1次,连续测定10 d。贝克曼分析系统的检测结果为(0.55±0.07)μg/dL,CV为12.9%,罗氏分析系统的检测结果为(0.052±0.009)μg/dL,CV为17.3%,两分析系统对于各自宣称皮质醇检出限附近浓度的样本检测结果CV<20%,表明二者宣称检测限能够作为临床检测的下限。
2.3参考范围确认两分析系统各自的宣称参考范围分别为6.7~22.6 μg/dL(贝克曼)和6.2~19.4 μg/dL(罗氏),考虑到本实验室所处地区、人群及操作差异,应建立实验室内部参考范围以辅助临床判断。根据C28-A3文件[7],分别采用两分析系统对120例健康人血清样本(早晨10:00前取血)进行皮质醇测定,评估本实验室内各检测系统的参考范围,贝克曼与罗氏分析系统说明书建议的参考范围分别为6.7~22.6、6.2~19.4 μg/dL,本实验室自建参考范围分别为6.5~21.3、7.1~24.4 μg/dL。
2.4方法学比对利用两分析系统对均匀分布于检测区间的40例临床血清样本进行测试,将测定值结果进行线性回归,如图1所示。两分析系统比对回归方程为Y=1.08X+1.84(其中X为贝克曼测定值结果,Y为罗氏测定值结果),线性回归系数r2=0.977。上述结果表明,二系统测试结果存在偏差(斜率k=1.08),但二者相关性良好。利用二分析系统进行临床判断时,应考虑到二者间测定值差异。
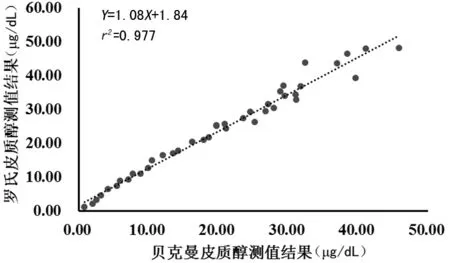
图1 贝克曼与罗氏分析系统测定皮质醇结果的线性回归分析
2.5阳性符合率和阴性符合率按照本实验室自建的临床参考范围,对上述40例临床样本的测试结果进行阳性符合率和阴性符合率分析,对比分析二者的检测结果,确认其阴性符合率和阳性符合率均为100%。两分析系统对皮质醇的检测结果表明,两者对临床判断的一致性较好。
3讨论
化学发光免疫法在临床检验中的应用日益增多,建立相应的评估方法,推动实验标准化,使检验结果更具溯源性,有着重要的意义。另一方面,根据CLSI的EP12-A2文件及ISO15189医学检验实验室认可的规定,临床检验科室应对分析试剂及配套检测仪器的主要分析性能(如精密度、功能灵敏度、方法学、符合率等)进行评估,以确保测定值的准确性。
化学发光免疫法和电化学发光免疫法结合发光系统高灵敏检测以及免疫法高特异性的优点,易于实现高通量、自动化分析,且具备优异的分析性能,受到临床检验科室的青睐。但在实际工作中,实验室人员发现两者的测定结果会有差异,如何对结果进行解读,是本次试验的出发点。
本文对实验室内贝克曼Access2ImmunoassaySystem化学发光免疫分析系统和罗氏COBASE411电化学发光免疫分析系统的皮质醇定量检测分析性能进行评估。由于发光原理的区别,这两套检测系统在试剂、仪器设计方面均存在显著区别,因而二者测定值结果可能存在系统性差异。试验结果表明,两分析系统均具备良好的精密度,其批间与批内CV均小于10%,符合CLSI的EP5-A2标准[8]。两分析系统的功能灵敏度均满足皮质醇临床检测的要求。为了进一步比较两分析系统间测定值准确性,实验室自建参考范围,并对40例临床样本进行检测结果的方法学比对,以及阳性符合率、阴性符合率分析,数据表明两分析系统对皮质醇的检测结果相关性好,线性相关系数r2=0.977,测定值略有偏差(线
性回归方程Y=1.08X+1.84,其中X与Y分别代表贝克曼与罗氏皮质醇测定值结果),但此测定值偏差并不影响临床判断,二者的阳性符合率、阴性符合率均为100%。
综上所述,本次研究遵循ISO15189实验室认可要求,建立了化学发光免疫法不同检测系统间的性能评价方法,应用贝克曼和罗氏化学发光免疫分析系统对皮质醇的分析性能进行评估,两分析系统均满足临床检验性能要求,并且系统间的测值相关性良好,但相互引证时需考虑二者间存在的系统性测定值偏差,在临床判断时需结合各自参考范围进行分析。
参考文献
[1]Foster LB,Dunn RT.Single-antibody technique for radioimmunoassay of cortisol in unextracted serum or plasma[J].Clin Chem,1974,20(3):365-368.
[2]Beisel WR,Diraimondo VC,Chao PY,et al.The influence of plasma protein binding on the extra-adrenal metabolism of cortisol in normal,hyperthyroid and hypothyroid subjects[J].Metabolism,1964,13(10):942-951.
[3]Newell-Price J,Trainer P,Besser M,et al.The diagnosis and differential diagnosis of Cushing′s syndrome and pseudo-Cushing′s states[J].Endocr Rev,1998,19(5):647-672.
[4]Schein RM,Sprung CL,Marcial E,et al.Plasma cortisol levels in patients with septic shock[J].Crit Care Med,1990,18(3):259-263.
[5]CLSI.EP12-A2 User protocol for evaluation of qualitative test performance;Approved guideline[S].2nd ed.Wayne,PA:CLSI,2008.
[6]李金明,申子瑜.正确认识临床实验室认可与提高检验质量之间的关系[J].中华检验医学杂志,2007,30(2):136-139.
[7]CLSI.C28-A3 Defining,establishing,and verifying reference intervals in the clinical laboratory;Approved guidelines[S].3rd ed.Wayne,PA:CLSI,2008.
[8]CLSI.EP5-A2 Evaluation of precision performance of quantative measurement methods;Approved guideline[S].2nd ed.Wayne,PA:CLSI,2004.
* 基金项目:广东省广州市科技计划项目(2014Y2-00031)。
作者简介:陈翊,女,副主任检验技师,主要从事临床检验研究。
DOI:10.3969/j.issn.1673-4130.2016.14.019
文献标识码:A
文章编号:1673-4130(2016)14-1949-03
(收稿日期:2016-01-12修回日期:2016-03-18)
Performance evaluation and comparison of different chemiluminescence immunoassay systems in detection of cortisol*
CHENYi1,LIYingneng2,CHENHuanhui1,LINTao1,TANGYongcai2
(1.CentralLaboratory,GuangzhouMunicipalWomenandChildren′sMedicalCenter,Guangzhou,Guangdong510120,China;2.DepartmentofClinicalLaboratory,GuangzhouMunicipalFirstPeople′sHospital,Guangzhou,Guangdong510180,China)
Abstract:ObjectiveTo compare the analytical performance and results correlation of cortisol detection by the Beckman Access 2 Immunoassay System chemiluminescence system and the Roche COBAS E 411 electrochemical luminescence system.MethodsThe precision,functional sensitivity,reference range,positive coincidence rate and negative coincidence rate of both Beckman Access 2 Immunoassay System and Roche COBAS E 411 systems for detecting cortisol were evaluated according to the method of ISO15198.ResultsBoth Beckman Access 2 Immunoassay System and Roche COBAS E 411 system exhibited better precision,the functional sensitivity conformed to the lower limit of clinical detection set by the manufacturers,after establishing the reference range of cortisol by the laboratory,the cortisol values detected by these two systems were performed the linear regression analysis,the results indicated that the correlation between them was good,the linear regression coefficient r2=0.977,and the positive and negative coincidence rates were 100%.ConclusionThe two analytical systems have excellent performance for cortisol,which all meet the clinical detection requirements.The methodological comparison shows good correlation between them,and the detection results could be cited between these two systems by the regression equation.
Key words:cortisol;chemoluminescence;electrochemical luminescence;performance evaluation

