易错PCR提高人源抗狂犬病毒单链抗体的亲和力
孙丽娜 李川 刘洋 李德新 梁米芳
·技术方法·
易错PCR提高人源抗狂犬病毒单链抗体的亲和力
孙丽娜李川刘洋李德新梁米芳
102206 北京,中国疾病预防控制中心病毒病预防控制所
【摘要】目的通过易错PCR技术提高1株人源抗狂犬病毒单链抗体RV08的亲和力。方法 采用Agilent公司GeneMorph II Random Mutagenesis Kit对RV08轻、重链可变区进行易错PCR扩增,随机引入突变,通过单链抗体(Single-chain antibody fragment ScFv)噬菌体呈现技术构建随机突变抗体文库,经狂犬病毒颗粒aG株固相富集筛选,通过ELISA和IFA鉴定阳性抗体克隆并进行序列测定。利用IgG表达载体VH/VK双质粒系统瞬时转染293T细胞实现IgG抗体的分泌型表达,通过非竞争ELISA测定突变抗体亲和力。结果RV08随机突变抗体库的库容为6×106 cfu/ml,目的基因插入率为100%。重链序列突变频率约为0.95%,轻链序列突变频率约为1.2%,最后获得5株高亲和力的抗体突变株,其中3株抗体HL46、HL2和HL37亲和力分别为原始克隆RV08的1.79倍、1.47倍和1.23倍。结论易错PCR技术与噬菌体抗体库技术相结合使得抗体亲和力获得明显提高,为抗体的体外亲和力成熟提供了参考方法。
【主题词】狂犬病毒;单链抗体;亲和力
Fund programs: State Project For Essential Drug Research and Development(2014ZX09201041004,2013ZX09304103001006)
狂犬病(Rabies)是由狂犬病毒引起的急性传染病[1]。根据世界卫生组织(World health organization, WHO)推荐的处理原则,III级暴露应立即处理伤口并注射抗狂犬病毒免疫球蛋白(rabies immune globulin,RIG),随后接种狂犬病疫苗[2]。由于RIG具有副反应,产品成本高,供应量有限并且存在潜在的血源性感染等缺陷,因此基因工程抗体是取代RIG用于狂犬病的暴露后预防的新方向。近年来关于人源抗狂犬病毒单克隆抗体国内外已有很多报道,但对于抗狂犬病毒人源单抗的亲和力成熟研究鲜有报道,抗体的功能特性与亲和力高低密切相关,抗体亲和力改造也是抗体工程需要解决和发展的重要技术之一。2012年研究组运用噬菌体表面展示技术,在国际上首次获得5株针对狂犬病毒糖蛋白Ⅱ号抗原位点的重组人源中和单抗[3],并在此研究基础上,扩大库容量和筛选规模,获得了6株中和抗体[4]。本研究采用易错PCR技术对狂犬病毒糖蛋白II号表位人源单抗RV08轻重链可变区进行随机突变,通过scFv噬菌体呈现技术构建随机突变抗体文库,对RV08进行亲和力改造,旨在提高抗体亲和力实现抗狂犬病毒抗体制剂成果转化应用。
1材料与方法
1.1细胞、载体、病毒293T细胞、BHK-21细胞和昆虫细胞Sf9购自美国菌种保藏中心(ATCC)。噬菌体抗体库建库载体为 pHAL14[5]。狂犬病毒aG株由中国疾控制中心病毒病所狂犬病室提供,狂犬病毒糖蛋白抗原由病毒病所出血热室构建表达[6]。
1.2抗体与试剂狂犬病毒糖蛋白单链抗体RV08由本室研制[3];对照抗体为抗汉坦病毒核蛋白人源单抗H34,由本室表达并保存。易错PCR试剂盒GeneMorph II Random Mutagenesis Kit购自美国Agilent公司的。胰酶、聚乙二醇(PEG)、转染试剂聚乙烯亚胺(PEI)购自美国Sigma公司。
1.3易错PCR扩增RV08轻重链可变区基因根据单链抗体RV08重链序列,设计特异正向引物:5′-CCCATGGCCCAGGTGCAGCTGCAG-3′,根据单链抗体RV08轻链序列,设计特异反向引物:5′-TTGCGGCCGCAGAGGACGGTGGGA-3′。采用Agilent公司的易错PCR试剂盒(GeneMorph II Random Mutagenesis Kit)以2 μl含有抗狂犬病毒糖蛋白单抗RV08轻重链基因的重组质粒pcom3b-RV08 为模板,进行易错PCR扩增。易错PCR技术关键要控制目的基因突变频率,根据试剂盒提供的突变频率条件如表1:
为了获得理想的突变效果,本研究将突变频率控制在9~12 bp/Kb范围内,根据突变频率要求,易错PCR反应条件如下:采用50 μl反应体系,模板按实际扩增目的片段模板50 ng每个反应添加,而非以整个RV08单链抗体质粒的浓度计算,此外分别加入Mutazyme II reaction buffer,40 mmol/L dNTP mix (200 μmol/L each final),正向反向引物(250 ng/ μl),Mutazyme II DNA polymerase (2.5 U/ μl),将反应液混合均匀,PCR的反应条件为95 ℃ 30 s、55 ℃ 30 s、72 ℃1 min,扩增30个循环,之后72 ℃延伸10 min。以此纯化后的PCR产物作为下一轮PCR的模板,重复完成6轮易错PCR。

表1 易错PCR突变条件及频率
1.4随机突变抗体库的构建及验证以pHAL4为建库载体,与易错PCR扩增获得的RV08单链抗体基因VH-linker-VL分别经NcoI和NotI双酶切后,二者经T4 DNA连接酶连接,电转化XLI-Blue MRF感受态细胞,涂于含有氨苄青霉素的LB平皿,计菌落数,按每ml抗体库所含的克隆数计算库容量。随机挑取10个克隆,测序检测转化效率并分析突变率,详细建库方法参考文献[5,6]。
1.5随机突变抗体库的富集筛选及单链抗体的诱导表达用 0.1 mol/L NaHCO3(pH8.6) 溶液将狂犬病毒aG株4 ℃包被过夜,用MPBST(PBS 加入1%脱脂奶和 0.05% Tween-20)封闭包被孔室温孵育2 h,之后用PBST洗涤3遍。向其中加入10 cfu/ml噬菌体抗体库,室温孵育2 h。移去上清,加100 μl 10 μg/ml的胰酶洗脱。洗脱下来的噬菌体感染新鲜的XLI-Blue菌液(OD600=0.5),经辅助噬菌体包装后进行下一轮筛选,如此反复3次后,随机挑选单克隆经IPTG诱导表达ScFv。具体富集方法及ScFv抗体的诱导表达按文献进行[5,7]。
1.6单链抗体的 ELISA 检测向包被有狂犬病毒aG颗粒的酶标板中加入单链抗体原核诱导表达上清,37 ℃孵育1 h;PBST洗板5遍后,加入anti-myc 鼠抗体(美国 Sigma),37 ℃孵育1 h;洗板后加入抗鼠酶标IgG全抗,37 ℃孵育1 h后显色,2M H2SO4终止反应后通过酶标仪测吸光度值,判定抗狂犬病毒scFv阳性克隆。阳性克隆测序后pubmed基因库中序列比较,获得抗体轻重链型别。
1.7IgG抗体表达纯化scFv抗体阳性克隆经测序后参照V-Base 2数据库比对分析,将获得的scFv抗体轻重链基因分别克隆入VH/VK全抗体表达载体[7],采用转染试剂聚乙烯亚胺(PEI)瞬时转染293T细胞,37 ℃ 5% CO2条件下培养48 h后收集上清,采用 Amersham 公司的 Protein-A 亲和层析柱直接纯化表达上清。
1.8非竞争ELISA法亲和力测定将纯化的狂犬病毒aG株颗粒按5 μg/ml、2.5 μg/ml、1.25 μg/ml、0.625 μg/ml的浓度包被酶标板,纯化待测抗体从1.8 mg/L起进行2倍稀释。具体操作和结果判定参考文献[3,8]。
2结果
2.1随机突变抗体库的构建及验证通过DNAStar MegAlign 对RV08突变体的突变位点进行比对显示,轻链序列和重链序列的实际的突变频率有一些差异,轻链的突变频率约为1.2%,重链的突变频率约为0.95%,二者均已达到构建突变抗体文库的预期要求。
2.2随机突变抗体库的富集筛选用狂犬病毒aG株进行富集筛选,3轮富集后随机挑取800个克隆,用狂犬病毒aG抗原ELISA检测scFv诱导表达上清,结果发现3轮富集筛选洗脱库容量逐轮递增,这表明特异性结合重组单链噬菌体抗体在逐步的富集。在198株通过ELISA检测阳性的克隆中,有163株克隆通过间接免疫荧光鉴定与狂犬病毒糖蛋白反应阳性(表2)。
2.3单链抗体的序列分析用 DNASTAR 序列分析软件进行分析处理,比较 Internet V-Base 2 基因库中的 IgG 序列,上述163株特异性结合狂犬病毒糖蛋白的人源scFv单克隆抗体,存在115株序列不同的抗体。

表2 抗狂犬病毒噬菌体抗体库的富集筛选
2.4IgG抗体表达及ELISA检测挑选39株抗原结合活性较高的scFv抗体,克隆到IgG全抗体表达载体,转染293T细胞,通过ELISA对收获上清进行抗人Fab和Fc片段以及抗aG抗原的检测,结果如图1所示。根据ELISA 检测结果,本研究挑选与抗原 结合滴度相对较高的抗体克隆进一步分析其亲和力,分别是HL2、HL37、HL46、HL49、HL75。
2.5抗体亲和力测定非竞争ELISA法测定RV08突变体亲和力常数,结果显示亲本株RV08的亲和力为2.33×10-9M;相比较而言HL75及HL49亲和力略低于亲本株,约为2.39X10-9M,2.69×10-9M;而HL46、HL2和HL37亲和力分别为1.30×10-9M、1.56×10-9M、1.88×10-9M,均高于RV08;亲和力最高的是HL46,约为RV08的1.79倍,可满足实际应用(图2)。
2.6IgG抗体互补决定区基因的氨基酸序列分析利用生物软件DNA Star对以上获得的5株突变抗体的轻重链可变区序列比对显示5株抗体重链和轻链的CDR区分别有氨基酸发生突变,而重链CDR3区均无突变发生。亲和力最高的HL46轻链重链CDR区分别有2个氨基酸发生突变,即共有4个突变,其次HL2和HL37分别有3和4个氨基酸突变,亲和力稍低的HL75和HL49分别有1个和2个氨基酸突变(表3)。
3讨论
近年来关于人源抗狂犬病毒单克隆抗体国内外已有很多报道[3,4,9],但对于抗狂犬病毒人源单抗的亲和力成熟研究鲜有报道,而抗体的功能特性与亲和力高低密切相关,真正实现临床应用需要通过多种手段实现体外亲和力成熟以提高抗体亲和力。目前常用的方法有:易错PCR、CDR区定向突变、DNA改组等。本研究采用易错PCR技术提高狂犬病毒糖蛋白人源单抗RV08的亲和力,经固相筛选获得了5株突变抗体,其中3株抗体HL46、HL2和HL37亲和力分别为原始克隆RV08的1.79倍、1.47倍和1.23倍,表明易错PCR突变后抗体亲和力获得明显提高。
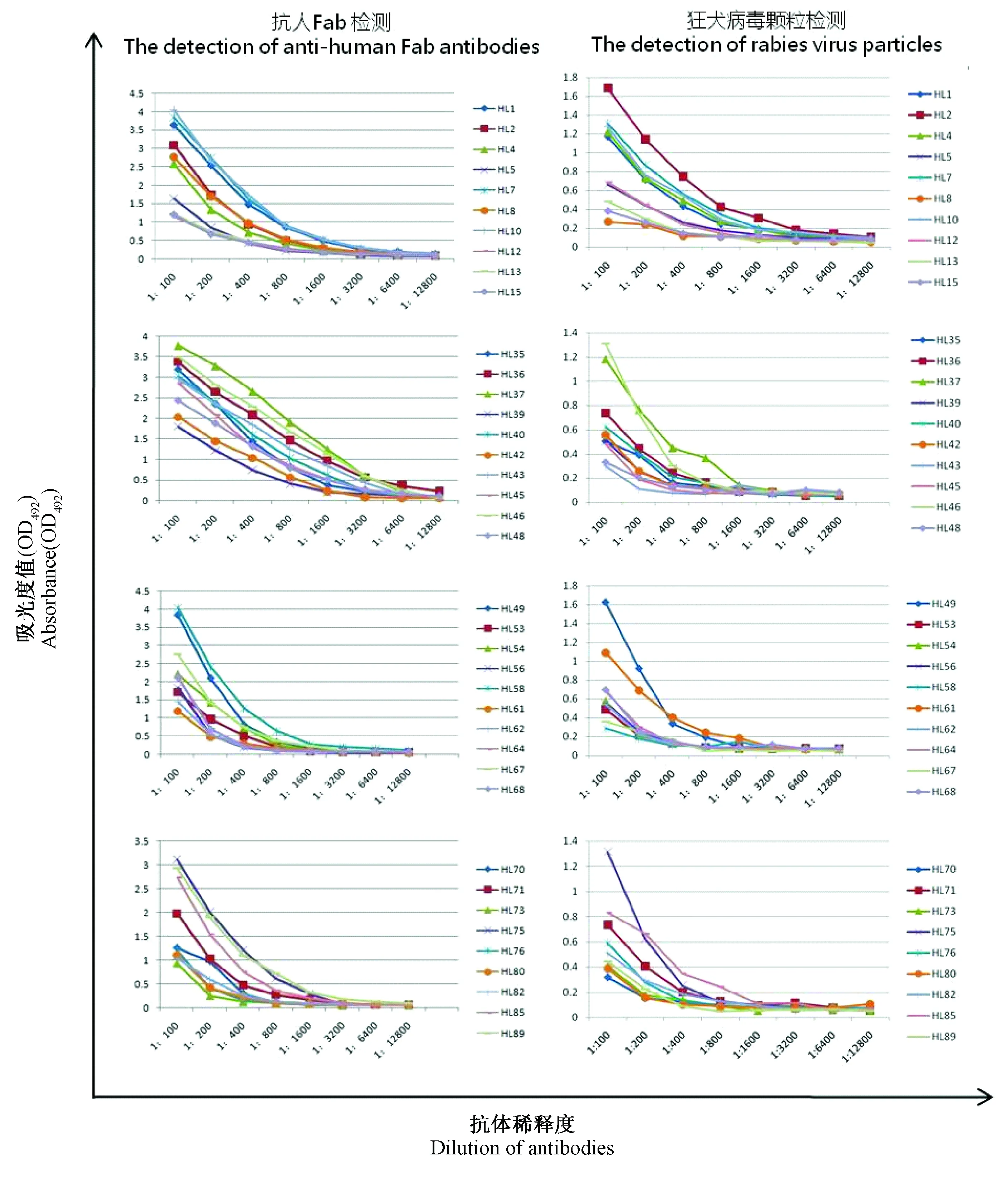
图1 人源抗狂犬病毒糖蛋白IgG抗体特异性表达的ELISA检测Fig.1 Expression of specfic human IgG antibodies against RV-G detected by ELISA

图2 非竞争ELISA测定人源重组抗体亲和力Fig.2 Measurement of human recombinant antibody affinity by non-competitive enzyme immunoassay

表3 抗狂犬病毒人IgG抗体互补决定区基因的氨基酸序列分析
抗体与抗原结合的关键部位存在于6个互补决定区(CDRs),其中重链CDR3的多样性变化最多,而且与抗体的结构和功能密切相关[10]。本研究发现突变抗体轻链和重链的CDR1、CDR2区分别有氨基酸发生突变,而重链CDR3区均没有突变产生,提示虽然抗体生成过程中重链CDR3序列变化最为丰富,但本研究中仅通过易错PCR的方法引入少量的碱基突变,难以得到重链CDR3区有意义的氨基酸突变。今后的工作将把研究重点放在CDR3区,以期获得到亲和力更高的抗体。
4参考文献
[1]俞永新. 狂犬病和狂犬病疫苗. 北京: 中国医药科技出版社, 2001, 7-14.
[2]World Health Organization. Strategies for the control and elimination of rabies in Aisa [M]. Geneva, Switzerland, 2001, 2.
[3]Sun L N, Chen Z, Yu L, et al. Generation and characterization of neutralizing human recombinant antibodies against antigenic site II of rabies virus glycoprotein [J]. Appl Microbiol Biotechnol, 2012, 96(2): 357-366. doi: 10.1007/s00253-012-4171-4.
[4]于礼, 孙丽娜, 金晶, 等. 人源抗狂犬病毒基因工程单链抗体的研究[J]. 中华实验和临床病毒学杂志, 2012, 26(3): 189-192.doi: 10.3760/cma.j.issn.1003-9279.2012.03.009.
[5]Hust M, Toleikis L, Dubel S. Antibody phage display.
Handbook of therapeutic antibodies [M]. Weinheim: Wiley-VCH, 2007: 45-68.
[6]陈哲,孙丽娜,李川,等. 人源中和性抗狂犬病毒基因工程抗体的研制[J]. 病毒学报, 2010, 26(3): 271-275.
[7]Pelat T, Hust M, Laffly E, et al. High-affinity, human antibody-like antibody fragment (single-chain variable fragment) neutralizing the lethal factor (LF) of Bacillus anthracis by inhibiting protective antigen-LF complex formation[J]. Antimicro Agents Chemother, 2007, 51(8): 2758-2764.
[8]Beatty JD, Barbara G. Beatty, William G. Vlahos. Measurement of monoclonal antibody affinity by non-competitive enzyme immunoassay[J]. J Immunol Methods,1987,100(1-2):173-179.
[9]Bakker AB1, Python C, Kissling CJ, Pandya P, et al. First administration to humans of a monoclonal antibody cocktail against rabies virus: safety, tolerability, and neutralizing activity[J]. Vaccine, 2008, 26(47): 5922-5927. doi: 10.1016/j.vaccine.2008.08.050.
[10]Zanetti M. Antigenized antibodies[J]. Nature,1992, 355 (6359): 476-477.
通信作者:梁米芳,Emai: mifangl@vip.sina.com
DOI:10.3760/cma.j.issn.1003-9279.2016.03.018
基金项目:重大新药创制(2014ZX09201041004,2013ZX09304103001006)
(收稿日期:2016-01-22)
Affinity maturation of a single-chain antibody against rabies virus
SunLina,LiChuan,LiuYang,LiDexin,LiangMifang
NationalInstituteforViralDiseaseControlandPrevention,ChineseCenterforDiseaseControlandPrevention,Beijing102206,ChinaCorrespondingauthor:LiangMifang,Email:mifangl@vip.sina.com
【Abstract】ObjectiveTo obtain a human single-chain antibody against rabies virus (RV) with high affinity by error-prone PCR technology. MethodsA combinatorial scFv antibody mutant library was constructed by error-prone PCR amplifying VH and VL of scFv RV08. After package by hyperphage, the scFv phage mutant library was panned by ELISA and IFA with purified RV AG. The selected mutant antibodies were converted to full human IgG antibodies with the VH and VK Express cassettes. The affinity of mutant antibodies was measured by non-competitive enzyme immunoassay. ResultsThe mutant antibody library with capacity of 6×106 cfu/ml contained target gene insertion rate of 100%. Heavy chain and light chain were sequenced with mutation frequency of about 0.95% and 1.2% respectively. Finally 5 mutant antibodies with high affinity were obtained, of which HL46, HL2 and HL37 had higher affinity with 1.79 times, 1.47 times and 1.23 times of RV08 respectively. ConclusionsIn this study, error-prone PCR technology and phage display technology combination enables to obtain significantly improved affinity of antibody.
【Key words】Rabies virus; Single-chain antibody; Affinity

