亚砜咪唑与诺森治疗消化性溃疡合并出血的临床效果
蔡秀芬
亚砜咪唑与诺森治疗消化性溃疡合并出血的临床效果
蔡秀芬
目的对比亚砜咪唑与诺森治疗消化性溃疡合并出血的临床效果。方法选择2013-10—2015-10收治的160例消化性溃疡伴出血患者,按照随机数字表法分为观察组和对照组,每组80例。对照组在常规治疗基础上给予亚砜咪唑静脉滴注,观察组在常规治疗基础上诺森静脉滴注,观察两组治疗效果。结果观察组总有效率88.8%,对照组总有效率67.5%,组间比较,P<0.05;两组患者治疗后幽门螺杆菌(Hp)感染、疼痛评分均有所改善,观察组改善效果更加理想,组间比较,P<0.05;两组患者治疗后pH值均明显升高,但观察组患者抑制胃酸分泌效果更为理想,组间比较,P<0.01;观察组Hp清除率86.3%,对照组Hp清除率51.3%,组间比较,P<0.01;两组不良反应发生率比较,差异无统计学意义,P>0.05。结论诺森治疗消化性溃疡合并出血可有效抑制胃酸分泌,清除Hp,安全性高,临床治疗效果满意。
亚砜咪唑;诺森;消化性溃疡合并出血
消化性溃疡是全球性常见病,部分患者可以不治而愈,但是一部分患者可能出现幽门梗阻、穿孔甚至是癌变等并发症,给治疗带来一定的困难[1]。消化性溃疡患者血管受到溃疡的侵蚀、破裂,常伴有出血,若出血量过多,可导致急性失血性休克,严重威胁患者的生命安全[2]。由于该病多因胃酸的侵袭及幽门螺杆菌(Hp)感染而发病,因此,治疗的关键是根治幽门螺旋杆菌。临床多采用胃镜下辅助治疗,虽然有一定的效果,但胃镜治疗只能作为辅助治疗的方法。本文对2013-10—2015-10收治的80例消化性溃疡伴出血患者采用亚砜咪唑和诺森治疗的效果进行对比分析,现报告如下。
1 资料与方法
1.1 一般资料选择我中心2013-10—2015-10收治的160例消化性溃疡伴出血患者,所有患者均经胃镜检查确诊,按照随机数字表法分为观察组和对照组,每组80例。观察组男72例,女8例;年龄28~72岁,平均(41.1±3.3)岁;初发78例,复发2例;快速尿素酶检测结果示80例患者中有76例Hp阳性;其中胃溃疡患者22例,十二指肠球溃疡41例,复合型溃疡17例。对照组男67例,女13例;年龄29~74岁,平均(42.5±3.8)岁;初发79例,复发1例;快速尿素酶检测结果示80例患者中有78例Hp阳性;其中胃溃疡患者19例,十二指肠球溃疡43例,复合型溃疡18例;两组患者一般资料差异无统计学意义,P>0.05,具有可比性。
1.2 纳入标准①上腹部闷痛、烧灼痛、隐痛、反酸2个月以上。②均经纤维胃镜确诊,溃疡大小在0.2~2.0 cm,数目1~2个。③检查有Hp感染,化验血尿便常规、肝肾功能均正常。④近期未服用非甾体类抗炎药。
1.3 排除标准①对治疗药物过敏患者。②合并严重心、肺、肝、肾功能障碍患者。③恶性肿瘤患者。④妊娠期或哺乳期妇女。
1.4 方法两组均给予常规治疗,包括:输液、禁食以及输血、维持水电解质平衡和营养支持等。在此基础上对两组患者实施不同的药物治疗。对照组:给予亚砜咪唑治疗,将药物40 mg加入到100 mL质量浓度为0.05 g/mL的葡萄糖溶液中进行静脉滴注,30 min内滴注结束,2次/d,连续治疗5 d。观察组:给予诺森40 mg加入质量浓度为0.009 g/mL的氯化钠注射液100 mL静脉滴注,调整滴速在30 min内滴完,1次/d,治疗5 d。
1.5 疗效判定标准显效:消化性溃疡及周围炎症全部消失,溃疡创面基本愈合;有效:溃疡创面明显改善,创面减少50%以上;无效:溃疡创面改善不明显,创面减少50%以下或症状加重。使用VAS标准对患者疼痛程度进行评分,总分10分,0~3分表示轻微疼痛,4~6分表示疼痛可耐受,7~10表示疼痛难以忍受,并对睡眠和食欲造成影响。治疗前后分别进行胃镜检查,于胃窦及胃体处取样,进行快速尿素酶试验和染色,两项试验均为阳性者确定为Hp感染,在治疗结束4周后复查,两项试验均为阴性者视为Hp清除。
1.6 统计学处理采用SPSS 18.00软件包,计数资料用率表示,采用χ2检验,计量资料用(±s)表示,采用t检验,P<0.05表示差异有统计学意义。
2 结果
2.1 两组疗效比较(表1)观察组总有效率88.8%,对照组总有效率67.5%,组间比较,差异有统计学意义,P<0.05。

表1 两组患者治疗效果比较[n(%)]
2.2 患者治疗前后Hp感染、疼痛评分变化情况(表2)两组患者治疗后Hp感染、疼痛评分均有所改善,观察组改善效果更加理想,组间比较,P<0.05。
表2 患者治疗前后Hp感染、疼痛评分变化情况[n(%),±s]

表2 患者治疗前后Hp感染、疼痛评分变化情况[n(%),±s]
?
2.3 两组患者治疗前后空腹胃液pH值(表3)两组患者治疗后pH值均明显升高,但观察组患者抑制胃酸分泌效果更为理想,组间比较,P<0.01。
表3 两组患者治疗前后空腹胃液pH值变化情况(±s)

表3 两组患者治疗前后空腹胃液pH值变化情况(±s)
组别例数治疗前治疗后观察组801.7±0.85.8±0.1对照组801.7±0.94.1±0.5 t 0.3396.579 P 0.2970.000
2.4 两组Hp清除率比较(表4)观察组Hp清除率86.3%,对照组Hp清除率51.3%,组间比较,差异有高度统计学意义,P<0.01。
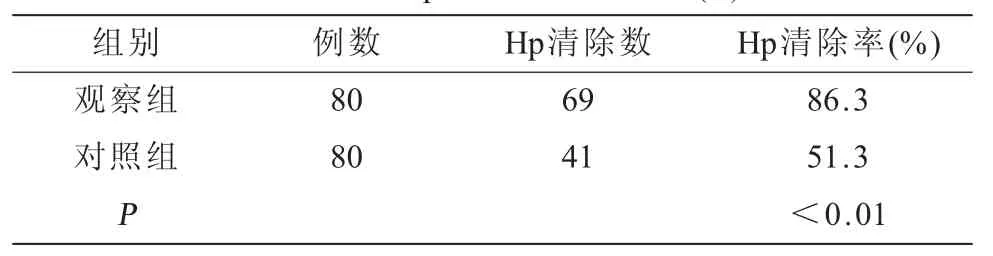
表4 两组Hp清除率情况比较(n)
2.5 两组不良反应情况比较(表5)两组不良反应发生率比较,差异无统计学意义,P>0.05。

表5 两组不良反应情况比较(n)
3 讨论
消化性溃疡合并出血的发病机制复杂,目前尚未完全明确,多认为是内在原因和外在因素共同作用的结果[3]。临床研究表明[4],消性化溃疡合并出血与胃酸分泌过多以及Hp感染有密切的关系,因此,治疗的关键是抑制胃酸的分泌及根治Hp。
诺森是一种质子抑制剂药物,属于苯并咪唑衍生物,它是一种强效的抑酸药物,该药的作用机制是由于质子泵(H-K-ATP酶)是位于壁细胞的光面管泡及泌酸小管膜上的一种酶,由a、b两个亚单位组成,在受体和第二信使的作用下,首先能过水解ATP获得能量,再进行H-K离子的细胞内外交换,使H离子能够在分泌小管腔内与Cl离子结合而形成酸,最后在与蛋白酶等有机物组成胃酸后排入胃腔。诺森可通过与质子泵特异性、不可逆性结合,改变其空间构象使之失活,使H离子向胃内释放的过程受到阻碍,而导致H离子与Cl离子无法结合,特异性地抑制胃壁细胞内H+-K+-ATP酶,而达到抑制胃酸分泌的目的,与其他类型的药物相比较,抑酸作用更强,同时它还可以促进胃黏膜的修复而发挥止血的临床效果[5]。此外,诺森还可以抑制Hp的侵入,降低Hp的活动力,这种抑制机制可能与质子泵抑制剂分子结构中含有类似咪唑结构的基团相关。Hp破坏胃肠道保护机制的重要因子之一就是尿素酶,如果药物能够使尿素酶得到有效的抑制或破坏就可以阻止Hp在胃内的黏附过程,进而起到抗菌的作用。Hp被清除后,恢复了胃肠道保护机制,胃酸无法对胃壁造成侵袭,达到治疗胃溃疡的目的。
综上所述,诺森治疗消化性溃疡合并出血可有效抑制胃酸分泌,清除Hp,安全性高,临床治疗效果满意。
[1]管丽红.消化道溃疡合并出血的内科疗效分析[J].中国实用医药,2013,8(32):58-59.
[2]张庆芝.奥美拉唑治疗消化道溃疡合并出血39例临床疗效观察[J].健康之路,2014,13(5):149-150.
[3]陆艳.泮托拉唑治疗消化性溃疡合并上消化道出血的疗效观察[J].中国社区医师:医学专业,2013,15(5):73.
[4]BoninEA,MoranE,GostoutCJ,etal.Naturalorifice transluminalendoscopicsurgeryforpatientswithperforated peptic ulcer[J].Surgical Endoscopy,2012,26(6):1534-1538.
[5]柴雪梅.泮托拉唑钠治疗过敏性紫癜并消化道出血的效果分析[J].吉林医学,2010,31(25):4290-4291.
2016-04-06)
1005-619X(2016)10-1084-02
10.13517/j.cnki.ccm.2016.10.034
113001抚顺市望花区创业园区社区卫生服务中心

